河南地区云南白药胶囊临床安全性集中监测研究报告
2018-11-19吕秋霞曹玉净李扬郭建阔徐永申朱建富王博王翔
吕秋霞 曹玉净 李扬 郭建阔 徐永申 朱建富 王博 王翔
云南白药胶囊具有化瘀止血、活血止痛、解毒消肿、愈伤等多重药理作用[1]。临床主要用于跌打损伤, 瘀血肿痛,吐血、咯血、便血、痔血、崩漏下血、手术出血、疮疡肿毒及软组织挫伤、闭合性骨折、支气管扩张及肺结核咯血、溃疡病出血以及皮肤感染性疾病等[2,3]。随着云南白药胶囊临床运用科室和病症的不断延伸, 以及用药人群年龄覆盖范围的不断扩展, 临床上偶见关于云南白药的不良反应的相关报道。本文作者以“云南白药”、“引起”、“致”、“不良反应”、“中毒”、“过敏”等为关键词, 在中国知网、万方、维普等数据库中进行检索整理相关报道文献后, 最终收集到与云南白药相关的不良反应个案报道文献36篇。经详细分析后发现, 云南白药导致的大部分不良反应均为皮肤过敏性反应和恶心呕吐、胃腹部不适等胃肠道反应, 经停药或采取相应治疗措施对患者进行处理之后, 症状均减轻或消失;有少部分患者则是由于因求愈心切, 而在短时间内过量服药, 而导致出现不同程度的不良反应, 但未造成严重后果[4-6];还有部分患者在服药后, 出现了过敏性休克的严重不良反应, 但采取相应处理措施之后, 患者症状均消失[7-9]。本文作者为进一步研究云南白药胶囊在真实世界临床使用过程中, 可能发生的不良反应及探索诱发这些不良反应的诱因, 联合了河南地区其他5家医院的骨科、妇科、眼科、外科等科室。在2015年6月~2016年12月, 采用前瞻性、多中心、巢式病例对照研究的方法, 通过对接受云南白药胶囊治疗的患者进行集中监测研究, 记录患者在研究期间出现的不良事件详细信息, 深入分析导致不良事件发生的原因, 全面认识云南白药胶囊的安全性。为今后临床医生合理用药, 尽可能规避有可能诱发不良反应的合并用药提供理论依据和科学支持, 也为临床医生向广大患者提供更加安全可靠的用药建议奠定基础。现报告如下。
1 资料与方法
1.1 一般资料 在2015年6月~2016年12月监测期内,河南省内6家二、三级综合性医院共906例接受云南白药胶囊治疗的患者作为研究对象, 涉及骨科、妇科、外科、眼科等多个科室。
1.2 方法 本研究的观察药物为云南白药胶囊, 由各科室牵头专家(副主任医师以上职称)负责提出用法用量、疗程、合并用药等用药方案建议。所有患者的最终给药方案均由各监测医院负责本次不良反应监测的医生制定, 给药方案的制定充分考虑了患者的病情, 同时结合医生的临床用药经验制订。本研究不作任何干预。
1.3 监测内容 研究期间, 患者的基本信息、既往史(过敏史、药品不良反应史等)及用药情况均进行详细的记录, 包括:患者一般资料信息、既往史、病情详述、合并用药的药品名称、生产批次、用法用量、疗程、治疗方案的变更等信息。研究中发生的任何不良事件均严格详细记录, 包括:不良事件特征、严重程度、发生时间、消失时间、处理措施、对原患疾病的影响及转归等信息。对于既往有肝肾功能损害者, 需要在治疗前后监测肝肾功能。不良事件相关信息由研究者记录到安全性监测病例报告表(CRF)中。
1.4 观察时点 由于患者病情各不相同, 服用云南白药胶囊的用法用量、疗程及合并用药, 由负责监测的临床医生确定。在研究期间, 需每天记录不良事件发生情况;治疗结束后第14天进行末次随访, 以观察迟发性不良反应, 并嘱患者在此期间一旦出现不良事件, 需主动报告。
1.5 统计学方法 采用SPSS19.0统计学软件对数据进行统计分析。计量资料以均数±标准差(±s)表示, 采用t检验;计数资料以率(%)表示, 采用χ2检验。P<0.05表示差异具有统计学意义。
2 结果
2.1 各中心病例及入组科室分布情况 河南省区参研单位共6家, 收集病例总数为906例;涉及骨科、妇科、外科和眼科等多个临床科室, 入组情况及科室分布。见表1。
2.2 患者人口统计学信息描述性统计 906例入组患者中,男性患者占总人数的57%, 女性患者占43%;骨科患者占68%, 外科患者占27%, 妇科患者占3%;眼科占2%。见表2。
2.3 患者基本生命体征 906例入组患者中, 收缩压为80.0~203.0 mm Hg(1 mm Hg=0.133 kPa), 舒张压为45.0~121.0 mm Hg,脉搏为55.0~130.0次/min, 呼吸为14.0~32.0次/min, 体温为35.3~38.5℃。见表 3。
2.4 患者就诊地点及病史统计 906例入组患者中, 门诊占比3.67%, 住院部占比96.33%, 有传染病史1.33%, 有过敏史占比6.00%, 有手术外伤史占比22.78%, 有伴随疾病占比24.22%, 有药品不良反应史占比2.44%。见表4。
2.5 患者云南白药胶囊的使用情况统计 906例入组患者中, 首次使用本胶囊占比65.44%, 口服用药占比99.44%, 每日用药量2.0~12.0粒, 用药天数1.0~70.0 d。见表5。
2.6 患者治疗期间合并用药及饮食情况统计 906例入组患者中, 治疗期间有合并用药占比96.66%, 饮酒占比0.11%,吸烟占比0.11%, 特殊饮食占比5.22%。见表6。
2.7 患者不良事件发生情况统计 在整个研究期间, 临床研究者共收集到不良事件10例, 通过我国6级法进行判定后,认为有2例很可能与云南白药有关, 有4例可能与云南白药有关, 有2例可能无关, 1例待评价, 1例无法评价。见表7。
2.8 被认定为与云南白药有关的不良反应分析 为进一步确保不良反应判定的准确性和科学性, 将整个研究期间收集到的10例不良事件提交由国内不良反应判定领域的权威专家组成的不良反应评定专家委员会, 对10例不良事件进行二次再判定。最终, 从收集到的10例不良事件中判定出3例与云南白药有关的不良反应。不良反应为痛痒、红疹、胃部不适、腹胀等, 均在药品说明书中有详细提及的不良反应病症。见表8。与云南白药胶囊有关的不良反应发生时段统计。见表9。对3例被认定为与云南白药胶囊有关的不良反应进行有针对性的分析。数据显示3例被认定为与云南白药有关的不良反应中, 无单用云南白药的患者, 3例均有合并用药。云南白药胶囊有合并用药情况下, 不良反应发生率为0.331%(3/906)。

表1 各中心入组科室分布情况
表2 患者人口统计学信息的描述性统计[n(%), ±s]

表2 患者人口统计学信息的描述性统计[n(%), ±s]
性别 例数(缺失) 900(6) 609(6) 30(0) 247(0) 14(0)男512(56.89) 362(59.44) 0 143(57.89) 7(50.00)女388(43.11) 247(40.56) 30(100.00) 104(42.11) 7(50.00)年龄(岁) 例数(缺失) 896(10) 606(9) 30(0) 246(1) 14(0)47.8±17.0 48.9±17.6 44.7±9.9 44.9±16.1 54.7±11.9体重(kg) 例数(缺失) 900(6) 609(6) 30(0) 247(0) 14(0)67.1±11.3 66.9±11.7 61.1±7.8 67.9±10.3 70.2±12.6体重指数(kg/m2) 例数(缺失) 900(6) 609(6) 30(0) 247(0) 14(0)23.7±3.1 23.8±3.3 23.3±2.6 23.5±2.4 26.2±3.6
表3 患者基本生命体征的描述性统计[n(%), ±s]

表3 患者基本生命体征的描述性统计[n(%), ±s]
分类 合计 骨科 妇科 外科 眼科收缩压(mm Hg) 例数(缺失) 900(6) 609(6) 30(0) 247(0) 14(0)127.8±15.9 128.1±15.8 113.5±19.0 128.3±15.1 133.2±16.1舒张压(mm Hg) 例数(缺失) 900(6) 609(6) 30(0) 247(0) 14(0)79.7±10.1 79.8±9.5 70.2±12.6 80.1±10.6 84.3±11.6脉搏(次/min) 例数(缺失) 900(6) 609(6) 30(0) 247(0) 14(0)79.7±9.1 79.1±8.2 79.4±4.9 81.2±11.4 78.3±2.9呼吸(次/min) 例数(缺失) 900(6) 609(6) 30(0) 247(0) 14(0)19.5±1.6 19.4±1.6 19.8±1.1 19.6±1.5 19.4±0.7体温(℃) 例数(缺失) 900(6) 609(6) 30(0) 247(0) 14(0)36.5±0.3 36.6±0.3 36.6±0.4 36.4±0.4 36.5±0.2
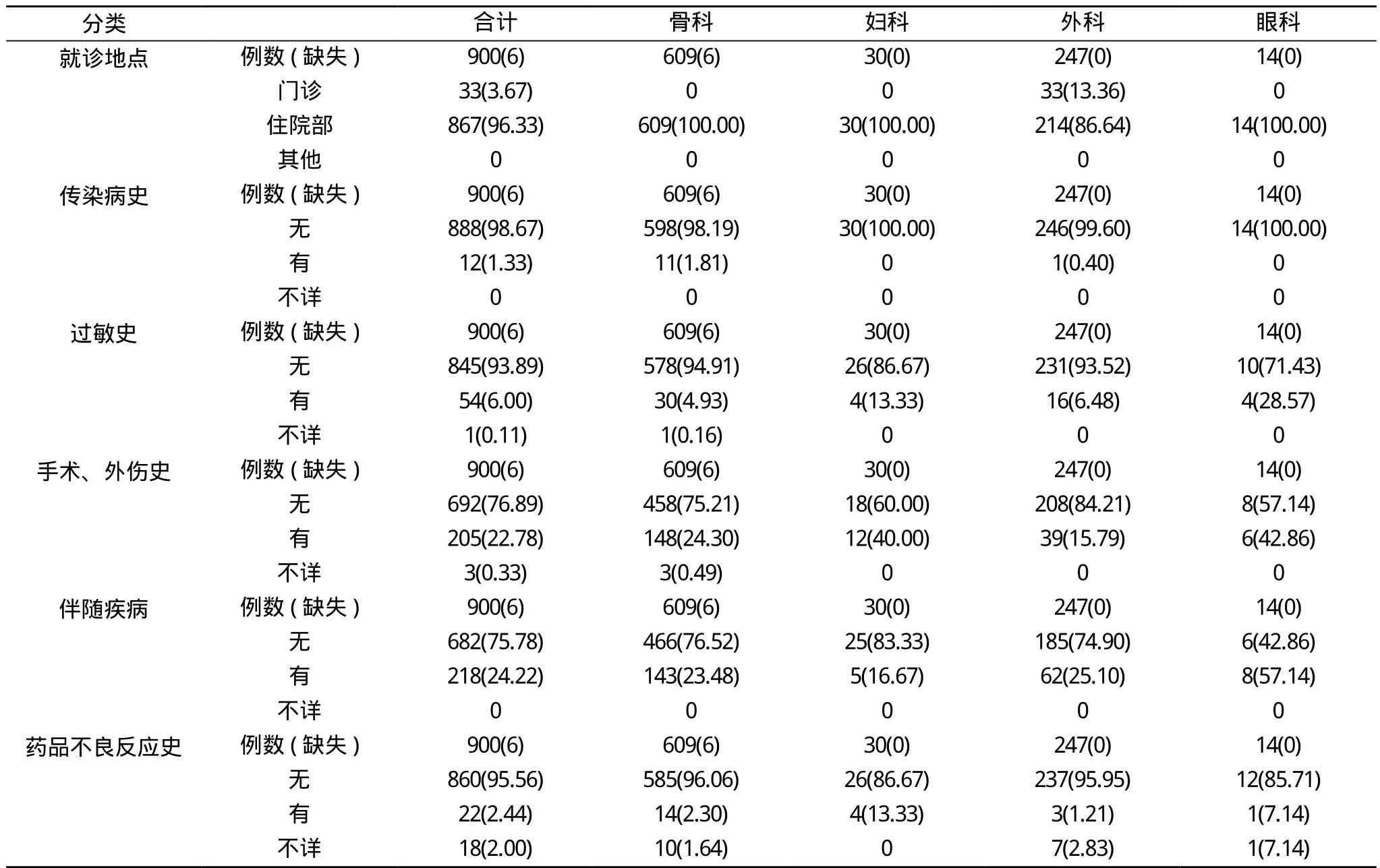
表4 患者就诊地点及病史的描述性统计[n(%)]
表5 患者云南白药胶囊使用情况的描述性统计[n(%), ±s]

表5 患者云南白药胶囊使用情况的描述性统计[n(%), ±s]
分类 合计 骨科 妇科 外科 眼科是否首次使用本胶囊 例数(缺失) 900(6) 609(6) 30(0) 247(0) 14(0)否100(11.11) 91(14.94) 4(13.33) 4(1.62) 1(7.14)是589(65.44) 346(56.81) 9(30.00) 226(91.50) 8(57.14)不详 211(23.44) 172(28.24) 17(56.67) 17(6.88) 5(35.71)用药方法 例数(缺失) 900(6) 609(6) 30(0) 247(0) 14(0)口服 895(99.44) 608(99.84) 30(100.00) 243(98.38) 14(100.00)外用 1(0.11) 0 0 1(0.40) 0口服+外用 3(0.33) 1(0.16) 0 2(0.81) 0口服+其他 1(0.11) 0 0 1(0.40) 0每日用药量(粒) 例数(缺失) 900(6) 609(6) 30(0) 247(0) 14(0)6.7±1.4 6.9±1.5 8.3±1.0 6.3±1.1 6.0±0.0用药天数(d) 例数(缺失) 889(17) 601(14) 30(0) 245(2) 13(1)14.5±8.0 14.9±8.5 7.8±1.9 14.2±6.9 11.5±5.1

表6 患者治疗期间合并用药及饮食情况的描述性统计[n(%)]
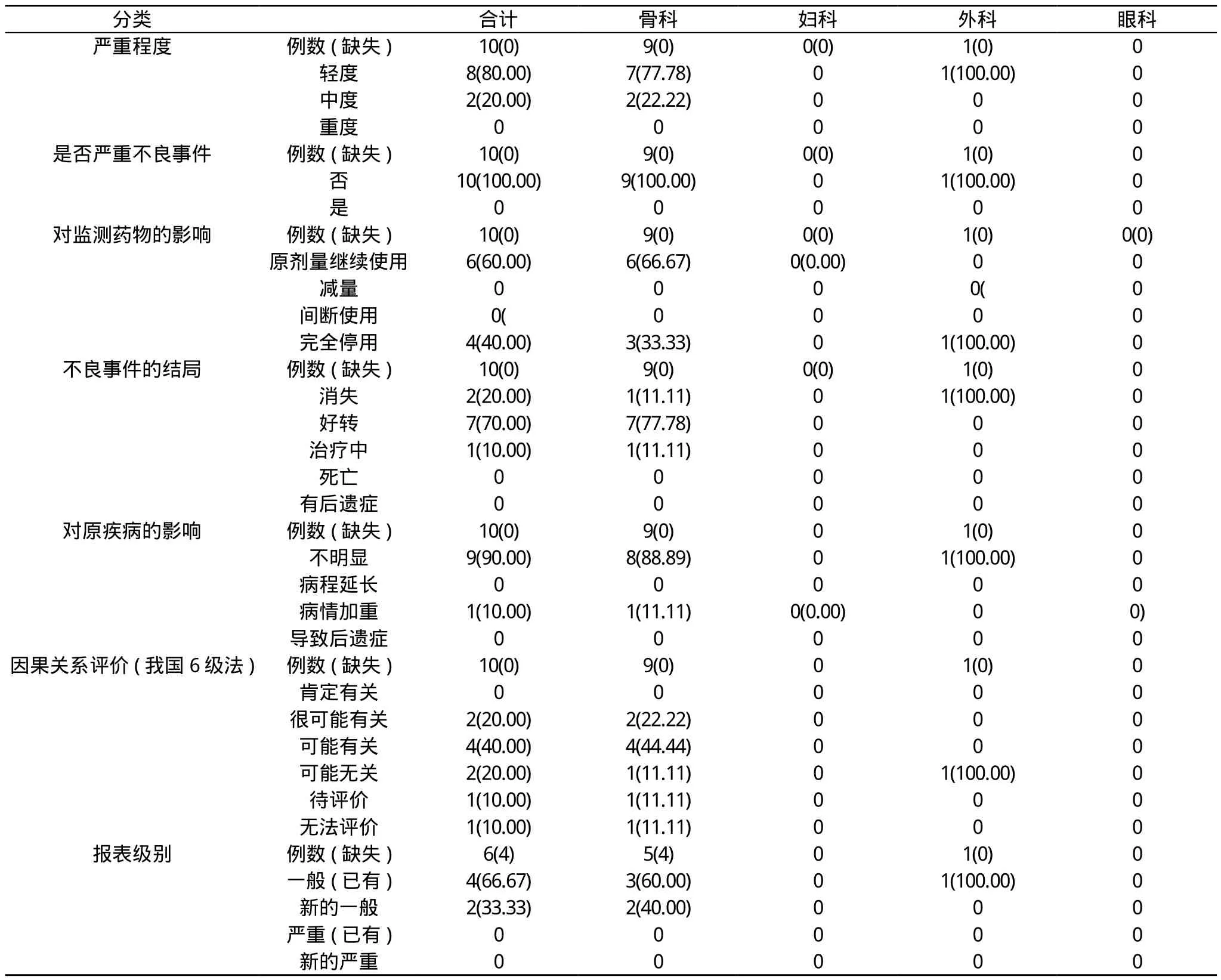
表7 患者在研究期间不良事件发生情况的描述性统计[n(%)]

表8 被认定为与云南白药胶囊有关的不良反应列表

表9 不良反应发生时间的统计(n, %)
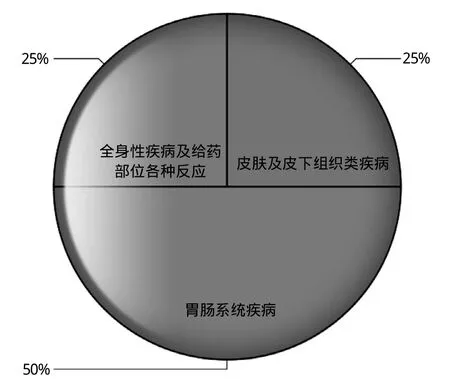
图1 不良反应类型图
2.9 与云南白药有关的不良反应分布特点 与云南白药胶囊有关的不良反应相对于河南省收集病例总体的发生率。见表10。3例与云南白药胶囊有关的不良反应的疾病系统类型构成情况。见图1。不良反应的严重程度及结局分布特点。见表11、12。

表10 不良反应各系统发生率(n, ‰)

表11 不良反应的严重程度分布(n, %)

表12 不良反应结局分析表(n, %)
3 讨论
3.1 云南白药的现代药理学研究 云南白药原名“曲焕章万应百宝丹”, 由我国彝族名医曲焕章老先生于1902年创制, 目前属于我国一级中药保护品种, 在临床各科室运用广泛。现代药理学研究发现[10,11], 云南白药能够促进血小板α颗粒和致密颗粒的释放, 活化血小板使其伸出更多的伪促, 加快机体止血过程;同时, 促进血管内皮细胞生长因子的(vascular endothelial growth factor, VEGF)表达, 改善局部微循环, 具有较好的止血、愈伤等作用。蔡丽等[12]研究发现,云南白药胶囊能有效降低血浆皮质醇含量, 解除对巨噬细胞的抑制作用, 快速发挥巨噬细胞的吞噬作用, 消除创面炎症,加快血管再生, 促进创面愈合。
3.2 云南白药胶囊的临床应用 云南白药胶囊具有活血化瘀、凉血止血、抗炎消肿等药理作用, 临床广泛应用于骨科、消化科、肛肠科、妇科、外科等临床多科室[13,14]。本次云南白药胶囊临床安全性集中监测研究的906例入组患者中,骨科患者有615例, 占68%;外科患者有247例, 占27%;妇科患者有30例, 占3%;眼科患者有14例, 占2%。入组患者年龄为3.0~89.5岁, 基本覆盖了全年龄段患者。
3.3 云南白药胶囊的安全性评价研究 由药物不良反应引发的安全性问题, 一直以来都受到了各国药品监督管理部门广泛而高度的重视, 药物安全性评价技术和方法更是各国学者研究的热点[15]。近年来, 中药新品种、新制剂不断涌现,各种安全性问题也逐渐被发现并报道;传统药物的安全性评价技术和方法已不能满足当前的临床观察需要, 寻找和建立快速、准确的药物安全性评价技术和方法已成为当前研究的热点[16]。
本次研究采用前瞻性、巢式病例对照研究的方法, 通过大样本、多中心对云南白药胶囊临床安全性进行全面评价。在906例入组患者中, 最终收集到3例与云南白药胶囊有关的不良反应。不良反应的症状主要是痛痒、红疹、胃部不适、腹胀等, 研究中监测到的不良反应症状均为云南白药胶囊说明书中已经载明的可能会出现的不良反应。在整个监测过程中, 未发现新的和严重的不良反应, 出现不良反应的3例患者在停药或采取相应的处理措施之后, 不良反应均消失或好转, 对患者原患疾病几乎未产生任何影响。
本研究中, 云南白药胶囊有合并用药的情况下, 不良反应发生率为0.331%, 属偶见级别。说明云南白药胶囊在临床上运用广泛, 不良反应发生率低, 安全性较高, 值得临床广泛推广使用。
