白杨素-钴配合物的合成及生物活性
2018-11-16王佳丽李丽敏
郭 蒙, 王佳丽, 李 丹, 李丽敏
(潍坊学院 化学化工与环境工程学院,山东 潍坊 261061)
0 引 言
本文通过紫外光谱法对制备白杨素-钴配合物的条件进行了优化,并研究了白杨素及其钴配合物在清除羟基自由基、抗氧化性等方面上的性能,为进一步拓展其应用提供支持与理论基础。
1 实验部分
1.1 仪器与试剂
TU-1901双光束紫外可见分光光度计(北京普析),WRS-2A/2微机熔点仪(上海仪电),pHS-3BW酸度计(上海理达),DZF-6020真空干燥箱(上海博迅)。硫酸钴(天津光复科技),白杨素(南京泽朗),其他所用试剂均为分析纯,实验用水为三次蒸馏水。
1.2 实验方法
(1) 白杨素-钴(Ⅱ)配合物制备。在浓度为21 mmol/L的HMTA-HCl缓冲溶液中,按摩尔比2∶1分别加入白杨素、钴溶液,在30 ℃下反应35 min后减压抽滤,50 ℃真空烘干,得白杨素-钴(Ⅱ)配合物,产物为黄绿色粉末状固体。
(2) 紫外光谱法。取一系列具塞比色管,分别加入HMTA-HCl缓冲溶液、钴离子溶液、白杨素溶液,定容至10 mL,在一定温度下反应一定时间后,以同浓度的缓冲溶液为参比溶液,在230~450 nm下进行紫外光谱扫描。
(3) 羟基自由基测定。取1.2 mL、7.5 mmol/L的FeSO4溶液、0.025mL、1%的H2O2溶液于比色管中摇匀,再加入1.0 mL的水杨酸-乙醇溶液,加入不同体积的白杨素、白杨素-钴溶液,在37 ℃恒温水槽中加热15 min后,再加入1.0 mL的水杨酸-乙醇溶液,再继续加热15 min,取出后用二次水定容至10 mL。在400~600 nm的范围内进行紫外光谱扫描。按下式计算羟基自由基清除率[15]
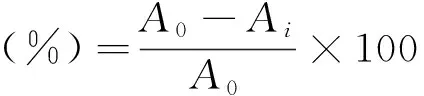
(1)
式中:A0为不加试样时溶液的吸光度;Ai为加试样时溶液的吸光度。
(4) 抗氧化作用。将白杨素-钴配合物用二甲亚砜溶解,制成溶液。取适量白杨素、白杨素-钴溶液加入装有定量鸭油的烧杯中混匀,同时用空白样作对照,在室温下培养,在干燥的碘量瓶中准确称取样品,先加入20 mL异辛烷溶解,再加入30 mL冰乙酸溶解,按照GB/T 5538—2005[16]方法测定,每隔1 d取样测定鸭油的过氧化值(P(mmol/kg)),并以此来表示鸭油的氧化速度
(2)
式中:V1为用于测定的硫代硫酸钠溶液体积(mL);V2为空白的硫代硫酸钠体积(mL);c为硫代硫酸钠浓度(mol/L);m为试样质量(g)。
2 结果与讨论
2.1 合成条件优化
白杨素、白杨素-钴的紫外光谱曲线如图1所示。由图可见,白杨素在272、347 nm处出现了强吸收峰,加入钴溶液后,在272 nm处的吸收峰发生了红移(272 nm → 275 nm), 吸收峰出现了减色效应,吸光度A由0.743降至0.545,在347 nm的吸收峰则完全消失。以上现象表明,两者之间发生了反应。所以在以后的研究中,以272 nm处吸收峰降低的程度(ΔA)作为反应是否完全的标准。

图1 紫外光谱图
(1) 缓冲溶液及pH的选择。反应体系的酸碱度对于白杨素与钴离子的反应有较大影响(见图2)。实验发现,在pH 7.7~8.5范围内,随pH的增大,吸光度差值ΔA呈现先增大后减小的现象,当pH值为8.23时,ΔA出现最大值,因此,实验时将反应pH值严格控制为8.23。
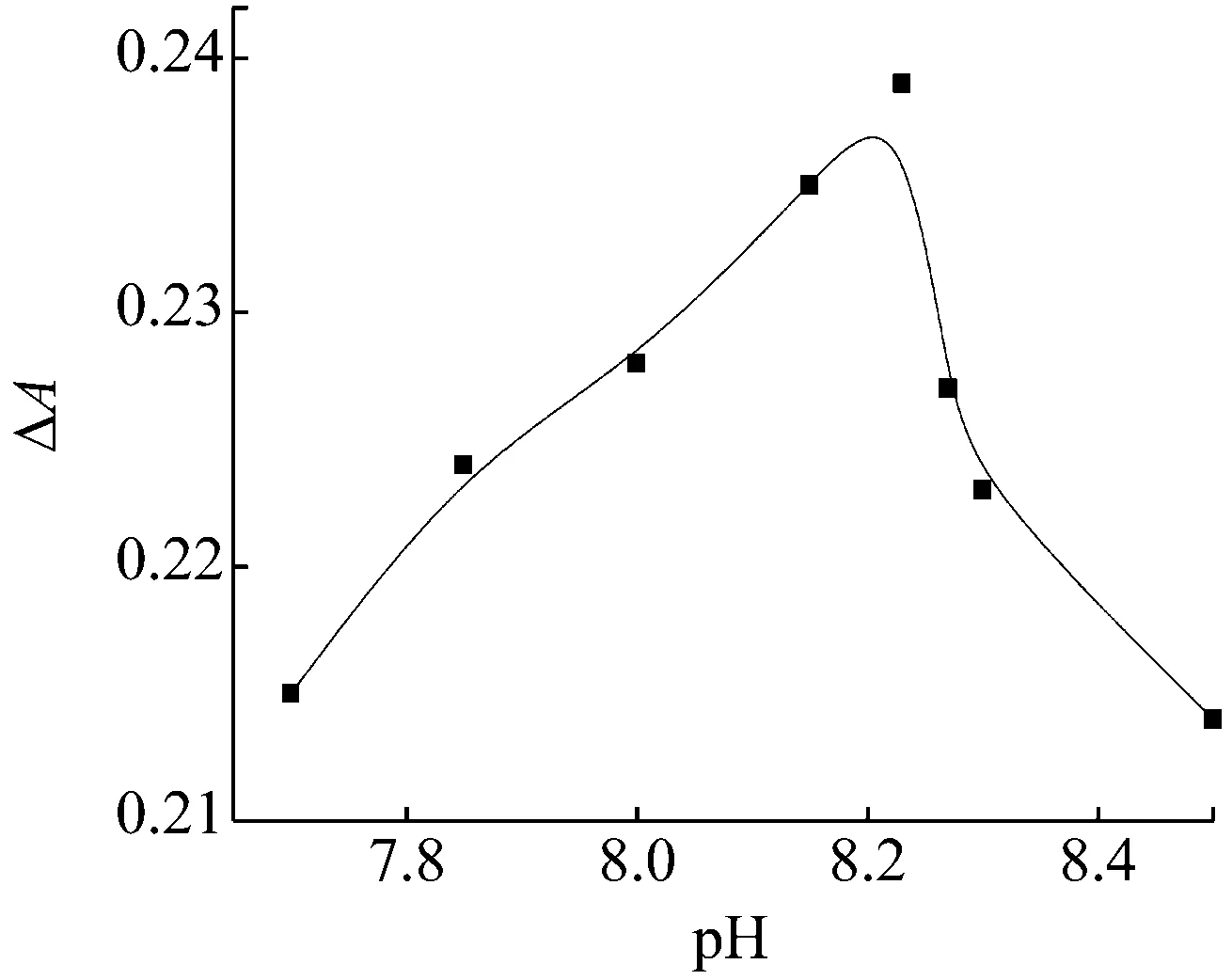
同样在对缓冲溶液的浓度研究时发现,当缓冲溶液的浓度为21 mmol/L时,该体系的ΔA呈现出最大值,故确定该反应的缓冲溶液浓度为21 mmol/L。通过对NH3-NH4Cl、HMTA-HCl、Tris-HCl、KH2PO4- K2HPO4、H3BO3-KOH等几种缓冲溶液进行选择研究,发现采用HMTA-HCl作为体系反应的缓冲溶液时,能导致反应体系的ΔA最大。
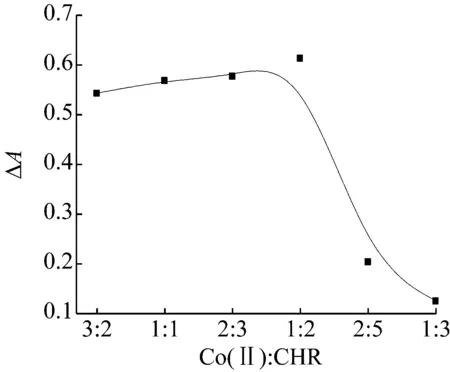
(2) 反应配比的影响。 固定其他条件,研究了白杨素与Co(Ⅱ)的摩尔比对于反应的影响,结果如图3所示。由图可见,反应体系的吸光度随白杨素与钴离子的络合比的增大呈现逐渐下降的现象,当配比达到2∶1时,体系的吸光度差ΔA最大,因此选择该反应的反应物配比为2∶1。
(3) 反应时间及温度的影响。在其他实验条件固定的情况下,通过吸光度差值研究了时间对于两者反应的影响。发现当时间达到35 min时,体系的吸光度差值ΔA达到最大;时间大于35 min后,ΔA基本稳定不变,故确定该反应的反应时间为35 min。同时,在对研究温度的影响时发现,30 ℃以前,吸光度变化剧烈,到达30 ℃后,体系的吸光度逐渐稳定,说明白杨素与钴(Ⅱ)已经反应完全。因此,确定该体系反应的最佳温度为30 ℃。
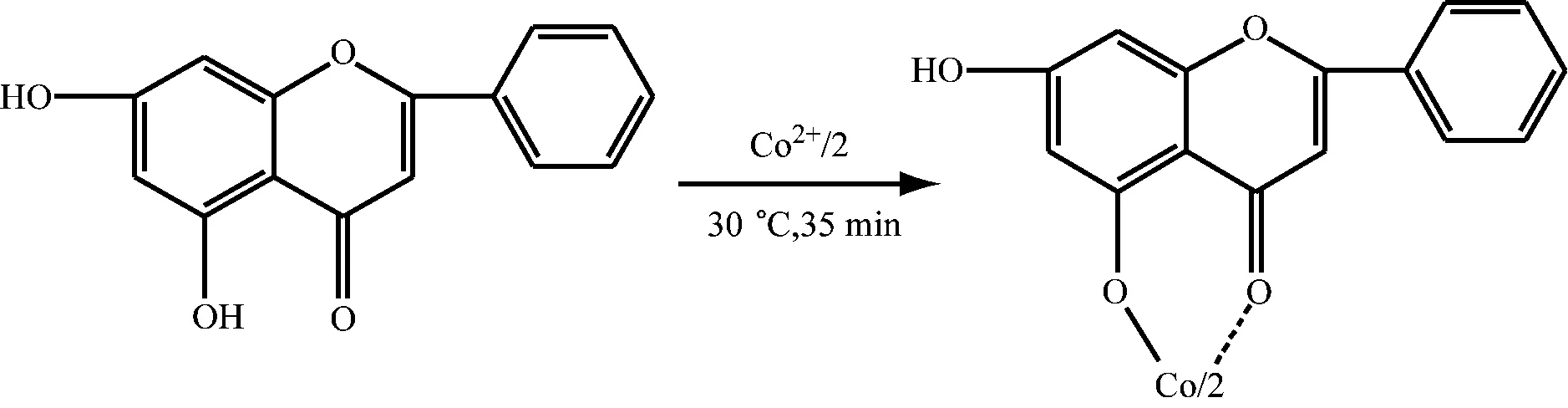
综上研究,认为白杨素与钴(Ⅱ)的最佳反应条件为:在21 mmol/L、pH 8.23的HTMA-HCl缓冲溶液中,白杨素与钴(Ⅱ)按摩尔比为2∶1,30 ℃下反应35 min。抽滤,真空干燥后称量,产率为73.4 %。在该条件下,合成的白杨素-钴配合物为黄绿色,不溶于水,微溶于无水乙醇、乙醚、丙酮等有机溶剂,可溶于二甲基亚砜(DMSO),其熔点大于341.5 ℃(341.5℃为熔点仪量程),同样条件下测得白杨素熔点288.8~289.2 ℃。推断白杨素与钴(Ⅱ)的反应可能为:
2.2 羟基自由基的清除作用
图4显示了不同浓度下的白杨素及其钴配合物清除羟基自由基的能力。由图可见,白杨素及白杨素-钴配合物都具有清除羟基自由基的活性。在较低浓度下,白杨素-钴清除羟基自由基的能力与白杨素接近;但当浓度大于0.15 mmol/L时,白杨素-钴的清除自由基活性能力急剧增大,且其能力大于白杨素。

图4 白杨素、白杨素-钴配合物对羟基自由基的清除作用
2.3 抗氧化作用
白杨素及白杨素-钴配合物对于鸭油的抗氧化作用实验结果如表1所示。由表可以看出,两者的P值均比空白对照组的P值低,表明白杨素与白杨素钴配合物都对鸭油均有一定的抗氧化作用,而且白杨素-钴在油脂的抗氧化性能方面优于白杨素。
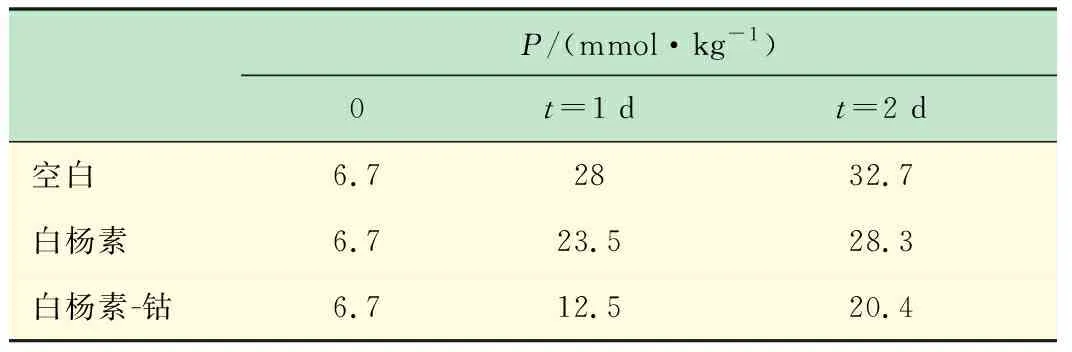
表1 不干胶薄膜样品相消波长
3 结 语
本文通过紫外光谱法研究了白杨素与钴(Ⅱ)溶液的反应条件:在21 mmol/L 、pH 8.23的HTMA-HCl缓冲溶液中,按摩尔比2∶1加入白杨素与钴离子,在30 ℃下反应35 min。同时研究发现,合成的白杨素-钴配合物在清除羟基自由基及抗氧化性能方面,其活性均优于白杨素,研究结果将会为新型抗癌药物的开发及生产提供支持与帮助。
