甲氨蝶呤联合艾拉莫德治疗类风湿关节炎的疗效与安全性的系统评价
2018-11-14孙静张琨吴丽萍张莉谢志军
孙静 张琨 吴丽萍 张莉 谢志军
类风湿关节炎(rheumatoid arthritis,RA)是一种自身免疫病,表现为对称性、多个周围关节的慢性炎症病变,临床表现为受累关节疼痛、肿胀、功能下降,病变呈继续、反复发作的过程。目前RA的治疗主要是非甾体抗炎药(non-steroidal anti-inflammatory drugs,NSAIDs)、慢作用抗风湿药 [slow acting anti-rheumatic drug,SAARDs,包括缓解病情抗风湿药(disease modifying antirheumatic drugs,DMARDS)和细胞毒药物]、糖皮质激素、生物制剂等。传统DMARDs是治疗RA的公认首选用药,2012年美国风湿病协会(American College of Rheumatology,ACR) 指南推荐甲氨蝶呤(methotrexate,MTX)和其他DMARDs联合的治疗方案[1]。MTX治疗RA起效时间4~8周,远期疗效好和耐受性高是ACR和欧洲风湿病联盟(European League Against Rheumatism,EULAR)将此药定为治疗RA首选药物的重要原因。MTX是一种叶酸拮抗剂,可竞争性地与二氢叶酸还原酶结合并阻止二氢叶酸向四氢叶酸转化,导致细胞内池还原叶酸的耗竭,干扰胸腺嘧啶脱氧核苷酸的合成,发挥抗细胞增殖作用,减轻症状和修复骨质破坏[2]。而艾拉莫德(Iguratimod,T-614)是一种小分子化合物,通过抑制NF-κB阻碍细胞因子(TNF-α、IL-6、IL-8等)的产生,调节B淋巴细胞,减少Ig的产生[3],降低单核细胞趋化蛋白 1(monocyte chemoattractant protein,MCP1)的生成,促进成骨细胞分化,有效阻止骨质破坏,减少患者的致残率和致畸率[4],是一种新型、具有多作用靶点的DMARDS。T-614在中国已完成Ⅲ期临床试验[5],2012年正式用于临床[6],但尚未普遍用于临床治疗。MTX联合T-614治疗RA的试验研究和临床已有相关报道,但没有两者联合使用治疗RA的系统评价。本研究对国内外有关MTX联合T-614治疗RA的随机对照试验(randomized controlled trial,RCT)文献进行了 4 个相关指标的Meta分析,这些分析为RA病情活动的相关指标,为MTX联合T-614治疗RA的疗效和安全性评价及临床应用提供依据,现报道如下。
1 资料和方法
1.1 文献检索 通过检索英文数据库PubMed、Cochrance Library、Wiley Online Library 和中文数据库CNKI、CBM、万方数据知识服务平台。收集从建库至2016年12月30日已公开发表关于MTX联合T-614治疗RA的相关文献,治疗时间至少12周,同时检索相关研究的参考文献。中文检索词:甲氨蝶呤、艾拉莫德、艾得辛、类风湿关节炎。英文检索词:Methotrexate、MTX、Iguratimod、T-614、rheumatoid arthritis、RA。
1.2 纳入与排除标准 纳入标准:(1)采用ACR 1987年提出的RA诊断标准[7]或2010年ACR和EULAR提出的新RA分类标准和评分系统[8]的RA患者,处于疾病活动期;(2)RCT;(3)干预措施:试验组为 MTX 联合T-614治疗,对照组为MTX治疗;(4)数据齐全。排除标准:(1)非 RCT;(2)试验结果数据不全;(3)重复发表的数据或论文。
1.3 文献质量评估 依照修改后的Jadad评分量表标准[9],由2位研究者对所有纳入研究的文献进行方法学质量评价。Jadad评分项目:(1)是否随机序列产生(1~3分);(2)是否随机化隐藏(0~3分);(3)是否盲法(1~3分);(4)是否描述撤出与退出的数目和理由(0~1分)。Jadad得分为0~7分,1~3分为低质量文献,4~7分为高质量文献。
1.4 数据提取 2位研究者分别对纳入研究的文献进行数据提取。数据包含第一作者、文献年份、试验组与对照组总数、ACR20、ACR50、ACR70(在所有的疼痛关节计数和肿胀关节计数中与基线相比至少有20%、50%、70%的改善)以及RA患者疾病活动度(DAS28,28个疼痛关节计数包括肩关节、肘、腕、掌指关节、近端指间关节、膝关节)。若2位研究者所提取的数据有差异,则进行讨论解决。
1.5 统计学处理 采用Revman 5.3统计软件,计量资料以表示,并对纳入研究进行异质性检验,根据I2判断异质性大小,I2≤25%为低度异质性,25%<I2<50%为中度异质性,I2≥50%为高度异质性。不同的研究之间根据异质性决定使用相应的固定或随机效应模型。选择优势比(OR)和95%可信区间(CI)为各效应值精确度。P<0.05为差异有统计学意义。
2 结果
2.1 文献检索一般情况 检索PubMed 35篇,Cochrane Library 9篇,Wiley Online Library 11篇,知网37篇,万方40篇,中国生物医学文献数据库22篇。初步获得154篇相关文献,经纳入和排除标准筛选,Endnote排重后共有15篇文献[10-24]纳入本次分析。共纳入研究者1 382例,试验组MTX联合T-614,对照组MTX。15项研究均为RCT,且报道了失访和退出情况。见表1、2。
2.2 ACR20/50/70与DAS28的Meta分析 本研究Meta 分析结果见图 1(a、b、c)和图 2,其中 6 篇文献Meta分析结果显示MTX联合T-614治疗RA后ACR20、ACR50 缓解率高于对照组(OR=3.54、2.85,95%CI:2.47~5.08、1.96~4.13,均P<0.01),其中 4 篇文献Meta分析结果显示ACR70缓解率较对照组高(OR=1.84,95%CI:1.02~3.29,P<0.05)。ACR20 比较异质性检验(I2=23%),ACR50比较异质性检验(I2=21%),ACR70比较异质性检验(I2=36%),异质性为低中度,均采用固定效应模型分析。其中8篇文献Meta分析结果显示DAS28 低于对照组(OR=-0.99,95%CI:-1.18~-0.73,P<0.01),异质性检验(I2=69%),异质性大,采用随机效应模型进行效应量的合并分析。在DAS28分析中,其中5篇文献中是DAS28,3篇文献中是DAS28-CRP,只对DAS28的文献分析,I2=82%,OR=-1.16,未从实质上改变结果,DAS28-CRP合并到DAS28中,结果可信。
2.3 不良事件发生比较Meta分析 所有纳入研究的不良事件比较Meta分析结果显示异质性检验I2=67%,采用随机效应模型分析。分析结果显示MTX联合T-614治疗RA出现的不良事件与对照组比较无统计学意义(OR=1.44,95%CI:0.75~2.79,P>0.05),安全性方面试验组与对照组比较无明显优势。
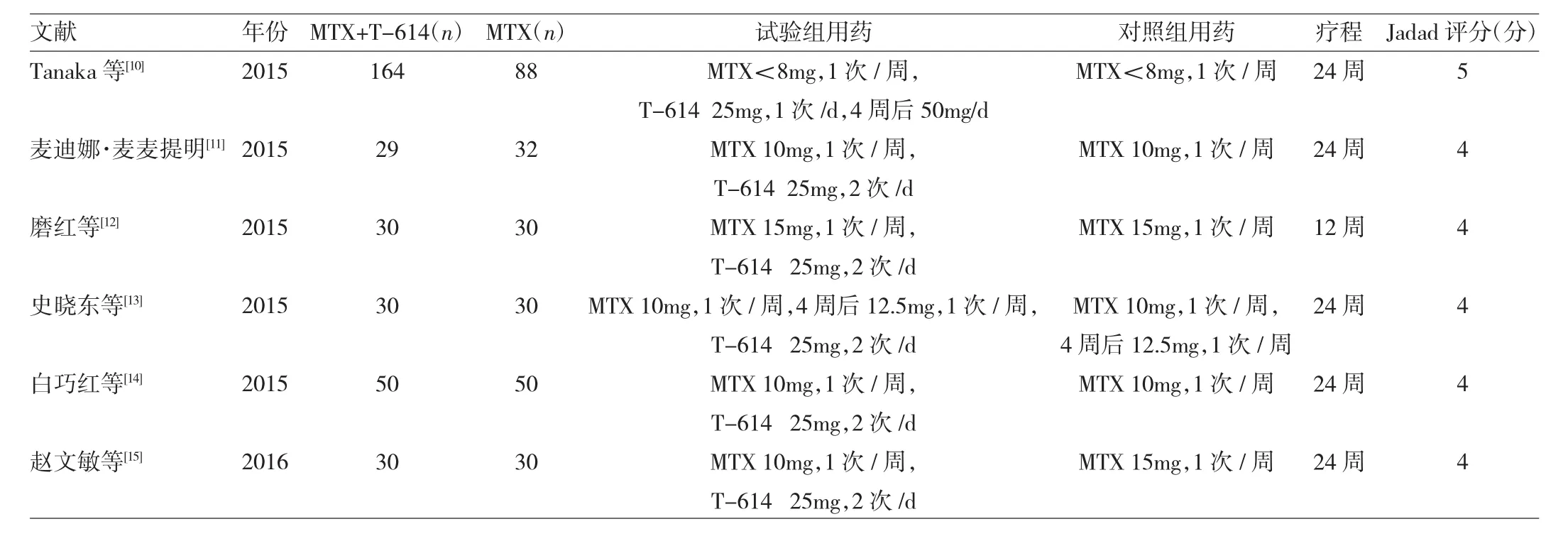
表1 ACR20、ACR50、ACR70纳入文献一般情况
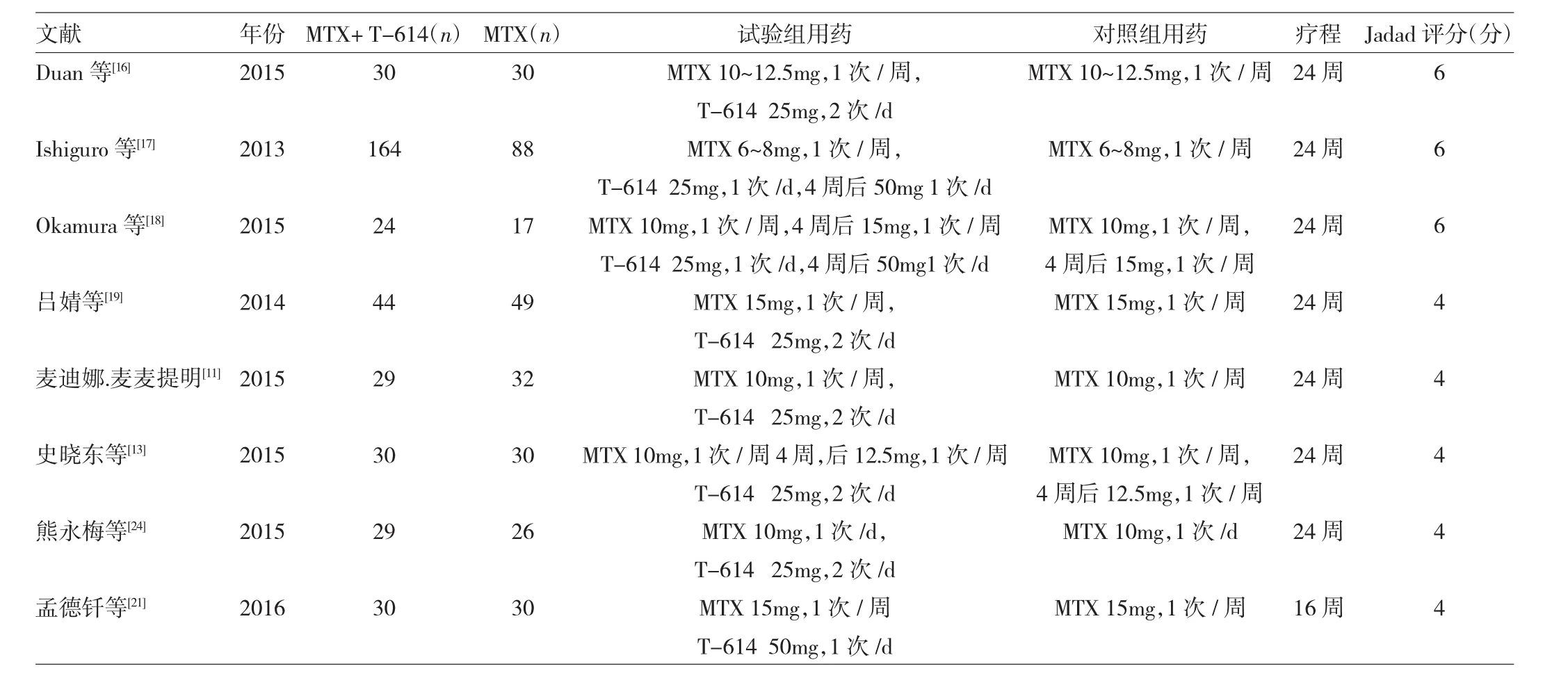
表2 DAS28纳入文献一般情况
3 讨论
RA目前发病原因不明,可能与感染、遗传、雌激素水平等有关,本病是以滑膜慢性炎症、血管新生、软骨和骨破坏为主的免疫疾病[25],常导致关节破坏和畸形,对患者和社会造成了严重的影响。在长期单药治疗效果不佳的情况下,DMARDS联合治疗越来越多地应用于早期RA患者的治疗,DMARDS可显著改善其预后,所以及时对患者的疾病活动度和治疗效果作出评估,早期正确用药非常重要。目前已有学者作过MTX联合T-614治疗RA的临床研究,但未有相关的系统评价。本研究Meta分析发现,MTX联合 T-614治疗 RA患者后ACR20、ACR50、ACR70的缓解率均较对照组高,差异均有统计学意义(均P<0.05),森林图显示麦迪娜·麦麦提明等[11]、史晓东等[13]研究95%CI的线条横跨无效竖线,即该研究无统计学意义。DAS28-CRP合并到DAS28中比较,Meta分析显示DAS28的异质性较大,I2=69%,结论为MTX联合T-614组治疗疾病活动度评分低于单用MTX组结果可信。孟德钎等[20]、李娟等[23]研究放在Meta分析中无统计学意义。由于T-614上市并用于临床时间短,MTX与其联合治疗RA的研究较少,安全性方面MTX联合T-614组与MTX组比较无统计学意义。在MTX联合T-614治疗RA的研究中,Okamura等[26]发现其不良反应主要是间质性肺炎、肝功能紊乱(ALP升高);Ishiguro等[17]发现其不良反应是肝酶升高(ALS升高)、口腔炎、咽炎、淋巴细胞数降低、白细胞总数降低、红细胞数降低。可见药物联合治疗疾病的不良反应依然存在,提高疗效与安全性需要更多的临床试验研究,需要扩大样本量和延长观察时间,以进一步评估其临床疗效和安全性。
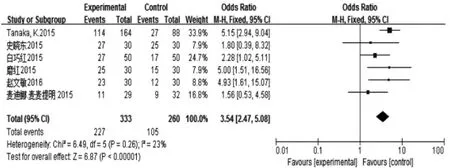
图1a 试验组与对照组ACR20比较森林图
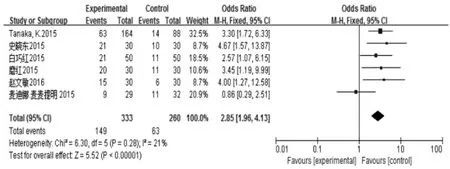
图1b 试验组与对照组ACR50比较森林图
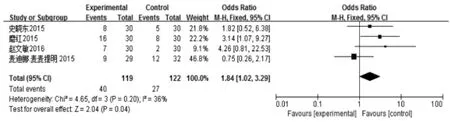
图1c 试验组与对照组ACR70比较森林图
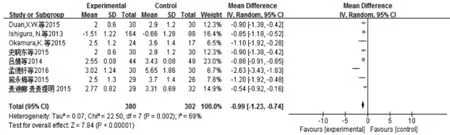
图2 试验组与对照组DAS28比较森林图
本研究中有纳入文献森林图显示横线过长,说明结果欠精确,无统计学意义。疾病活动度评分存在有意义的异质性,考虑为纳入的研究样本量少,各个研究中的MTX联合T-614组与MTX组的用药量、用药经验、观察时间、疗程、研究质量、患者所在地区等不完全一致,未来需要更多的多中心、大样本、随机、对照试验为临床提供高质量证据。
