脾切除对原发性胆汁性肝硬化小鼠肝组织纤维化影响研究*
2018-11-09郭晓霞郭琲婷孔祥璐
郭晓霞,郭琲婷,孔祥璐
原发性胆汁性肝硬化(primary biliary cirrhosis,PBC)是一种病因未明的进行性非化脓性胆管炎性疾病,女性发病率较高,以肝内胆汁淤积为特征,常并发其他自身免疫性疾病,肝组织病理学表现为肝内胆管进行性破坏,伴汇管区炎症和纤维化,发生门脉高压症,最终导致肝硬化[1]。门静脉压力越高,患者肝脏病变程度、肝功能减退程度和出现临床并发症的风险越大[2]。脾功能亢进症是继发于肝硬化门静脉高压症的一种常见临床表现,此类患者易发生胃食管静脉曲张破裂出血而危及生命。因此,PBC患者伴脾功能亢进症的临床治疗不容忽视[3]。脾切除术对门静脉高压的疗效日益受到广大学者的关注,有学者指出,在门静脉高压症早期脾脏具有抗肝纤维化功能,而到进展期则无此作用。因此,在门脉高压早期应当保留脾脏,而在进展期则应切除脾脏[4]。本研究以聚肌胞苷酸腹腔注射制备PBC小鼠模型,探讨了脾切除术对PBC小鼠肝组织纤维化程度的影响。
1 材料与方法
1.1 动物、试剂与仪器雌性 C57BL/6小鼠40只,5~6周龄,SPF级,体质量为18±2 g,购自北京华阜康生物科技股份有限公司【许可证号:SCXK(京)2014-0004】。饲养于山西省中医药研究院中心实验室,室温控制在22~25℃,保持湿度为40%~60%,12 h昼夜交替光照,给以充足的标准实验饲料(北京科澳协力饲料有限公司,产品批号:15043311)和水饲养。依据山西省中医院中心实验室操作指南,所有受试动物均受到良好的待遇,本研究经山西省中医院动物伦理委员会审核通过。聚肌胞苷酸(太原博科生物有限公司,批号CAS24939-03-5),检测小鼠肠组织 TNF-α 的ELISA试剂盒(上海酶联生物科技有限公司),兔抗TGF-β1多克隆抗体、RNA提取试剂盒(EasyPure RNA Kit,北京全式金生物技术有限公司,批号J20519),cDNA 逆 转 录 试 剂 盒(TransScript First-Strand cDNA Synthesis SuperMi,北京全式金生物技术有限公司,批号J31212),荧光定量PCR试剂盒(QuantiFast SYBR Green PCR Kit,德国QIAGEN公司,批号151039406)。AU5821全自动生化分析仪(日本Olympus公司),Image-Pro Plus 6.0多功能图象分析管理系统(美国Media Cybernetics公司),CX41正置显微镜(OLYMPUS公司),Auegrax-30k低温台式离心机(美国Beckman Coulter公司),Addcare ELISA 600酶联免疫吸附检测分析工作站(烟台艾德康生物科技有限公司),Finesse325石蜡切片机(美国ThermoScientific公司),9902 Veriti定性PCR分析仪(美国 Applied Biosystems公司),T25 ULTRA-TURRAX组织匀浆机(德国IKA公司)。
1.2 PBC小鼠模型的制备 将40只雌性C57BL/6小鼠随机分为正常对照组、模型组、脾切除组和假手术组,每组10只。参照文献[5]给予模型组、脾切除组和假手术组动物1%聚肌胞苷酸(poly I:C)5 mg·kg-1腹腔注射,2次 /w,建立 PBC 模型,给予正常对照组等体积生理盐水腹腔注射。在第20 w时,各组随机抽样行组织病理学检查证实PBC形成。在制备PBC模型成功后,参照文献方法[6]行脾切除术,给予脾切除组小鼠3.5%水合氯醛(0.01 ml·g-1)腹腔注射,腹部剃毛、消毒。沿腹中线自剑突下1 cm处行横行切口,进入腹腔,游离脾脏,结扎脾动脉和脾静脉,切除脾脏;假手术组小鼠行腹壁切开后,轻微翻动脾脏,不切除;正常对照组小鼠不行任何处理。继续普通饲养喂养各组动物至32 w。
1.3 标本采集与处理 在20 w和32 w,各组随机抽取5只小鼠送检,禁食24 h,眼眶取血。称体质量,处死动物,采集小鼠全部肝脏、末端回肠,用生理盐水冲洗。将肝脏用滤纸吸干水分,称量肝脏湿质量,计算各组小鼠肝脏指数[肝脏质量(mg)/体质量(g)]。将部分肝组织置入4%多聚甲醛溶液中固定,常规制片,HE和Masson染色,光镜下观察肝组织病理形态学变化。将剩余肝组织和末端回肠组织迅速置于-80℃冰箱中保存,以备组织蛋白和mRNA提取。
1.4 血生化指标检测 将全血3000 r/m离心10 min,取上层血清,送至山西省中医院检验科检测。
1.5 肝组织 TGF-β1 mRNA水平检测 采用RT-PCR 法,提取组织总 RNA,取 RNA 5 μg,行逆转录反应,合成cDNA,总反应体系为20μl。采用SYBR Green染料PCR法,反应体系为25 μl。应用 Primer Premier 5引物设计软件设计筛选各基因特异性引物。所有引物均交由上海生工生物工程技术服务有限公司设计、合成。TGF-β1引物:上游5'-TGCTAATGG TGGACCGCAA-3', 下 游 5'-CACTCTTCCCGAATGTCTGA-3',扩增产物 100 bp;β-actin引物:上游5'-AGGCCAACCGTGAAAA-GATG-3',下游 5'-ACCAGAGGCATACAGGGACAA-3',扩增产物101 bp;TβRI引物:上游5'-ATGGTTCCGAG AGGCAGAGAT-3', 下 游 5'-CCATGTCCCATTGTCTTTGTTG-3', 扩 增 产 物 97 bp;TβRII引物:上游5'-CCAGAAGTCCTGCATGAGCAA-3',下游 5'-TGGCAAACCGTCTCCAGAGT A-3',扩增产物117 bp。扩增条件:95℃预变性5 min,95℃变性 10 s,60℃退火延伸 30 s,扩增设定为40个循环。在反应结束后,由电脑自动分析各样本的Ct值,通过2-△△Ct计算mRNA相对水平,并由熔解曲线判断PCR反应的特异性。
1.6 末端回肠TNF-α水平检测 自-80℃冰箱取出回肠组织,恢复至室温,称量后用0.9%生理盐水20倍稀释,匀浆,所得混悬液经5000 r/m离心15 min,取上清液,采用ELISA法检测,在酶标仪450 mn波长下测定吸光度(OD值),用标准品绘制标准曲线,获得样品TNF-α水平。
1.7 统计学方法 应用SPSS 21.0统计软件进行统计学处理,计量资料以±s表示,组间比较采用单因素方差分析,组间两两比较采用LSD-t或SNK检验,等级资料采用秩和检验,P<0.05为差异有统计学意义。
2 结果
2.1 各组小鼠肝脏指数和肝功能指标变化比较 术前,各组小鼠肝脏指数之间差异无显著统计学意义(P>0.05),模型组、脾切除组和假手术组血清ALT和AST水平均显著高于对照组(P<0.05);术后,模型组、脾切除组和假手术组肝脏指数均较正常对照组显著下降,差异具有统计学意义(P<0.05),脾切除术组肝功能指标有所改善,显著低于模型组(P<0.05,表1)。
表1 各组小鼠脏器指数和肝功能指标(±s)比较

表1 各组小鼠脏器指数和肝功能指标(±s)比较
与对照组比,①P<0.05;与模型组比,②P<0.05
例数 肝脏指数 ALT(U/L) AST(U/L) ALP(U/L)术前 对照组 5 34.6±4.6 33.5±5.6 146.3±31.1 131.0±26.8模型组 5 37.5±1.6 49.1±10.7① 167.5±25.0① 148.6±20.2①脾切除 5 37.2±5.0 47.3±17.1① 169.8±29.5① 146.4±29.8①假手术 5 37.4±53.9 48.6±12.5① 165.3±21.9① 150.1±23.6①术后 对照组 5 53.2±2.1 40.0±0.3 154.0±4.1 175.8±9.0模型组 5 39.1±1.0① 52.0±9.0 183.4±12.4 195.3±62.6脾切除 5 41.5±5.2① 43.5±6.4② 157.7±20.9② 178.1±38.0②假手术 5 39.6±7.5① 53.4±11.2 186.5±15.8 198.9±41.5
2.2 各组小鼠肝组织病理学变化 术前,正常对照组小鼠肝小叶结构清晰,无炎性细胞浸润和胶原纤维沉积。模型组、脾切除组和假手术组小鼠肝组织内均可见肝小叶结构紊乱,汇管区周围淋巴细胞浸润明显,有少量细小的胆管增生、畸形,汇管区周围可见蓝色胶原纤维环绕形成的纤维间隔(图1、图2);术后,正常对照组肝小叶结构清晰,无明显炎性细胞浸润和胶原纤维沉积。模型组和假手术组肝小叶结构紊乱,汇管区及损伤的胆管周围淋巴细胞浸润,类上皮样肉芽肿围绕损伤胆管,界板出现碎屑样坏死,汇管区周围有大量的蓝色胶原纤维环绕,形成明显的纤维间隔。脾切除组小鼠肝组织汇管区周围部分胆小管畸形、扩张,有少量的蓝色胶原纤维沉积(图3、图 4)。
2.3 各组肝组织TGF-β1、TβRI和TβRII mRNA水平比较 术前,模型组、脾切除组和假手术组小鼠肝组织 TGF-β1、TβRI、TβRII mRNA 水平明显升高,与对照组比较差异具有统计学意义(P<0.05)。脾切除组、假手术组与模型组之间差异无明显统计学意义(P>0.05);术后,脾切除组小鼠肝组织TGF-β1、TβRI、TβRII mRNA 水平明显降低,与模型组比,差异有统计学意义(P<0.05,表2)。

图1 各组小鼠肝组织病理学表现 术前(HE,100×)
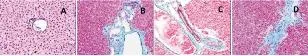
图2 各组小鼠肝组织病理学表现 术前(Masson,100×)

图3 各组小鼠肝组织病理学表现 术后(HE,100×)
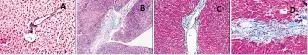
图4 各组小鼠肝组织病理学表现 术后(Masson,100×)
表2 各组小鼠肝组织TGF-β1 、TβRI和TβRII m RNA水平(±s)比较
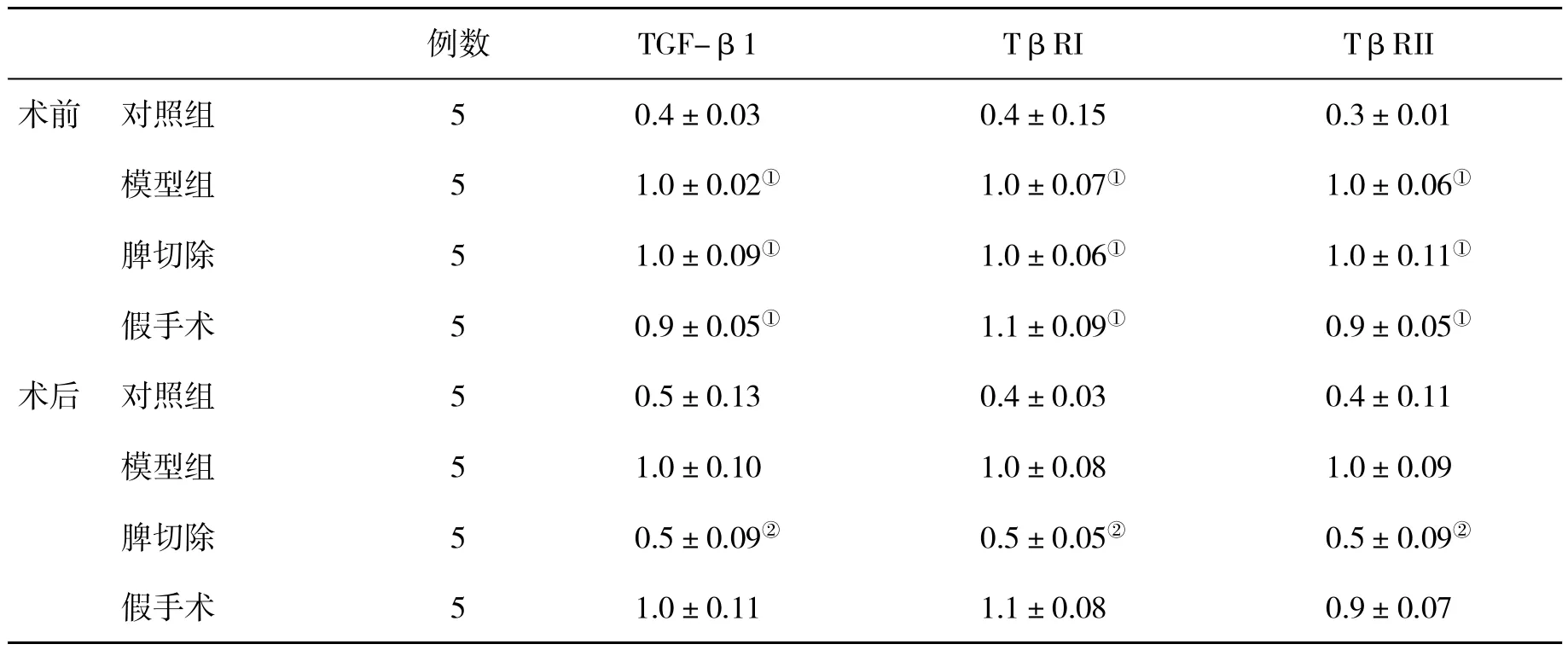
表2 各组小鼠肝组织TGF-β1 、TβRI和TβRII m RNA水平(±s)比较
与对照组比,①P<0.05;与模型组比,②P<0.05
例数 TGF-β1 TβRI TβRII术前 对照组 5 0.4±0.03 0.4±0.15 0.3±0.01模型组 5 1.0±0.02① 1.0±0.07① 1.0±0.06①脾切除 5 1.0±0.09① 1.0±0.06① 1.0±0.11①假手术 5 0.9±0.05① 1.1±0.09① 0.9±0.05①术后 对照组 5 0.5±0.13 0.4±0.03 0.4±0.11模型组 5 1.0±0.10 1.0±0.08 1.0±0.09脾切除 5 0.5±0.09② 0.5±0.05② 0.5±0.09②假手术 5 1.0±0.11 1.1±0.08 0.9±0.07
2.4 PBC小鼠末端回肠TNF-α水平变化 术前,模型组、脾切除组和假手术组小鼠末端回肠TNF-α水平均明显高于正常对照组,差异具有统计学意义(P<0.05);术后,脾切除组小鼠回肠TNF-α水平明显降低,与模型组比差异有统计学意义(P<0.05,表3)。
表3 各组小鼠末端回肠TNF-α水平(±s)比较
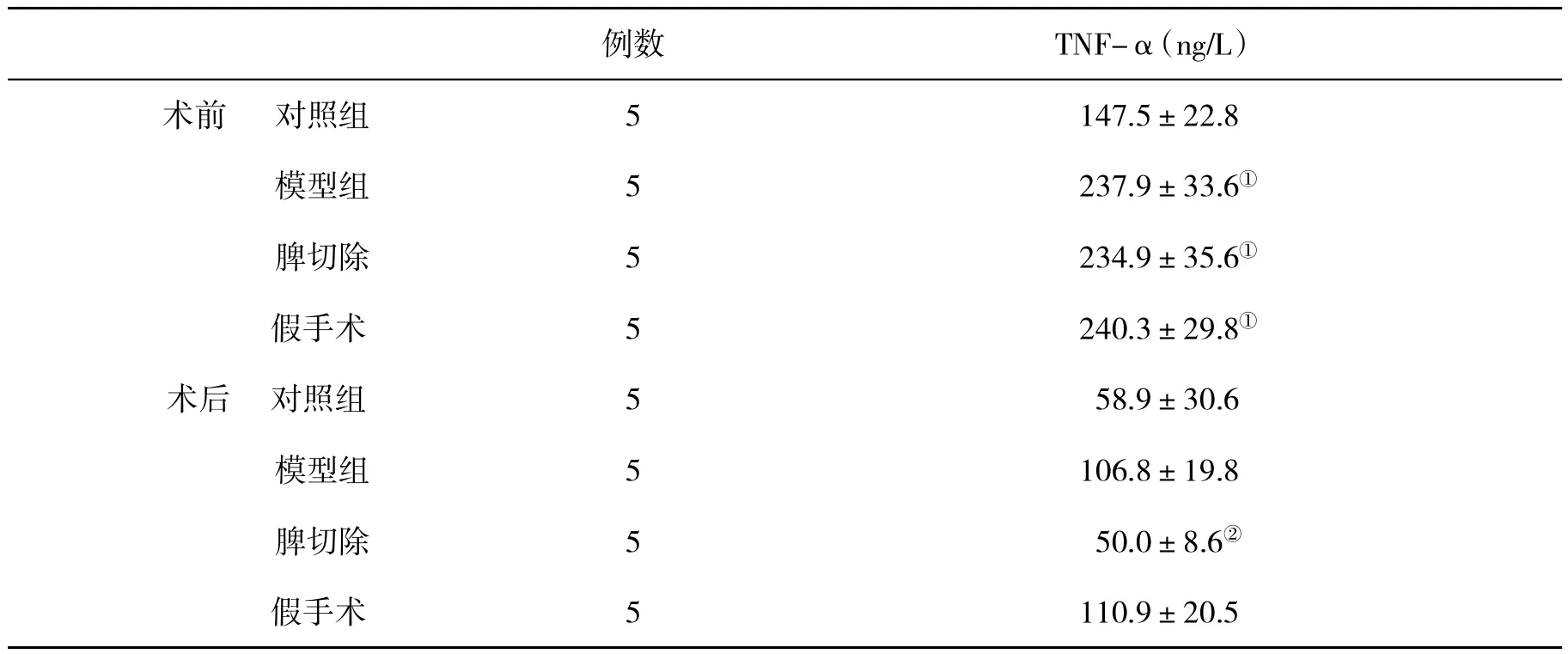
表3 各组小鼠末端回肠TNF-α水平(±s)比较
与正常组比,①P<0.05;与模型组比,②P<0.05
例数 TNF-α(ng/L)术前 对照组 5 147.5±22.8模型组 5 237.9±33.6①脾切除 5 234.9±35.6①假手术 5 240.3±29.8①术后 对照组 5 58.9±30.6模型组 5 106.8±19.8脾切除 5 50.0±8.6②假手术 5 110.9±20.5
3 讨论
PBC是以胆管上皮细胞损伤为特点的自身免疫性肝病,可发生于所有的种族和民族。文献报道,本病年发病率为0.33/10万~5.8/10万,患病率为1.91/10万~40.2/10万,其中北美和北欧国家发病率较高[7]。近年来,我国文献报道的PBC病例数呈快速上升趋势[8]。PBC后期可发生肝硬化和门静脉高压的一系列并发症,甚至在疾病早期就可出现门静脉高压症[9]。新发门脉高压是预后不良的征象,发生静脉曲张后的1 a和3 a生存率分别为83%和59%[10]。门静脉高压症的临床表现为脾肿大、脾功能亢进症和腹水等。治疗门静脉高压症的外科方法有脾切除、断流术、分流术和肝移植手术等[11]。有学者指出,脾切除术可快速有效地缓解脾功能亢进症,减缓肝硬化进程,降低肝癌发生率[12]。
本实验结果显示脾切除组、假手术组和模型组肝脏指数明显增加,肝功能异常,肝组织病理学损伤明显,提示肝硬化模型制备成功。在此基础上行脾切除术,术后脾切除组肝脏体积明显大于假手术组和模型组,肝功能及肝组织病理学损伤均较模型组有明显的改善,与文献报道结果一致[13],提示肿大的脾脏对患者肝功能有损害作用,脾切除术可促进肝再生,改善肝功能,延缓肝纤维化发生。
TGF-β/Smads信号通路被认为在PBC发病过程中起关键作用[14]。研究表明肝硬化时脾脏合成TGF-β1和TNF-α增加,可能是引起肝脏纤维组织过度增生的关键所在[15]。TNFα和TGF-β等能触发或参与了肝脏炎症反应[16]。有学者发现脾切除可降低血清 TGF-β1水平而改善肝功能,延缓肝纤维化发展[17]。本研究结果发现术前脾切除组和模型组肝组织 TGF-β1、TβRI、TβRII mRNA水平明显高于正常对照组,术后脾切除组肝组织TGF-β1、TβRI、TβRII mRNA 水平有所下降,提示脾切除可下调TGF-β1表达,从而抑制PBC进展。
临床上,高达80%肝硬化患者存在不同程度的胃肠道症状,门静脉高压性肠病发病率约为25%~70%[18],肠道分泌TNF-α和IL-6等增加,进一步破坏肠道免疫功能,是影响患者生活质量和预后的重要原因[19,20]。本研究发现术前脾切除组和模型组小鼠末端回肠TNF-α水平均明显高于正常对照组,提示TNF-α在肝脏疾病的进展中发挥了重要作用。脾切除术后回肠TNF-α有所下降,或许能减轻肠道免疫损伤。
