替诺福韦治疗慢性乙型肝炎患者疗效及安全性分析*
2018-11-09王耀峰
王耀峰
目前,作为一线抗病毒药物的替诺福韦(TDF)和恩替卡韦(ETV),一直是WHO、美国肝病协会(American Association for the Study of Liver Disease,AASLD)和我国防治指南认可和推荐的药物[1-5]。本研究应用TDF和ETV治疗慢性乙型肝炎(CHB)患者,观察了临床疗效和安全性,以为临床治疗CHB患者提供科学依据。
1 资料与方法
1.1 一般资料 2015年1月~2016年12月我中心诊治的CHB患者60例,40例,女20例;年龄30~55岁,平均年龄为(35.0±7.41)岁。体质指数为(18.7±2.5)kg/m2。符合《慢性乙型肝炎防治指南》(2015年版)的诊断标准,纳入患者均为未接受过核苷(酸)类或α-干扰素抗病毒治疗者,血清HBeAg阳性,HBV DNA>1×105copies/mL,血清丙氨酸氨基转移酶(ALT)水平升高超过正常值上限2倍。排除标准:①合并HCV和HIV感染者;②患有酒精性肝病、自身免疫性肝病、药物性肝损伤患者;③妊娠或哺乳期妇女。采用随机数字表法将患者分成两组,两组在年龄、性别、体质指数和肝功能损害程度等一般资料方面比较,差异均无统计学意义(P>0.05),具有可比性。本研究经过本院医学伦理委员会批准,患者签署知情同意书。
1.2 治疗方法 30例患者接受替诺福韦酯片【韦瑞德,葛兰素史克(天津)有限公司,国药准字H20153090】300 mg口服,1次 /d;给予另 30例患者恩替卡韦片(博路定,中美上海施贵宝制药有限公司,国药准字H20080798)0.5 mg口服,1次/d。两组均观察96 w。
1.3 检测方法 使用罗氏P800全自动生化分析仪检测肝肾功能指标;采用CHEMCLIN1500化学发光法检测HBV血清标志物(北京科美生物技术公司);采用CFX Connet实时荧光定量PCR法检测血清HBV DNA(美国伯乐公司仪器和湖南圣湘生物技术公司试剂)。
1.4 统计学方法 应用SPSS 22.0软件处理数据,计量资料以(±s)表示,采用独立样本t检验;计数资料的比较采用x2检验,P<0.05为差异具有统计学意义。
2 结果
2.1 两组血清HBV DNA和ALT水平比较 观察96 w,两组血清HBV DNA水平均迅速降低,血清ALT水平恢复正常,但在早期,TDF治疗组疗效优于 ETV 组(P<0.05,表 1、表 2)。
2.2 两组病毒学应答率比较 在前12 w,TDF组病毒学应答率显著高于ETV组,差异具有统计学意义(P<0.05);随着连续服药抗病毒治疗,两组病毒学应答率无显著性差异(P>0.05,表 3)。
2.3 两组血清ALT复常率比较 各观察时段,两组血清ALT复常率无显著性相差(P>0.05,表4)。
2.4 两组血清HBeAg转阴率比较 在观察期内,两组血清HBeAg阴转者都很少(表5)。
表1 两组血清 HBV DNA 水平(lg IU/m L,±s)比较
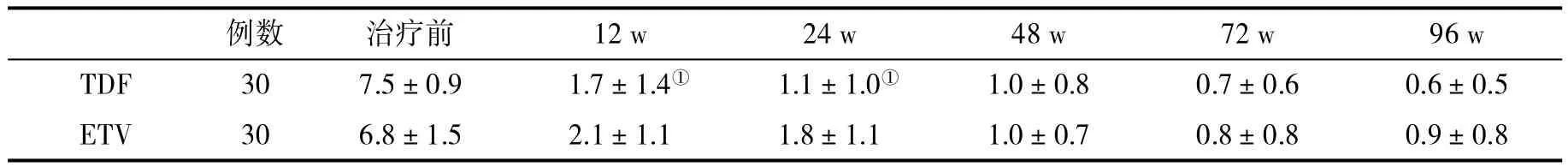
表1 两组血清 HBV DNA 水平(lg IU/m L,±s)比较
与ETV组比,①P<0.05
例数 治疗前 12 w 24 w 48 w 72 w 96 w TDF 30 7.5±0.9 1.7±1.4① 1.1±1.0① 1.0±0.8 0.7±0.6 0.6±0.5 ETV 30 6.8±1.5 2.1±1.1 1.8±1.1 1.0±0.7 0.8±0.8 0.9±0.8
表2 两组血清 ALT水平(U/L,±s)比较
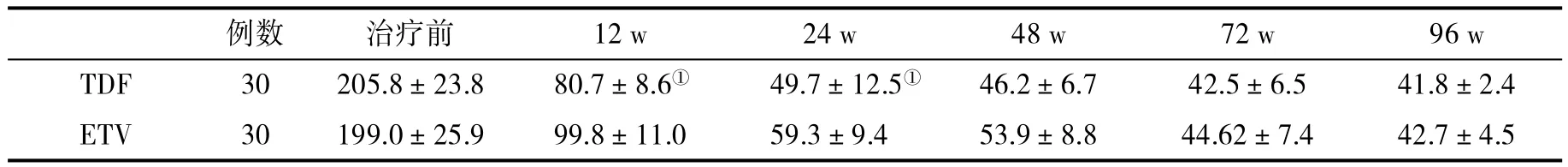
表2 两组血清 ALT水平(U/L,±s)比较
与ETV组比,①P<0.05
例数 治疗前 12 w 24 w 48 w 72 w 96 w TDF 30 205.8±23.8 80.7±8.6① 49.7±12.5① 46.2±6.7 42.5±6.5 41.8±2.4 ETV 30 199.0±25.9 99.8±11.0 59.3±9.4 53.9±8.8 44.62±7.4 42.7±4.5
2.5 两组治疗完成和不良反应发生情况比较 在治疗过程中,两组均无中断治疗的患者;TDF治疗组出现四肢无力2例,头晕1例,ETV治疗组出现皮疹3例,肝区不适2例。

表3 两组病毒学应答率(%)比较
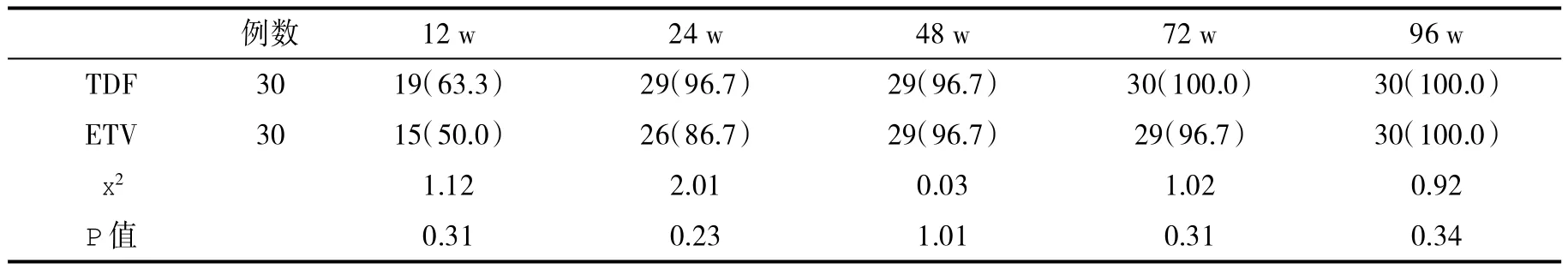
表4 两组血清ALT复常率(%)比较
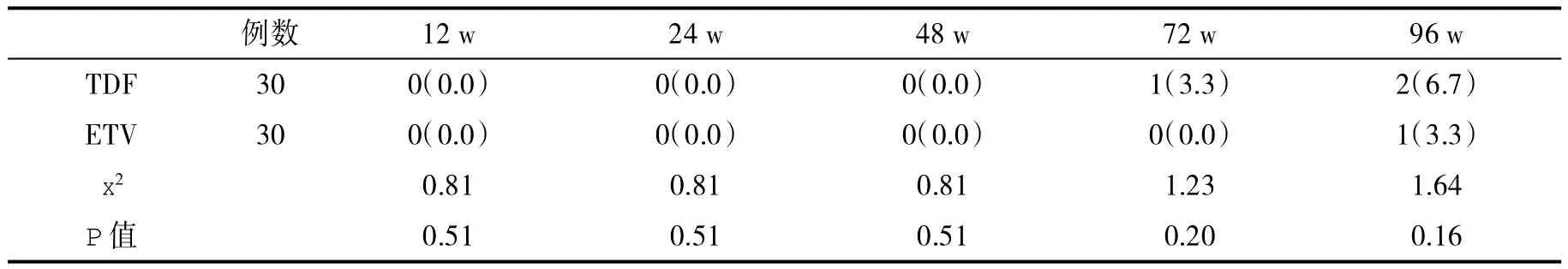
表5 两组血清HBeAg转阴率(%)比较
3 讨论
HBV感染者在任何时期其血液都具有传染性,而传播HBV的主要途径是经血传播。除此之外,也可以是母婴传播[6,7],携带HBV的母亲在分娩前后通过血液或密切接触传染给婴儿,而一旦健康的胎儿和新生儿感染了乙型肝炎病毒,有90%以上的概率将成为慢性病毒携带者;密切接触也是最常见的传播HBV感染的常见方式,比如性接触传播[9]。还有一种传播途径就是医源性传播,如使用了受污染或者不严格消毒的采皿器、针头和针管等,但这种情况已非常少见。
在免疫功能低下的患者,如白血病、肿瘤,艾滋病、血液透析或肾移植受者,感染HBV后容易发展为慢性乙型肝炎。在有慢性肝病、疟疾、结核病、血吸虫病史的患者,感染HBV后不仅易发展为CHB,而且预后更差。
荟萃分析表明,应用普通干扰素治疗慢性乙型肝炎患者,血清HBeAg转换率、HBsAg清除率、肝硬化发生率和HCC发生率均优于未经干扰素治疗者。国际多中心随机临床对照试验显示,血清HBeAg阳性的CHB患者在接受聚乙二醇化干扰素α-2a治疗48周,停药随访24周时,血清HBeAg转换率为32%[10,11]。国外研究显示,对于 HBeAg阳性的 CHB 患者,应用聚乙二醇化干扰素α-2b也可取得类似的病毒学应答率,有一些患者能获得血清HBeAg转换和HBsAg消失[12,13]。但应用核苷类药物,往往只能获得病毒学应答,而少有血清学应答者[14]。
拉米夫定和阿德福韦酯是早期被应用于治疗CHB患者的口服抗病毒药物[15,16]。研究发现,长期应用会导致耐药的发生。随机双盲对照临床试验表明,对于HBeAg阳性的CHB患者,恩替卡韦治疗48周时血清HBV DNA下降者为67%,血清ALT复常者为68%,有肝组织学改善者为72%,均优于接受拉米夫定治疗者,但血清HBeAg转换率也只有21%[17]。长期随访研究表明,对于获得病毒学应答的CHB患者,继续治疗可保持较高的血清的持HBV DNA抑制效果。一项研究显示应用恩替卡韦3年累积耐药率为1.7%~3.3%。全球多中心临床试验表明,对于血清HBeAg阳性患者,应用TDF治疗52周时,血清HBV DNA下降至PCR法检测水平以下者为60.0%,血清ALT复常率为77.2%、耐药发生率为5.0%、肝组织学应答率为64.7%,均优于拉米夫定治疗组[18]。
近几年来,国内外应用抗病毒药物的临床试验研究比较多[19,20],显示经过核苷(酸)类似物的治疗,CHB患者病情得到有效的控制,能够最大程度地抑制HBV DNA复制,改善肝功能,抑制肝纤维化,控制肝硬化病情,治疗效果显著,无明显的不良反应,安全性高。
TDF是一种新型核苷酸类逆转录酶抑制剂,适用于治疗CHB患者,能够有效对抗多种病毒。与食物同时服用,其生物利用度高达40%。TDF能够通过其活性成分替诺福韦双磷酸盐与天然脱氧核糖底物相竞争,抑制HBV逆转录酶活性,从而达到终止病毒DNA复制,减轻肝损害,降低各指标的目的。ETV也是一种核苷酸类似物,能够对HBV DNA多聚酶有抑制作用,经过磷酸化进一步转变成具有活性的三磷酸盐,胞内半衰期为15 h。同样,通过与天然脱氧核糖底物竞争,其三磷酸盐能抑制病毒逆转录酶的合成和复制。TDF适用于病毒DNA复制活跃、血清ALT水平持续升高、肝组织学显示活动性病变的CHB患者的治疗。
本研究显示,在治疗观察的96周里,两组患者血清HBV DNA和ALT水平均显著下降,但在治疗的早期,TDF组下降幅度要明显大于ETV组,显示出其能更快速地发挥作用。两组HBV DNA转阴率也不断升高,但两组血清HBeAg转阴病例均很少。观察表明,两组不良反应发生率均很低,且一些患者在应用药物过程中的不适,很难确定与服药有关。
综上所述,应用TDF或ETV两种药物对初治的CHB患者均能获得有效快速的抑制HBV DNA复制,恢复血清ALT水平,取得良好的病毒学应答和生化学应答的治疗目的,不良事件发生率很低。相比之下,TDF具有较强的抗病毒和早期快速发挥效力的能力,抗病毒效果和安全性或许更优,但长期应用的效果如何,以及应用核苷(酸)类抗病毒治疗很难获得血清学应答的问题,仍需要进一步研究解决。
