注射人脐带间充质干细胞到耻尾肌及膀胱颈对压力性尿失禁的疗效比较
2018-10-31孙晓莹
孙晓莹,孟 斐
(沈阳医学院附属中心医院 产科,辽宁 沈阳 110024)
人类进化历经从爬行到直立,由于重力的作用,位于骨盆最低点的盆底组织成为支撑盆腔脏器的重要结构。研究表明,妊娠、绝经及产伤会造成盆底肌肉、筋膜、神经的过度牵拉受损,导致盆底结构及功能异常,最终出现各种盆底功能障碍性疾病,其中以压力性尿失禁(SUI)最常见。目前主流观点认为尿道括约肌功能缺陷是造成SUI的原因之一,因此恢复括约肌的正常结构和功能成为治疗的关键[1]。目前用于纠正泌尿功能障碍或修补和重建缺陷膀胱的外科和内科治疗方法是不理想的,并与明显的并发症有关[2],因此探索一种简单有效的治疗方法势在必行。10年来,干细胞以其强大的再生修复优势出现,如果干细胞移植能修复受损的尿道括约肌,那么SUI女性的漏尿现象将明显改善。本研究将人脐带间充质干细胞(hUCMSC)注射到SUI大鼠的膀胱颈(尿道内括约肌)和耻尾肌(尿道外括约肌),通过尿动力学检测结果来探讨干细胞移植的最佳位点,现报告如下。
1 材料和方法
1.1 材 料
1.1.1 实验动物:清洁级成年雌性SD大鼠44只,体重190~220 g;雄性SD大鼠11只,体重220~250 g;由北京华阜康生物科技有限公司提供(实验动物质量合格证号:SCXK(京)2009-0004)。
1.1.2 主要试剂盒及仪器:BL-420S生物机能实验系统(成都泰盟科技有限公司);微量输液泵(史密斯医疗器械(北京)有限公司);血球计数板(上海市求精生化试剂仪器有限公司);低温离心机(eppendorf, centrifuge 5810 R);倒置相差显微镜(OLYMPUS,日本);CO2孵箱(Thermo scientific,美国);Hyclone DMEM高糖培养、Hyclone 南美胎牛血清及胰蛋白酶(赛默飞世尔生物化学制品有限公司)。
1.2 方 法
1.2.1 hUCMSC的采集、鉴定培养:提取胎儿侧脐带5 cm,冲洗干净后剪碎,组织块培养法分离培养贴壁细胞。第3代细胞留置待用。以表面抗原检测CD34、CD45、CD44、CD105鉴定为间充质干细胞。另将部分干细胞继续培养传代,观察到其扩增能力未受到影响。
1.2.2 动物分组及SUI模型的建立:大鼠4∶1雌雄比例合笼,4周后获得孕鼠42只,正常产后8只作为正常对照组,34只构建SUI模型。造模方法:产后即时腹腔注射20%氯胺酮(10 mL/kg)麻醉,切除双侧卵巢后F12导尿管插入阴道,固定,使气囊膨胀后挤压阴道中下段而不脱出。气囊注入4 mL水,放平导尿管,远端连接150 g砝码牵引4 h后拆除。造模大鼠1只死于麻醉,1只死于感染,最终造模32只。造模成功判定:产后4周,与正常对照组相比,造模大鼠漏尿点压力(LPP)均低,指压实验阳性率均高,差异有统计学意义(P<0.05),说明SUI模型构建成功。
1.2.3 尿动力学评估及指压实验:产后4周(注射前)所有大鼠进行检测。20%氯胺酮(10 mL/kg)肌注麻醉大鼠,仰卧位固定。下腹纵切口找到膀胱,膀胱顶小切口插入硬膜外导管,深1.5~2 cm,缝合固定,关腹。将硬膜外导管与BL-420生理记录仪及微量输液泵连接,排空气体,调节微泵0.3 mL/min,向膀胱内泵入无菌美兰PBS液,大鼠首次自动排尿时调停微泵,排尿结束后尿动力学检测仪校“0”。同时开启微泵和生理记录仪,开始检测。尿道口出现第1滴尿液时,在生理记录仪上做以标记,计算当时微泵泵入的液体量并记录当时的膀胱内压力作为最大膀胱容积(MCC)及漏尿点压力(LPP)。重复上述操作,每只大鼠检测2次,取平均值。指压实验:待大鼠自动排空膀胱,注入1/2最大膀胱容积的PBS液,避开膀胱区,以两指缓慢挤压大鼠腹部,观察辨别尿道口有无蓝色液体漏出(少量为漏尿,大量为排尿),记录各组漏尿阳性大鼠数量。产后8周(注射后1个月)再次重复上述操作。
1.2.4 细胞移植:hUCMSC浓度1.0×106个/10 μL,每只用量30 μL,细胞数3.0×106个。移植方法:造模大鼠随机均分为治疗A组(n=8):消毒外阴,将经膀胱底置入的硬膜外导管继续向下,经过膀胱颈及尿道出尿道外口,上提硬膜外导管尿道外口侧,作为移植注射时尿道解剖位置的确切标记。以距尿道外口1.5 cm、尿道旁1 mm,60 °角进针,深度2 mm,将hUCMSCs注射到中段尿道两侧的耻尾肌内后抽出硬膜外导管,缝合膀胱切口并关腹;治疗B组(n=8):少许游离膀胱颈部,将hUCMSC分次注射到膀胱颈3点、9点、12点的平滑肌内,关腹。对照A组(n=8)、对照B组(n=8):同法分别注入等量生理盐水于耻尾肌、膀胱颈。
1.3 统计学方法

2 结 果
与正常对照组相比,造模大鼠LPP均低,指压实验阳性率均高,差异有统计学意义(P<0.05)。移植前后治疗A组与对照A组比较,MCC差异无统计学意义(P>0.05);治疗A组LPP变化不大,对照A组LPP下降,差异有显著统计学意义(P<0.01)。与对照B组比较:治疗B组MCC增加较多,差异有统计学意义(P<0.05);LPP升高更明显,差异有显著统计学意义(P<0.01)。见表1、2。
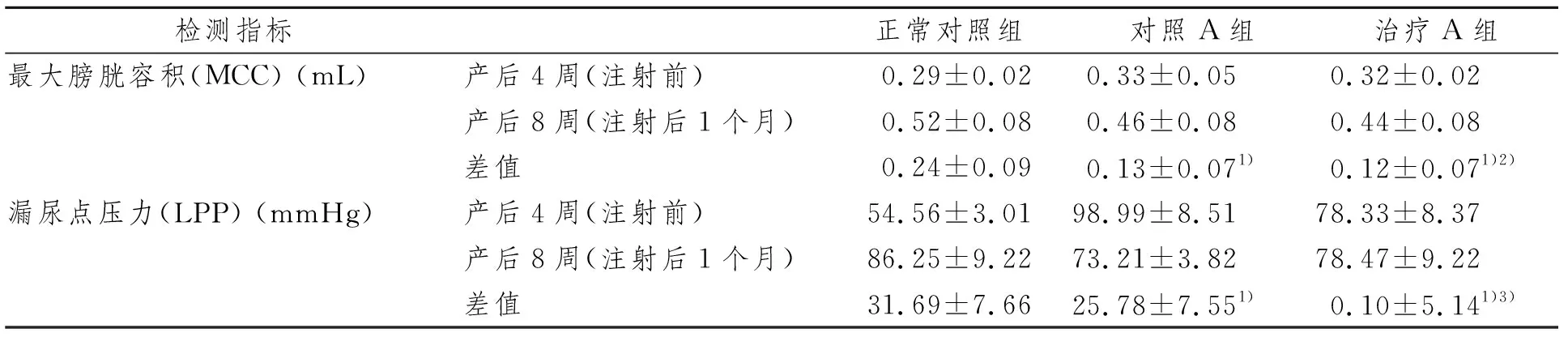
表1 hUCMSC耻尾肌注射治疗压力性尿失禁不同时期尿动力学检测结果
1)与正常对照组相比,P<0.05;2)与对照A组相比,P<0.05;3)与对照A组相比,P<0.01

表2 hUCMSC膀胱颈注射治疗压力性尿失禁不同时期尿动力学检测结果
1)与正常对照组相比,P<0.05;2)与对照B组相比,P<0.05; 3)与对照B组相比,P<0.01
3 讨 论
ICS定义规定:压力性尿失禁(SUI)指腹压突然增加导致的尿液不自主流出。该病发病率高,治疗难度大[3],发病人群主要为中老年女性,产伤和绝经是发病主要原因。其发病机制至今未完全明确,大多数观点认为尿道周围支持结构、尿道固有括约肌的缺失以及神经功能障碍是其主要原因,肥胖、多产和滞产是其主要危险因素[4]。虽然其诊断以症状为主,但尿动力学检查一定程度上反映了储尿能力。漏尿点压力(LPP)测定是一种定量反映尿道闭合功能的方法,可判断SUI的程度。最大膀胱容积(MCC)是指膀胱充盈期患者不能再延迟必须排尿时的膀胱容量。Bai等[5]研究表明,LPP结合MCC可以代表动物的储尿能力。
目前对压力性尿失禁的治疗方法以外科手术(包括各种补片、吊带)为主,疗效差、并发症多,存在复发后处理困难等问题。而非手术疗法只对轻度患者有效,且短期易复发。基于以上缺陷,注射疗法因简便、安全、微创的特点而逐渐受到重视和欢迎。注射疗法是将药物或化学制剂注射到后尿道或膀胱内口周围粘膜下及肌层中,使尿道腔缩小、变窄和拉长,可不同程度弥补固有括约肌的功能不足,增加尿道阻力,从而改善压力性尿失禁症状。其常用注射材料有硅树脂颗粒、Teflon(特氟隆)、微球体等。虽近期疗效较好,但远期疗效逐渐降低,且有明显副反应,究其原因是缺乏组织再生和整合的特性。干细胞的出现有望为弥补现有疗法的局限性提供新的途径,因为理论上讲,注入的细胞可以恢复功能性肌肉细胞,改善患有括约肌相关失禁的妇女的尿道括约肌活动。用于这种治疗目的的干细胞类型有骨髓干细胞、人间充质干细胞、人脐血干细胞、人羊膜干细胞、诱导多能干细胞[6]。Blaganje 等[7]曾把肌源性干细胞注射在38例SUI患者的尿道外括约肌上,6个月后随访,其中9例患者认为治愈,20 例患者认为症状改善。而与肌源性干细胞相比,人脐带间充质干细胞(hUCMSC)具有来源广泛、取材方便、易于分离培养、免疫原性低等优点,故本实验选用hUCMSC进行局部注射的方法研究干细胞对压力性尿失禁的治疗作用。
盆底解剖结构复杂,耻尾肌位于盆底中心位置,内缘构成泌尿生殖裂孔和直肠裂孔,内侧尚有部分肌纤维进入尿道及阴道壁,分别围绕着两个脏器,前者支持膀胱底肌纤维收缩能提高膀胱,使尿道形成角度,后者收缩,使阴道下段向前与宫颈形成角度,以支持盆腔脏器的正常位置[8],可见耻尾肌对维持盆底正常结构及功能发挥着重要的作用。膀胱颈由平滑肌组成,解剖上成“Ω”形,后部肌纤维缺如,有研究发现,膀胱颈注射填充物可增加尿道闭合压,提高尿道出口阻力,进而达到控制尿失禁症状的目的[9]。
因此本实验模拟疾病的发生过程构建SUI动物模型,利用“指压实验”及LPP、MCC对动物SUI进行诊断及检验造模是否成功方法可靠。按照尿道的走行通过将hUCMSCs注射到耻尾肌(横纹肌)和膀胱颈(平滑肌)的方法研究hUCMSC对SUI雌鼠的治疗作用,对研究SUI的发病机制及选择最佳移植位点提供实验依据。本实验结果表明:与正常对照组相比,造模大鼠LPP均低,指压实验阳性率均高,差异有统计学意义(P<0.05)。这说明SUI模型构建成功。治疗A组与对照A组比较:两组MCC均增加,差异无统计学意义(P>0.05);治疗A组的LPP变化不大,对照A组的LPP下降,差异有显著统计学意义(P<0.01)。这说明耻尾肌注射hUCMSC可提高SUI大鼠的尿道闭合压,但不能改善储尿能力。与对照B组比较:治疗B组的MCC增加较多,差异有统计学意义(P<0.05);治疗B组的LPP升高,对照B组的LPP下降,差异有显著统计学意义(P<0.01)。这说明膀胱颈注射hUCMSC可提高SUI大鼠尿道闭合压的同时改善储尿能力。是否可以通过同时向耻尾肌和膀胱颈注射hUCMSC累加这种正向作用?疗效的发挥是来自于单纯的细胞分化还是细胞的旁分泌作用?亦或是二者兼而有之?尚需进一步研究探寻病理学等方面的证据。
