苯丙氨酸取代的丝氨酸八聚体离子的红外光解离光谱及其在手性分析中的应用
2018-10-25李树奇孔祥蕾
任 娟,马 媛,李树奇,孔祥蕾,2*
(1.南开大学 化学学院 元素有机化学国家重点实验室,天津 300071;2.南开大学 天津化学化工协同创新中心,天津 300071)
与传统色谱法及其他方法相比,基于质谱的手性分析方法具有分析速度快、样品用量少、灵敏度高等优势,近年来受到了人们的广泛关注[1-15]。而各种软电离方法的发展,尤其是电喷雾电离(ESI)的广泛应用,极大地促进了质谱技术在手性分析中的应用[3-8]。电喷雾电离方法可在气相中产生非共价复合离子,从而为对映异构体提供手性环境。常用的基于质谱的手性区分方法主要有3种:①广泛使用的动力学方法,即通过比较非对映体复合离子碰撞诱导解离质谱的碎裂模式差异实现手性分析[2-8];②比较相对丰度法,即测量由分析物和特定参照分子形成的非对映异构配合物离子的相对丰度[9];③主客体交换反应法,即研究非对映异构主客体复合物与中性试剂(客体)反应的交换速率[10-11]。
近年来,电喷雾质谱-红外解离光谱(ESI MS-IRPD)在手性分析中得到了快速发展[14-15]。该技术结合了电喷雾质谱和红外光谱的优点,通过电喷雾方法产生一系列气相离子,利用不同的质谱仪实现离子的选择和囚禁后,引入可调谐红外激光,当具有连续波长的红外激光照射目标离子时,通过观察产物离子的相对强度或母体离子的衰减可得到相应的红外解离光谱,从而能够提供相应的离子结构信息,并利用其光谱和质谱的差异实现手性区分。
而利用质谱-红外多光子解离光谱法的前提则是相应非对映异构体复合物离子的产生,即必须为待分析的手性分子在气相中提供一个有效的手性环境。在氨基酸类的手性分子分析方面,丝氨酸八聚体离子极具代表性。Cooks等[16]最早在电喷雾质谱中观察到一种特殊的幻数团簇离子——质子化的丝氨酸八聚体。研究发现该团簇离子存在显著的同手性优势,这种特殊的幻数团簇离子极易发生取代反应,且取代后的丝氨酸八聚体仍存在同手性优势[17-19]。本课题组曾利用ESI-IRPD技术分别研究了脯氨酸与苏氨酸取代的丝氨酸八聚体的手性效应,并根据得到的红外解离质谱图与红外解离光谱图实现了相应取代团簇离子中取代单元的手性区分,对两种氨基酸取代的丝氨酸八聚体的结构有了新的认识[14-15]。本文基于傅立叶变换离子回旋共振(FT ICR)质谱仪和ESI-IRPD研究平台对苯丙氨酸取代的丝氨酸八聚体团簇离子的质谱和红外解离光谱进行了研究,通过比较光谱图在某些波数处的差异成功实现了同手性和异手性取代团簇的手性区分。
1 实验部分
1.1 实验试剂
丝氨酸(Ser)、苯丙氨酸(Phe)(色谱纯,Sigma公司),甲醇(色谱纯,J.T.Baker公司),乙酸(色谱纯,天津市光复精细化工研究所)。
分别配制50 mmol/L的L-Ser溶液与20 mmol/L的L/D-Phe溶液,取一定体积进行混合后,稀释为含0.5 mmol/LL/D-Phe和3 mmol/LL-Ser的混合溶液,混合溶液的溶剂体积比为H2O∶MeOH∶CH3COOH=49∶49∶2,将混合溶液振荡10 min,混匀后储存于冰箱冷藏室中备用。
1.2 仪器条件及实验方法
所有的质谱实验均在7.0 T傅立叶变换离子回旋共振(FT ICR)质谱仪上进行(IonSpec,Varian,Lake Forest,CA,USA)。所有离子均通过电喷雾电离(ESI)离子源产生,其中ESI源喷针的电压为3.6 kV。为使ESI电离过程比较温和,实验中源内加热温度设为60 ℃,低于一般ESI实验温度(80 ℃)。样品溶液的流速为1 μL/min。ESI产生的离子经由四极杆离子传导装置,最终被引入FT ICR分析池中进行检测。质谱检测均采用正离子模式,探测范围为m/z200~2 000。将傅立叶变换离子回旋共振质谱仪与可调谐的OPO激光器等光学器件搭建成ESI-IRPD的研究平台,以获得相应体系的红外解离光谱[20]。实验中将激光器发射的红外激光射入FTICR MS 圆形洞孔的分析池中。OPO激光器(Msquared公司的Firefly-IR激光器)覆盖的波数范围为2 700~4 000 cm-1,因此能提供O—H、N—H和C—H等的红外特征吸收信息。[L-Ser6+L-Phe2]H+激光输出功率和线宽分别为200 mW和5 cm-1,使用机械快门控制激光照射时间。波长的光谱强度计算公式:I=-ln(Ip/(∑If+Ip)),其中Ip和If分别为母离子和碎片离子的强度[14-15]。
2 结果与讨论
2.1 ESI质谱
图1为Ser/Phe混合溶液的ESI质谱图,由图可知,(L-Ser)8H+与L、D-Phe均发生了取代反应,主要生成了一、二取代产物,但L-Phe与D-Phe的离子信号分布存在明显差异,如L-Phe与(L-Ser)8H+发生取代反应后相对强度最高的离子由(L-Ser)8H+变为[L-Ser7+L-Phe1]H+(图1A),而在D-Phe的取代结果中,(L-Ser)8H+仍为强度最高的离子(图1B)。从两者的离子分布差异可知(L-Ser)8H+与同手性的L-Phe更容易发生取代反应,即苯丙氨酸取代的丝氨酸八聚体团簇具有显著的同手性优势,这与文献报道的脯氨酸、苏氨酸以及其它氨基酸分子取代的实验结果相同[14,16]。

2.2 IRPD质谱与光谱
为进一步研究不同手性的苯丙氨酸取代的丝氨酸八聚体的结构和特征,本实验将激光器输出激光的波数调至3 110 cm-1,分别对4种取代团簇离子照射20 s,得到各自的红外解离质谱图(见图2)。首先对单一苯丙氨酸取代后团簇离子的解离结果进行比较(见2A、B),可看出同手性和异手性团簇离子产生的碎片离子及其分布大体相似,两者解离均形成了[Sern+Phe1]H+(n=1~4),且[Ser1+Phe1]H+的相对强度最高,说明单一苯丙氨酸取代的同手性和异手性团簇离子在红外激光照射后,丢失若干Ser单元并形成[Ser4+Phe1]H+,然后再连续丢失1个Ser单元,直至得到最终的[Ser1+Phe1]H+;但两者仍有细微不同,在同手性团簇的解离碎片中观察到较弱的[Ser5+Phe1]H+,而在单一D-苯丙氨酸取代的团簇中并未观察到该离子,可能提示[L-Ser5+L-Phe1]H+较[L-Ser5+D-Phe1]H+有着更好的稳定性,但也可能是来自于L-或D-苯丙氨酸取代的八聚体在解离通路上存在的细微差别。

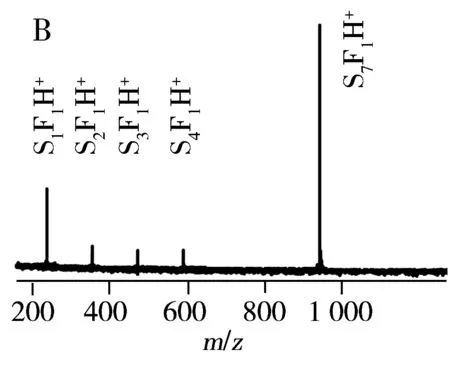
图2 [L-Ser7+L-Phe1]H+(A)、[L-Ser7+D-Phe1]H+(B)、[L-Ser6+L-Phe2]H+(C)及[L-Ser6+D-Phe2]H+(D)的红外解离质谱图
Fig.2 IRPD mass spectra of [L-Ser7+L-Phe1]H+(A),[L-Ser7+D-Phe1]H+(B),[L-Ser6+L-Phe2]H+(C) and [L-Ser6+D-Phe2]H+(D)laser wavelength:3 110 cm-1;irradiation time:20 s
在苯丙氨酸二取代离子的光解离质谱图中(2C、D),可发现同手性和异手性团簇也出现了不同的解离碎片,两者首先丢失Ser2单元形成[Ser4+Phe2]H+,其后连续丢失Ser单元直至全部丢失,最终得到Phe2H+,此后同手性与异手性团簇离子的解离路径出现差异,同手性的二取代离子出现1个丢失Phe单元的碎片,即[Ser1+Phe1]H+,而在异手性团簇中未观察到该碎片。基于二取代离子解离碎片的差异,可实现同手性和异手性苯丙氨酸取代的丝氨酸八聚体团簇离子的手性区分。
与前期报道的脯氨酸和苏氨酸的取代结果比较,本实验发现3种氨基酸的单一取代的同手性和异手性团簇离子的解离碎片和解离路径相似,而二单元取代的团簇离子却存在明显差异。在脯氨酸取代的团簇离子中,只出现丢失Ser单元的碎片,碎片离子种类单一[14];在苯丙氨酸取代体系中,解离路径除了丢失Ser单元,还出现了丢失Phe的情况,但这种解离路径所占比例很小,只有[Ser1+Phe2]H+丢失1个Phe形成[Ser1+Phe1]H+;而在苏氨酸体系中,几乎每一种[Sern+Thr2]H+(n=1~4)碎片离子均会丢失Thr单元,碎片离子的种类非常丰富[15]。此现象可归因于4种氨基酸的质子亲和势的差异,丝氨酸的质子亲和势为217.3 kcal/mol,而在取代的3种氨基酸中,脯氨酸最高(为224.0 kcal/mol),苯丙氨酸次之(为220.6 kcal/mol),苏氨酸最低(为218.7 kcal/mol),这3种氨基酸的质子亲和势均比丝氨酸高,所以在这3种取代体系中均存在丢失中性Ser单元的解离路径,且该解离路径为主要解离路径,而随着丝氨酸与取代氨基酸的质子亲和势差值减小,丢失质子亲和势较高的取代氨基酸单元的路径逐渐占优势。此外,3种取代体系结构的差异也可能是造成解离路径不同的主要原因。

图3 [L-Ser8]H+(A)、[L-Ser7+D/L-Phe1]H+(B)及[L-Ser6+D/L-Phe2]H+(C)的红外解离光谱图Fig.3 IRPD spectra of [L-Ser8]H+(A),[L-Ser7+D/L-Phe1]H+(B)and [L-Ser6+D/L-Phe2]H+(C)laser wavelength:2 700~3 600 cm-1
通过调谐输出激光的波长,最终可获得苯丙氨酸取代的丝氨酸八聚体在2 700~3 600 cm-1范围内的红外解离光谱图(图3)。与其他氨基酸取代体系类似,在2 800~3 250 cm-1范围内所有的苯丙氨酸取代团簇离子均观察到强烈的吸收峰。此外,在3 335、3 425、3 465 cm-1等波数处也存在规律性变化,如3 335 cm-1吸收峰在单一取代的同手性和异手性团簇中全部消失,但在二取代的同手性团簇中仍存在;3 425 cm-1的吸收峰在单一取代的同手性团簇中存在,在异手性团簇中蓝移至3 465 cm-1;而在二单元取代的光谱图中,可观察到同手性团簇离子的3 425 cm-1吸收峰略微红移,而在异手性团簇离子中由于取代效应的作用使得3 465 cm-1处的吸收峰明显展宽。
根据这些光谱的差异,可快速实现苯丙氨酸一、二取代的同手性和异手性的丝氨酸八聚体团簇离子的手性区分,也可以通过选择合适的激光波长,利用光解离质谱快速实现单元的手性区分。从图3可知,对于二单元取代的团簇离子,其光解离光谱在2 780~2 830 cm-1存在差别,[L-Ser6+L-Phe2]H+的光谱强度明显强于[L-Ser6+D-Phe2]H+。这一差别在对于波段的光解离质谱中更容易体现。图4显示,激光波长在2 805 cm-1处时,[L-Ser6+L-Phe2]H+的光解离碎片强度明显优于[L-Ser6+D-Phe2]H+,而产生的碎片[Ser+Phe]H+并未在[L-Ser6+D-Phe2]H+的光解离质谱被观察到,体现出手性取代单元给体系带来结构上的差异。值得注意的是,尽管在相同的实验条件下对此体系进行了多次实验,其光谱也获得了较好的重复性,但考虑到丝氨酸八聚体本身结构中存在的多态性[19],一些重要的实验条件(如溶剂、离子源的结构和参数)对实验结果的影响需受到重视。

3 结 论
本文通过电喷雾电离的方法经傅立叶变换离子回旋共振质谱仪产生了不同手性的苯丙氨酸取代的丝氨酸八聚体团簇离子,并结合IRPD技术对这些团簇离子的红外解离光谱与手性效应进行了研究。通过比较各自的ESI质谱图发现在两种取代团簇中均存在显著的手性优势,即丝氨酸八聚体可将其所具有的手性优势传递给苯丙氨酸,同时对各自的光解离路径进行了初步探究。实验分别得到2种取代团簇离子在2 700~3 600 cm-1范围内的红外解离光谱,通过比较光谱图在某些波数处的差异成功实现了同手性和异手性取代团簇的手性区分。其对应的红外解离光谱变化反映了取代效应的存在,同时也反映了ESI-IRPD方法在研究非共价复合物大分子结构方面的特点,从而为手性分子的识别提供了新的思路和方法。
