内镜下逆行胰胆管造影术围手术期用药专家共识意见(2018年,南昌)
2018-10-25中国医师协会内镜医师分会消化内镜专业委员会中国医师协会胰腺病专业委员会中华消化杂志中华消化内镜杂志中华胰腺病杂志胃肠病学杂志中国实用内科杂志
中国医师协会内镜医师分会消化内镜专业委员会 中国医师协会胰腺病专业委员会 中华消化杂志 中华消化内镜杂志 中华胰腺病杂志 胃肠病学杂志 中国实用内科杂志
内镜下逆行胰胆管造影术(endoscopic retrograde cholangiopancreatography, ERCP)已广泛应用于胆胰疾病的诊治,但ERCP操作有一定并发症发生率,主要包括术后胰腺炎(post-ERCP pancreatitis, PEP)、出血、感染,穿孔等。围手术期合理应用药物可有效降低ERCP术后并发症,然而目前对ERCP的围手术期合理用药认识存在明显不足,围手术期合理使用预防药物的比例较低[1-2]。目前关于ERCP围手术期用药的研究繁多,但结论不一,2015年我国制定了《内镜下逆行胰胆管造影术后胰腺炎药物预防专家共识意见(2015年,上海)》[3],近年来随着对ERCP围手术期用药研究的报道数量不断增加,其中来自中国的临床研究占30%以上,为此中国医师协会内镜医师分会消化内镜专业委员会与中国医师协会胰腺病专业委员会于2018年5月在江西南昌组织召开了“ERCP围手术期用药专家共识意见研讨会”,经与会专家充分讨论后形成了本共识意见,供广大临床医师参考借鉴。
一、基本定义
1.ERCP:是指将内镜插至十二指肠的降部,并经十二指肠乳头开口或瘘口等部位插入相关器械,向胰胆管内注入造影剂。若仅注入造影剂显示胰胆管或进行细胞刷检、活检取材或Oddi括约肌测压等诊断目的称诊断性ERCP;若通过各种器械对胰胆管病变进行治疗性操作则称治疗性ERCP。
2.PEP:1991年Cotton等[4]制定了关于ERCP术后并发症的共识意见,将PEP定义为ERCP术后出现胰腺炎相关的临床症状持续超过24 h,同时伴有血淀粉酶超过正常值上限3倍。若ERCP术后仅有血淀粉酶升高,而无胰腺炎的临床表现则称ERCP术后高淀粉酶血症(post-ERCP hyperamylasemia,PEH)。PEP的诊断也可参考2015年发布的《中国急性胰腺炎多学科诊治(MDT)共识意见(草案)》[5],根据PEP的病情严重程度可以分为轻、中、重3级(表1)。
3.ERCP围手术期:指从确定行ERCP操作至本次ERCP诊疗结束的一段时间,包括术前准备、术中操作、术后恢复的全过程。
二、ERCP的适应证与禁忌证
ERCP适应证与禁忌证详见《内镜下逆行胆胰管造影术(ERCP)诊治指南(2010版)》[6-8]。

表1 PEP严重程度分级
三、ERCP常见并发症
1.PEP:PEP是ERCP术后最常见并发症,总体发生率为3%~10%[9-10],高危患者PEP发生率为15%~20%[11]。一项纳入13 296例患者的荟萃分析显示PEP总体发生率为9.7%,高危患者发生率为14.7%,绝大多数为轻度胰腺炎,总体病死率为0.7%[12-13]。南京鼓楼医院回顾性分析4 234例ERCP患者发现PEP发生率为5.3%[14]。Inamdar等[15]回顾性分析3 628例育龄期女性的ERCP术后并发症,其中妊娠患者907例,结果发现妊娠患者PEP发生率为15%,明显高于非妊娠患者。Koksal等[16]一项小样本研究认为胰岛素抵抗是PEP的独立危险因素,但是需要大样本研究证实。既往研究认为慢性胰腺炎可能是PEP的保护因素,但近期上海长海医院研究显示慢性胰腺炎患者PEP发生率与胆管疾病相当(4.5%比4.8%)[17]。
2.消化道出血:发生率为0.3%~2%,主要原因是括约肌切开术,少见原因包括胆道狭窄扩张、胆道活检等[18]。可分为术中出血和迟发性出血,迟发性出血可以发生在术后数小时甚至数周[4]。Freeman等[19]分析2 347例ERCP术后患者,发现消化道出血发生率约为2%,其中2例迟发性出血患者死亡。Masci等[20]分析2 444例ERCP术后患者的消化道出血发生率为1.2%。
3.胆系感染:主要包括急性胆管炎、急性胆囊炎,其中前者最常见,其发生率为0.5%~3%[21-23]。主要临床表现包括腹痛、发热及黄疸。南京鼓楼医院回顾性分析4 234例ERCP发现感染发生率为2.4%[24]。
4.消化道穿孔:发生率为0.08%~0.6%[25-26],以十二指肠最为常见。主要原因包括内镜粗暴操作、括约肌切口过长、导丝穿透及支架移位[27-28],拉直内镜过程偶尔也可发生穿孔。穿孔需要及时诊断及治疗,否则将导致严重后果,延迟诊断可导致患者败血症及多器官功能衰竭,病死率为8%~23%[29-30]。
四、ERCP术后并发症的危险因素
明确ERCP术后并发症高危因素对选择合适的预防对象有重要意义[31]。对大样本量、高质量临床研究综合分析,认为ERCP术后并发症的危险因素主要包括患者相关因素及ERCP操作相关因素(表2)。这些危险因素间存在协同作用,即存在的危险因素越多,发生术后并发症的风险也越高[32]。因此,预防术后并发症的首要措施是严格掌握ERCP的适应证,减少不必要的ERCP操作。

表2 ERCP术后并发症相关危险因素
五、ERCP术后并发症的药物预防
(一)ERCP围手术期合理用药的目标
为内镜医师提供良好的操作环境、保障操作安全、预防并发症、促进患者康复。用药种类主要包括解痉药、抑酶药、抗生素、镇静止痛剂等。
(二)ERCP围手术期用药建议
1.合并梗阻性黄疸或凝血功能障碍的患者建议术前使用维生素K。
2.镇静止痛、解痉药:为减轻ERCP患者术中的疼痛不适,可在ERCP术前静脉注射地西泮5 mg和(或)盐酸哌替啶50 mg。有条件的单位也可由麻醉医师采用镇静/麻醉行ERCP。建议在术前使用解痉药(山莨菪碱、丁溴东莨菪碱等)以有效抑制十二指肠蠕动,保持相对稳定的操作环境。需注意合并严重心脏病、消化道机械性梗阻、重症肌无力、青光眼、前列腺增生的患者禁用。
3.祛泡剂:祛泡剂是否能缩短ERCP操作时间、减少ERCP术后腹胀等不良事件发生率目前尚无相关研究,但临床经验表明祛泡剂能改善消化道内镜操作视野,有利于内镜操作顺利完成,因此今后有必要进一步研究其是否在ERCP术前有应用价值。
(三)预防PEP的药物
PEP的药物预防一直是临床研究的热点,最佳的PEP预防药物应该同时具备有效、副作用小、成本效益比高、便于获取、给药方便等特点。
1.有明确预防效果的药物:(1)非甾体类抗炎药(nonsteroidal anti-inflammatory drugs, NSAIDs)。大量研究显示NSAIDs可有效抑制磷酸酯酶A2活性,降低PEP的发生率[33]。2014年欧洲消化内镜协会推荐ERCP患者常规使用100 mg NSAIDs纳肛预防PEP[32]。最近的大多数随机对照研究(random ized controlled trials, RCT)及荟萃分析认为NSAIDs可以明显降低高危患者的PEP发生率,术前30 min内或术后NSAIDs纳肛的效果明显,而口服或肌肉注射无效[34-37]。近期一项RCT研究认为非选择性ERCP患者100 mg吲哚美辛纳肛与安慰剂组比较,PEP发生率差异无统计学意义,因此不推荐所有ERCP患者使用NSAIDs预防PEP[38]。而一项纳入24个临床研究的荟萃分析认为,吲哚美辛能明显降低非选择性ERCP患者术后PEP发生率[39]。另外两项纳入12个和9个RCT的荟萃分析认为 NSAIDs对PEP高危及低危患者都有预防作用[40-41]。但最近国内一项纳入3 013例患者的荟萃分析显示并非所有ERCP患者使用NSAIDs均能有效预防PEP,仅对PEP高危患者能显著降低PEP发生率[42]。关于NSAIDs的最佳使用时机,最近我国一项大样本量多中心RCT研究认为患者术前30 min内100 mg吲哚美辛纳肛较术后即刻吲哚美辛纳肛能更显著降低PEP发生率[43]。
推荐意见:对无消化道出血、心功能衰竭和肾功能衰竭等禁忌证的拟行ERCP患者,NSAIDs(双氯芬酸钠100 mg或吲哚美辛100 mg)纳肛能明显降低高危患者的PEP发生率(图1),但能否降低所有ERCP患者PEP发生率仍需要进一步研究,NSAIDs在我国人群中的最佳剂量尚待探索。
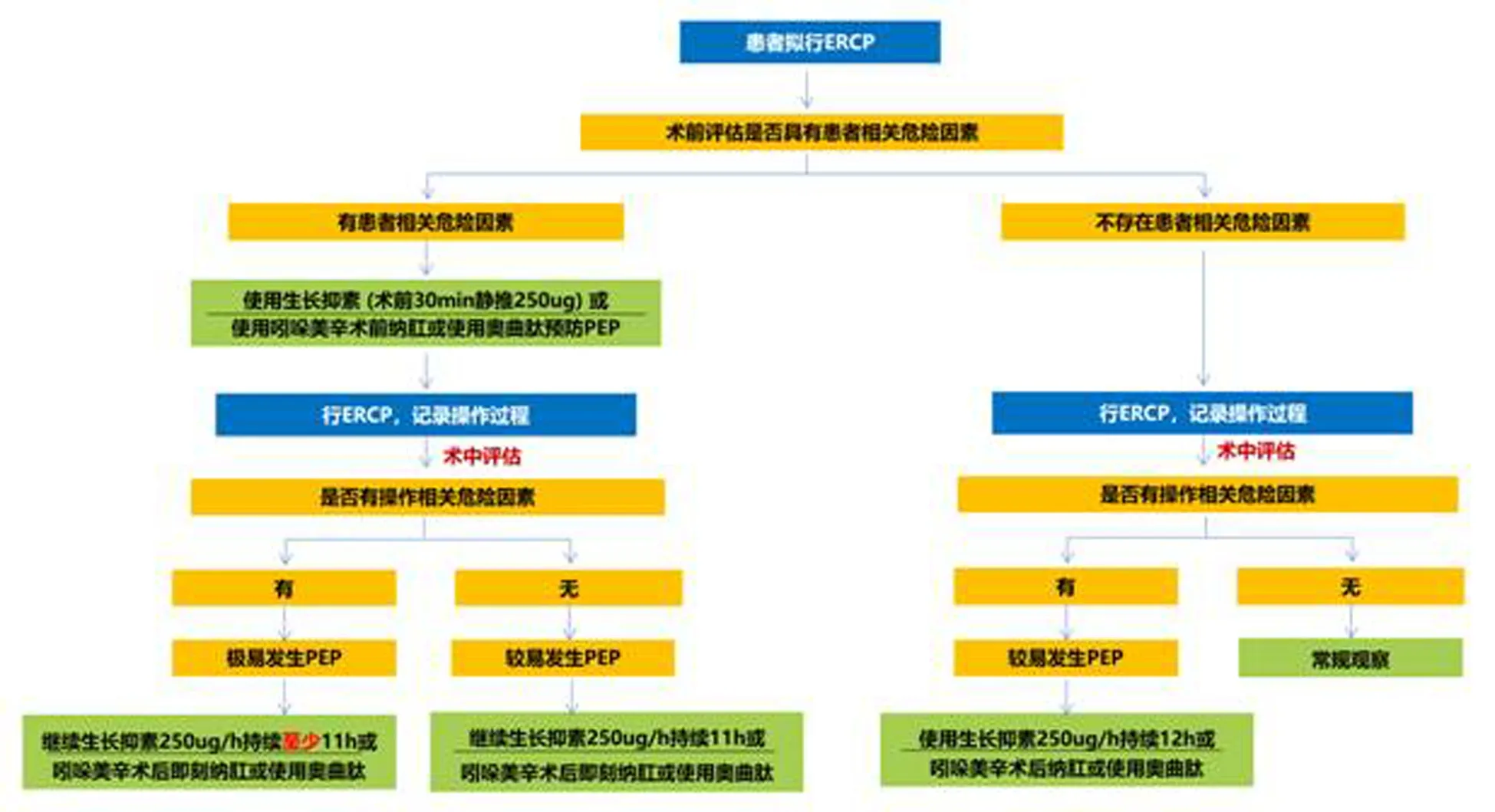
图1 PEP药物预防推荐流程图
(2)生长抑素(somatostatin)及其类似物奥曲肽(octreotide)。生长抑素可以抑制多种内分泌激素的分泌,还可减少胰腺的内外分泌以及小肠和胆囊的分泌,降低消化酶活性,对胰腺细胞有保护作用,具有极好的安全性,不良反应少见[44]。近年我国11家医院共同完成一项纳入900例患者的大样本量、多中心RCT,证实ERCP围手术期使用生长抑素(250 μg术前静脉推注+250 μg/h术后静脉滴注11 h)可显著降低PEP发生率(7.5%比4.0%),且无严重不良事件发生[45]。近期2项荟萃分析也认为生长抑素可降低PEP发生率[46-47]。生长抑素类似物奥曲肽同样可抑制多种内分泌激素,减少胰腺分泌。一项由我国12个中心完成的RCT证实围手术期使用奥曲肽(ERCP术前1 h奥曲肽0.3 mg持续静滴至术后5 h,静滴结束后6 h及12 h奥曲肽0.1 mg皮下注射)可明显降低PEP发生率及PEH[48]。近期2项荟萃分析结果显示大剂量奥曲肽(≥0.5 mg)预防PEP的效果更为显著[49-50]。
推荐意见:ERCP围手术期使用生长抑素能降低PEP发生率,推荐剂量为ERCP操作开始前250 μg静脉推注+ERCP术后250 μg/h静脉滴注至少11 h。生长抑素类似物奥曲肽也可降低PEP发生率,推荐使用剂量≥0.5 mg(图1)。
2.可能有预防效果的药物
(1)蛋白酶抑制剂(加贝酯、乌司他丁、萘莫司他)。蛋白酶抑制剂可抑制胰蛋白酶、激肽释放酶等蛋白酶的活性,减轻胰腺损伤,主要包括加贝酯、乌司他丁及萘莫司他。目前无论是高质量RCT研究还是荟萃分析,均没有明确加贝酯及乌司他丁是否对PEP有预防作用[51-52]。最近一项荟萃分析认为乌司他丁仅能预防中低危患者PEP发生率[53]。萘莫司他是一种新型的蛋白酶抑制剂,一项荟萃分析纳入5项RCT研究结果显示萘莫司他降低PEP低危患者最为显著,而对高危患者无明显的预防作用[51]。最近一项单中心RCT研究发现萘莫司他能减少低危患者PEP发生率,但由于该研究中高危PEP患者都置入胰管支架,因此其对高危患者的预防作用需要进一步研究[54]。
推荐意见:目前没有足够证据支持加贝酯及乌司他丁能预防PEP;萘莫司他可降低低危患者PEP发生率,但目前我国尚无相关的高质量临床研究证据,因此不建议常规使用蛋白酶抑制剂预防PEP。
(2)硝酸甘油。早期研究发现硝酸甘油可松弛Oddi括约肌,降低ERCP时操作难度[55-56],而且硝酸甘油还可缓解括约肌痉挛导致的胰管梗阻,因此硝酸甘油有预防PEP的潜在价值。既往对硝酸甘油预防PEP的RCT及荟萃分析显示,硝酸甘油可有效预防PEP,但是静脉给药途径的全身不良反应较多,而透皮贴剂的预防效果不明显,因此舌下含服可能具有最佳的预防效果[57]。近期一项纳入455例患者的RCT研究舌下含服硝酸甘油联合静脉注射胰高血糖素对ERCP插管的影响,发现深插管成功率明显提高、PEP发生率显著下降,提示硝酸甘油舌下含服对预防PEP可能具有较好的应用价值[58],但是最佳剂量和给药时机尚待进一步研究。
推荐意见:舌下含服硝酸甘油可能预防PEP发生,但是其最佳剂量及给药时机需要进一步研究。
(3)乳酸林格液(lactated ringer solution,LRS)。乳酸林格液一般用于液体复苏,最近有研究发现乳酸林格液对PEP有一定的预防作用。一项纳入395例PEP高危患者的RCT研究发现,ERCP术后即刻给予大剂量乳酸林格液(3 ml·kg-1·h-1)静滴8 h能显著降低高危患者PEP发生率[59]。最近一项纳入7项RCT 的荟萃分析发现大剂量乳酸林格液较标准剂量乳酸林格液能明显降低PEP及PEH[60]。一项纳入192例高危PEP患者的RCT研究发现大剂量乳酸林格液联合吲哚美辛能明显降低PEP发生率,但是与单用大剂量乳酸林格液或吲哚美辛组无差异[61]。最近国内一项纳入3个RCT共722例患者的荟萃分析认为大剂量乳酸林格液能明显降低PEP发生率[62]。但目前我国尚无乳酸林格液预防PEP的高质量临床研究。
推荐意见:大剂量乳酸林格液能降低高危患者PEP发生率,但是否能降低所有患者PEP发生率,以及大剂量乳酸林格液是否能用于心肺功能或肾功能不全患者及高龄患者尚需进一步研究。
(4)其他。2项RCT比较了ERCP时在十二指肠乳头局部喷洒肾上腺素对PEP的影响,结果均显示PEP的发生率明显下降,但是这2项RCT纳入的患者只接受单纯诊断性ERCP,在插管时不使用导丝,插管时间较长,研究对PEP的定义不规范[63-64]。由于这些缺陷,目前暂不推荐在十二指肠乳头局部喷洒肾上腺素预防PEP。
推荐意见:十二指肠乳头局部喷洒肾上腺素是否能预防治疗性ERCP术后胰腺炎尚需进一步研究。
3.无预防效果的药物:对糖皮质激素[65]、白介素10[66-67]、肝素[67]、抗氧化剂[68-70]及降低Oddi括约肌压力药[71-74],如肉毒素、利多卡因、硝苯地平等药物,无论是RCT还是荟萃分析结果显示这些药物均不能降低PEP的发生率。
推荐意见:糖皮质激素、白介素10、肝素、降低Oddi括约肌压力药及抗氧化剂等药物目前证实对PEP无预防作用,不推荐使用。
(四)预防ERCP术后感染的药物
对于肝门部胆管癌、硬化性胆管炎等预计难以获得完全胆道引流患者以及免疫力低下者(化疗、肝移植等),建议术前1 d开始预防性使用抗生素[75],主要覆盖革兰阴性菌和肠球菌[21]。在抗生素的选择上,可考虑喹诺酮类或头孢类抗生素,研究发现两者效果相当[76]。
(五)止血药物
对于ERCP术后出血主要采用内镜下止血、血管栓塞止血以及外科手术[77-78]。止血药物对于ERCP术后出血的预防和治疗作用尚未证实,部分药物有血栓风险,不推荐作为一线药物常规使用。
六、特殊人群ERCP术后并发症的预防
1.老年患者:最近一项荟萃分析结果报道老年患者(>65岁)ERCP并发症情况,PEP发生率1.31%,出血发生率0.77%,穿孔发生率0.38%,胆道感染发生率1.61%,与年轻患者相比并发症发生率无明显增加,总体而言ERCP对老年患者是安全的,但是随着年龄的增长,出血率、心肺疾病并发症发生率以及病死率升高,而PEP的发生率无明显升高[79]。
2.接受长期抗血小板/抗凝治疗患者:目前关于抗血小板/抗凝药物对ERCP术中及术后出血影响的研究数量较少,主要来自日本的小样本研究。Hamada等[80]认为服用阿司匹林对于乳头括约肌切开或气囊扩张是安全的。一项纳入95例患者的小样本研究发现服用双抗/抗血小板联合抗凝/三抗的整体出血率为4%[81]。亚太消化病学会(APAGE)及亚太消化内镜学会联合指南(APSDE)认为对于低危出血风险操作(放置胆管支架或胰管支架、黏膜活检)不推荐停用抗血小板/抗凝药物;对于高危出血风险操作(乳头括约肌切开、气囊扩张、内镜下乳头切除)推荐停用抗血小板/抗凝药物5~7 d[82]。英国胃肠病学会(BSG)及欧洲胃肠内镜学会(ESGE)推荐对于低危出血风险操作(放置胆管支架或胰管支架)继续使用抗血小板/抗凝药物,但停用手术当天上午新型口服抗凝药物(如利伐沙班);对于高危出血风险操作(乳头括约肌切开、气囊扩张)、低血栓形成风险患者可停用抗血小板/抗凝药物5 d,若服用双抗(阿司匹林及氯吡格雷),继续服用阿司匹林;对于高血栓形成风险患者建议继续服用阿司匹林;暂时停用华法林,使用低分子肝素替代治疗;口服新型抗凝药物患者,建议至少停用48 h;对于肾功能不全患者(肾小球滤过率30~50 ml/min)至少停药72 h,同时需要请心内科医师等多学科协作,评估患者停药益处/风险以及是否需要替代治疗[83]。美国消化内镜协会(ASGE)推荐对于低危出血风险操作(放置胆管支架或胰管支架),继续服用抗血小板/抗凝药物/新型口服抗凝药;对于高危出血风险操作(乳头括约肌切开、气囊扩张),建议停用抗血小板治疗5~7 d,推迟冠脉支架置入/急性冠脉综合征(ACS)患者手术时间;对于高危血栓风险患者,手术结束确定止血后当天继续使用华法林或新型口服抗凝药[84]。
3.肝硬化及肝移植患者:一项纳入3 228例肝硬化患者的大样本研究认为肝硬化患者ERCP术后出血风险增加(2.1%比1.2%)[85]。我国一个小样本研究认为对肝功能Child A与Child B级的肝硬化患者进行ERCP是相对安全的,而肝功能Child C级患者出血风险增加[86]。一项纳入121例肝移植患者的单中心研究发现肝移植患者PEP发生率为3.7%,胆系感染发生率为3.3%,术后出血发生率为1.6%,肝移植患者与非肝移植患者并发症发生率相当[87]。
七、结语
每年我国有数十万患者需进行ERCP诊疗,如何有效地预防术后并发症是一个重要的临床问题,目前我国在ERCP领域的大样本量、多中心、高质量RCT数量较少,临床证据大多源自于欧美国家的临床研究结果。因此,期待国内的同道们积极合作开展高水平的临床研究,进一步完善符合中国国情的预防ERCP术后并发症用药规范。
参与本共识意见讨论的专家组成员(按姓氏拼音排序):
柏愚(海军军医大学附属长海医院消化内科)、别平(陆军军医大学西南医院肝胆外科)、陈幼祥(南昌大学第一附属医院消化内科)、杜奕奇(海军军医大学附属长海医院消化内科)、冯秋实(北京大学附属第一医院普外科)、冯缨(中华消化杂志编辑部)、郭学刚(空军军医大学西京医院消化内科)、韩雅玲(北方战区总医院心血管内科)、韩树堂(江苏省中医院消化内科)、郝建宇(北京朝阳医院消化内科)、胡冰(海军军医大学附属东方肝胆外科医院内镜科)、黄留业(烟台毓璜顶医院消化内科)、冀明(北京友谊医院消化内科)、贾林(广州市第一人民医院消化内科)、蒋晓玲(胃肠病学杂志编辑部)、金震东(海军军医大学附属长海医院消化内科)、李维勤(东部战区总医院普外科)、李文(天津市人民医院内镜中心)、李汛(兰州大学附属第一医院普外科)、李延青(山东大学附属齐鲁医院消化内科)、李兆申(海军军医大学附属长海医院消化内科)、令狐恩强(解放军总医院消化内科)、吕芳萍(中华胰腺病杂志编辑部)、吕农华(南昌大学第一附属医院消化内科)、麻树人(北方战区总医院消化内科)、毛恩强(上海交通大学附属瑞金医院急诊科)、缪林(南京医科大学附属第二医院消化内科)、聂时南(东部战区总医院急救医学科)、任旭(黑龙江省医院消化内科)、沙卫红(广东省人民医院消化内科)、孙明军(中国医科大学附属第一医院消化内科)、唐国都(广西医科大学附属第一医院消化内科)、唐涌进(中华消化内镜杂志编辑部)、田字彬(青岛大学附属医院消化内科)、王邦茂(天津医科大学总医院消化内科)、王雯(南京军区福州总医院消化内科)、徐红(吉林大学附属第一医院消化内科)、颜廷梅(中国实用内科杂志编辑部)、游苏宁(中华医学会继续教育部)、张澍田(北京友谊医院消化内科)、智发朝(南方医科大学附属南方医院消化内科)、周平红(复旦大学附属中山医院内镜中心)、邹晓平(南京大学附属鼓楼医院消化内科)
执笔:柏愚(海军军医大学附属长海医院消化内科)、李德锋(暨南大学附属第二医院(深圳市人民医院)消化内科)、王树玲(海军军医大学附属长海医院消化内科)、赵胜兵(海军军医大学附属长海医院消化内科)
