沙棘果渣生物炭对尼泊金乙酯的吸附特性研究
2018-10-17唐志书宋忠兴
张 娱 , 陈 琦 , 李 渊 ,唐志书, 宋忠兴, 王 春
沙棘广泛分布于欧亚大陆寒温带地区,常用于沙漠绿化,随着食用药用价值被挖掘,逐渐成为我国西部地区最具代表性的经济作物之一。沙棘果实营养丰富,包括维生素、蛋白质、氨基酸、有机酸及人体所需的多种微量元素等,具有很高的保健价值。自 1977年《中国药典》将沙棘列为药食两用后,沙棘产业链得到了快速发展,沙棘相关产品从饮料、果酱扩展到保健品、药品、食品以及化妆品等十几个领域。随着沙棘果实加工品产量的提高,沙棘果渣产量也随之增加[1-2]。近年来兴起的生物炭技术,一方面能够为低价值或废弃的生物质提供良好的转化途径;另一方面,制备的生物炭可以作为一类新型的环保材料用于污染水体、土壤的治理和修复。生物炭是一种常用的高效吸附材料,是指由含碳量丰富的生物质在无氧或限氧的条件下低温热解而得到的一种细粒度、多孔性的碳质材料。生物炭由于在炭化过程中非碳元素的分解,从而形成了疏松多孔的结构,作为一种很好的吸附材料,在吸附有机污染物、改善土壤环境等方面引起研究人员越来越多的关注[3-4]。据报道,生物炭对有机污染物的吸附能力远远强于其它形式天然有机质。所以生物炭在治理环境污染方面有巨大潜力,并且生物炭原料来源广泛,因此其有望作为廉价的吸附剂而广泛应用[5-6]。
尼泊金乙酯是一类常见的药物及个人护理品,主要用作食品、化妆品、医药的杀菌防腐剂。据报道,尼泊金乙酯具有内分泌干扰作用,是一类新的环境雌激素污染物,广泛存在于各种水体中[7-8]。因此研究有效地控制尼泊金乙酯在水中的浓度对环境污染的修复具有重大的意义。
本研究以沙棘果渣为原料,在不同热解温度下制备生物炭来吸附废水中的尼泊金乙酯,研究热解温度、尼泊金乙酯初始浓度、吸附温度和吸附时间对尼泊金乙酯吸附效率的影响,揭示沙棘果渣生物炭对尼泊金乙酯的吸附特性,为沙棘果渣的资源化利用提供参考。
1 实验
1.1 材料
尼泊金乙酯(ethyl paraben,EP),分析纯,购自天津市致远化学试剂有限公司。
仪器设备:紫外可见分光光度计(日本岛津)、马弗炉(北京科伟永兴)、水浴恒温振荡器(常州丹瑞)、粉碎机(天津鑫博得)、电热鼓风干燥箱(北京科伟永兴)、电子天平(德国赛多利斯)。
1.2 试验设计
设置20、30、40、50、60、70、80 mg/L,共7个EP初始浓度梯度,研究不同热解温度沙棘果渣生物炭对不同初始浓度EP的去除率。
分别在 25℃、35℃和 45℃下进行恒温振荡吸附,研究不同吸附温度对不同温度热解沙棘果渣生物炭吸附作用的影响。
震荡吸附4 h,分别在5、10、30、60、90、120、150、180、210、240、270 min取样,测量EP吸附率,研究不同温度热解生物炭对EP的吸附率随时间的变化情况。
1.3 方法
1.3.1 沙棘果渣生物炭的制备
沙棘果渣取自陕西省西咸新区某制药厂,清洗晾干后放入烘箱在60℃下烘干72 h,粉碎后置于瓷坩埚中,盖上盖子,放入马弗炉中,以2℃/min 的升温速率升至目标温度(300℃、400℃、500℃),随后保持2 h。冷却后取出,研磨过60目筛,储存于干燥器中备用。标记为BC300、BC400、BC500。
1.3.2 生物炭的结构表征
沙棘果渣生物炭的结构和表面形态采用扫描电子显微镜(型号:FEI Quanta-200)表征。取10 mg左右生物炭样品粘在样品台上,然后使用扫描电镜观察其大小、形态和表面特征,操作加速电压为20.0 kV,温度为室温。
1.3.3 EP 含量的测定
采用紫外分光光度法检测EP的含量,以背景溶液为空白,在200~400 nm波长内扫描,得到EP 的最大吸收波长为247 nm。每组进行3个平行试验,取其平均值。精密称取EP 0.125g,置于250 mL容量瓶中,加蒸馏水稀释至刻度,得到EP的500 mg/L储备液。分别量取此溶液用蒸馏水稀释至10、20、30、40、50 mg/L,用紫外分光光度计(岛津UV-2600,日本)在247 nm波长下分别测得吸收值,得回归方程y=0.070 9 x+0.012 7,R2=0.999 9(n=5)。
1.3.4 沙棘果渣生物炭对EP的等温吸附
分别精密称取0.1 g BC300、BC400 和 BC500,加入25 mL浓度分别为20、30、40、50、60、70、80 mg/L的EP溶液,置于恒温振荡器中,在温度分别为25、35、45℃、转速为150 r/min下充分振荡4 h后过0.45 μm滤膜,用紫外可见分光光度法(λ=247 nm)测定吸附后的EP浓度,每组进行3个平行实验,取其平均值。达到吸附平衡后的EP吸附量qe及去除率η,由下列公式(1)、(2)计算。

式中:qe为平衡时的吸附量,mg/g;C0和Ce分别为吸附前和吸附后溶液中EP的含量,mg/L;V为溶液体积,L;W为吸附剂投加量,g。
1.3.5 吸附随时间的变化
分别精密称取0.2 g BC300、BC400 和 BC500,加入50 mL浓度为50 mg/L的EP溶液,置于恒温振荡器中,在温度分别为30℃、转速为150 r/min下充分振荡,分别在5、10、30、60、90、120、150、180、210、240、270 min取样,测定剩余EP浓度,研究不同热解温度生物炭对EP的吸附随时间的变化情况。
1.3.6 等温吸附模型拟合
用Langmuir和Freundlish模型拟合三种沙棘果渣生物炭对EP的吸附等温线。Langmuir方程是用于描述吸附平衡行为中一种应用十分广泛的模型。Langmuir模型是理想的单分子层吸附模型,单分子吸附公式如式(3)所示。

式中,qe为吸附容量,Ce为吸附平衡浓度,a、b为常数,其倒数式如式(4)所示。

从式中可以看出,qe-1与Ce-1成线性关系。根据Freundlish经验式如式(5)所示。

式中,K为常数,其方程式的线性形式如式(6)所示。

1.4 数据分析
实验所得数据采用Sigmaplot 10.0软件进行拟合。
2 结果与分析
2.1 扫描电镜分析
不同热解温度下制备的沙棘果渣生物炭的扫描电镜图如图1所示,图1中的a、b、c分别为BC300、BC400、BC500放大 5000倍的扫描电镜图片,展示了不同温度下制备的生物炭的表面孔隙结构的变化特征。
从图1可以看出,随着热解温度的升高,沙棘果渣生物炭表面孔穴逐渐增加;随着沙棘果渣生物质的不断分解,纤维的链状结构被大量破坏。热解温度为 300℃时,生物炭的自身结构破坏不是很严重,纤维壁坚硬、平整。当温度升高到400℃时,生物炭表面结构出现变化,纤维链状结构被大量破坏。当热解温度升高到500℃时,生物炭的片状结构表面产生了许多微孔。由图可知裂解温度对生物炭表面形态有较大的影响,不同温度下制备的沙棘果渣生物炭的表面形态差异明显。随着热解温度升高,沙棘果渣生物炭中的有机质被消耗,孔结构发生明显的变化,微孔数量增加,比表面积增大。

图1 沙棘果渣生物炭的SEM图
2.2 不同热解温度沙棘果渣生物炭对EP的吸附
2.2.1 沙棘果渣生物炭对不同初始浓度EP的去除率
如图2所示,三种热解温度下的沙棘果渣生物炭对EP的去除率随EP初始浓度的增加整体上呈逐渐降低趋势。BC300在EP初始浓度为20 mg/L时,对EP的去除率最高,达 43.7%;BC400在EP初始浓度为30 mg/L时,对EP的去除率最高,达65.4%;BC500在EP初始浓度为20 mg/L时,对EP的去除率最高,达85.7%。
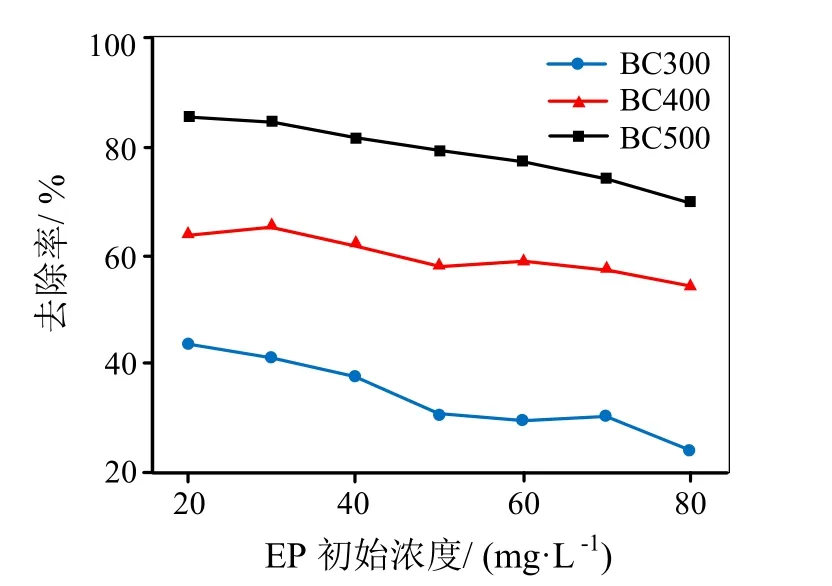
图2 沙棘果渣生物炭对不同初始浓度EP的去除率
综上可见,不同热解温度沙棘果渣生物炭对 EP的吸附效率有很大差异,在所选的三个温度范围内,随着热解温度升高,去除率逐渐增大,热解温度300℃时的平均去除率在30%左右,当热解温度升高到400℃时的平均去除率提高到了60%左右,当热解温度继续升高至500℃时的平均去除率达到80%左右。500℃热解的沙棘果渣生物炭对EP的吸附率最高,其原因可能是BC500的微孔数量最多,孔隙度和比表面积最大,吸附率相应最高。
2.2.2 温度对沙棘果渣生物炭吸附EP的影响
BC300、BC400、BC500分别在25、35、45℃吸附4 h后的EP去除率如图3所示。三种热解温度下的沙棘果渣生物炭对EP的去除率随温度的升高整体上呈逐渐增加的趋势。从图3可知,BC300对EP的最大去除率为52.2%,出现在EP初始浓度30 mg/L、吸附温度为45℃时;BC400对EP的最大去除率为71.3%,出现在EP初始浓度20 mg/L、吸附温度为45℃时;BC500对EP的最大去除率为90.9%,出现在EP初始浓度20 mg/L、吸附温度为45℃时。随着EP初始浓度的加大,BC300、BC400、BC500对EP的去除率逐渐降低。

图3 温度对BC300、BC400、BC500吸附不同浓度EP的影响
从整体上看,高温有利于吸附。温度对EP的吸附有明显的影响,在所选温度范围内,随着温度的升高,去除率逐渐增加,在45℃下,BC500对初始浓度20 mg/L的EP的去除率高达91%。
物理吸附过程一般是放热反应,温度升高不利于吸附的进行,化学吸附有些是吸热反应,有些是放热反应,总体上认为温度升高有利于化学键的形成从而有利于化学吸附。
2.2.3 沙棘果渣生物炭对EP的吸附率随时间的变化
从图4可知,在反应开始阶段,沙棘果渣生物炭对EP的去除率增速较快,在最开始的30 min内增加迅速,随着反应的进行,去除率逐渐增大,在30 min至150 min内吸附率缓慢上升,之后吸附过程慢慢趋于平稳,反应进行210 min后,延长反应时间,去除率基本保持不变,在充分振荡270 min后吸附反应达到平衡。由此可知,用沙棘果渣生物炭吸附EP,作用时间为270 min,吸附反应即可达到平衡状态。随着吸附时间的推移,沙棘果渣生物炭能够继续保持较高的去除率,几乎没有出现解吸现象,说明在吸附位点形成了较强的化学键,一旦吸附就不容易解吸。在相同的吸附时间内,三种生物炭对EP吸附能力高低为:BC500>BC400>BC300。当达到吸附平衡后,BC300的吸附率约为50%,BC400的吸附率接近59%;BC500的吸附率在74%左右。

图4 沙棘果渣生物炭对EP的吸附率与吸附时间的关系
2.3 吸附等温模型
由表1可知,不同吸附温度下沙棘果渣生物炭对EP的吸附均符合Langmuir和Freundlich 吸附等温方程。Langmuir方程中b代表吸附平衡常数,是吸附与解析速率常数的比值,b值越大,表明吸附能力越大。由表1可见,随吸附温度的降低,b值变小,说明高温有利于生物炭对EP的吸附。Freundlich方程中吸附常数K反映吸附能力的强弱,K值越大,表征吸附能力越强。由表1可见,随吸附温度的降低,K值变小,说明降低温度不利于生物炭对EP的吸附。BC300的Freundlich方程中的吸附常数K随温度的升高而降低,说明 BC300有可能同时存在是物理吸附与化学吸附,不同于 Langmuir的単分子层吸附理论,Freundlich是经验公式,Freundlich方程的拟合结果与实际情况可能存在偏差。
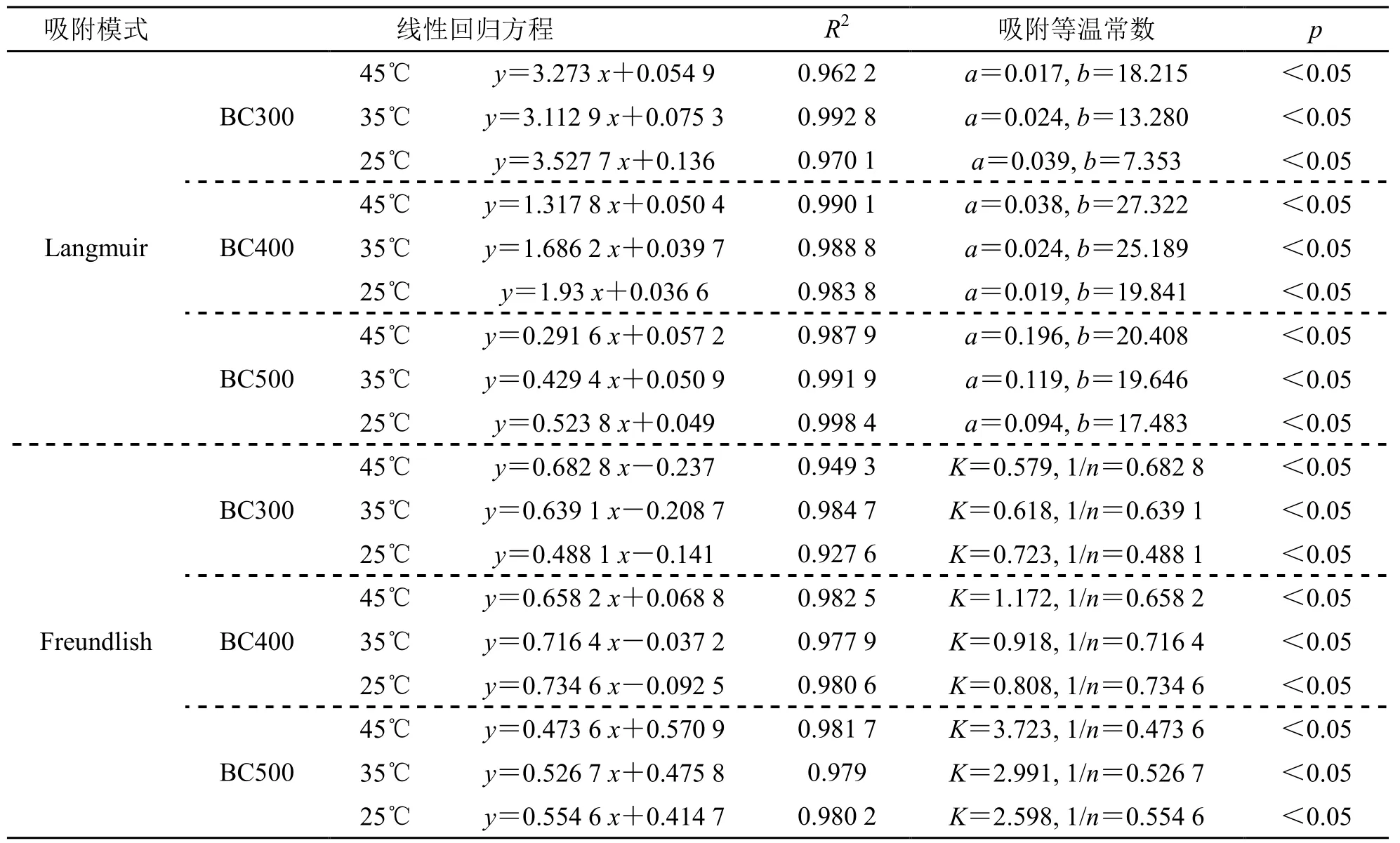
表1 Langmuir和Freundlich模式吸附常数和确定系数
2.4 讨论
俞花美[9]的研究表明,生物炭对阿特拉津的吸附是一个先快后慢的过程,Freundlich 模型对阿特拉津在生物质炭土壤上的吸附数据拟合结果均较好。在本研究中,生物炭对EP的吸附也是一个先快后慢的过程,在270 min后达到吸附平衡。郎印海[10]用花生壳和小麦秸秆制备生物炭吸附水中的五氯酚,发现同种原料不同热解温度下生物炭吸附效果表现为 400℃>600℃>300℃,这与本文的研究结果不同,可能是由生物炭的制备原材料差异所导致的;与本文研究结果高温有利于沙棘果渣生物炭吸附EP不同的是,他们发现低温有利于花生壳和小麦秸秆生物炭吸附五氯酚,这可能是由生物炭性质的不同和吸附对象不同而导致的。代银分[11]等研究表明,Langmuir方程能很好的描述水葫芦、秸秆、松针等五种来源不同的生物炭对磷的等温吸附,与上述研究结果相似,本文也发现Langmuir方程能够很好的描述生物炭对EP的等温吸附。由于生物炭表面含氧基团呈碱性的独特性质,使生物炭在改善土壤环境,提高土壤肥效,改善植物生长环境,保护环境等方面都有巨大潜力,张振国[12]等指出在黄土中添加由小麦秸秆制成的生物炭可以有效地提高黄土对 NP 的饱和吸附量。表明在土壤中添加生物炭,能有效地减少土壤污染,生物炭在治理农业面源污染、提升耕地质量、修复污染农田、应对气候变化、维持和稳定农业生态系统功能及保障农业环境安全等方面具有重要意义和应用价值。
3 结论
1)沙棘果渣生物炭对低浓度尼泊金乙酯有较强的吸附作用,作为一种新型的吸附剂,原料易得且制作方法简单,具有较高的开发应用价值。
2)热解温度为500℃时,沙棘果渣生物炭对尼泊金乙酯的去除率最大。在45℃下,500℃生物炭对初始浓度为20 mg/L EP的去除率接近91%。BC300对EP的最大去除率为52.2%,出现在EP初始浓度30 mg/L、吸附温度为45℃时;BC400对EP的最大去除率为71.3%,出现在EP初始浓度20 mg/L、吸附温度为45℃时;BC500对EP的最大去除率为90.9%,出现在EP初始浓度20 mg/L、吸附温度为45℃时。沙棘果渣生物炭是一种很好的吸附剂,在污水处理领域有广阔应用前景。
3)沙棘果渣生物炭对尼泊金乙酯的吸附等温线符合Langmuir和Freundlish两种模式。
