荷叶中荷叶碱的溶出度考察△
2018-10-17韩婷婷任晓亮任德飞王萌
韩婷婷,任晓亮,任德飞,王萌
(天津中医药大学 中药学院,天津 300193)
荷叶为睡莲科植物荷叶NelumbonuciferaGaerth.的干燥叶,味苦涩,性平,其作为天然有效的保健食品和药物,越来越受到人们的青睐。荷叶中含有的荷叶碱是一种阿朴啡型生物碱,药理研究表明其为荷叶中主要的降脂成分[1]。中药材的有效成分含量直接影响中成药和中药饮片的质量。在中药中,有效成分从药材中转移至提取液中,除受溶解度的影响,还受溶出度的影响。本实验对不同粒径荷叶粉体中荷叶碱的体外溶出度进行研究,考察在不同粒径、pH下溶出规律,并采用Weibull模型进行拟合,初步探讨粉碎度及pH对有效成分溶出度的量变关系。采用相对较正因子法(f2)对不同条件下的溶出曲线进行相似性评价,以期为中药开发和应用提供方法和思路。
1 材料
1.1 药品
对照品荷叶碱(批号:111566-2000703,含量99.7%)购于中国食品药品检定研究院。
药材:荷叶(产地:山东),为莲NelumbonuciferaGaerth.的叶(鉴定专家:天津中医药大学,李天祥教授)。
1.2 试剂
甲醇(美国sigma公司,色谱纯);乙醇(天津市康科德科技有限公司,分析纯);甲酸(天津化学试剂批发公司,分析纯);蒸馏水(屈臣氏集团有限公司)。
1.3 仪器
Waters ACQUITY UPLCTM超高效相色谱仪,美国Waters公司;Shimadzu LC-20AT高效液相色谱仪,日本Shimadzu公司;TG16-WS台式高速离心机,长沙湘仪离心机仪器有限公司;S312-90电动搅拌器,山海申生科技有限公司;PB-10 pH计,德国Sartorius公司;BT125D十万分之一天平,德国Sartorius公司;2、4、5、6、7号药典筛,浙江上虞市五星冲压筛具厂。
2 方法与结果
2.1 粒径、pH值对荷叶中荷叶碱体外溶出度的影响
2.1.1 色谱条件及方法学考察
2.1.1.1 色谱条件 色谱柱:Acquity UPLC BEH shield RP18(2.1×100 mm,1.7 μm)(Waters科技有限公司)
流动相:B为甲醇,A为0.1%甲酸-水,进样量:3 μL;流速:0.2 mL·min-1;柱温:45 ℃。检测波长:270 nm。荷叶碱的保留时间为5.64 min。
2.1.1.2 对照品的配制 称取荷叶碱对照品4.03 mg于5 mL容量瓶中,加甲醇溶解并定容制成0.806 g·L-1的对照品贮备液。
2.1.1.3 标准曲线的绘制 取对照品溶液适量,加甲醇配制成0.787 1 μg·mL-1至50.38 μg·mL-1的对照品溶液,进样分析并记录峰面积。以对照品质量浓度C(μg·mL-1)为横坐标,峰面积(A)为纵坐标,以最小二乘法求得回归方程,荷叶碱回归方程Y=45 441X-4 523.4(r=0.999 9),结果表明荷叶碱在0.787 1~50.38 μg·mL-1线性关系良好。
2.1.1.4 精密度试验 精密吸取细粉样品,连续进样6次,以峰面积计,RSD为0.4%,表明仪器精密度良好。
2.1.1.5 重复性试验 取荷叶细粉10 g,精密称定,分别置于溶出杯中,浆降入溶出介质中,以脱气纯净水900 mL为溶出介质,温度为(37.0±0.5) ℃,转速为100 r·min-1,搅拌2 h,吸取溶液2 mL,离心取上清液,经0.22 μm滤膜过滤,按照“2.1”项色谱条件测定,平行6份,RSD为2.6%,重复性良好。
2.1.1.6 稳定性试验 取“2.1.1.5”项下配制好的溶液,室温放置,分别于0、2、4、8、12、24 h测定,RSD% 为2.7%,样品溶液在24 h内稳定。
2.1.1.7 加样回收率 向配制好的样品溶液中加入一定量荷叶碱对照品,测定其含量,测得荷叶碱加样回收率为96.98%,RSD为2.3%,符合方法学要求。
2.1.2 不同粒径荷叶粉体制备 取荷叶药材适量,经粉碎机粉碎过筛得粗粉、中粉、细粉、最细粉:
粗粉(全过2号筛,能通过4号筛的为20%);
中粉(全过4号筛,能通过5号筛的为30%);
细粉(全过5号筛,能通过6号筛的为97%);
最细粉(全过6号筛,能通过7号筛的为97%)。
2.1.3 不同pH缓冲溶液配制 pH 1.2盐酸溶液:取8.33 mL盐酸稀释至1000 mL;
pH 4.5磷酸缓冲溶液:取0.2 mol·L-1磷酸二氢钾250 mL,加至1000 mL量瓶中,稀释至刻度;
pH 6.8磷酸缓冲溶液:取0.2 mol·L-1磷酸二氢钾250 mL,加至1000 mL量瓶中,加0.2 mol·L-1氢氧化钠119 mL,稀释至刻度,以pH计对所制备的溶液进行校正。
2.1.4 不同粒径荷叶中荷叶碱溶出度的测定[2-5]采用2015年版《中华人民共和国药典》(二部)制剂通则0931溶出度测定方法中第二法进行测定。以脱气纯净水900 mL为溶出介质,温度(37.0±0.5) ℃,转速为100 r·min-1,取荷叶粗粉、中粉、细粉、最细粉10 g(平行3份)分别置于杯中,浆降入溶出介质中立即计时,至1、5、10、15、20、40、60、80、100 min时取样2 mL,离心取上清经微孔滤膜(0.22 μm)滤过,备用(同时补充同温介质2 mL及离心沉淀)。按“2.1.1”项下色谱条件测定荷叶碱溶出量,计算累积溶出百分率,并绘制累积溶出曲线。不同粒径荷叶中荷叶碱累积溶出曲线见图1;不同粒径荷叶中荷叶碱溶出量见表1。
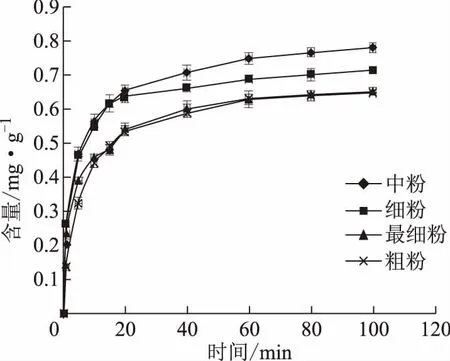
图1 不同粒径荷叶粉体中荷叶碱累积溶出量曲线

t/min粗粉/mg·g-1中粉/mg·g-1细粉/mg·g-1最细粉/mg·g-110.135 1±0.0090.202 4±0.0090.264 0±0.0130.233 5±0.00550.323 1±0.0170.469 1±0.0200.464 2±0.0030.391 1±0.010100.437 8±0.0120.561 2±0.0230.548 7±0.0030.457 0±0.010150.492 5±0.0120.615 7±0.0240.615 3±0.0120.481 0±0.015200.533 5±0.0100.653 4±0.0160.633 3±0.0140.538 9±0.022400.585 0±0.0100.706 3±0.0210.660 9±0.0100.600 1±0.025600.626 6±0.0160.747 8±0.0160.686 9±0.0110.628 1±0.010800.637 8±0.0150.765 4±0.0130.700 4±0.0190.643 0±0.011 11000.645 3±0.0080.778 4±0.0150.714 4±0.0080.650 4±0.013
2.1.5 不同pH荷叶中荷叶碱溶出度的测定[6-7]采用2015年版《中华人民共和国药典》(四部)制剂通则0931溶出度测定方法中第二法进行测定。以脱气pH 1.2,pH 4.5,pH 6.8,蒸馏水(试验中蒸馏水pH 6.79)900 mL为溶出介质,温度为(37.0±0.5) ℃,转速为100 r·min-1,取荷叶细粉,置不同pH溶液中(平行三份),浆降入溶出介质中立即计时,至1,5,10,15,20,40,60,80,100 min时取样2 mL,离心取上清经微孔滤膜(0.22 μm)滤过,备用(同时补充同温介质2 mL及离心沉淀)。按“2.1.1”项下色谱条件测定荷叶碱溶出量,计算累积溶出百分率,并绘制累积溶出曲线图2。不同pH下粉体中荷叶碱溶出量见表2。
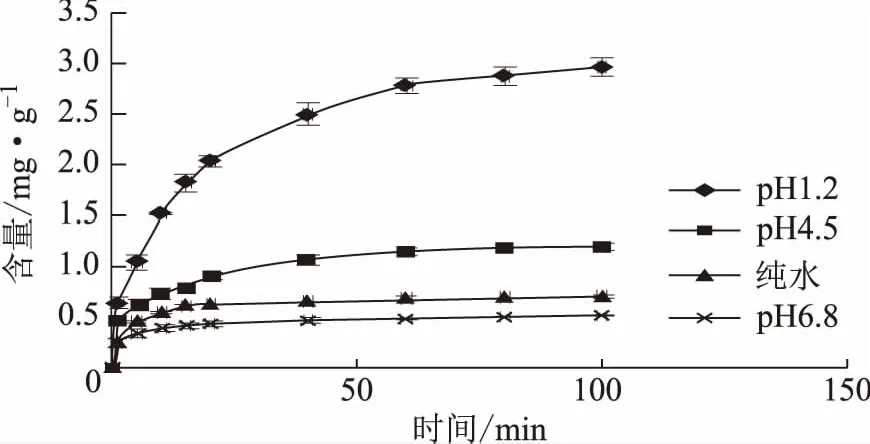
图2 荷叶细粉在不同pH溶液中荷叶碱累积溶出曲线
2.1.6 Weibull分布参数的处理 分别以不同粒径荷叶粉体2 h溶出量0.662 5,0.790 8,0.738 4,0.668 1 mg·g-1为荷叶粗粉、中粉、细粉、最细粉中荷叶碱100%溶出量。以细粉在不同缓冲溶液中2 h的溶出量3.005,1.200,0.539 9,0.738 4 mg·g-1作为pH 1.2,pH 4.5,pH 6.8,纯水中的平衡溶出量[8-10]。
根据荷叶碱的累积溶出百分率,按照Weibull模型进行数据处理,以X=lnt、Y=ln[-ln(1-F)]为变量(F为累积释放百分数),求得不同粒径、不同pH下荷叶粉体中荷叶碱的溶出时间与累积溶出百分率的关系,结果见表3。
并求出各溶出度参数T50、Td、Q45、m(T50:累计溶出50%的时间;Td:累积溶出63.2%的时间;Q45:45 min时的累积溶出率;m:曲线形状参数),结果见表4。
不同粒径荷叶粉体荷叶碱溶出量无显著性差异(P>0.05),采用Weibull模型对数据处理,由拟合所得溶出度参数计算荷叶碱溶出速率。至各样品溶出50%进行考察,溶出速率:细粉>最细粉>中粉>粗粉;不同pH下,溶出速率为pH 6.8>水>pH 4.5>pH 1.2。
表2 不同pH下荷叶细粉中荷叶碱累积溶出量
注:水由超纯水仪制备,pH 6.77。

表3 不同粒径、不同pH荷叶粉体中荷叶碱溶出回归方程(X=lnt,Y=ln[-ln(1-F)])

表4 不同粒径、不同pH下荷叶粉速率溶出参数
注:T50:累计溶出50%的时间;Td:累积溶出63.2%的时间;Q45:45 min时的累积溶出率;m:曲线形状参数。

图3 不同粒径荷叶碱溶出拟合曲线(X=lnt,Y=ln[-ln(1-F)])
2.1.7 相似因子法(f2)评价溶出曲线的相似 相似因子法为美国FDA推出的采用溶出曲线评价药物内在品质的方法,计算公式如下:
(1)
Rt为参比制剂平均累积溶出量,Tt为t时间自制制剂的溶出度,n为取样点数目(3≤n≤5,参比制剂累积溶出量大于85%的取样点数目≤1)。若50≤f2<100,则认为两条溶出曲线相似[11]。荷叶细粉在pH 1.2盐酸溶液,pH 4.5,pH 6.8磷酸缓冲溶液和水中f2分别为89.7,99.2,99.8(n=5),表明各缓冲溶液中荷叶碱溶出行为与其在水中溶出行为具有相似性。
不同粒径荷叶粉体在蒸馏水中溶出行为,粗粉与中粉、粗粉与细粉、粗粉与最细粉间的f2分别为99.84,99.85,99.97(n=5),表明在蒸馏水中,各粒径荷叶粉体中荷叶碱溶出规律与粗粉中荷叶碱溶出规律具有相似性。
3 讨论
3.1 采用Weibull模型考察粒径和pH对荷叶碱溶出规律结果
不同粒径荷叶粉体中荷叶碱的溶出量随时间延长而增加,溶出量为中粉>细粉>粗粉>最细粉。提示不同粒径粗粉、中粉、细粉、最细粉荷叶碱体外溶出过程中宜将粒径控制在适宜范围,不宜过细,为药材粉碎工艺提供参考。不同pH溶出介质中,溶出量为pH 1.2>pH 4.5>水>pH 6.8,即随pH的降低溶出量增大。
3.2 Weibull模型参考意义
不同pH溶出介质中,荷叶中荷叶碱溶出量随时间延长增加。pH 4.5,pH 6.8,蒸馏水中细粉在60 min后荷叶碱溶出量增加趋于平缓,pH 1.2缓冲溶液中荷叶细粉中荷叶碱在80 min后溶出量趋于平缓。建立与溶出度有关的Weibull模型,具有一定参考意义,因Weibull模型只能描绘不能充分突出药物溶出动力学性质[12]。试验中分别采用超声、浆法对平衡溶出量进行了测定,当超声测定所得溶出量与100 min时测得溶出量相差较大时,采用Weibull方程拟合所得曲线线性关系较差,故采用浆法120 min所得荷叶碱含量作为溶出量。从溶出量分析,荷叶粉体在所考察的溶出介质经2 h后溶出量不存在显著性差异。
3.3 相似因子法(f2)评价溶出曲线的相似性
结果显示各粒径荷叶粉体中荷叶碱溶出行为与粗粉中荷叶碱溶出规律具有相似性;各缓冲溶液中荷叶碱溶出行为与荷叶碱在水中溶出行为具有相似性。
