瑞舒伐他汀在蛛网膜下腔出血早期脑损伤中的作用机制研究
2018-10-12,,
, ,
自发性蛛网膜下腔出血是一种常见的急性脑血管事件。据统计,其在西方国家的发生率约为9/10万。尽管只占全部中风事件的5%,但蛛网膜下腔出血的预后很差,死亡率和致残率均较高[1]。
早期脑损伤通常于蛛网膜下腔出血后72 h内发生,其机制包括颅内压升高,氧化应激导致炎症,血脑屏障破坏和脑缺血。这些因素共同导致神经元细胞死亡和脑水肿,加重颅内压以及早期脑损伤[2]。
他汀类药物是羟甲基戊二酸单酰辅酶A还原酶抑制剂,除作为降胆固醇药物,还具有对抗炎症[3]、抗氧化[4]、抗脑血管痉挛以及抑制血小板聚集[5]的作用。然而他汀类药物对蛛网膜下腔出血后早期脑损伤的作用和机制尚未阐明。本研究探讨瑞舒伐他汀对蛛网膜下腔出血后早期脑损伤的作用和机制。
1 材料与方法
1.1 动物处理 实验中所用81只新西兰白兔购自无锡太湖医院动物中心。实验前对白兔投喂标准饲料,饲养于正常湿度和完成22 ℃室温下。瑞舒伐他汀的喂服剂量为5 mg/(kg·d)。在蛛网膜下腔出血模型完成之前3 d和22 h之后测定白兔血压和体重,并给予瑞舒伐他汀灌胃,每日1次。在蛛网膜下腔出血模型完成后第24小时评价白兔神经损伤状况,之后立即处死白兔。
1.2 实验方法 随机将81只白兔分为3组:假手术组、蛛网膜下腔出血组(出血组)和瑞舒伐他汀治疗组(治疗组),各27只。治疗组灌服瑞舒伐他汀方法如前述。通过灌注固定处死每组各9只白兔,取各组处死白兔的海马体进行原位末端标记染色;再取每组各9只白兔,进行脑组织水含量检测;最后的每组各9只白兔处死后取出脑组织,干燥冷冻,用于检测相关生化指标。在处死白兔前,通过股静脉抽取各组白兔血液标本进行内皮素1(ET-1)检测。
1.3 蛛网膜下腔出血模型制备 利用10%的水合氯醛对白兔进行麻醉。在无菌条件下,用23号蝴蝶针穿刺至小脑延髓池,在流出1 mL脑脊液时,说明穿刺针进入蛛网膜下腔,注入2 mL未抗凝的自体血液。所有白兔均采取低头30°角体位30 min,以确保血液从小脑延髓池顺利进入基底池。之后将白兔送回动物房,并于48 h后进行第2次注血,方法同前。
1.4 行为评分 对所有的白兔进行行为评分,评价神经功能,评分标准详见表1。

表1 行为评分标准
1.5 脑组织含水量检测 在处死白兔后获取脑组织立即称重,之后将脑组织置于100 ℃下24 h,再次称重。依据公式(湿重-干重)/湿重×100%计算脑组织含水量百分比。
1.6 灌注-固定脑组织 将每组各8只白兔应用10%水合氯醛进行麻醉。之后迅速开胸,在白兔左心室进行插管,并切开右心房。先用1 500 mL生理性磷酸盐缓冲液灌注,之后应用1 000 mL 10%甲醛缓冲液灌注。灌注完成后,脑组织将固定于甲醛溶液中。
1.7 细胞及生化指标检测 细胞凋亡采用原位末端标记法检测;应用酶联免疫吸附试验检测ET-1;采用Western blot检测水孔蛋白4和半胱天冬酶3。

2 结 果
2.1 基本情况 在实验间隔期和实验末期,各组血压和体重比较差异无统计学意义。蛛网膜下腔出血组死亡率为33.3%(9/27),治疗组死亡率为18.5%(5/27),假手术组无死亡白兔。治疗组死亡率显著低于蛛网膜下腔出血组(P<0.05)。在构建模型的过程中,根据死亡数据补充新的白兔进行造模。
2.2 行为评分 出血组和治疗组的行为评分均显著高于假手术组(P<0.01),而治疗组的行为评分显著低于出血组(P<0.05)。表明瑞舒伐他汀能够提高蛛网膜下腔出血后白兔的神经功能。详见图1。

与假手术组比较,*P<0.01;与出血组比较,#P<0.05。
图1各组行为评分比较
2.3 脑组织水含量 出血组和治疗组脑组织水含量较假手术组显著增加(P<0.01),而治疗组脑组织水含量显著低于出血组(P<0.01)。详见图2。
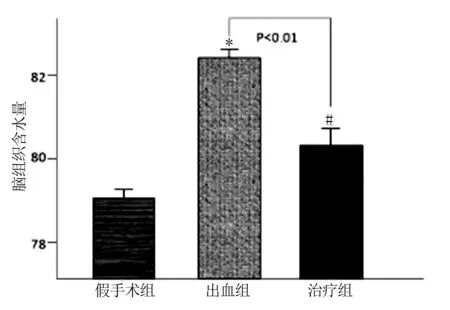
与假手术组比较,*P<0.01;与出血组比较,#P<0.01。
图2各组脑组织水含量比较
2.4 原位末端标记染色和死亡细胞检测 假手术组中原位末端标记染色几乎未见到染色阳性细胞。治疗组和出血组染色阳性细胞显著多于假手术组,而治疗组阳性细胞数显著低于出血组。详见图3。
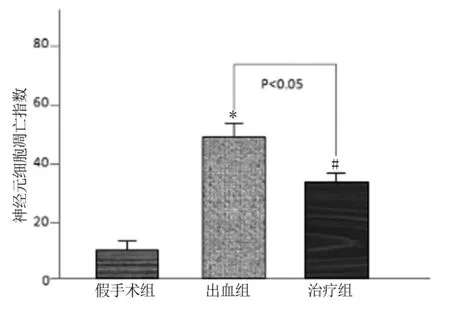
与假手术组比较,*P<0.01;与出血组比较,#P<0.05。
图3各组海马体神经元细胞凋亡指数比较
2.5 ET-1蛋白表达 与假手术组比较,出血组和治疗组ET-1蛋白表达水平均显著增加(P<0.01)。而治疗组显著低于出血组(P<0.01)。详见图4。
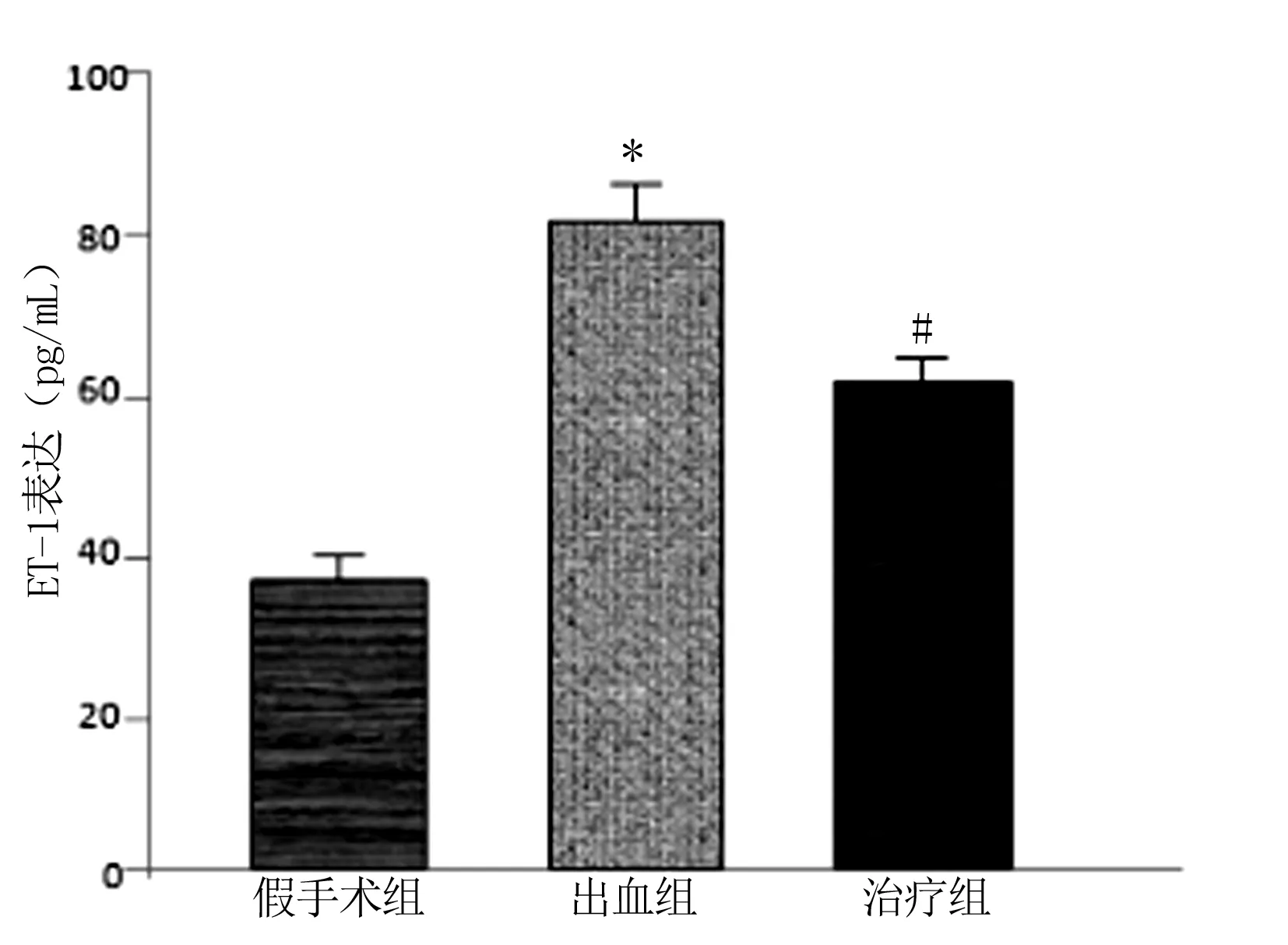
与假手术组比较,*P<0.01;与出血组比较,#P<0.01。
图4各组脑组织ET-1表达水平比较
2.6 水孔蛋白4表达 出血组水孔蛋白4表达水平显著高于假手术组(P<0.05);而治疗组显著降低了蛛网膜下腔出血引起水孔蛋白4表达,与出血组比较差异有统计学意义(P<0.05)。详见图5。
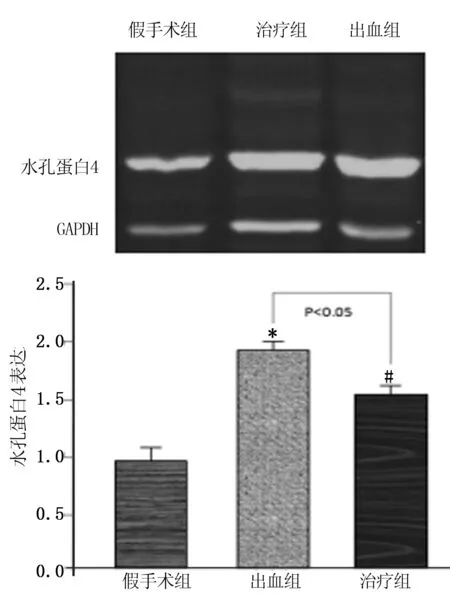
与假手术组比较,*P<0.01;与出血组比较,#P<0.05。
图5各组水孔蛋白4表达水平比较
2.7 半胱天冬酶3表达 蛛网膜下腔出血显著增加了半胱天冬酶3在海马体中的表达,而治疗组半胱天冬酶的表达水平显著低于出血组(P<0.05)。详见图6。
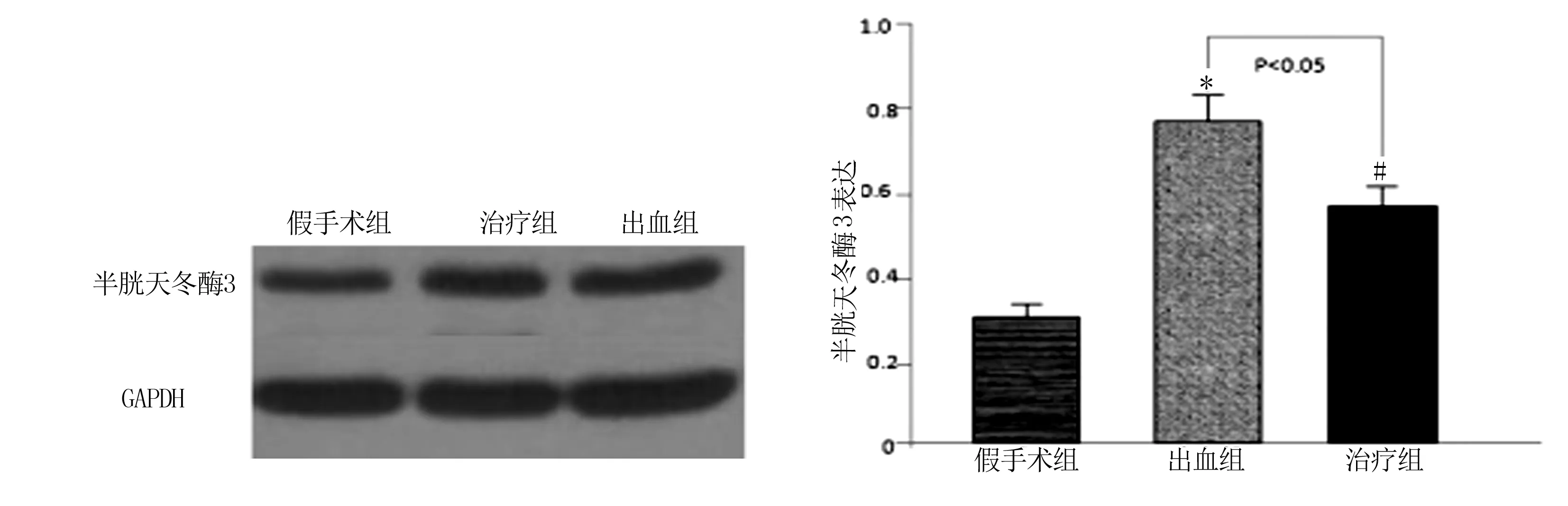
与假手术组比较,*P<0.01;与出血组比较,#P<0.05。
图6各组半胱天冬酶3表达水平比较
3 讨 论
瑞舒伐他汀是一种羟甲基戊二酸单酰辅酶A还原酶抑制剂,前期相关研究证实他汀类药物具有对抗炎症、抗氧化、抗脑血管痉挛以及抑制血小板聚集的作用。蛛网膜下腔出血引发的早期脑损伤机制包括颅内压升高,氧化应激导致炎症,血脑屏障破坏和脑缺血。本研究探讨瑞舒伐他汀对蛛网膜下腔出血后早期脑损伤的作用和分子机制。
本实验中采取二次注血的方式构建了蛛网膜下腔出血模型,过程中,假手术组未见动物死亡,而出血组和治疗组分别发生9例和5例动物死亡,两组动物死亡率比较差异有统计学意义(P<0.05)。提示瑞舒伐他汀能够增加蛛网膜下腔出血白兔的耐受性,降低其死亡率。本研究结果显示,出血组和治疗组行为评分较假手术组升高,而治疗组行为评分显著低于出血组。表明瑞舒伐他汀能改善蛛网膜下腔出血导致的神经功能障碍。通过比较各组白兔实验后的脑组织水含量,证实了蛛网膜下腔出血后又发生了显著的脑水肿,而瑞舒伐他汀能够减轻脑水肿,进而改善神经功能。原位末端标记染色显示,与假手术组比较,出血组和治疗组海马体神经元细胞死亡数显著增加,而瑞舒伐他汀可降低神经元细胞死亡数。以上结果表明,瑞舒伐他汀能够在蛛网膜下腔出血早期减轻脑水肿,降低神经元细胞死亡,改善神经功能,增加白兔对于蛛网膜下腔出血的耐受性。
ET-1能够与平滑肌上的特殊受体结合,引发血管收缩和内皮细胞增殖,这一过程能够破坏体内水平衡,加重蛛网膜下腔出血后脑水肿[6]。相关研究证实,水孔通道蛋白4促进脑水肿过程中的水聚集,加重脑水肿症状[7]。本研究结果显示,瑞舒伐他汀可降低蛛网膜下腔出血白兔的脑组织ET-1和水孔通道蛋白4表达,但具体机制仍需进一步研究。蛛网膜下腔出血早期损伤中伴随神经元细胞坏死和凋亡。本研究检测细胞凋亡相关因子半胱天冬酶3,证实在蛛网膜下腔出血动物中半胱天冬酶3显著升高,而瑞舒伐他汀能降低半胱天冬酶3水平。表明瑞舒伐他汀可能通过抑制半胱天冬酶3表达来抑制蛛网膜下腔出血白兔神经元细胞死亡。
综上所述,瑞舒伐他汀能够通过抑制ET-1、水孔通道蛋白4和半胱天冬酶3的表达来抑制蛛网膜下腔出血脑组织水肿和神经元坏死,改善早期脑损伤预后。
