血管内再通治疗症状性非急性期颅内大动脉闭塞初步效果
2018-09-29王永亮谭华桥徐霁充韩洪杰
王永亮, 马 林, 谭华桥, 方 淳, 封 灏, 徐霁充, 严 烁, 韩洪杰
既往认为亚急性和慢性颅内大血管闭塞患者已建立侧支循环,不宜进一步手术干预。但近年研究发现症状性颅内大动脉亚急性和慢性闭塞是不良预后、死亡和脑卒中复发的独立预测因素[1]。尤其是伴有血流动力学障碍患者,尽管接受严格药物治疗,症状仍可能持续[2],再发脑卒中风险达 6%~22.7%[3-5]。此外,颅内大动脉慢性闭塞患者长期接受颅内低灌注,可导致认知功能障碍[6]。近年国内外不少医疗中心尝试采用血管内再通术治疗症状性颅内大血管非急性期闭塞,但大多涉及椎-基底动脉[7-15],前循环颅内段大血管相关报道甚少[16-18]。 有关颅内大动脉非急性期闭塞血管内再通术患者选择、再通技术及相关并发症等经验仍相当欠缺。本研究回顾性收集15例症状性非急性期颅内大动脉闭塞血管内再通术患者临床资料,探讨该血管内再通治疗可行性、安全性和近期效果。
1 材料与方法
1.1 临床资料
本研究得到上海市同济医院医学伦理委员会批准,入选患者均签署知情同意书。2015年10月至2017年12月共收治15例亚急性及慢性颅内大动脉闭塞患者(表1),其中男14例,女1例,中位年龄60(32~71)岁;首次发病至血管再通中位时间30(2~120)d,影像学证实颅内大动脉闭塞至血管再通中位时间11(2~60)d。术前所有患者均经严格内科药物治疗,12例临床症状仍反复发作,3例进展;改良 Rankin量表(mRS)评分 1分 6例,2分 4例,3分3例,4分2例;前循环闭塞13例[大脑中动脉(MCA)M1段10例,颈内动脉(ICA)C6段 3例],后循环闭塞2例(优势侧椎动脉V4段伴另侧椎-基底交界重度狭窄1例,双侧椎动脉V4段1例);闭塞远端前向血流检测显示脑梗死溶栓(TICI)血流分级0级5例,1级10例;头颅MRI均显示脑梗死,其中10例为亚急性期或慢性期分水岭型;头颅CT灌注(CTP)成像或MR灌注加权成像(PWI)均提示闭塞血管供血区域灌注较正常侧明显降低,美国介入和治疗性神经放射学会(ASITN)/美国介入放射学学会(SIR)侧支循环分级≤3。
患者纳入标准[8-12,15,18]:①CTA/MRA 诊断且DSA造影证实颅内大动脉,包括ICA颅内段、MCA M1段、优势侧椎动脉V4段、基底动脉闭塞,闭塞远端前向血流TICI分级0~1级,且预估闭塞时间48 h~3个月;②经严格内科药物治疗仍反复有短暂性脑缺血发作(TIA)和/或卒中,或症状进展如美国国立卫生研究院卒中量表(NIHSS)评分增加4分或mRS评分增加1分以上,或存在血流动力学障碍如直立位或血压低时症状加重;③MRI表现为分水岭梗死或头颅CTP或PWI存在灌注不良,或ASITN/SIR侧支循环分级≤3;④闭塞远端存在血管床,且闭塞血管直径预估>2 mm,闭塞段长度<15 mm。排除标准:①原发性或继发性血管炎所致颅内大血管闭塞;②梗死后出血转化或非闭塞血管供血区新发脑梗死所致症状波动;③预估闭塞时间>3个月或闭塞段长度>15 mm;④闭塞段血管壁严重弧形钙化或闭塞段严重成角;⑤严重感染、高热、心肾功能不全、低血容量或全身性低血压所致症状波动;⑥氯吡格雷、阿司匹林抵抗或不耐受;⑦>80岁高龄或伴发其它疾病,预期生存时间<2年。

表1 15例颅内非急性期大动脉闭塞患者临床资料及血管内再通治疗结果
1.2 血管内再通术
术前均予所有患者口服双联抗血小板药物(阿司匹林 100 mg/d,氯吡格雷 75 mg/d)3~5 d,并完善血栓弹力图检查。控制血压、血糖、血脂等危险因素。术前12 h禁食,术前2 h始微泵注入尼莫地平(2 mL/h)预防脑血管痉挛。
手术在全身麻醉下进行,全身肝素化,维持活化凝血时间(ACT)在250~300 s,控制收缩压在100~120/60~80 mmHg(1 mmHg=0.133 kPa),穿刺股动脉成功后置入6 F导管鞘,6 F导引导管送至闭塞血管近端ICA或椎动脉建立路径。对椎-基底动脉闭塞和ICA颅内段闭塞,参照既往非急性期血管内再通方法[8-11],造影确认闭塞血管长度、远端血管床,双血管同步路图下Echelon-10微导管(美国ev3公司)和Traxcess-14微导丝(美国MicroVention公司)相互配合探查通过闭塞段;对MCA M1段闭塞,若同侧大脑前动脉A1段发育正常,MCA供血区由同侧软脑膜支部分代偿,则经同侧ICA造影确认闭塞血管长度、远端血管床,若同侧A1段发育不良或不发育,由对侧ICA经前交通部分代偿,则双侧ICA造影确认闭塞血管长度、远端血管床,路图下Echelon-10微导管和Traxcess-14微导丝相互配合探查通过闭塞段。微导管通过闭塞段后立即撤出微导丝,造影证实微导管头端位于闭塞段远端血管真腔,换用300 cm Transend微导丝(美国Boston科技公司),头端送至闭塞远端血管床,回撤微导管;根据预估闭塞段血管直径和长度选择合适规格球囊,沿交换导丝将其送至闭塞段进行预扩张,根据预扩张后血管造影、闭塞段近端血管迂曲程度及成角情况选择不同再通策略,如自膨式支架、球扩支架植入及单纯球囊扩张。术后即刻造影评估残余狭窄,根据TICI分级评估再通血管远端血流灌注。残余狭窄<30%,且TICI分级≥2b,定义为再通成功;TICI分级未改变或未达2b,定义为再通失败。
所有患者术后6~8 h均维持麻醉状态。术后即刻复查头颅CT排除脑出血,随后转至重症监护室。予排除脑出血患者替罗非班(2 mL/h)微泵注射维持24 h,此后1周维持双联抗血小板药物治疗,严格控制血压在100~120/60~80 mmHg,观察是否有新发神经功能缺损,术后3~7 d行头颅MR观察再通血管供血区是否有伴发新发脑梗死及其与新发神经功能缺损是否相关。记录围手术期并发症,如末梢栓塞、血管夹层/破裂、支架内急性亚急性血栓形成、高灌注综合征、穿支事件。出院后口服阿司匹林(100 mg/d)和氯吡格雷(75 mg/d)6~12 个月,随后口服阿司匹林(100 mg/d)维持。
1.3 术后随访
术后3、6、12个月随访,随后每年1次。随访时记录患者再通血管供血区是否有再发脑卒中或TIA,根据mRS评分评估功能改善情况,mRS评分减少1分或以上认为改善,无变化认为稳定,增加1分或以上认为加重(恶化);血管造影观察再通血管是否发生再狭窄或闭塞,记录再通血管管腔丢失直径。再狭窄定义为随访时再通血管较术后即刻管径丢失≥50%。
2 结果
15例患者中13例(86.7%)成功再通,2例失败(1例术中并发夹层前向血流TICI分级2a,1例微导丝导管无法通过闭塞段)。成功再通患者中7例为球囊扩张结合球扩支架植入,4例为球囊扩张结合自膨支架植入,1例支架机械取栓,1例单纯球囊扩张。术中发生末梢栓塞事件7例(症状性3例,无症状性4例),血管夹层1例;术后1例(支架机械取栓)出现脑出血,转至神经外科清除血肿。所有患者均存活,未发生高灌注综合征。成功再通患者中12例出院时症状好转,1例脑出血患者症状无明显改善;再通失败患者中1例症状波动并恶化,1例症状无明显改善。
13例获3~12个月血管造影随访,平均5.8个月。1例术中并发夹层再通失败患者术后3个月随访时病变段血管再闭塞,12例成功再通患者中1例术后12个月支架内再狭窄(约80%),再次球囊扩张后残余狭窄<20%,其余11例均无血流动力学意义上再狭窄。14例获3~12个月临床随访,平均5.6个月,12例成功再通患者中除1例支架内狭窄发生再通血管供血区相关TIA外,均无再发脑卒中;90 d mRS评分0分2例,1分8例,2分2例,均为功能改善;再通失败2例90 d mRS评分均恶化。
典型病例(患者 4):男,55岁,“突发左侧肢体无力伴口齿不清2周”入院。入院头颅MRI示右半卵圆区脑梗死(图1①);CTA示右ICA C6段闭塞,严格内科药物治疗2周,肢体症状无缓解且反应迟钝加重,mRS评分1分;CTP示右MCA区灌注不良(图1②);右ICA造影示右ICA C6段闭塞(图1③),左ICA和椎动脉造影示右侧一、二级侧支代偿不全,静脉循环时间较左侧延迟(图1④⑤)。术中微导丝成襻通过右ICA C6段闭塞段(图1⑥),头端到达闭塞段远端真腔(图1⑦),交换微导管置入300 cm Transend微导丝,依次以 1.5 mm×12 mm、2.5 mm×12 mm球囊缓慢预扩张闭塞段并予开通(1⑧⑨);植入 Apollo支架(3.5 mm×13 mm)1 枚(1⑩),复查造影示闭塞段血管成功再通,前向血流TICI分级3级(图1 ⑪)。出院时患者症状明显缓解,术后3个月mRS评分1分,复查造影示支架内狭窄(约40%)(图1 ⑫)。随访期间未再发任何脑缺血事件。
3 讨论
3.1 非急性期血管内再通术患者选择
颅内大动脉亚急性和慢性闭塞是一高度异质性疾病,其临床表现和预后因脑血管侧支循环代偿程度个体差异而不同。侧支循环代偿较好患者无任何临床症状,侧支循环代偿不良患者则发生头晕、反复脑卒中和TIA等事件。因此,对侧支循环代偿不良的颅内大动脉亚急性和慢性闭塞患者采取积极干预措施,已逐渐受到认可。近年国内外不少医疗中心基于颅内大血管急性闭塞血管内再通获益经验,对症状性非急性期颅内大血管闭塞患者尝试采用血管内再通治疗。许多研究表明,症状性非急性期颅内大动脉闭塞患者经选择予以血管内再通术,有助于预防反复脑血管缺血事件发生,促进患者残疾功能恢复,但开通技术复杂,并发症发生率高[7-18],因此选择最能从血管内再通治疗中获益患者至关重要。既往椎-基底动脉亚急性及慢性闭塞血管内再通研究表明,低灌注引起临床症状患者是最能从血管内再通治疗中获益人群[9-11]。本研究仅选择侧支循环代偿不良且经严格内科药物治疗效果仍不佳的亚急性和慢性闭塞患者行血管内再通治疗,此类患者发病机制上存在血流动力学障碍,理论上最有可能从血管内再通治疗中获益。本组13例成功再通患者中12例出院时临床症状明显改善,术后90 d mRS评分显示功能良好,除1例支架内80%再狭窄患者TIA发作外,均无再发脑卒中和TIA。
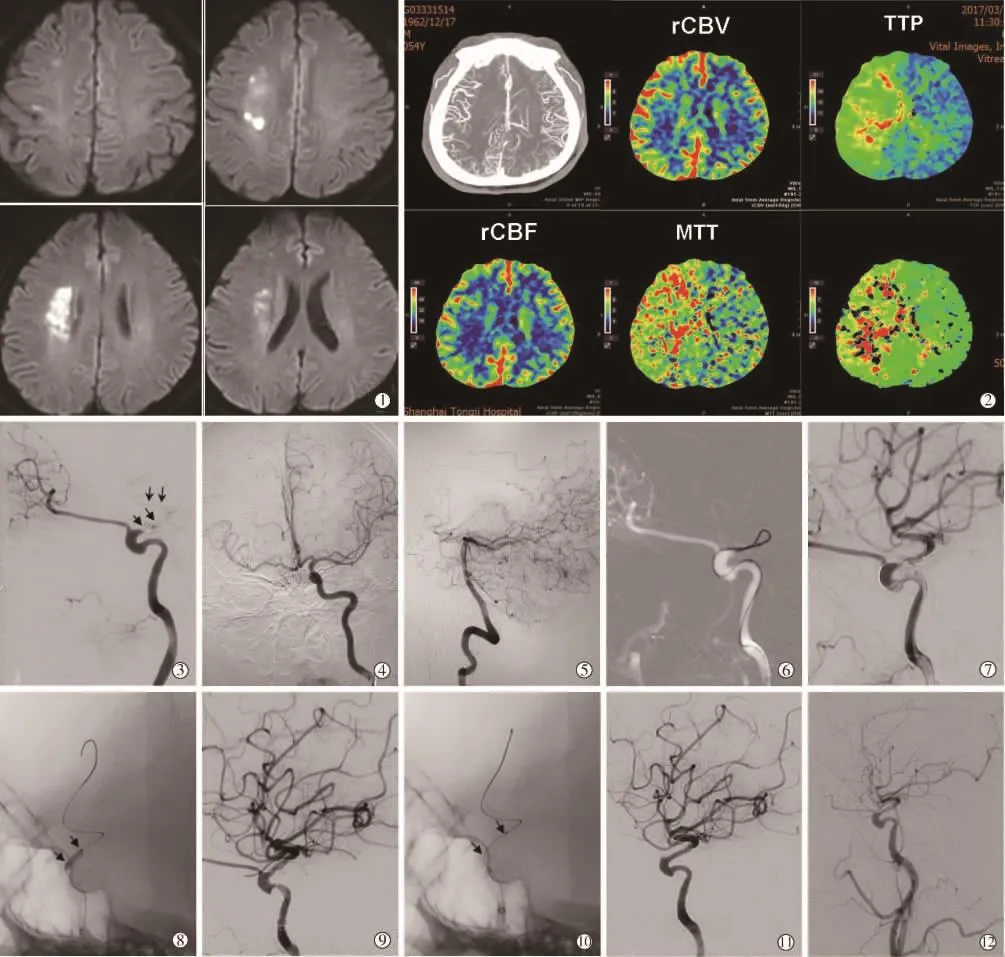
图1 典型病例血管内再通治疗前后影像
非急性期颅内大动脉闭塞血管内再通技术难度大。不同于颅内大动脉狭窄血管成形术,非急性期颅内大动脉闭塞病变段血管腔在DSA造影下无法显示,缺乏可视的血管路径,微导丝通过闭塞段缺乏导向,很大程度上依赖于术者操作经验。此外,微导丝能否顺利通过闭塞段,不仅取决于闭塞段病变性质、闭塞病变长度、闭塞时程,而且取决于闭塞段病变成角程度。闭塞长度和闭塞时间过长,血管内血栓发生机化、纤维化及钙化,导致斑块逐渐变硬,微导丝通过困难;闭塞长度过长和闭塞段病变严重成角很难判断血管走行,导丝探查过程中偏离闭塞段血管轴向极易导致穿孔、夹层。慢性冠状动脉完全闭塞血管内再通术经验表明,病变血管闭塞长度<15 mm,闭塞时间<3个月患者再通成功率高,而中度-严重钙化、闭塞近端血管或闭塞段严重成角病变血管再通成功率低[19-20]。本研究中入选预估闭塞时间3个月内患者,增加了微导丝通过病变可能性;通过头颅CTA或/和高分辨率MRI评估仅入选闭塞段长度<15 mm、闭塞段无严重成角和钙化患者,术前预判闭塞段血管走行,以确保再通技术可行,规避医源性风险;术中参照既往文献报道[8-11],对ICA颅内段及椎动脉闭塞采用双鞘-双血管同步路图导引,对MCA M1段闭塞则采用同侧动脉晚期图像作路图,以同时显影闭塞远端和近端血管,使术者对血管走行和闭塞段观察更为直观,对导丝和导管操控更有预见性;10例动脉早期显示血管闭塞,动脉晚期显示闭塞段远端极为缓慢前向血流患者中9例获得成功再通,因而推测与慢性冠状动脉完全闭塞病变血管内再通类似,闭塞远端前向血流TICI分级1级患者有可能预示可成功再通。
3.2 非急性期血管内再通潜在并发症
非急性期颅内大动脉闭塞血管内再通术另一重要忧虑是所伴随并发症,如末梢栓塞事件、血管夹层与穿孔、高灌注综合症、穿支血管闭塞以及支架内急性、亚急性血栓形成[7-11,17-18,21-22]。 文献报道并发症发生率为 8.3%~44%[7-8,10,13-15]。 末梢栓塞是主要并发症之一,是否会加剧临床症状、恶化预后尚不清楚。研究表明颅内大动脉闭塞多由动脉粥样硬化性狭窄基础上叠加血栓形成所致[17],因此血管内再通术中面临斑块和血栓脱落危险,继之随着前向血流建立发生漂移并栓塞末梢。近端非急性期ICA闭塞血管内再通术可通过近端保护装置逆转血流或远端保护装置收集脱落斑块碎片,或血栓有效避免末梢栓塞,而颅内血管闭塞再通术不适宜应用远端保护装置,近端保护装置也无法逆转血流回收斑块碎片或血栓,因而很难避免末梢栓塞事件。最近,Lee等[16]报道血管内再通术治疗症状性亚急性期颅内大血管闭塞,发生末梢栓塞事件高达27.6%。本研究中末梢栓塞事件总发生率为46.7%,但症状性发生率仅为20%,且通过内科药物治疗出院时症状完全缓解;因此认为末梢栓塞是非急性期血管内再通术常见并发症,但并不一定造成严重临床危害。
血管夹层、穿孔与破裂是血管内再通术治疗非急性期颅内大动脉闭塞严重顾虑的并发症,既往已有不少个案报道[8,12-14]。血管夹层和穿孔发生原因主要是闭塞段开通不同于颅内血管狭窄成形,术中无法辨识血管走向,且颅内血管走行迂曲,导丝探查中偏离闭塞段血管轴向则极易发生穿孔和夹层[10,14]。尽管术中发生夹层并不一定造成严重临床事件,可经支架植入覆盖处理,但如发生动脉穿孔与破裂,则可能导致蛛网膜下腔出血,严重致残或致死。因此,术中不能强求一定要成功再通[10-11,14]。本组仅 1 例术中并发夹层,这可能得益于术前严格筛选病例。
穿支或分支血管闭塞是血管内再通非急性期颅内大血管闭塞潜在并发症之一,既往研究报道发生率为 7.7%~11.1%[8,11]。 本组无一发生穿支或分支血管闭塞事件。刘恋等[11]认为血管内再通术穿支或分支事件发生机制不同于颅内大动脉狭窄血管成形术,前者是血管球囊扩张或支架植入过程中斑块移位或雪犁效应所致,后者是再通过程中发生夹层影响到闭塞段远端血管穿支所致。本中心与上述观点一致,支持穿支事件不会发生于闭塞段血管,而是闭塞段远端血管穿支或分支。
再灌注损伤和梗死灶出血转化是血管内再通非急性期颅内大动脉闭塞另一重要忧虑,其发生率因缺乏大宗病例研究尚不清楚。Aghaebrahim等[12]报道采用血管再通术治疗24例颅内动脉慢性闭塞患者,结果发生1例症状性出血转化和1例再灌注综合征。Lee等[16]最近报道血管内再通症状性亚急性期颅内大血管闭塞后出血转化发生率为29%,但77.8%为出血性梗死,22.2%为脑实质血肿,进一步研究发现亚急性期血管内再通出血转化发生率和再灌注损伤标志物水平与急性期血管内再通无明显差异。本组患者围手术期均未发生再灌注综合征和出血转化,可能与严格的围手术期处理有关,术后所有患者6~8 h维持麻醉状态,防止过早复苏血压波动,随后严格控制血压,降压幅度控制在15%~25%。
再通血管急性或亚急性血栓形成、闭塞是非急性期颅内闭塞性病变血管内再通治疗潜在并发症之一,既往研究中有不少个例报道[8,13-14]。 本组患者围手术期未发生再通血管急性或亚急性血栓形成,可能得益于术前严格双抗治疗、术中充分肝素化和术后血小板糖蛋白Ⅱb/Ⅲa抑制剂应用。
3.3 血管再通后通畅性
以往研究发现颅内动脉硬化性狭窄患者经皮血管成形和支架植入术后约1/3会发生支架内再狭窄/闭塞[23-24],非急性期颅内闭塞性病变血管内再通后狭窄/闭塞发生率是否与之类似,甚至更高尚不清楚。Xu等[13]血管内再通治疗8例慢性颅内椎动脉完全闭塞患者,影像学随访3例见2例支架内再狭窄<50%。Lin等[7]血管内再通治疗3例症状性慢性椎基底动脉闭塞患者,影像学随访显示1例支架内无症状性再狭窄>70%。刘恋等[11]血管内再通治疗13例症状性慢性椎基底动脉闭塞患者,影像学随访9例中1例支架内无症状性再狭窄。Ma等[17]血管内再通治疗2例慢性MCA闭塞患者,1例术后12个月支架内症状性再狭窄80%。He等[15]血管内再通治疗21例椎基底动脉闭塞患者,术后影像学随访10例平均10.6个月,4例支架内再狭窄/闭塞中2例为症状性。Dashti等[8]血管内再通治疗9例亚急性-慢性基底动脉闭塞,影像学随访6例平均8.6个月,4例支架内再狭窄中2例轻度狭窄均无症状,1例明显狭窄有症状,1例明显狭窄无症状。本组12例成功再通患者获3~12个月血管造影随访,1例术后12个月支架内再狭窄80%(再次球囊扩张治疗后残余狭窄<20%),11例均无血流动力学意义上再狭窄。
总之,本研究结果表明在严格筛选患者、术中选择恰当操作、做好围手术期处理基础上,采取血管内开通术治疗非急性期颅内大动脉闭塞是可行、安全的,近期内能改善患者脑缺血症状,降低卒中再发率,但远期疗效有待长期随访证实。
