危重症患者万古霉素血药浓度监测与临床结局的相关性研究
2018-09-28时正媛顾红燕杨欣妤
时正媛,顾红燕,杨欣妤,鄢 丹
0 引言
万古霉素为糖肽类抗生素,临床上主要用于耐甲氧西林金黄色葡萄球菌(MRSA)、表皮葡萄球菌和肠球菌引起的严重肺部感染和肾盂肾炎的治疗,其不良反应多见于耳、肾毒性,静脉滴注相关性不良反应和血液系统毒性等[1]。由于万古霉素治疗指数窄、个体差异大、影响因素多,在治疗药物监测指导下调整给药剂量极为重要[2]。目前,已有研究对万古霉素血药浓度监测结果及用药合理性进行回顾性总结和分析,然而,很少有研究比较进行药物监测与未进行监测的情况下,患者临床结局有何差异。本文回顾性调查了我院自2015年7月开展万古霉素血药浓度监测以来,MRSA感染并使用万古霉素治疗的危重症患者中,进行血药浓度监测与未监测患者的信息及相关资料,评价血药浓度监测与万古霉素临床疗效及不良反应的相关性,旨在为临床合理用药提供参考。
1 资料与方法
1.1 患者筛选与研究设计[3-5]选择我院2015年7月至2017年9月期间,MRSA感染并应用万古霉素的危重症患者(19~90岁)。万古霉素疗程在3 d以上、给药后10 d内监测血清浓度的患者纳入血药浓度监测组(TDM组),排除手术中使用万古霉素治疗的患者,对其治疗时间、累计剂量、血药浓度监测结果、CRP水平、肾功能进行统计分析,比较两组间临床疗效与不良反应的差异。
1.2 干预措施 注射用盐酸万古霉素,商品名:稳可信,规格:每瓶500 mg,礼来苏州制药有限公司生产。TDM组(81例),监测万古霉素给药达稳态后的血药浓度,根据TDM结果,调整万古霉素给药剂量;非TDM组(143例),不经TDM,由医生确定万古霉素的给药剂量。
1.3 血药浓度监测方法 万古霉素血清标本采用化学发光微粒子免疫检测法(吖啶酯,美国雅培)进行测定,检测范围为3.0~100 μg/ml。峰浓度血标本在达稳态后静脉滴注结束后30~60 min留取,谷浓度血标本则在达稳态后给药前30 min留取。血清样本经离心分离后,在2~8 ℃储存,4 h内进行检测。
1.4 肾毒性评估 通过查阅相关患者的原始病历,分析应用万古霉素前、后血清肌酐值(SCr)的变化,评估TDM组与非TDM组的肾毒性发生率,万古霉素治疗相关性急性肾功能损伤:应用万古霉素患者48 h内血肌酐上升≥26.4 μmol/L,或血肌酐较基线上升50%,或尿量减少[<0.5 ml/(kg·h)]超过6 h而不能用其他原因解释者[6]。
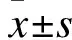
2 结果
2.1 两组相关治疗参数变化比较 两组治疗前后的CRP浓度、万古霉素平均治疗天数比较差异无统计学意义;TDM组万古霉素平均累计使用总剂量比非TDM组约少4.1 g,差异有统计学意义(P<0.05)。见表1。
2.2 两组肾毒性发生率比较 两组间患者的性别分布、平均年龄与初始血清肌酐值比较差异无统计学意义。两组血清肌酐浓度增加≥26.4 μmol/L或较基线上升50%时的比率分别为9.9%和16.1%,TDM组血清肌酐水平增加比率小于非TDM组,两组比较差异有统计学意义(P<0.05)。见表2。
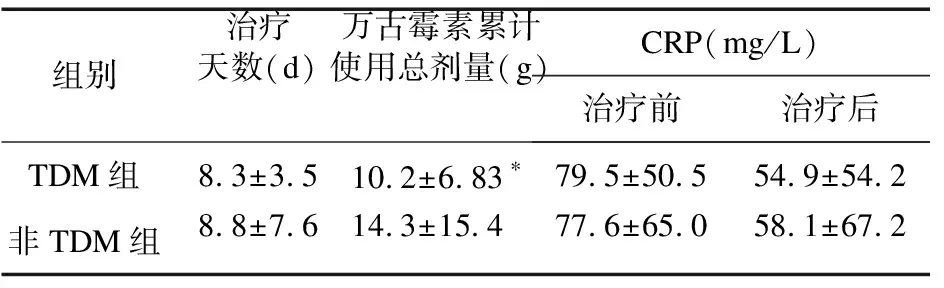
表1 两组患者相关治疗参数
注:与非TDM组比较,*P<0.05
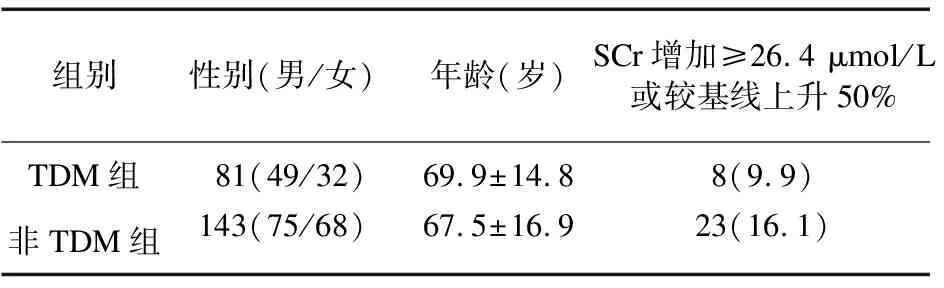
表2 两组患者肾功能相关参数比较(例,%)
2.3 两组万古霉素血药浓度与治疗天数的相关性比较 TDM组万古霉素血清峰浓度与治疗天数的对数相关性结果见图1(50例)。Spearman相关性分析结果表明,峰浓度与治疗天数显著性相关(r=0.487,P<0.01)。峰浓度低于25 g/ml的患者与峰浓度高于25 g/ml的患者相比,治疗时间延长。TDM组万古霉素血清谷浓度与治疗天数的对数相关性结果见图2(57例)。谷浓度与治疗天数呈显著相关(r=0.652,P<0.01)。谷浓度高于10 g/ml的患者与谷浓度低于10 g/ml的患者相比,治疗时间延长。
图1 万古霉素治疗天数与峰浓度的相关性
3 讨论
万古霉素的治疗指数窄、患者的个体差异大、影响因素较多,临床上易发生不良反应或出现疗效不佳的现象[7]。
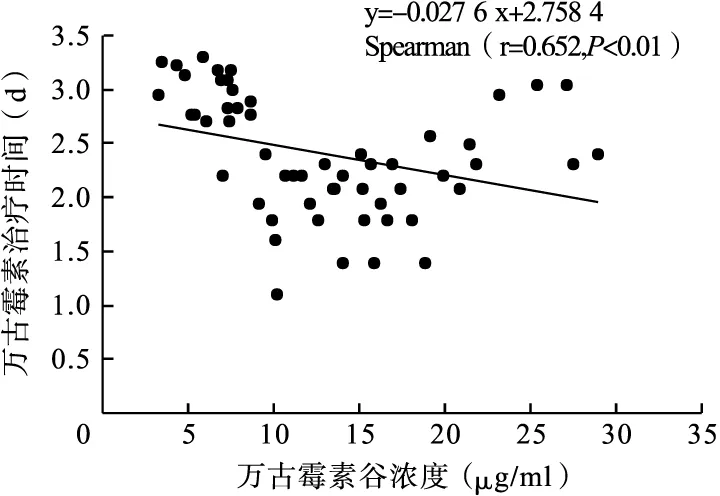
图2 万古霉素治疗天数与谷浓度的相关性
药品说明书上会指导能给予患者的最佳给药剂量,但通常并不包括特别针对危重症患者有效给药剂量的相关信息。此外,说明书上的用药信息也是基于非危重症患者的临床试验总结而来,该指导数据外推到危重症患者可能并不十分准确。危重症患者发生一个或多个器官系统的功能障碍,与普通患者相比,其体内抗生素血药浓度可能发生了极大的改变,若没有合理地调整给药剂量,这些血药浓度变化极易导致患者临床治疗失败、出现耐药菌感染甚至药物毒性反应,潜在地进一步恶化了患者的临床结局。因此,未来很有必要监测其血药浓度,促进个体化给药。
