HPLC法测定雪莲浸膏粉中绿原酸、芦丁、槲皮苷的含量
2018-09-28马庆东严俊仓唐雪君王新宇王金辉
马庆东, 严俊仓, 于 乾, 唐雪君, 王新宇, 杨 璐, 王金辉
(1新疆医科大学药学院, 乌鲁木齐 830011; 2新疆天山莲药业有限公司, 新疆 阜康 831599;3新疆林业科学院, 乌鲁木齐 830063; 4哈尔滨医科大学药学院, 哈尔滨 150081)
天山雪莲为菊科凤毛菊属植物天山雪莲[Saussureainvolucrata(Kar. et. Kir.)Sch. Bip.]的干燥地上部分,又名新疆雪莲、大苞雪莲,主要分布于我国新疆,在哈萨克斯坦、吉尔吉斯斯坦和蒙古也有分布,多生长在海拔2 400 m~4 100 m的山坡、山谷、草甸和石砾之中[1]。研究表明天山雪莲中主要含有黄酮类、倍半萜类、苯丙素类、香豆素类化学成分,具有抗肿瘤、抗关节炎、抗氧化、抗衰老、抗疲劳、抗缺氧、神经保护、免疫调节等药理作用,临床上主要用于关节炎、不孕不育、哮喘、心血管等疾病的治疗[2]。雪莲浸膏粉是新疆天山莲药业有限公司以天山雪莲为原料,经提取、浓缩、除杂等技术制取的雪莲制剂产品,但产品质量控制缺乏化学成分含量测定项目。产品原药材中化学成分绿原酸和芦丁已被中国药典作为天山雪莲含量测定项目的标示性成分[3]。本研究采用高效液相色谱(HPLC)法测定雪莲浸膏粉中绿原酸、芦丁、槲皮苷的含量,现报道如下。
1 仪器与试药
1.1仪器LC-2010AHT型高效液相色谱仪(日本岛津公司),SunFireTM-C18型色谱柱(4.6 mm ×150 mm,5 μm,美国Waters科技有限公司),KQ3200型超声仪(昆山超声仪器有限公司),FA1104型电子天平(上海天平仪器厂),SZ-93A型双重水蒸馏器(上海亚荣生化仪器厂)。
1.2试剂绿原酸标准品(中国食品药品检定研究院,批号110753-201415),芦丁标准品(中国食品药品检定研究院,批号100080-201408),槲皮苷标准品(中国食品药品检定研究院,批号111538-201606),甲醇(上海埃彼化学试剂有限公司,批号20170313),磷酸(天津市鼎盛鑫化工有限公司,批号20161102),试剂均为分析纯,乙腈(美国Sigma公司,批号:SL06061),水为双重蒸馏水。
1.3药材天山雪莲药材采自新疆巴音郭楞蒙古自治州,经新疆医科大学中医学院徐海燕副教授鉴定为菊科凤毛菊属植物天山雪莲Saussureainvolucrata(Kar. et. Kir.)Sch. Bip.的地上干燥部分,雪莲浸膏粉是由新疆天山莲药业有限公司生产的。
2 方法与结果
2.1色谱条件以十八烷基硅烷键合硅胶为填充剂,乙腈为流动相A,0.4%磷酸为流动相B,梯度洗脱:0~30 min,6%A(94%B)- 28%A(72%B),检测波长为330 nm,流速1 mL/min,柱温40℃,进样量10 μL,绿原酸、芦丁、槲皮苷理论塔板数均不低于8 000。
2.2对照品混合溶液的制备分别取绿原酸对照品、芦丁对照品、槲皮苷对照品适量,加甲醇制成每1 mL含绿原酸10 μg、芦丁28 μg、槲皮苷13 μg的混合溶液,备用。
2.3供试品溶液的制备称取雪莲浸膏粉40 mg(过80目筛),置具塞锥形瓶中,加入25mL甲醇,称重,超声10 min,放至室温,补重,摇匀,滤过,取续滤液,备用。
2.4系统适应性实验取“2.2”、“2.3”项下对照品混合溶液和供试品溶液,按“2.1”项下方法测定,记录色谱,结果显示对照品混合溶液和供试品溶液中绿原酸、芦丁、槲皮苷色谱峰的对称因子、分离度、理论塔板数均符合要求,提示色谱系统系统适应性良好,见图1、2。
2.5线性关系考察分别吸取“2.2”项下对照品混合溶液1、5、10、15、20 μL注入液相色谱仪,测定峰面积,以浓度为横坐标(X),峰面积为纵坐标(Y),绘制标准曲线,并计算绿原酸回归方程为Y=27 227.96X+1 625.20 (r=0.999 9),浓度范围1.06~21.12 μg/mL;芦丁回归方程为Y=14 062.87X+2 158.01 (r=0.999 9),浓度范围2.81~56.17 μg/mL;槲皮苷回归方程为Y=17 028.94X+1 003.52 (r=0.999 9),浓度范围1.38~27.54 μg/mL,进样浓度与峰面积呈良好线性关系。
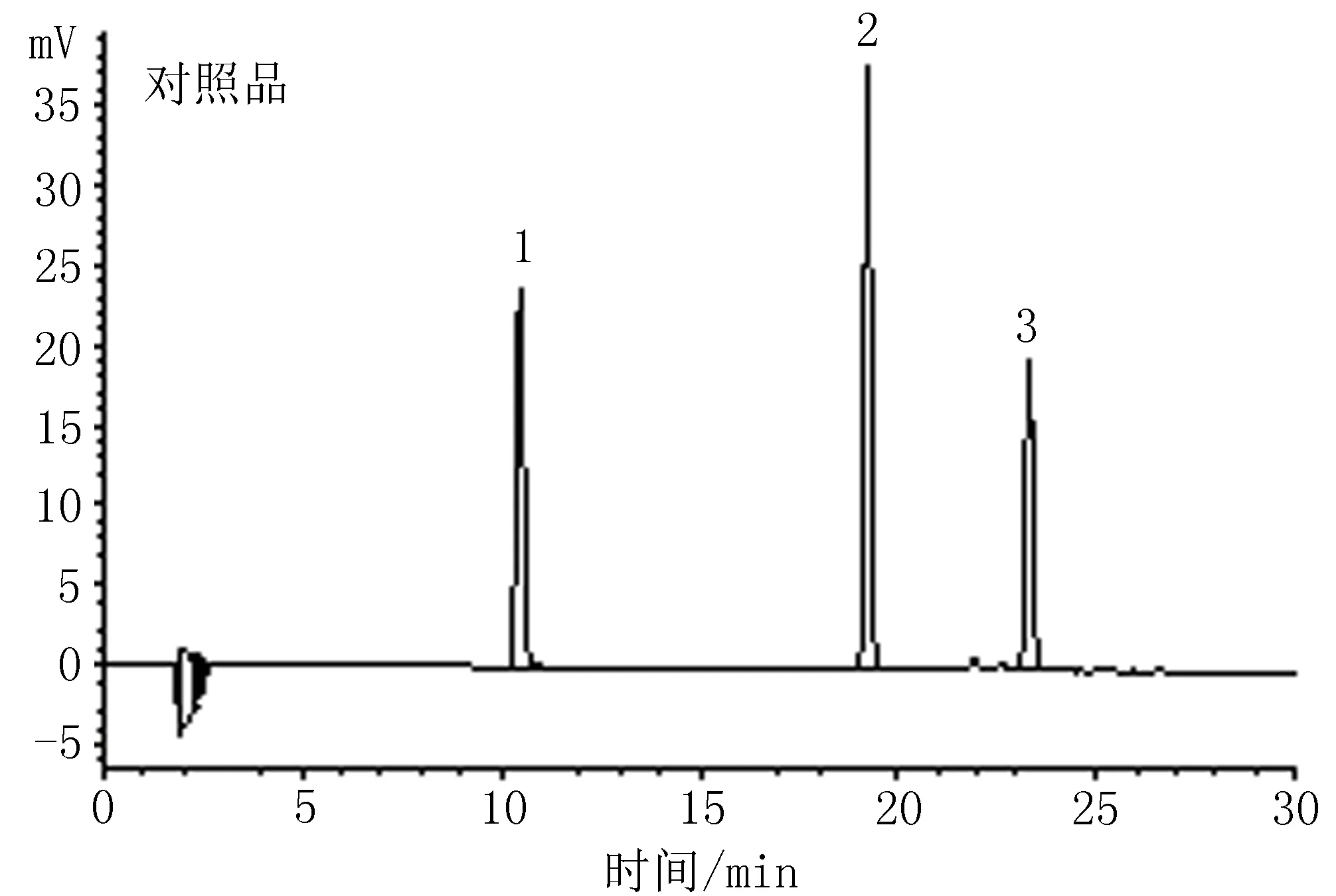
图1 对照品混合液的HPLC谱图
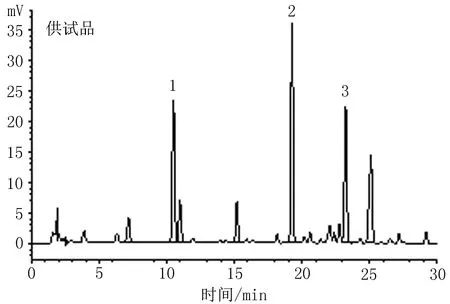
图2 浸膏粉供试品溶液的HPLC谱图
2.6精密度试验吸取“2.3”项下同一份供试品溶液10 μL,连续进样5次,绿原酸、芦丁、槲皮苷峰面积的RSD值分别为0.7%、0.6%、1.5%(n=5),表明方法精密度良好。
2.7稳定性试验吸取“2.3项”下同一份供试品溶液10 μL,分别于0、4、8、12、24 h进样,绿原酸、芦丁、槲皮苷峰面积的RSD值分别为0.6%、0.4%、0.4%,表明供试品溶液在24 h内稳定。
2.8重复性试验称定雪莲浸膏粉粉末6份,每份40 mg,按“2.3”项下方法制备供试品溶液,分别进样10 μL,用外标法分别计算供试品溶液中绿原酸、芦丁、槲皮苷浓度,根据称样量,折合浸膏粉中3种化学成分含量分别为(6.05±0.17)mg/g、(15.97±0.38)mg/g、(9.14±0.25)mg/g,RSD 分别为2.9%、2.4%、2.8%,表明方法重复性良好。
2.9加样回收率试验分别称取适量已知绿原酸、芦丁、槲皮苷含量样品6份,加入3种对照品适量,按“2.3” 项下法制备供试品溶液,按“2.1”项下方法测定,绿原酸、芦丁、槲皮苷的平均回收分别为99.31%、99.20%和96.23%,见表1。
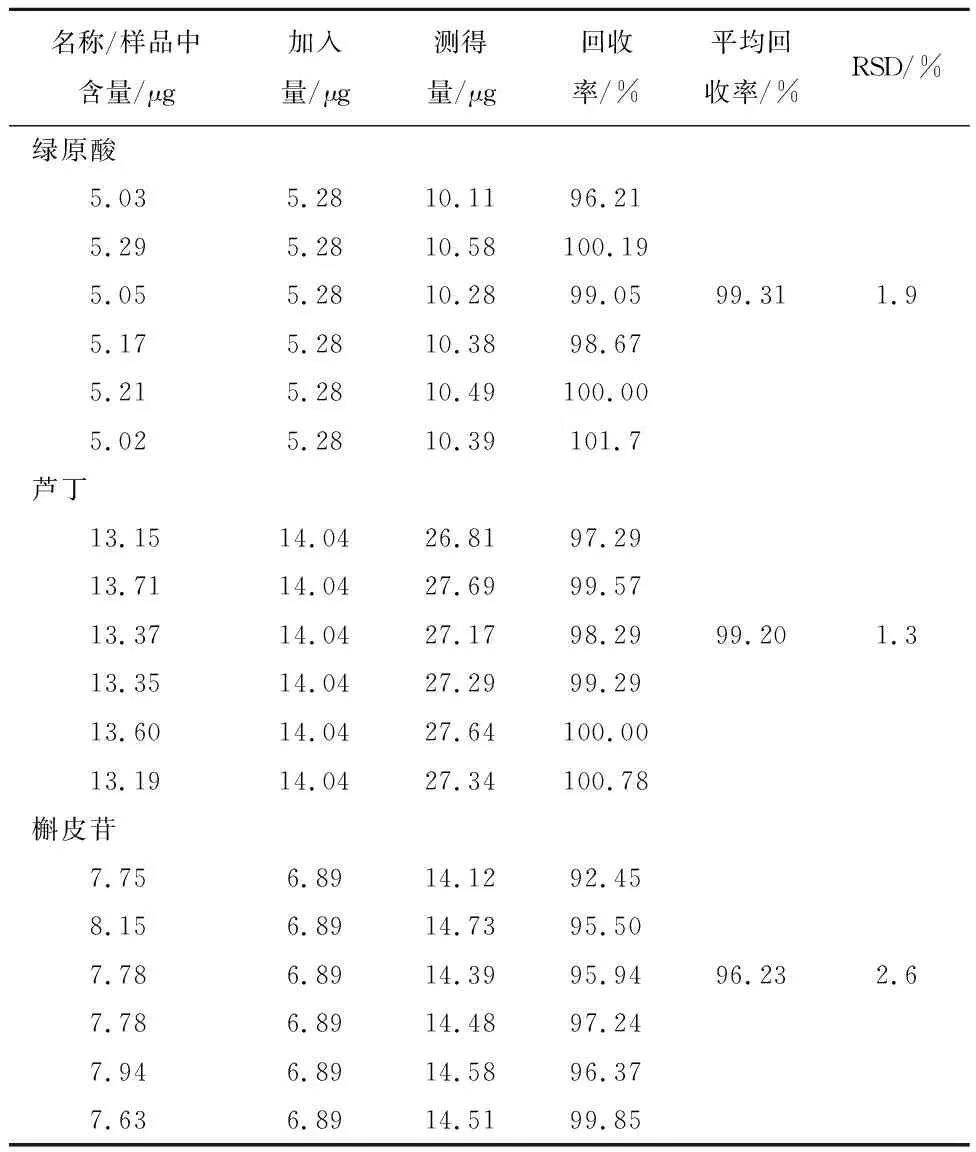
表1 雪莲浸膏粉中绿原酸、芦丁、槲皮苷回收率试验
2.10雪莲浸膏粉样品测定吸取 “2.3”项下供试品溶液,按“2.1”项下方法测定3个批次雪莲浸膏粉中绿原酸、芦丁、槲皮苷含量,平行测定,按外标法分别计算其在供试品溶液中浓度,根据称样量,折合在浸膏粉中含量,见表2。
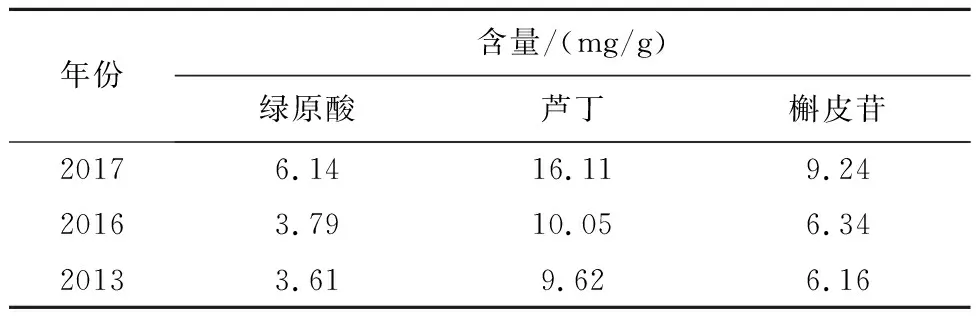
表2 雪莲浸膏粉中绿原酸、芦丁、槲皮苷含量测定结果
3 讨论
本研究色谱条件是在参考文献[4]的方法基础上进行优化得到最佳色谱条件,还考察了Inertsil ODS-SP(4.6 mm×250 mm,5 μm,GL Sciences),ZORBAX SB-C18(4.6 mm×150 mm,5 μm,Agilent),SunFireTM-C18(4.6 mm×150 mm,5 μm,Waters)3种色谱柱在相同色谱条件下对同一样品色谱峰分离效果,结果SunFireTM-C18色谱柱峰形最佳。
本研究实验发现,不同批次之间雪莲浸膏粉中绿原酸、芦丁和槲皮苷含量差异大,分析原因首要因素是原药材天山雪莲的质量,在不同生产环境、不同采收季节,药材的有效成分含量有明显差异。CHEN等[5]研究表明天山雪莲在第一收割期的黄酮含量最高,在生产加工过程是影响产品中化学成分含量的重要因素。张倩等[6]研究发现绿原酸类成分结构母核相同,在受热等外在条件下可以通过分子内酯基迁移发生异构化,从而导致绿原酸含量发生变化。最后,包装和储存条件也会影响产品中化学成分含量变化。周群等[7]研究证实了芦丁稳定性差的特性,药品包装的完整性和储存温度会引起芦丁含量变化。综上所述,本方法简便、快捷、重复性好,适用于雪莲浸膏粉中绿原酸、芦丁、槲皮苷的含量测定。
