咪喹莫特对BALB/c和C57BL/6小鼠银屑病样皮损诱导作用的比较
2018-09-26吴剑平张军峰史丽云
吴剑平,谢 倩,陈 林,张军峰,史丽云,詹 瑧
(南京中医药大学,南京 210023)
银屑病是以皮肤反复出现炎性增生为典型表现的自身免疫性疾病,目前其发病机制尚未完全阐明[1-2]。咪喹莫特作为Toll样受体激动剂,可通过与TLR-7/8结合,诱导皮肤出现表皮增厚、棘层肥厚、角化不全、嗜中性粒细胞聚集等银屑病样表现,目前常被用于银屑病动物模型的诱导剂[3]。BALB/c和C57BL/6小鼠是目前最常用于该类动物模型研究的两种小鼠品系,但这两种模型有无差异,哪种模型更适用于人类银屑病研究则鲜见报道。本研究即采用BALB/c和C57BL/6两种小鼠品系,比较不同时间点咪喹莫特诱导的两种模型小鼠皮肤形态学、病理组织学等方面的差异,并探讨IL-23/IL-17炎症轴在模型进展中的作用。
1 材料和方法
1.1 实验动物
SPF级BALB/c小鼠和C57BL/6小鼠各24只,均为雌性,体重20~22 g, 7~8周龄,由北京维通利华实验动物技术有限公司南京分公司提供[SCXK (苏) 2016-0003]。实验期间小鼠均饲养在屏障环境[SYXK (苏) 2014-0001]中,按照国标GB 14925-2010[4]的有关要求控制环境参数。实验前先给予3 d健康适应期,饲养和实验期间动物自由饮食。
1.2 主要试剂与仪器
明欣利迪乳膏(5%咪喹莫特)购自四川明欣药业有限责任公司;SuperScriptTMIII First-Strand Synthesis SuperMix购自Invitrogen公司;实时荧光定量PCR引物购自生工生物工程(上海)股份有限公司;Power SYBR® Green PCR Master Mix购自Applied Biosystems公司。Olympus显微镜购自日本;CFX384多重实时荧光定量PCR仪购自美国Bio-Rad公司。
1.3 实验方法
1.3.1 分组处理
咪喹莫特诱导的小鼠银屑病模型观察期多为4~6 d[3, 5-6],故本研究选择6 d作为模型观察终点。BALB/c小鼠和C57BL/6小鼠均随机分为4组,每组6只,分别为涂药0 d组(即正常对照组)、涂药2 d组、涂药4 d组和涂药6 d组。
各组处理如下:动物于涂药前一天背部剃毛,形成约2 cm × 3 cm大小的皮肤暴露区。涂药组小鼠每天涂抹5%咪喹莫特乳膏62.5 mg,并分别于涂药后2 d(涂药2 d组)、4 d(涂药4 d组)、6 d(涂药6 d组)采样。涂药0 d组小鼠背部剃毛后,不做任何处理,第2天直接采样。采样时小鼠先颈椎脱臼处死,剪下背部涂药部位皮肤,分成两块,一块放入10%甲醛中固定,另一块放入-80℃冻存。本实验研究的IACUC号为ACU170704,实验过程中严格按照实验动物使用的3R原则给予人道主义关怀。
1.3.2 皮损严重程度(psoriasis area and severity index,PASI)评分
PAIS评分标准如下:0,无;1,轻度;2,中度;3,重度;4,极重度。采用相机每天拍照记录小鼠皮损情况,同时按PAIS标准对皮肤红斑(erythema)、鳞屑(scales)及浸润增厚程度(thickness)进行0~4的评分,将3种积分累计得到总积分。绘制各组小鼠积分变化趋势图,观察各组小鼠皮损的变化情况。
1.3.3 皮损病理组织学检测
HE染色观察小鼠皮肤有无变性、坏死、溃疡、痂皮形成,上皮层有无增厚、表面角化不全或角化过度、真皮或皮下组织内有无充血、水肿、炎细胞浸润等病变。之后在200倍光镜下,采用计算机图像分析系统(DP2-BSW)测量每只动物的表皮层厚度。
1.3.4 实时荧光定量PCR检测
采用实时荧光定量PCR(RT-PCR)法测定各组小鼠皮肤组织IL-23/IL-17轴相关免疫因子IL-23、IL-17A和IL-17F mRNA的相对表达量。以β-actin为内参,实验结果采用2-△△Ct法进行相对定量。各引物序列如下:IL-23(上游):5’-AACAACAGCTCGGATTTGGTAT-3’;IL-23(下游):5’-ATGACCAGGACATTCAGCAGT-3’;IL-17A(上游):5’-TCAGCGTGTCCAAACACTGAG-3’;IL-17A(下游):5’-CGCCAAGGGAGTTAAAGACTT-3’;IL-17F(上游):5’-TGCTACTGTTGATGTTGGGAC-3’;IL-17F(下游):5’-CAGAAATGCCCTGGTTTTGGT-3’;β-actin(上游):5’-CTGAGAGGGAAATCGTG CGTGAC-3’;β-actin(下游):5’-GAACCGCTCG TTGCCAATAGTGAT-3’。
1.4 统计学方法

2 结果
2.1 各组背部皮肤形态学变化
如图1可见,正常对照组(0 d组)小鼠皮肤均光滑,无鳞屑、皱褶、红斑等。涂药2 d后,BALB/c小鼠背部即开始出现细小鳞屑和点状红斑。第3天开始出现少量皱褶。涂药4 d后,背部皮肤明显增厚,鳞屑变为小块状、红斑连成片状,皱褶呈条状隆起。涂药6 d后,鳞屑开始部分脱落,脱落部位可见点状出血。与BALB/c小鼠比较,C57BL/6小鼠于涂药3 d后才出现少量鳞屑及点状红斑,之后症状缓慢加重。同一时间段比较,C57BL/6小鼠鳞屑、皱褶、红斑、皮肤增厚等症状均较轻,至涂药第6天鳞屑未见脱落。见图1。
2.2 各组背部皮损PAIS评分变化
按PAIS评分标准绘制病变积分趋势线,随涂药天数增加,病变积分逐渐增高,与形态学观察结果一致,且同一时间段BALB/c小鼠的积分均高于C57BL/6小鼠,差异有显著性(P< 0.05或P< 0.01)。见图2。
2.3 背部皮损病理组织学变化
HE染色结果可见,正常组皮肤较薄,表面有少量角化,无充血、出血及炎症细胞浸润。涂药2 d后表皮开始出现增厚,皮肤表面出现痂皮及少量角化。真皮可见轻度充血及少量炎细胞浸润,以中性粒细胞和单核巨噬细胞浸润为主。与同时间段C57BL/6小鼠比较,BALB/c小鼠皮肤增厚及角化不全较重。涂药4 d后,BALB/c小鼠鳞状上皮和表皮增厚、角化不全、炎症浸润等情况均较C57BL/6小鼠严重。涂药6 d后,BALB/c小鼠被覆厚层鳞状上皮,表皮进一步增厚,角化不全严重,真皮层有轻度充血、出血,炎症细胞浸润增多。与BALB/c小鼠比较,C57BL/6小鼠表皮增厚、角化不全等病变程度明显较轻。通过表皮厚度测量可见,2 d组、4 d组和6 d组BALB/c小鼠表皮厚度均大于同时间段C57BL/6小鼠,差异均有显著性(P< 0.05或P< 0.01)。见图3。
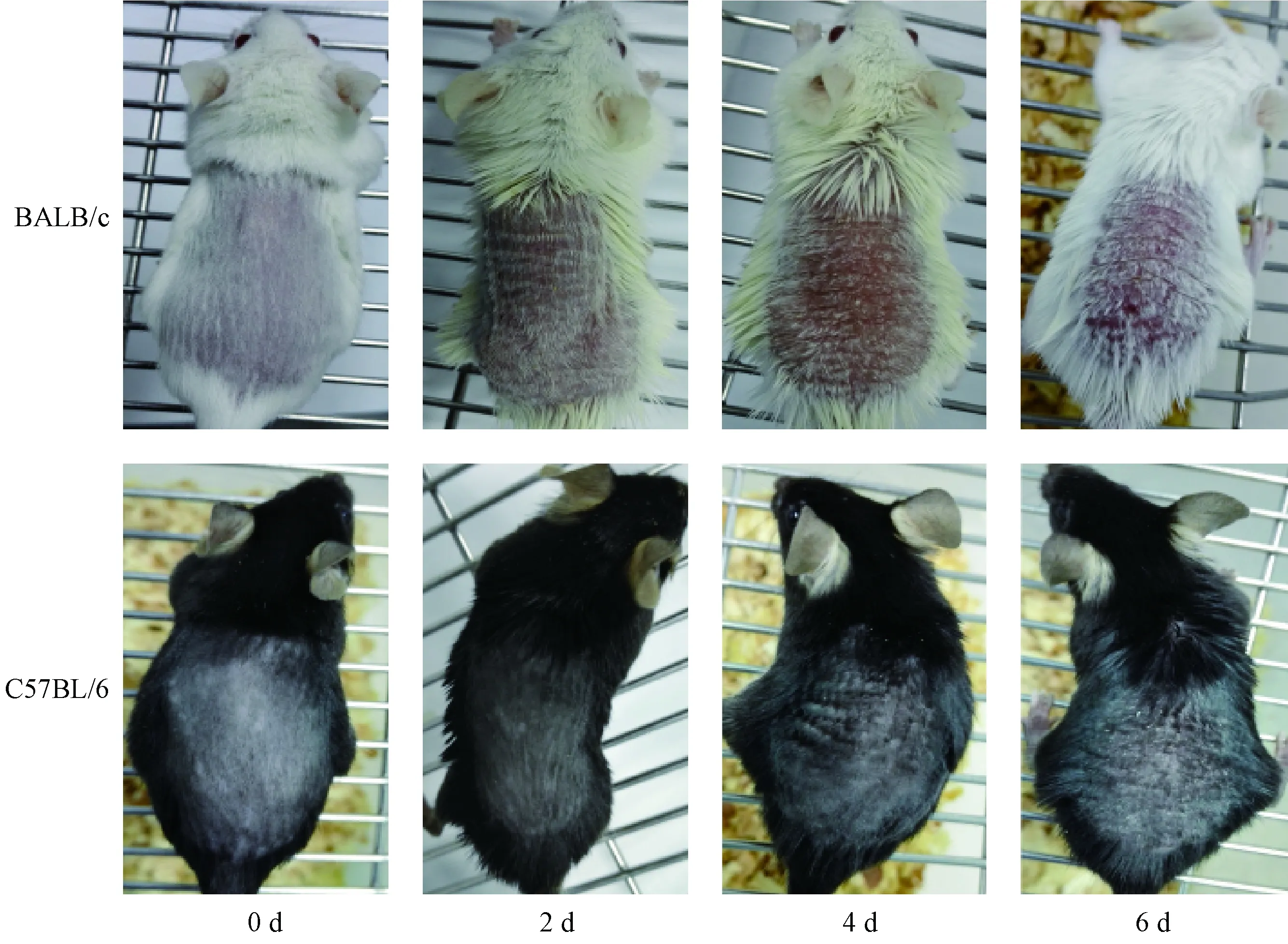
图1 不同品系小鼠背部皮肤形态学变化Figure 1 Morphological changes of mouse back skin in different strains

注:同一时间点,BALB/c小鼠与C57BL/6小鼠比较,*P< 0.05,**P< 0.01。图2 小鼠背部皮损PASI评分变化趋势图Note. BALB/c mice compared with C57BL/6 mice at the same time,* P< 0.05,**P< 0.01.Figure 2 The PASI scores of skin lesions in the mouse

注:A:涂药局部皮肤病理组织学变化(HE染色,× 100);B:表皮厚度变化。同一时间点,BALB/c小鼠与C57BL/6小鼠比较,* P< 0.05,**P< 0.01。图3 各组小鼠皮损病理组织学的变化Note. A: Histopathological changes of the local skin after drug was applied. HE staining (× 100). B: Changes of epidermal thickness. BALB/c mice compared with C57BL/6 mice at the same time,* P< 0.05,**P< 0.01.Figure 3 The histological changes of mouse skin lesions

注:与BALB/c小鼠0 d组比较,* P< 0.05,**P< 0.01;与C57BL/6小鼠0 d组比较,# P< 0.05,## P< 0.01。图4 不同品系小鼠皮损组织IL-23、IL-17A、IL-17F mRNA的相对表达量Note. Compared with BALB/c mice of the 0 d group,* P< 0.05,**P< 0.01. Compared with C57BL/6 mice of the 0 d group,# P< 0.05,## P< 0.01.Figure 4 The relative expression of IL-23, IL-17A, and IL-17F mRNA in skin lesions of different strains of mice
2.4 IL-23/IL-17轴相关细胞因子mRNA的表达
BALB/c和C57BL/6小鼠在造模后,其IL-23、IL-17A、IL-17F的mRNA相对表达量均呈抛物线样变化。与0 d组比较,两种小鼠在造模2,4,6 d后,IL-23、IL-17A、IL-17F均有明显升高(P< 0.05或P< 0.01)。其中,BALB/c小鼠IL-23、IL-17A、IL-17F的mRNA表达水平在用药2 d后即达到峰值,之后逐渐降低。C57BL/6小鼠IL-23、IL-17A、IL-17F的mRNA表达水平在用药4 d后达到峰值,之后逐渐降低。见图4。
3 讨论
银屑病是目前最常见的自身免疫性疾病之一,发病率高达2%左右[7-8]。其病因及发病机制尚未完全阐明,且尚无有效的治愈方法[9]。银屑病的临床特点主要为反复发作的皮肤过度角化、鳞屑、红斑形成,并伴有炎细胞浸润、新生血管形成、IL-6、TNF-α等细胞因子的分泌。银屑病的动物模型有多种,如药物诱导型模型、阴道上皮模型、基因突变及转基因模型等[10-12]。咪喹莫特诱导的小鼠模型,因其制作方法简单、致病机制与人类银屑病类似等原因,近年来被广泛用于人类银屑病研究[3, 13-14]。据文献报道及本实验室以往的研究经验发现,该方法诱导的模型,一般于造模第6天银屑病样症状达高峰,之后症状逐渐减弱直至完全缓解,因此模型观察期一般以6 d为宜[3, 15-16]。
本研究显示,通过背部连续6 d涂抹62.5 mg的5%咪喹莫特乳膏(明欣利迪)后,可诱导BALB/c小鼠和C57BL/6小鼠逐渐出现鳞屑、红斑、皮肤增厚及皱褶等典型银屑病样皮损,病理组织学鳞状上皮与表皮增厚、角化不全、角化过度、真皮充血、出血、炎症细胞浸润等改变均类似人类银屑病表现。但同时间段两种模型动物比较,BALB/c小鼠银屑病样症状出现更早、进展更迅速,且症状更严重,银屑病样皮损更典型。于涂药2~3 d后,BALB/c小鼠即开始出现细小鳞屑、红斑等症状,4 d后鳞屑、皮肤增厚、红斑等症状逐渐加重,到第6天达高峰。PAIS评分各项指标比较,BALB/c小鼠也均高于C57BL/6小鼠。HE染色发现,随着涂药天数的增加,两种动物模型表皮增厚、皮肤表面痂皮、角化不全、真皮充血、出血、炎症细胞浸润等表现均逐渐加重。但与形态学改变一致,BALB/c小鼠的各项病理指标变化均更显著且典型。
相关文献报道,咪喹莫特作为Toll样受体(TLR-7/8)激动剂,其诱导小鼠银屑病样皮损的机制与IL-23/IL-17轴的激活有关[3, 17]。本研究同时测定了IL-23/IL-17轴相关细胞因子的表达。结果发现,BALB/c小鼠的IL-23、IL-17A和IL-17F等细胞因子的表达在涂药2 d后即达高峰,之后逐渐回落,而C57BL/6小鼠在涂药4 d后各项细胞因子才达高峰,之后逐渐回落,该结果与van der Fits等人[3]的结果趋势一致,提示在咪喹莫特诱导的银屑病模型中,IL-23/IL-17轴的激活要先于银屑病样皮损的出现,也进一步揭示IL-23/IL-17轴的激活是皮损出现的诱导因素。同时BALB/c小鼠IL-23/IL-17轴的激活要先于C57BL/6小鼠,提示IL-23/IL-17轴的优先激活是BALB/c小鼠模型进展更加迅速的主要原因之一。
综上可见,咪喹莫特可诱导BALB/c小鼠和C57BL/6小鼠皮肤均出现银屑病样皮损表现,其中BALB/c小鼠症状出现更早,进展更迅速,鳞屑、皮肤增厚、角化过度及不全、炎症细胞浸润等皮损改变更典型。鉴于该模型病程短,且具有自限性等特点,BALB/c小鼠可能更适合用于人类银屑病研究。此外,本研究表明IL-23/IL-17轴的激活可能是诱发小鼠银屑病样皮损的关键因素之一。
