乙硼烷制备和纯化方法的探讨
2018-09-20禹金龙傅铸红陈艳珊
禹金龙,傅铸红,陈艳珊
(广东华特气体股份有限公司,广东 佛山 528241)
0 引 言
乙硼烷,又称六氢化二硼、硼乙烷,分子式为B2H6,相对分子量为27.67。乙硼烷的分子构型非常特殊,分子中的6个氢原子中的4个氢原子和两个硼原子以正常的共价键结合,另外两个氢原子每个氢原子同时和两个硼原子靠两个电子互相结合成键,形成B-H-B键,分别作为连接两个硼原子的“桥梁”。按正常的价键理论,乙硼烷需14个价电子,而它只有12个价电子,因此它是一个典型的“缺电子”化合物[1]。
在电子工业中乙硼烷作为气态杂质源、离子注入和硼掺杂氧化扩散的掺杂剂,主要用做P-型半导体芯片生产中的掺杂剂。亦可作为火箭和导弹使用的一种高能燃料。由于其缺电子的特性,可与其他电子对给予体之间形成配合物,也用于制备有机合成中常用的还原剂。在有机合成、金属焊接、制药、精细陶瓷领域中有着广泛的应用。
1 乙硼烷的理化性质
乙硼烷通常条件下(15℃,101.325 kPa)呈气态,是一种无色、易燃、易分解、具有令人恶心的烟火气味和微甜味道的高毒气体。沸点(101.325 kPa)-164.85℃,熔点-165.5℃。
乙硼烷是一种非常活泼的化合物,常温下就不很稳定,会缓慢地分解生成各种不同含量的高级硼氢化合物,同时会放出氢气。温度升高,分解加速,分解产物随温度高低而变化。如果在常温储藏的乙硼烷中加入少量的氢气,则可以有效地抑制乙硼烷的分解。
乙硼烷遇水立即水解,最终得到硼酸和大量的氢气。乙硼烷在室温干燥状态下一般不燃烧,但在与潮湿空气接触条件下,即使在低温也能与空气中氧发生爆炸性燃烧反应,并且放出较高的燃烧热值。含有75%~98%乙硼烷的空气混合物遇火花即燃烧,即使没有火种,只要其体积浓度大于0.5%,在空气或氧气中都有可能发生燃烧爆炸。在与氧化物表面的反应中呈现出强还原剂的效应。
乙硼烷不腐蚀任何普通金属材料,对橡胶、聚酯、脂肪、润滑油、聚乙烯、聚苯乙烯、聚酰胺、酚醛树脂、聚氯乙烯等材料有腐蚀作用。在用某些方法使用和生产乙硼烷的过程中,容易产生三氟化硼等腐蚀性气体,应使用可抵抗三氟化硼腐蚀的材料[1]。
2 乙硼烷的制备
工业生产乙硼烷有几种不同的制备方法,其中收率较高的方法有放电法;氢化铝锂、硼氢化锂或其他金属氢化物与三卤化硼的乙醚溶液反应;三烷基硼与氢气反应等。
专利US19460668466[2]提出采用金属硼氢化物与卤化硼反应,如:
3NaBH(OCH3)3+4B(BF3·C2H5OC2H5)→
3B(OCH3)3+3NaBF4+4B2H6+4(C2H5)2O
反应温度在50~70℃尤佳,此反应温度生成的乙硼烷容易分解。
专利US19450576502[3]提出采用金属氢化物与卤化硼反应,在有机溶剂中有利于加快反应速度,有机溶剂可选用乙二基乙烯、甲基醚、丁基醚等。反应如下:
6MeH+2BX3→B2H6+6MeX
6MeH+8BX3→B2H6+6MeBX4
专利EP20110176448[4]提出在催化剂存在下通过均相或多相催化将硼烷偶联的步骤,该催化剂包括从Ti、Zr、HF、Rh、Ir、Ni、Pd和Pt中选择的过渡金属,使用的反应较少,毒性较小,快速、简单,产生较少的废料。
专利JP20100023725[5]提出硼氢化钠与乙硼烷反应,然后再与三氯化硼反应。本发明根据杂质的产生机理对乙硼烷的制造方法进行探讨,解决了由于传统方法获得的乙硼烷含有以甲基氯化物(CH3Cl)和甲烷(CH4)为杂质的问题。
2NaBH4+B2H6→2NaB2H7
6NaB2H7+2BCl3→7B2H6+6NaCl
在第一阶段的反应中不使用三氯化硼,而是在第二阶段的反应中,所消耗的废物被耗尽。因此,不产生甲烷杂质。另外,通过抑制由溶剂的分解引起的杂质的产生,能够提高可循环利用的溶剂的成品率。
专利JP20100023738[6]公开了一种生产乙硼烷的方法,允许硼氢化钠与三氯化硼反应,并进一步与酸反应。
通过使溴化氢和三氯化硼发生反应生成反应中间体NaB2H7的第一阶段的反应如下面的反应式所示。通过反应中间体与酸发生反应,生成乙硼烷的第2阶段的反应
7NaBH4+BCl3→4NaB2H7+3NaCl
2NaB2H7+H2SO4→2B2H6+Na2SO4+2H2
由于在第二阶段的反应中没有使用三氯化硼,而是消耗殆尽,所以溶剂被分解。既不产生氯化甲基,又可获得乙硼烷。另外,通过抑制由溶剂的分解引起的杂质的产生,能够提高可循环利用的溶剂的成品率。
专利US19810303387[7]提出一种干法制备乙硼烷,在没有溶剂的情况下,将锂或硼氢化钠与三氟化硼反应而成,从而避免了与先前类似反应中使用的乙醚溶剂有关的危险。这种反应似乎是通过硼氢化物的氢化物萃取而不是氢化物-卤化物交换机理进行的,在乙醚溶液中,相应的反应可以达到95%左右的收率。干法流程产生的乙硼烷没有溶剂污染,但是产品含大量未反应的三氟化硼,且此反应缓慢,产率很低。
专利99807228.1[8]提出采用硼氢化钾与三卤化硼反应,气态三卤化硼连续通入一个含固态硼氢化物反应的容器,理想的是将三卤化硼冷凝在硼氢化物反应剂上。
3KBH4+4BF3→2B2H6+3KBF4
反应在约-130~20℃下进行,反应剂包括至少20%硼氢化钾,反应步骤不存在溶剂。
图1为本专利实施方案的设备图。
3 乙硼烷的纯化方法
粗品的乙硼烷均含有一定量的杂质,不同工艺方法制备的乙硼烷所含杂质的种类、数量不尽相同。其来源主要有反应副产物、反应物带入和漏入的空气及与反应物、生成物反应的产物。与主组分乙硼烷相比,按照其挥发性,可将杂质分为难挥发杂质、易挥发杂质和挥发性接近杂质。纯化方法主要有吸附法、精馏与吸附组合、连续精馏等方法。

图1 实施方案的设备图
3.1 吸附分离提纯制取高纯B2H6
根据粗制乙硼烷的杂质种类、含量,选用SP型硅胶作为吸附剂,采用低温吸附、升温脱附的办法将B2H6原料CH4、CO2等杂质大部分除去。杂质C2H6由于其沸点(-88℃)、相对分子量(30)与B2H6十分接近,而导致吸附分离法除去C2H6的效果很差。采用硼氢化钠与碘在二乙二醇二甲醚溶液中反应的方法制备乙硼烷,产品收率高、纯度高(99.0%~99.9%),杂质少、易分离,采用吸附分离纯化可得到4NB2H6产品。
3.2 精馏与吸附组合制取高纯B2H6
该方法是将含有H2、N2、O2、Ar、CO、CH4等低沸点轻组分和(C2H5)2O、CH3Cl、C2H5Cl、B4H10、B5H9、B5H11等高沸点重组分利用精馏方法进行分离,与B2H6沸点接近的CO2、C2H6两种杂质在精馏分离不彻底的情况下,选择对这两种杂质由选择吸附性的吸附剂进行吸附分离,即采用精馏+吸附的组合方法进行纯化生产,充分发挥两种纯化法的优点,将总杂质降低至1 ppm以下,制备4N5、甚至5N质量水平的B2H6产品。
3.3 连续精馏法制备高纯B2H6
该方法在充填塔下部安装的进料管线连续供给B2H6原料,经精馏分离出来的高沸点重组分根据其含量高低在再沸器下部连续控制排出;根据在线检测结果,在充填塔顶部连续抽取适量的合格高纯B2H6产品。与B2H6沸点接近的CO2、C2H6两种杂质在精馏分离不彻底的情况下,选择对这两种杂质由选择吸附性的吸附剂进行吸附办法进行分离。
3.4 多种专利文献的纯化方法
1.专利201010169560.1[9]提出从含有低沸点和高沸点成分的粗B2H6中制取高纯B2H6,通过选择吸附与B2H6沸点接近的、难以用蒸馏法分离的微量CO2、C2H6等杂质和蒸馏法组合,制取高纯B2H6。
吸附精馏塔使用内径Φ31 mm,有效长度1000 mm的SUS316管,其中充填4A沸石分子筛,平均细孔径0.4 mm作为吸附剂。
原料气导入前,将系统置换成无氧状态。此后,充入粗B2H6到再沸器,冷凝器冷却到-178℃,吸附精馏塔冷却到-76℃,再沸器温度逐渐上升,蒸发粗B2H6,蒸馏压力保持在0.15 MPa。
进行全回流运转后,放出冷凝器顶部凝缩的低沸点气体,分析纯化的液态B2H6,当CH4浓度达到10×10-6时,将纯化的液态B2H6存放到产品接收器。
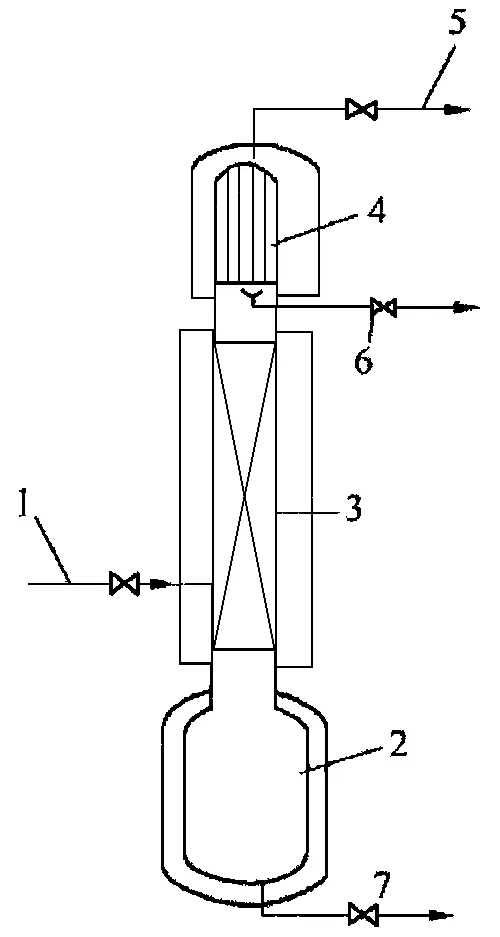
图2 精馏塔结构示意图
2.专利201010169571.X[10]提出粗B2H6通过原料气进口管送到精馏塔再沸器蒸发,作为上升蒸气。在填料塔中进行精馏,在塔顶形成含高沸点杂质含量较低的B2H6蒸气。在冷凝器中冷凝回流,低沸点成分通过安装在冷凝器上部的流量调节阀由低沸点杂质排放管放出除掉。纯化的液态B2H6通过流量调节阀抽出,贮存到产品接收槽。
再在蒸馏装置系统内反复进行气化和液化,实现了精馏,将低沸点和高沸点成分分离,在塔顶不断浓缩为高纯B2H6。与沸点接近的CO2及C2H6等在填料塔中进行气液接触,通过充填的吸附剂高效率的吸附除掉,系统内的B2H6得到了纯化。见图3。
3.专利US19490114900[11]公开采用吡啶与乙硼烷形成复合物,乙烷不反应,乙烷采用精馏方式去除,然后采用氯化物与吡啶复合物反应,得到乙硼烷。
4.专利JP19890238474[12]提出通过在较低的压力下蒸馏,通过吸收填料中的杂质和蒸馏分离出高纯度的乙硼烷,从而获得适合半导体元件生产的高纯度乙硼烷:在提高压力下低温蒸馏净化含有低沸点和高沸点成分的粗乙硼烷时,采用塔式蒸馏法对含有低沸点和高沸点的粗乙硼烷进行分离。填料用吸附剂、CO2、C2H6等吸附剂,在低沸点的杂质中,其沸点接近乙硼烷,不能用常规精馏除去,被吸附和除去,吸附剂为沸石分子筛,用于蒸馏操作条件,再沸器的温度在-90~-20℃。
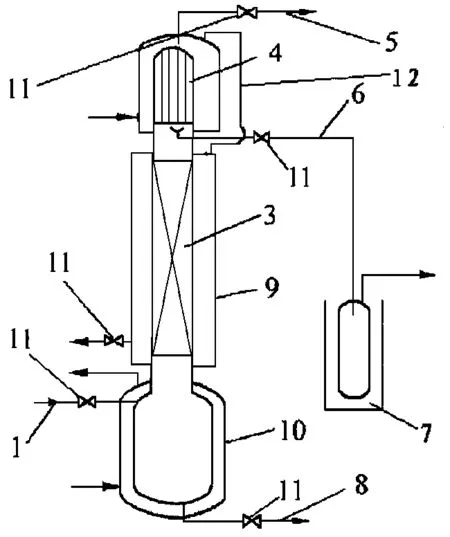
图3 纯化设备结构示意图
5.专利JP19880282362[13]提出通过使乙硼烷与硼化镍接触,有效地去除乙硼烷中的氧,使其达到超低浓度:粗乙硼烷与硼化镍接触,去除粗乙硼烷中的氧,粗乙硼烷中的氧浓度通常约为100 ppm,但可去除到0.01 ppm左右,再用氢、氮、氮气稀释至0.01 ppm左右。Ni2B或Nib,通常被称为镍硼化物,而硼以其他各种形式与镍结合的物质可用作硼化镍。例如,使乙硼烷与镍接触的方法可作为一种简单的方法来获取镍硼化物。
6.专利99807228.1[8]采用无机氢氧化物选择性地清除乙硼烷中的三卤化硼和二氧化碳杂质,无机氢氧化物中可能含有一种或多种碱金属氢氧化物、碱土氢氧化物等。试剂组合物基本上由氢氧化物或多种氢氧化物组成,以固体形式出现,例如粉末、球状、颗粒或包覆在惰性载体如矾土或硅土上,在使用前进行预处理。除杂温度保持在低温状态,可以使乙硼烷的分解降到最低,优选干冰温度。
4 小结
电子特种气体,尤其是高纯电子气体作为电子化工材料这一新门类,是制约集成电路可靠性和成品率的重要因素。随着电子信息技术的飞速发展,集成度越来越高,对基础原材料的纯度要求也越来越高,因此制备高纯电子特种气体技术更显得迫在眉睫。
乙硼烷在电子工业中作为气态杂质源、离子注入和硼掺杂氧化扩散的掺杂剂,主要用做P-型半导体芯片生产中的掺杂剂。
目前乙硼烷制备技术尚未完善,制作方法工艺复杂,较难掌握,生产的产品尚不能全面满足相关电子产品的需要,只能用于制造低规格的产品[9],而乙硼烷化学性质不稳定,从国外进口基本上按混合后的方式进来,使用起来十分不便[14];因此,迫切需要解决乙硼烷的生产纯化关键技术,实现高纯乙硼烷的国产化,以推进半导体等相关行业的发展。
