磷酸盐对纳米TiO2在土壤中迁移的影响
2018-09-20刘诚,孙强,张刚,张玥,徐楠
刘 诚,孙 强,张 刚,张 玥,徐 楠
(苏州科技大学 化学生物与材料工程学院,江苏 苏州 215009;江苏省环境功能材料重点实验室,江苏 苏州 215009)
尺寸小于100 nm的纳米材料的性质,例如小尺寸和高表面能,赋予纳米材料大量生产的可能以及其他潜在应用。作为一种重要的无机功能材料,纳米二氧化钛(nTiO2)在油漆、防晒化妆品、遮光剂、半导体和电子陶瓷领域具有良好的应用[1-5]。然而,在其工业生产和应用过程中,纳米颗粒(NP)不可避免地进入土壤,对人类健康和生活环境存在潜在的危害。据报道,nTiO2和nZnO对土壤环境有害,导致了小麦产量的显著减少[6]。
生活条件在不断改善,经济的大力发展,特别是磷化工业的快速发展,使得环境污染的程度不断扩大。磷是一种营养元素,磷的过量释放会使水体产生富营养化现象,危害环境。在自然界中,磷大多以磷酸盐的形式存在,磷酸盐吸附在nTiO2颗粒表面会改变其物理化学特性,从而影响nTiO2颗粒在土壤中的迁移性[7-8]。目前,在农田中化肥(特别是磷肥)施用过量,这样通过灌溉水或雨水冲刷方式会把土壤中大量可溶性磷酸盐淋溶释放出来,从而进入地下水中。当nTiO2颗粒与磷酸盐在农田中大量存在时,会促进nTiO2的迁移从而进入地下水环境,造成潜在的危害。因此,考察磷酸盐对nTiO2颗粒迁移的影响至关重要,这方面的研究目前少见报道。有研究表明,离子强度、电解质类型、溶液的pH值和溶解的天然有机质对纳米颗粒在水体系中的稳定性有着重要的影响[9-13]。笔者通过改变NaNO3背景溶液浓度,探究在有无磷酸盐溶液存在条件下,nTiO2颗粒表面Zeta电位的变化及磷酸盐对nTiO2在真实土壤中迁移的影响。
1 材料与方法
1.1 纳米TiO2磷酸盐悬浮液的制备
所用的nTiO2(20 nm)购自上海高全化工有限公司,其他化学药品均为分析纯,购置于国药集团。称取1 g nTiO2溶于1.0 mM磷酸盐溶液和不同浓度NaNO3电解质溶液中,用超声波清洗器(KQ 2200B,上海超声仪器股份有限公司)超声30 min,用于迁移实验。
1.2 土壤样品采集与分析
土壤样品参数见表1。

表1 土壤样品参数
实验所用土壤取自苏州科技大学石湖校区宿舍3号楼北侧。将采集到的土壤敲碎铺开,放在阴凉通风处风干,使用30网目标准分样筛,筛取收集粒径0.60 mm与0.71 mm之间的土壤颗粒,做土壤柱迁移试验。
采用1∶1的硝酸-盐酸在加热的条件下对实验中所采用的土壤进行硝解,然后再进行ICP分析测试主要物质组分,得到了土壤理化参数,结果见表1。
1.3 纳米TiO2颗粒表面Zeta电位的测试
称取0.25 g nTiO2颗粒和5 g的土壤于250 mL锥形瓶中,配制成不同条件的悬浮液。不同条件分别为电解质NaNO3浓度(0.1~10.0 mM)和P浓度(0.0和1.0 mM)。然后将配制好的nTiO2颗粒的悬浮液用保鲜膜封口,放入恒温震荡器45℃恒温震荡24 h。此处应控制震荡频率相同,以免影响实验。24 h后,将锥形瓶取出,转入烧杯中,静置,吸取2 mL上清液,测出粒径、电位。超声结束后,将悬浮液置于搅拌器上搅拌30 s。然后,用马尔文Nano-ZS90测试nTiO2颗粒的Zeta电位,所有样品测试三次,取平均值作为最终的Zeta电位值。
1.4 土壤柱迁移实验
参考Fang等的研究方法[14],以柱淋溶实验研究nTiO2的迁移行为。选用长19 cm、内径25 mm的层析柱。填装10 cm高的风干土壤,并留有9 cm高的水头。柱淋溶实验开始前,对土壤柱进行预饱和处理。将20.0 mM CaCl2溶液于0.083 mL·min-1的流速条件下自下而上注入填充柱,维持该过程约1.0 h,然后将流速提高至0.16 mL·min-1,再维持约6.5 h。当土壤胶体稳定后,将CaCl2溶液换成NaNO3背景电解质溶液,即于流速为0.16 mL·min-1的条件下注入背景溶液约6.5 h,最后将流速提高至目标流速(1 mL·min-1),维持该过程约4.0 h。整个预饱和过程大约需要注入60 PV(PV为孔隙体积)的CaCl2溶液。研究表明,当溶液瞬时性质发生变化时,如降低离子强度或增加孔隙水流速会导致土壤胶体的移动,因此,通过预饱和试验来防止(或最大程度地抑制)土壤胶体的移动,以排除土壤胶体对纳米粒子检测的干扰。通过在210.0 nm波长处全程监测出流液的吸光度,发现其吸光度均小于0.001,表明预饱和程序能有效地稳定土壤胶体,抑制其移动,因此,保证了纳米粒子检测的准确性。
柱子实验开始时,向层析柱注入大约5个孔隙体积数(PV)的上述nTiO2悬浮液,用自动部分收集器(BS-100A,上海沪西)每10 min收集流出液10 mL,收集20管流出液。然后继续注入5 PV的NaNO3背景溶液,收集流出液,待测试。具体不同条件下nTiO2颗粒悬浮液和土壤柱的参数见表2(表中数据为可以迁移出层析柱的实验,在层析柱中blocked的迁移实验所对应的参数未放在表中)。
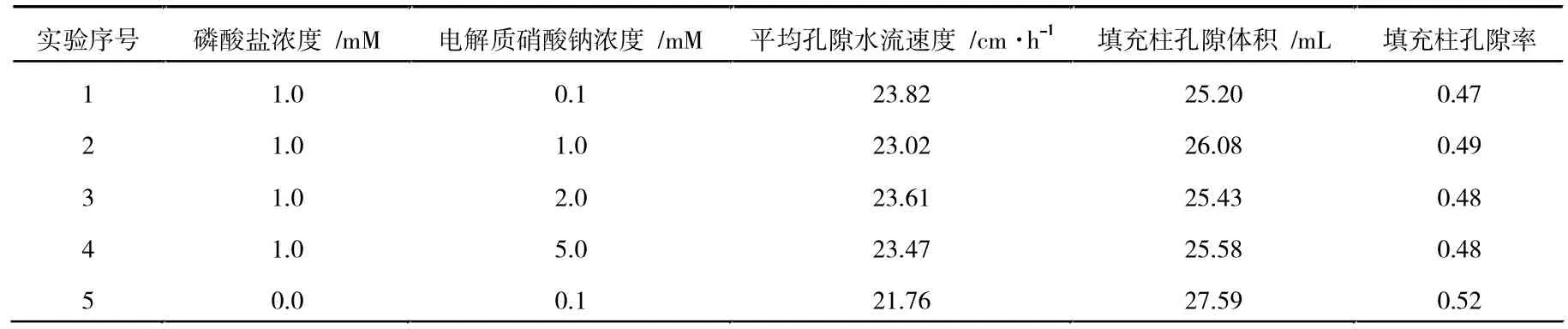
表2 穿透实验中nTiO2悬浮液和饱和石英砂柱的物理特性
1.5 钛浓度的分析与测定
钛(Ti)的分析与测定:取2.0 mL nTiO2悬浮液置于25 mL的烧杯中,向烧杯中加入1.0~2.0 mL硫酸-硫酸铵消解液,置于加热板上,在220℃下加热1.0~1.5 h。消解完全后,溶液转移至50 mL的容量瓶中定容。从中取 5.0 mL 移入 50 mL 容量瓶中,依次分别加入 8 mL(V盐酸∶V去离子水=5∶1)稀盐酸,2 mL(10 g·L-1)抗坏血酸,10.0 mL(50 g·L-1)二安替比林甲烷盐酸溶液(按照V盐酸∶V去离子水=1∶5溶解称量好的二安替比林甲烷粉末),定容。用紫外分光光度计(TU-1901,日本岛津)在 390.0 nm波长下测定 Ti的浓度。用1 000 mg·L-1的钛标准溶液(基质为 0.15 mol·L-1HNO3)稀释成浓度梯度为 1.0~5.0 mg·L-1的溶液,相同条件下测吸光度,做标准曲线并求出钛的浓度。
1.6 迁移参数
nTiO2颗粒质量回收率可以通过对其迁移曲线进行面积积分得到

式中,Q 为孔隙流速(L3·T-1),C0和 C 分别为入流液和出流液 nTiO2浓度(mg·L-1),t为时间,T0为脉冲持续时间。
nTiO2颗粒在石英砂表面吸附的概率称之为吸附效率(α)为

式中,L为柱子的长度,θ为填充柱的孔隙率,dc为砂子的直径,η0为理论单一介质接触效率。
净床渗透系数

颗粒物沉积速率系数

式中,νp为水流速度,k为时间和距离相关的系数。
nTiO2颗粒的最大迁移距离定义为当99.9%的nTiO2颗粒被截留时nTiO2颗粒所移动的距离,可以表示为

1.7 两点动力学模型
实验选用两点动力学吸附模型(TSKAM),其方程为[15-16]
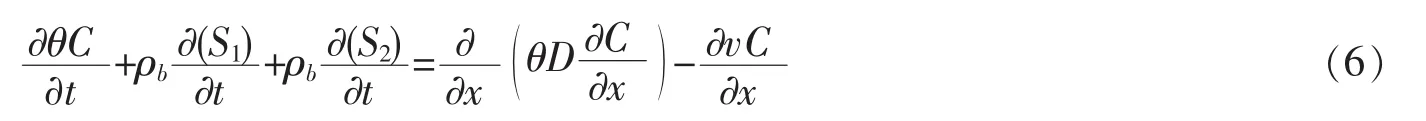
其中,θ是石英砂柱的孔隙率,C表示溶液中nTiO2颗粒的浓度,ρb表示石英砂的容重,x表示空间垂直坐标轴,D表示水力学弥散系数,v表示水流速度,S1和S2分别表示滞留位点l和位点2。TSKAM模型的核心是将石英砂表面上利于nTiO2颗粒吸附的位点分为位点1和位点2,滞留在位点1上的nTiO2颗粒受对流-弥散控制,质量守恒方程为一阶动力方程为一阶动力学吸附、解吸方程

K1和K1d分别为位点1上的吸附、解吸速率,nTiO2颗粒在位点1上的吸附属于可逆逆吸附。
位点2上的质量守恒方程为

K2为胶体在位点2上的吸附速率,位点2上的吸附是不可逆吸附。Ψx是与填充柱深度有有关的函数[15]

其中dc是石英砂的平均粒径,x0是坐标轴上的距离,在此距离时nTiO2颗粒滞留与柱深度有关,β是经验系数,控制着空间滞留曲线的形状,nTiO2颗粒的穿透曲线通过HYDRUS-1D软件计算数值,得到参数K1、K1d及K2[17-18]。通过Hydrus-1D软件模拟nTiO2在多孔介质中的迁移情况。位点1吸附效率(K1)、解吸效率(K1d)以及位点2吸附效率(K2)值越小,表明颗粒在石英砂上的滞留越少、其迁移性越高。位点1吸附效率(K1)、解吸效率(K1d)以及位点2吸附效率(K2)值的获得是将原始数据输入到软件之中,软件自动生成所得。
2 结果与讨论
2.1 磷酸盐对nTiO2表面Zeta电位的影响
nTiO2在NaNO3电解质溶液中表面Zeta电位的变化如图1所示。在所有条件下,nTiO2颗粒表面的Zeta电位都是负值。当悬浮液中没有磷酸盐时,nTiO2颗粒表面Zeta电位随这NaNO3浓度的增加,变化明显,从-38.2 mV降低到-22.2 mV;相应的,有磷酸盐存在时,随着NaNO3从 0.1 mM升高到 10.0 mM,nTiO2颗粒的Zeta电位变化很小,说明P在nTiO2颗粒表面产生特定吸附。另外,相同背景溶液浓度下,磷酸盐存在条件下的nTiO2颗粒表面Zeta电位的值更负。例如当NaNO3浓度为10.0 mM时,无P条件下的nTiO2颗粒表面Zeta电位为-22.2 mV,而加P时,它的表面Zeta电位则是-34.1 mV。结果表明,由于P吸附在nTiO2颗粒的表面,通过表面羧基的去质子化,提高了nTiO2颗粒表面的电荷密度[19]。因此,nTiO2颗粒和吸附P的nTiO2颗粒之间以及nTiO2颗粒与土壤之间的静电排斥作用加强[20],最终导致nTiO2颗粒悬浮液的弥散稳定性的提高。所以,磷酸盐促进了nTiO2颗粒在土柱中的迁移。

图1 不同浓度硝酸钠背景溶液中nTiO2的表面zeta电位
2.2 不同浓度NaNO3电解质对nTiO2表面Zeta电位的影响
如图1所示,在不同电解质浓度下,nTiO2颗粒表面的Zeta电位都是负值,并且随着溶液中NaNO3浓度的不断增加,nTiO2颗粒表面Zeta电位降低(绝对值降低,即负的越来越少),例如,在没有磷酸盐(P)存在的条件下,当NaNO3浓度从0.1 mM增加到10.0 mM时,相应的Zeta电位从-38.2 mV改变到-22.2 mV,这主要是因为随着溶液中NaNO3的溶度的不断增加,nTiO2颗粒表面的电荷屏蔽效应和静电双电层被压缩[21-22],nTiO2颗粒表面的净负电荷减少,从而导致nTiO2颗粒表面Zeta电位降低,因此,nTiO2颗粒悬浮液的弥散稳定性也降低。磷酸盐存在的条件下,观察到同样的现象。
2.3 磷酸盐对nTiO2颗粒在土壤柱中迁移的影响
nTiO2在NaNO3电解质溶液中的穿透曲线如图2所示,由图2可见,nTiO2的出流比(C/C0流出液中nTiO2的浓度与初始浓度的比值)随着孔隙体积(PV)的变化。
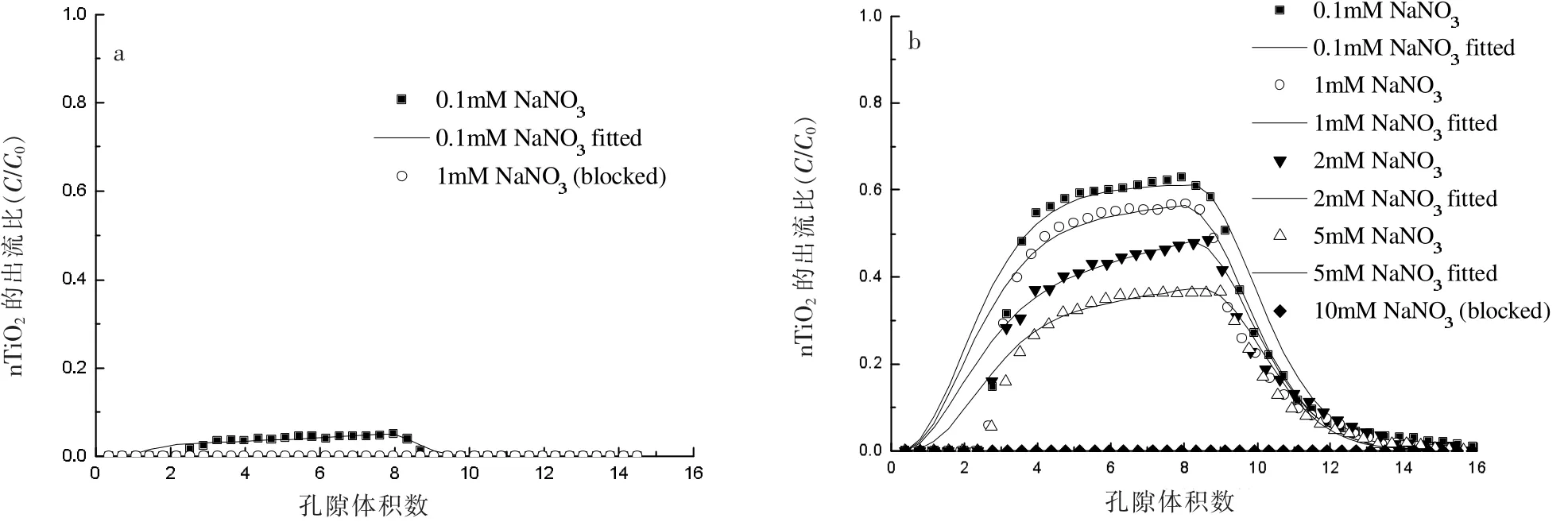
图2 无磷酸盐(a)和有1.0 mM磷酸盐(b)时,不同浓度硝酸钠背景浓度中nTiO2在土壤柱中的穿透曲线
对比图2(a)和2(b),没有P存在的条件下,nTiO2在土壤柱中的迁移能力很有限,几乎在所有的背景溶液浓度下都发生堵塞。而当nTiO2悬浮液中加入了1.0 mM P时,迁移能力明显增加。以0.1 mM NaNO3背景溶液浓度为例(实验1与实验5,表3),在没有P时,nTiO2的出流比仅为4.60%,而当P存在时,nTiO2的出流比增加到61.92%,表明P促进了nTiO2颗粒在土壤柱中的迁移,这与Zeta电位实验结果一致。之前的工作中,探究了P存在时,nTiO2在饱和石英砂柱中的迁移行为[23]。结果显示,在饱和石英砂柱中,P同样促进nTiO2的迁移,且随着P浓度的增加,促进效果趋好。当NaNO3背景溶液浓度为10.0 mM时,存在0.1 mM的P即可将nTiO2在石英砂柱中的出流比提高至60%左右,而在土壤柱中,图2中NaNO3背景溶液浓度为10.0 mM时,迁移试验发生了堵塞。因此可以确定,由于性质及所含物质不同,土壤柱与石英砂柱存在很大差异。从表1可看出,土壤的pH值接近中性,与石英砂柱中迁移实验所处的pH环境近似。然而土壤中Pd、Zn、Fe的含量较高,易与磷酸盐结合生成难溶的磷酸铅、磷酸锌及磷酸铁,从而抑制了nTiO2在土壤柱中的迁移。另外,土壤中总磷的重量百分比仅为0.21%,含量非常低,可以排除在实验中解吸出的磷受到土壤中磷释放的影响,确保了实验数据的可靠性。
不同离子浓度下,nTiO2颗粒在土壤表面的吸附效率(α)、沉积速率系数(κ)和单一介质接触效率(η0)见表3。相同背景溶液浓度,无P和有P条件下,nTiO2颗粒在土壤表面的吸附效率以及沉积速率系数差异明显。无 P 存在时,α 和 κ 分别为 4.46×10-4、3.481 h-1;P 存在时,α 和 κ 分别减小到为 6.25×10-5、0.542 h-1。吸附效率降低,沉积速率降低,nTiO2颗粒在土壤中的悬浮性更好。同时,Lmax也从无P时的22.434 cm增加到144.123 cm,迁移距离更大,更有利于nTiO2颗粒在土壤中的迁移。
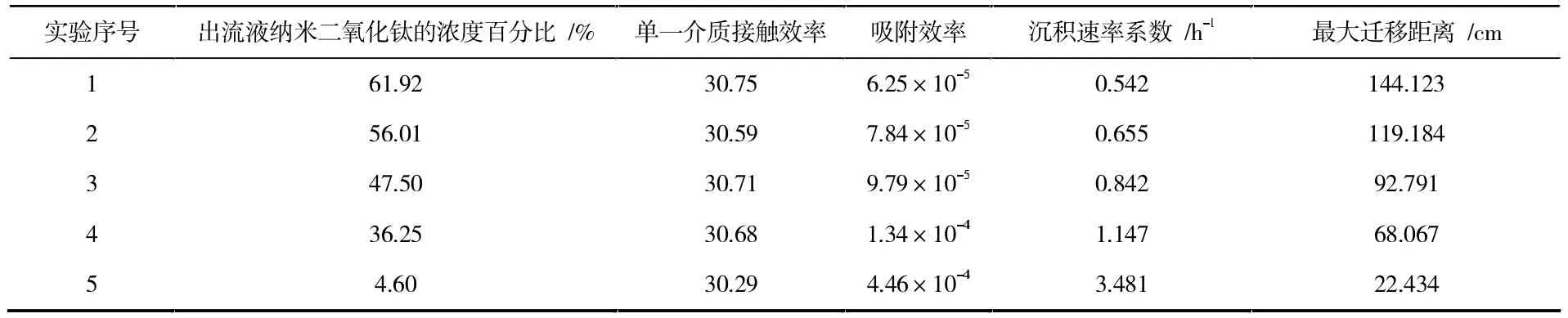
表3 迁移实验中纳米二氧化硅颗粒和石英砂的物理参数和计算参数
2.4 有磷酸盐时NaNO3电解质浓度对nTiO2颗粒在土壤柱中迁移的影响
从图2(b)中可以看出,随着背景NaNO3电解质溶液浓度的增加,nTiO2的出流比逐渐减小。背景溶液NaNO3浓度为0.1 mM时,nTiO2的出流比为61.92%;当NaNO3电解质溶液的浓度逐渐增加到5.0 mM时,nTiO2的出流比下降到36.25%;当NaNO3电解质溶液的浓度增加到10.0 mM时,柱子发生了堵塞。
从表3可以看出,在nTiO2颗粒悬浮液中,当NaNO3浓度增加时nTiO2颗粒的吸附效率也随着增加。当NaNO3从0.1 mM增加至5.0 mM时,吸附效率由6.25×10-5增加到1.34×10-5,此外,沉积速率系数随着离子浓度的变化有着相同的规律,当离子浓度从0.1 mM升高至5.0 mM时,沉积速率系数变化很大,从0.542 h-1增加至1.147 h-1,而单一介质接触效率在离子浓度变化过程中维持在 30.7左右。当离子浓度进一步增加到10.0 mM时,柱子发生了堵塞。因此,nTiO2颗粒的迁移规律与一般的纳米颗粒在水体系中的迁移行为一致,即随着离子浓度的增加,纳米颗粒的吸附效率也随着增加,加快沉积,这样使得高的离子浓度时,nTiO2颗粒更容易滞留在土壤柱中,因此减少了nTiO2颗粒在土壤柱中的迁移。也就是说,高的吸附效率和沉积速率导致nTiO2颗粒低的迁移率。结果如图2b观察到的nTiO2颗粒的出流比随着NaNO3浓度的增加不断减少。此外,最大迁移距离(Lmax)也能说明nTiO2颗粒在石英砂柱中的迁移情况。当溶液中NaNO3从 0.1 mM增加至5 mM时,nTiO2颗粒最大迁移距离由144.123 cm减小到68.067 cm,表明高浓度NaNO3的存在抑制了nTiO2颗粒在土壤柱中的迁移,见表3。此外,据报道nTiO2颗粒在球形玻璃珠的柱子中最大迁移距离为10 cm,而在土壤柱中,由于土壤的特定作用,nTiO2颗粒的最大迁移距离为370 cm[14,24]。这一现象说明纳米颗粒的迁移情况受到纳米颗粒本身的特性和多孔介质的性质共同作用。
用两点动力学(TSKAM)模型模拟的曲线同样见图2,相应的参数见表4。表4中的R2都在0.9以上,说明两点动力学模型能较好的模拟nTiO2在真实土壤柱中的迁移情况。由表4可知,在土壤柱中,位点1(K1)的吸附系数远大于位点1(K1d)的解吸系数,K1d/K1的值都小于1,表明nTiO2颗粒在位点1上有较强的吸附作用或阻塞效应[25]。这一规律与nZnO在土壤柱中的迁移规律一致。此外,随着NaNO3浓度的增加,位点2(K2)的吸附系数逐渐增加,表明应变作用随着NaNO3浓度的增加而增加,这也与迁移实验的结果一致。

表4 不同实验条件下两点动力学吸附模型模拟参数
3 结语
(1)磷酸盐存在时,nTiO2表面负电荷更多,其弥散稳定性也随之提高。(2)随着电解质NaNO3浓度的增加,nTiO2颗粒表面Zeta负电位逐渐减少。(3)磷酸盐的加入,促进了nTiO2颗粒在土壤柱中的迁移性。(4)电解质NaNO3浓度的增加,抑制了nTiO2颗粒在土壤柱中的迁移性。(5)两点动力学吸附模型能够很好地模拟了纳米材料在土壤柱中的迁移穿透曲线。模型结果表明,nTiO2颗粒在位点1有较强的吸附作用或阻塞效应,当P存在时,吸附作用或阻塞效应明显减弱,且随着电解质NaNO3浓度的增加,使得应变作用增加,从而抑制了nTiO2颗粒在土壤柱中的迁移性。
