肥胖型与非肥胖型多囊卵巢综合征患者内分泌代谢的差异
2018-09-18
(大同市第二人民医院,山西 大同 037005)
多囊卵巢综合征(polycystic ovary syndrome,PCOS)是育龄期妇女最常见的一组内分泌及代谢紊乱性疾病之一。根据美国国立卫生院共识会议最新指南推荐,世界范围内发生率为6%~10%,而在我国19~45岁的育龄妇女中患病率为5.6%[1]。PCOS的病因至今尚未阐明,目前研究认为其原因可能为遗传因素与环境因素相互作用所致。PCOS患者具有家族密集性,目前认为属常染色体显性遗传性疾病,即患者的母亲、姐妹、女儿有50%的可能患此病。其中,“母亲月经不规律、父亲早秃、父亲高血压”为三大独立危险因素;其次父亲糖尿病,母亲多毛为相关危险因素[2]。环境方面:如果宫内高雄激素环境,无论卵巢还是肾上腺分泌的雄激素都有影响,低出生体重儿、地域环境、营养不良都与PCOS相关。但是PCOS的三大特征却较明确:a)异质性:不同患者的临床表现不同,很多内分泌特征也不同,比如70%的患者有卵巢多囊样改变,而正常人群中也有16%~22%的人同时伴有卵巢多囊样改变。b)不可治愈性:PCOS目前无法根除,需要长期管理的,故一定要与患者有良好的沟通,提高其治疗的依从性。c)进展性发展的疾病:PCOS患者如果不能很好地管理,会比同龄人早10~20年患代谢性疾病、心血管疾病、及子宫内膜癌,所以要早期识别、积极治疗、终身管理。
鉴于以上特点,本次研究旨在探讨体质量不同的患者,不同的内分泌特征、不同的临床表现,以便于早期发现、管理这方面的患者,使患者从中受益。
1 资料与方法
1.1 一般资料
选取2013年1月~2017年8月在大同市第二人民医院就诊的318例初诊肥胖型PCOS患者为研究组,68例非肥胖型PCOS患者为对照组。年龄17~40岁,平均年龄:前者为(23.26±10.67)岁,后者为(23.88±10.27)岁。
1.2 PCOS的诊断标准
诊断标准依据2003年美国生殖医学会和欧洲人类生殖与胚胎学会提出的鹿特丹标准:a)稀发排卵、无排卵;b)高雄激素血症或高雄激素的临床表现;c)卵巢多囊样改变(3选2)。而本次研究诊断标准依据我国于2011年颁布的标准:把月经不规律、稀发排卵、无排卵,作为诊断的必要条件,其余2项选1项。所以首先需要排除引起排卵障碍的其他疾病:比如高泌乳素血症、甲状腺功能异常、低促性腺激素性闭经、肾上腺功能异常、卵巢功能减退等。其次需要排除引起高雄激素血症的其他疾病:比如先天性肾上腺皮质增生症、卵泡膜细胞增生症、cushing综合征、分泌雄激素的肿瘤等。
1.3 观察指标
1.3.1 一般指标 研究对象的年龄、月经情况、身高、体重、腰围、臀围。测量身高、体重时需脱掉外衣;测量腰围时,取髂前上棘和第12肋下缘连线的中点水平;在臀部最突出部位测量的周径为臀围;根据身高、体重计算体重指数。
1.3.2 内分泌指标 月经规律者取月经第2~3d空腹静脉血;月经不规律、闭经者取空腹随机静脉血,如综合指标不符合早卵泡期时则摒弃不用。测血T、LH、FSH值。
1.3.3 超声检查 月经周期第5d,阴超测直径2~9mm窦卵泡数;对于无性生活者行经直肠超声,卵泡数目测量包括横向和纵向扫描,一个平面的数目。
1.4统计学方法

2 结果
两组患者LH、LH/FSH、T相比较,差异均有统计学意义(P<0.05)。肥胖型与非肥胖型PCOS患者内分泌特征有差异。见表1~3。
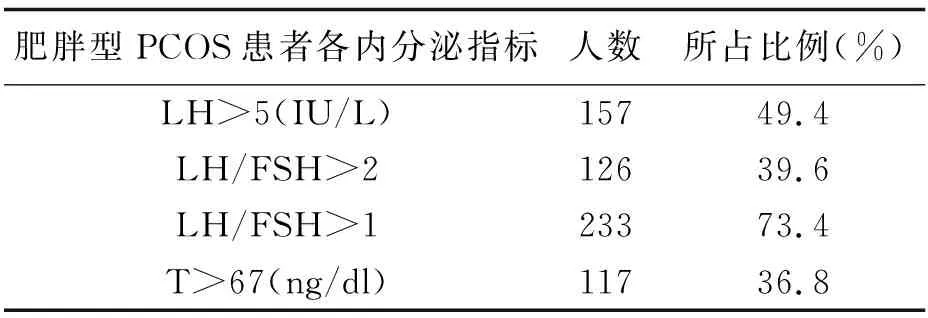
表1 肥胖型PCOS患者各指标所占比例 例

表2 非肥胖型PCOS患者各指标所占比例 例

表3 肥胖型与非肥胖型PCOS患者各内分泌指标比较±s)
3 讨论
PCOS患者不仅表现为近期的稀发排卵、不排卵、月经不调、不孕等问题,其远期的代谢方面症候群包括糖尿病、高血压、高血脂、冠心病、血栓性疾病、子宫内膜癌等发病率也高达33.60%[3]。因此,PCOS不仅是一种生殖内分泌疾病,更是一种代谢性疾病,如不加以干预,其远期并发症必将严重影响患者的生活质量甚至是生命安危。尤其是肥胖型PCOS患者,如果完成了生育问题,检查其内分泌指标虽有异常,但未达诊断标准,往往不过多的干预,而造成一系列的后续的代谢问题,其生命结局堪忧。其实,并非其内分泌指标低,而是肥胖的特殊体质造成其体内发生一系列复杂的代谢方面的改变,结局是其内分泌指标不能尽如人意的展示其本来的高度,比如:肥胖的患者产生瘦素抵抗,可降低垂体LH的释放幅度,所以临床查到的LH值,未必是患者本身的LH值,虽然我国的PCOS诊断标准未把早卵泡期LH/FSH>1作为诊断标准,但是日本一直是把这一项指标作为诊断标准[4]。而且临床工作中,大部分肥胖型PCOS患者早卵泡期LH/FSH>1,对于此类患者,如不给于过多的关注,势必会漏掉,以后会花费大量的精力去纠正、挽救这些后遗问题,而且目前不诊断不等于不治疗。况且,日本这方面的研究也可以代表亚洲、黄种人的特质。所以需关注肥胖型而LH不高的PCOS患者。此外,肥胖还可以产生严重的胰岛素抵抗,后者一方面直接抑制雄激素向雌激素转化,从而使总睾酮升高,同时使性激素结合蛋白降低,使游离睾酮升高,还可使胰岛素样生长因子结合蛋白降低,胰岛素样生长因子升高,从而也使雄激素升高,此外,还可直接作用于卵泡膜细胞生成雄激素,直接作用于垂体,升高肾上腺来源的雄激素[5]。总之,肥胖本身是一种疾病,肥胖的多囊卵巢综合征患者有一些特殊的、复杂的生理、病理、代谢过程,不能简单的一概而论,而要个性化管理。近年来对于抗苗勒管激素及抑制素B的研究日益增多,对于多囊卵巢综合征患者来说,无疑是一个福音,阮祥燕等[1]的研究得出AMH预测PCOS的值为4.84μg/L,INHB预测PCOS的cut-off值为70.8ng/L,此项研究对于肥胖型PCOS,其他妇科内分泌指标不明显的患者可提高检出率,此次研究因地域问题尚未加入AMH、INHB值,在以后的研究中将逐步完善各项指标。
