基于任务分析的化学方程式整体化教学
2018-09-04甘成秋
甘成秋
(尤溪县教师进修学校,福建 尤溪 365100)
化学方程式是用于表征物质化学性质及其变化的符号系统,是认识化学现象及其本质的思维工具,具有简约表达、内涵丰富的特点。[1]因此,教学过程中应引导学生对化学变化内涵进行全面认知,并用简洁的符号表达之。然而,很多教师常以水通电分解为例,先写反应文字(符号)表达式,后从微观角度点拨,接着讲解最小公倍数、奇偶法等配平方法,并且总结化学方程式的书写规则“写、配、标”,最后大量练习化学方程式书写技能。将化学方程式教学重点放在书写技能训练层面,其结果是学生在运用时,会出现随意捏造不存在的反应或物质;将化学计量数写在化学式中间;漏写“↑”“↓”;不能从新情境中获取已熟悉的化学方程式等现象。究其原因是教师无法呈现化学方程式意义,使学生失去自觉学习心理倾向;学生未对化学反应过程深入思考与探究,以至于不能准确把握其内涵实质,忽视了背后所隐含的认识思维。
一、整体化教材逻辑分析
教材将化学方程式安排在氧气性质及其制取,水的组成,分子、原子,元素、化学式等相关章节之后,其目的是通过氧气相关知识的学习,使学生获得化学变化的感性素材;水通电分解微观分析过程让学生初步体验物质发生变化的微观本质;元素、化学式的学习让学生感悟到国际性的化学语言具有表达简洁、内涵丰富、交流方便的特点,突显化学符号简约之美。后续课程“根据化学方程式进行简单计算”是建立在对化学变化过程中原子总是按照一定比例进行重组的准确认识基础上的。因此,应将化学方程式概念内涵意义与书写步骤当作一个整体看待,辩证地认识到前者是后者的基础,后者又是前者的外在表现形式。[2]促进学生在意义理解的基础上,掌握化学方程式的书写规则,同时发展对化学变化的思维认识。
二、整体化教学任务设计
基于以上思考,教学过程分为四个阶段:一是感知与认同。感知文字(符号)表达式存在缺陷,引发对化学方程式的价值认同,同时触发如何正确书写化学方程式的认识冲动。二是分析与建构。从物质种类、组成物质的微粒及其化学式等方面分析,让学生充分体验他们之间的联系,厘清反应前后各种原子重组过程,并用化学方程式表征其过程。三是模仿与内化。通过模仿练习进一步完善对化学方程式内涵认识及内化书写规则。四是应用与提升。在应用过程中,逐步提升化学方程式整体认知水平,促进书写达到自动化。
阶段1:感知与认同,产生心理倾向
任务1:(1)回忆并说出碳在氧气中燃烧现象;(2)说出反应物、反应条件、生成物分别是什么?哪些事实证明你的判断是正确的;(3)请用不同方式将该反应表示出来;(4)找出不同种表示方式之间的差异,并谈谈用哪种方式表示化学反应更加简便、可靠。
设计意图:表征化学反应的准确程度依赖于实验现象的清晰再现与准确复述。为此,突出碳与氧气反应现象再现,从中推断出反应物、生成物、反应条件。为进一步证实推断的正确性,学生必须提供更加可信的“往反应后的集气瓶中加入澄清石灰水,观察到石灰水变浑浊”获得生成物为二氧化碳实验证据,从而树立证据意识。在此基础上,要将自己对反应的理解用合适的文字、化学符号、图示等方式表达出来,通过对比,意识到任何表达方式都是建立在客观事实的基础上,不随意捏造不存在的反应;体会到用化学式表征物质具有简约性和便于交流的特点。
阶段2:分析与建构,促进整体认识
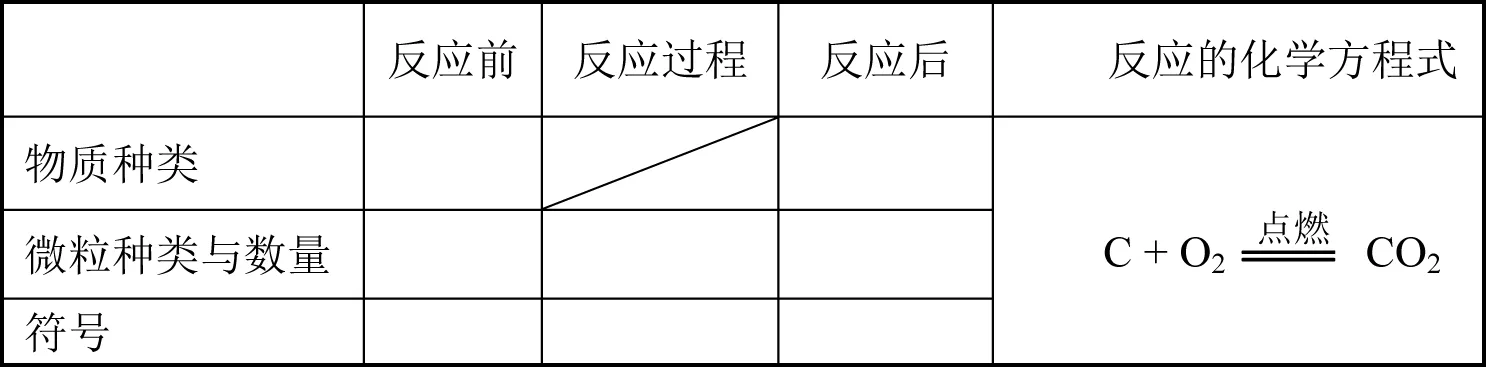
表1 碳与氧气反应过程分析
设计意图:通过表达式中箭号与等号,触发学生的认知冲突,形成要探究等号意义的学习倾向。在此基础上,引导学生运用原子分子观点演绎碳与氧气生成二氧化碳过程,加深对组成物质的微观粒子相互作用认识;加深对反应前后的原子种类、个数不变的感知,加深对反应需要遵循质量守恒定律的理解。同时,在运用元素符号、化学式等化学符号表示物质与微粒时,充分体验“宏观—微观—符号”三重表征相互转换过程。[3]
任务3:(1)查阅资料获知:碳在氧气不足时燃烧会产生一氧化碳,对照表1分析过程,写出该反应的化学方程式;(2)谈谈对书写化学方程式的认识。
设计意图:学生已经初步建立化学反应需遵守质量守恒定律,但在这个反应中,反应前后氧原子个数无法相等,与之前的认识产生了矛盾。该如何解决?根据任务的提示,学生就会从微粒间相互作用的角度思考:1个碳原子其实是与1个氧原子结合形成1个一氧化碳分子,而1个氧分子中含有2个氧原子就需要2个碳原子与之结合形成2个一氧化碳分子。此过程渗透了化学计量数的概念[43],能避免配平时将化学计量数写在化学式中间的错误认识。
阶段3:模仿与内化,形成书写规则
任务4:(1)按照你的认识,书写水在通电条件下反应的化学方程式。(2)从微观角度分析反应物与生成物之间的质量比。
任务5:(1)观察下列实验并描述现象:往装有1~2 mL氯化铜溶液中逐滴加入氢氧化钠溶液;(2)查阅资料获悉:氯化铜溶液存在Cu2+和Cl-;氢氧化钠溶液中存在Na+和OH-;Cu(OH)2为蓝色固体。模仿表1中的思路及物质组成的角度,写出上述反应的化学方程式。(3)讨论在书写化学方程式时应考虑哪些内容。
设计意图:根据对化学方程式表征了实际参加反应物质微粒的认识和提炼出书写化学方程式的思路指导学生运用已架构的书写思路,模仿练习水的电解、氯化铜与氢氧化钠反应的化学方程式书写,进一步检验书写思路的正确性,完善其书写规则。
阶段4:应用与提升,完善认识思路
任务6:写出下列反应的化学方程式:(1)实验室用过氧化氢与二氧化锰制氧气;(2)红磷在空气中燃烧;(3)往澄清石灰水〔Ca(OH)2〕中通入二氧化碳生成白色沉淀(CaCO3)。
设计意图:本阶段主要目的是让学生利用已建立起来的化学方程式书写规则,审视化学反应。通过知识的应用,促进学生进一步反思书写时是否关注反应现象;是否关注反应物、生成物、反应条件以及相关的微粒种类、数量;是否正确书写出各物质的化学式;是否正确配平;是否关注有气体(或沉淀)生成物的状态。在对以上问题做出准确回应后,对有关化学方程式本体知识就构建起清晰认识思路与完整的书写规则。
任务7:从物质种类、反应条件和质量方面考虑,化学方程式“2HgO====△2Hg+O2↑”能提供给你哪些信息?
设计意图:利用具体的化学方程式,反向考查学生在物质组成、微粒间的个数比、反应条件、生成物状态的认知,有利于学生系统认识化学方程式意义,将定性认识与定量认识建立起有效联系,完善知识结构,发展思维品质。
三、结语
综上,教学过程中应当让学生充分感知引入此类概念的价值,在此基础上通过观察和分析情境中的物质组成以及性质,将观察和分析结果用恰当的化学符号进行表征,并在新情境中检验用化学符号表征认识思路的合理性,从而深化对“宏观—微观—符号”三者之间的理解。
