补气药人参、黄芪防治心脑疾病的网络药理学研究
2018-09-04周荣荣李志勇郭非非许海玉唐仕欢
周荣荣,李志勇,郭非非,许海玉,唐仕欢
(1.中国中医科学院中药研究所,北京 100700;2.山西中医药大学基础医学院,山西 晋中 030600;3.中央民族大学药学院,北京 100081)
人参(Ginseng)为五加科植物人参的干燥根和根茎,性甘、微温;味微苦;归脾、肺、心、肾经;黄芪(Astragalus)为豆科植物蒙古黄芪或膜荚黄芪的干燥根,古称“黄耆”,性甘、微温;归肺、脾经。人参、黄芪均是《神农本草经》的上品药材,《神农本草经》言人参:“味甘微寒。主补五脏,安精神,定魂魄,止惊悸,除邪气,明目,开心益智”;言黄芪:“味甘,微温。主治痈疽,久败疮排脓止痛,大风癞疾,五痔,鼠瘘,补虚,小儿百病”。对比《神农本草经》中人参和黄芪的性味功效,发现两者在功效主治上明显不同,人参主补五脏、安神止惊等内科疾病;黄芪主治痈疽疮痈等外科疾病。汉末张仲景著作《伤寒杂病论》中没有人参和黄芪同时使用的描述,统计《伤寒论杂病论》含人参的方剂共42首,涉及的疾病20余种;而关于含黄芪的方剂有7首,主要涉及“痉湿暍病”、“血痹虚劳病”、“水气病”3种内伤杂病,结果显示两者的主治疾病差异明显。后世医家则认为人参、黄芪均味甘,具有均有补中益气,自东晋·葛洪的《肘后备急方》以后,便开始有人参、黄芪共用的记载[1],常将两者作药对相须为用,以补气助阳,随之出现了保元汤、补中益气汤、归脾汤等经典方剂。从人参、黄芪的功效特点进行分析,两者同为补益药,却同中有异,人参的功效偏补五脏,安神志;黄芪的功效偏固表升提。
人参、黄芪补气作用显著,中医认为,人是由气血组成,气能生血、行血、摄血,《灵枢·邪客篇》:“营气者,泌其津液、注之于脉、化以为血”。气虚无力助心行血,而导致血虚,日久发生血瘀、出血,元气大亏甚至会气血匮竭[2]。心主血脉,主藏神,气血运行不畅、心气不足导致心脉无力鼓动气血,最终导致气虚血瘀、心神失养。中医认为心脑疾病与中风、胸痹、心痛、眩晕等多种疾病有关,“气虚血瘀”是心脑疾病的基本病因病机,高血压、动脉粥样硬化、高血脂等是心脑疾病的主要发病因素[3]。研究表明人参、黄芪均在高血压、冠心病、缺血性脑卒中等多种心脑疾病方面疗效显著[4-5]。
中药整合药理学平台[6]整合中医药、系统生物学、药物化学等数据资源,结合数据挖掘、等方法,建立的“中药-成分-靶标-疾病”多维分析平台,可有效的从分子水平揭示中药药效物质与疾病作用关系。为了从分子层面解析补气代表中药人参、黄芪功效的异同点,同时分析两者应用于心脑疾病的作用机制,本研究采用中药整合药理学平台V1.0(http://www.tcmip.cn),探究补气药人参、黄芪在治疗以中风、冠心病为主的心脑疾病的活性成分及其可能的分子作用机制。
1 数据和方法
1.1 数据来源
整合药理学平台V1.0包括中药方剂数据库、中药材数据库、中药成分数据库及疾病/症状靶标数据库。整合药理学平台详细收录了400多中药材的基本信息(中文名称、拉丁名、性味归经等)及其化学成分信息(成分名称、中英文名称、分子式等),并从Drugbank、OMIM(Online Mendelian Inheritance in Man)、HPO(human phenotype ontology)、TTD(Therapeutic Target Database)、KEGG(Kyoto Encyclopedia ofGenes and Genomes)等数据库中整合疾病基因、药物靶标基因及相关生物信息等资源。
1.2 研究步骤
1.2.1 信息设定
登陆中药整合药理学平台,新建“人参”、“黄芪”、“人参与黄芪”3项任务,按照“人参”、“黄芪”、“人参、黄芪”分别添加保存;由于平台检索词限制,以“中风”、“冠心病”、“心血管疾病”相关的英文名称“Stroke”、“Coronary”、“Cardiovascular”、“Cerebrovascular”作为关键词进行检索,将目标检索结果筛选后保存。
1.2.2 设定相似性
分数设定相似性分数为0.8,用以筛选药物潜在靶标。结构类似的生物分子化合物具有类似的物化性质和生物活性[7],相似性分数(卡值)越高,候选化合物相似的药物相对越少。整合药理学平台采用化合物二维结构相似性搜索,通过与FDA(Food and Drug Administration,美国食品和药物管理局)上市药物进行Tanimoto系数计算相似性分值。
1.2.3 一站式计算
信息设定与相似性分数设置完成后,点击“确认”,进行“靶标预测、共性靶标分析、网络构建、核心靶标(Core targets)的筛选、可视化等”一站式分析。
1.2.4 拓扑特征值
中药整合药理学平台基于蛋白-蛋白相互作用建立药物靶标和疾病靶标关系,选取满足3种拓扑结构特征值“连接度(degree)”、“介度(betweenness)”、“紧密度(closeness)”的节点,作为中药方剂矫正疾病失衡网络的候选靶标。
2 结果和分析
2.1 人参和黄芪所含化学成分和药物间共同靶标分析
通过整合药理学平台收集到关于心脑疾病的相关靶标信息有212条;收集人参、黄芪化学成分187个,显示人参共158个化学成分,主要为人参皂苷类、人参多糖类、氨基酸、生物碱、黄酮、甾醇等多种化学成分;黄芪29个化学成分,主要是黄芪皂苷类、黄芪多糖类、氨基酸类等;人参和黄芪的共性靶标显示160个。对人参、黄芪的化学成分进行结构靶标预测,相似性分数为0.8时,黄芪的预测靶标数是230个,人参的预测靶标数是2 000个。
2.2 人参-黄芪预测靶标分析及核心靶标(Core targets)分析
2.2.1 人参-黄芪药物预测靶标GO(Gene Ontology)富集分析、KEGG通路富集分析
对人参-黄芪的预测靶标进行GO(Gene Ontology)富集分析、KEGG通路富集分析,本机自动保留具有统计学意义(P-value<0.01)的条目,得到208条GO(Gene Ontology)富集分析结果,发现人参-黄芪的预测靶标与mitochondrial electron transport(线粒体电子传递)、NADH to ubiquinone(NADH泛醌)、NAD binding(NAD结合)、cytosol(细胞质)、mitochondrion(线粒体)、mitochondrial matrix(线粒体基质)、oxidation-reduction process(氧化还原过程)、GTPase activity(GTP酶活性)、extracellular exosome(胞外体)、biotin metabolic process(生物素代谢过程)、pyruvate metabolic process(丙酮酸的代谢过程)、tricarboxylic acid cycle(柠檬酸循环)、cardiac muscle cell apoptotic process(心肌细胞凋亡过程)等生物功能信息有关;74条KEGG通路富集分析结果,发现人参、黄芪的预测靶标与Carbohydrate metabolism(碳水化合物代谢)、Parkinson's disease(帕金森氏病)、Citrate cycle(TCA cycle)(柠檬酸循环)、Propanoate metabolism(丙酸代谢)、Purine metabolism(嘌呤代谢)、Alzheimer's disease(阿尔茨海默病)、Huntington's disease(亨廷顿病)、Oxidative phosphorylation(氧化磷酸化)等生物通路有关。
2.2.2 人参-黄芪“药物-靶标-疾病”网络的核心节点(Hub)分析
平台以“节点连接度(degree)”的2倍中位数为卡值选取Hub节点,并对核心节点(靶标)进行GO(Gene Ontology)富集分析、KEGG通路富集分析。结果得到1 598个核心节点,2 523条GO(Gene Ontology)富集分析结果和206条KEGG通路富集分析结果。
2.2.3 核心靶标分析
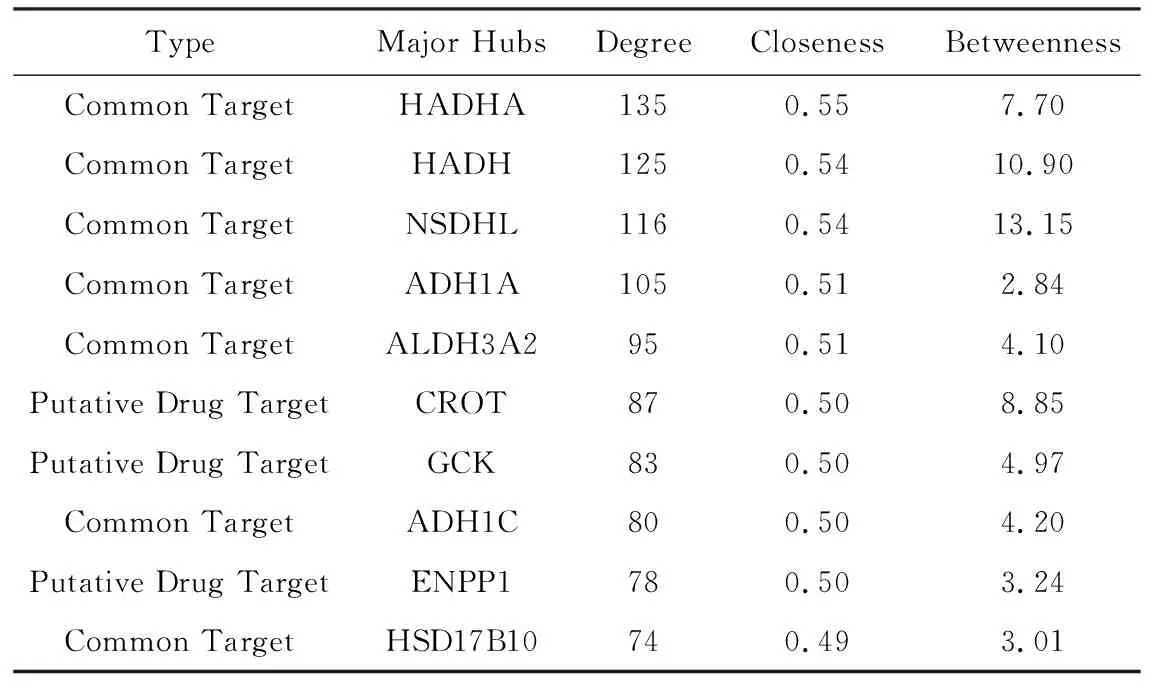
表1 人参、黄芪抗心脑疾病核心靶标表(Degree值排名前10位)Tab.1 The Core target of Ginseng and Astragalusagainst cardio-cerebral diseases
平台设定同时满足大于节点“连接度(degree)”、“介度(betweenness)”、“紧密度(closeness)”的中位数为卡值,选取关键核心靶标,并进行核心靶标的GO(Gene Ontology)富集分析、KEGG通路富集分析,建立核心靶标网络图和“中药-成分-关键药靶-通路”网络图。结果得到463条核心靶标信息,其中Common Target(共同靶标)62条、Putative Drug Target(潜在药物靶标)131条、Known Disease Target(已知疾病靶标)25条。如表1;
2.2.4 可视化分析
核心靶标可视化图是按照degree值由大到小排列取其前100位进行绘制的。核心靶标网络图(图1)显示HADHA,HADH,NSDHL等33个共同靶标(绿色);CROT,GCK,HSD17B10等46个潜在药物靶标(橘红色);MAPK3,POMC,DLG4,GCGR,P2RY12,GLP1R等6个已知靶标(黄色),若干其它靶标(灰色)。人参-黄芪“中药-成分-关键药靶-通路”网络可视化图(见图2)是按照核心靶标KEGG通路中P-Value值由小到大排列,取其前30位进行绘制的。
2.2.5 关键靶标GO(Gene Ontology)富集分析和KEGG通路富集分析
平台对人参-黄芪干预心脑血管疾病的关键靶标分析,得到1759条GO(Gene Ontology)富集分析结果和188条KEGG通路富集分析结果。GO富集分析显示人参和黄芪通过参与cytosol(细胞质)、mitochondrion(线粒体)、ATP binding(ATP结合)mitochondrial matrix(线粒体基质)、mitochondrial inner membrane(线粒体内膜)等基因本体表达生物功能,如表2所示;KEGG通路分析预测人参和黄芪在关于Purine metabolism(嘌呤代谢)、Carbon metabolism(碳代谢)、Endocrine system(内分泌系统)Carbohydrate metabolism(碳水化合物代谢)、Nucleotide metabolism(核苷酸代谢)、Pyruvate metabolism(丙酮酸代谢)、Neurodegenerative diseases(神经退化性疾病)、Huntington's disease(亨廷顿病)、Parkinson's disease(帕金森氏病)等主要疾病靶标通路,如表3所示。
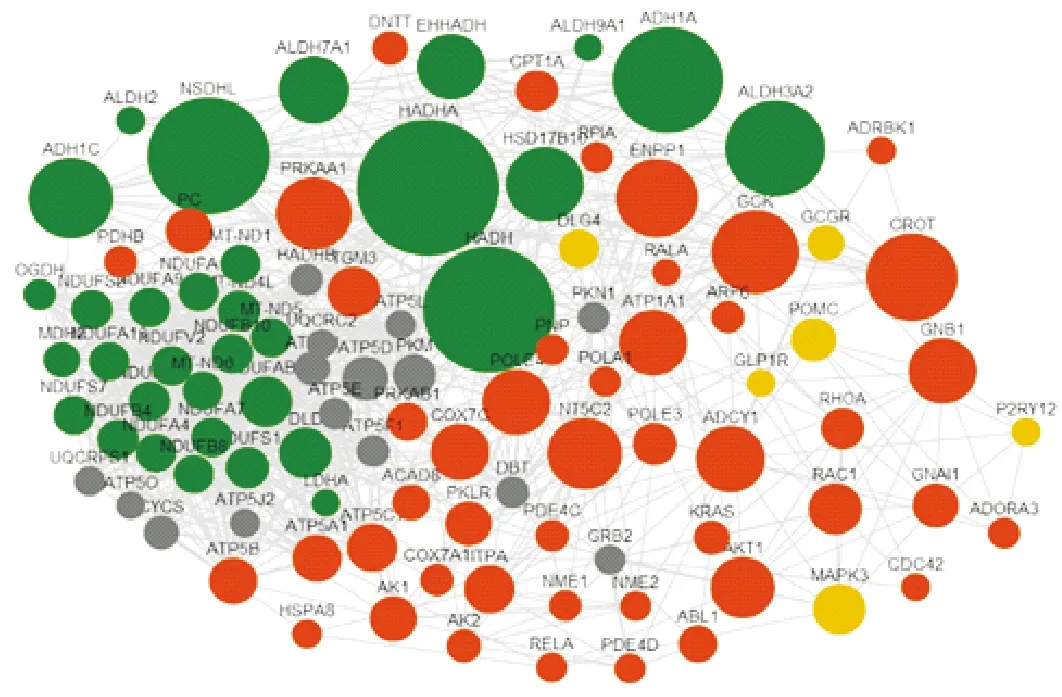
图1 核心靶点网络Fig.1 The key target network
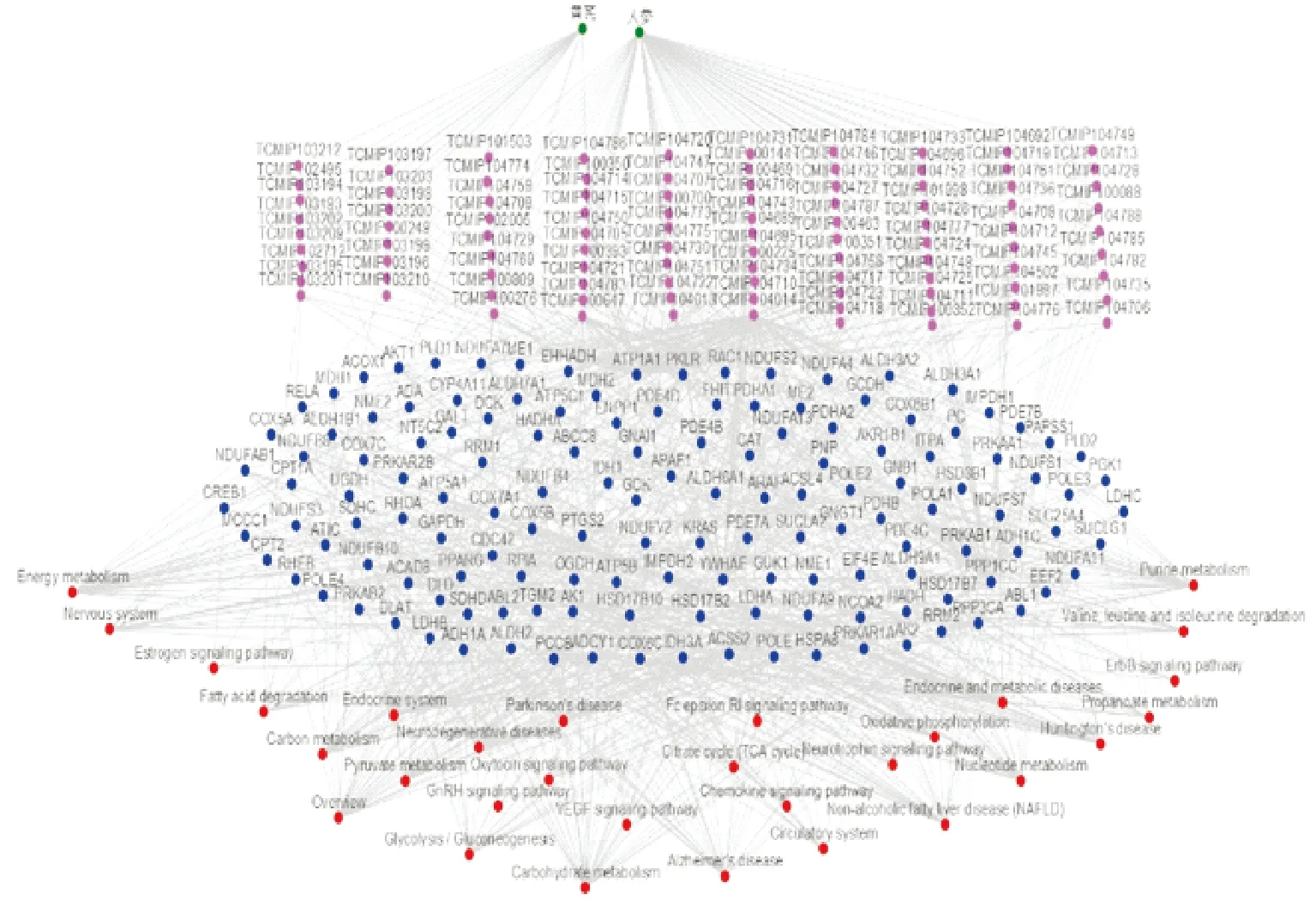
绿色-中药;紫色-成分;蓝色-关键靶标;红色-通路图2 人参、黄芪“中药-成分-关键药靶-通路”网络Fig.2 The "Traditional Chinese Medicine-ingredient-key drug target-pathway" network of Ginseng and Astragalus
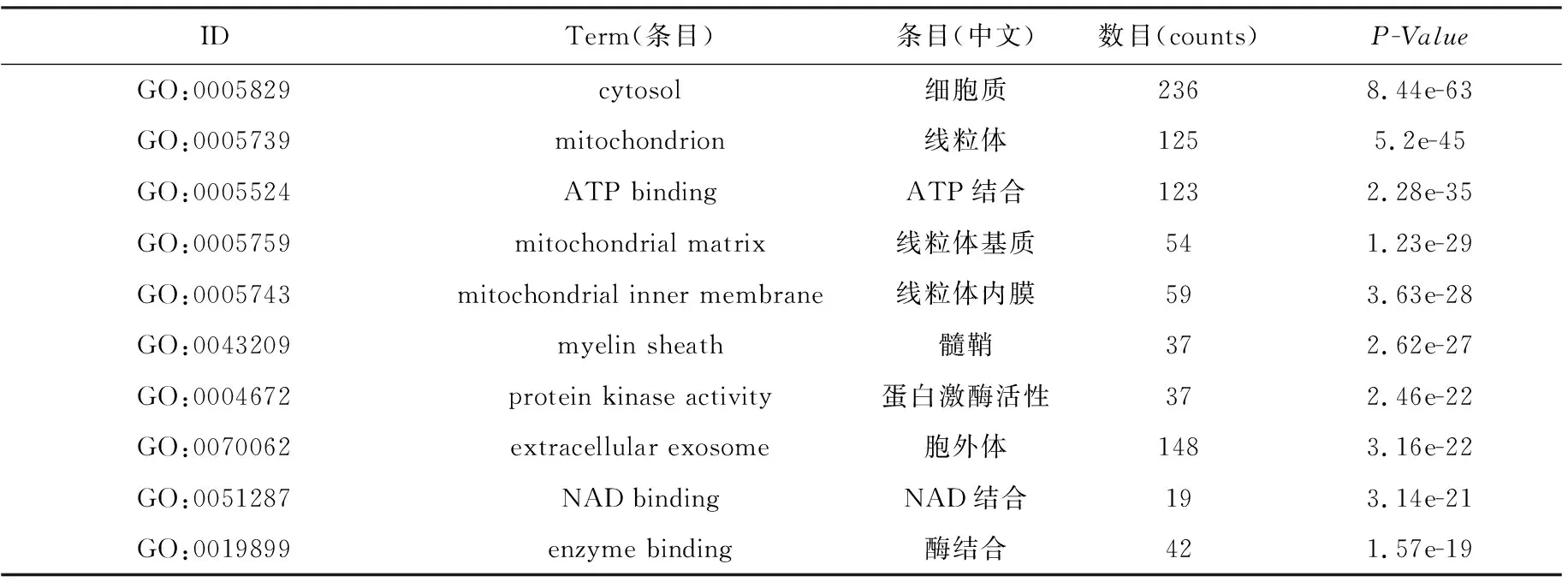
IDTerm(条目)条目(中文)数目(counts)P-ValueGO:0005829cytosol细胞质2368.44e-63GO:0005739mitochondrion线粒体1255.2e-45GO:0005524ATP bindingATP结合1232.28e-35GO:0005759mitochondrial matrix线粒体基质541.23e-29GO:0005743mitochondrial inner membrane线粒体内膜593.63e-28GO:0043209myelin sheath髓鞘372.62e-27GO:0004672protein kinase activity蛋白激酶活性372.46e-22GO:0070062extracellular exosome胞外体1483.16e-22GO:0051287NAD bindingNAD结合193.14e-21GO:0019899enzyme binding酶结合421.57e-19
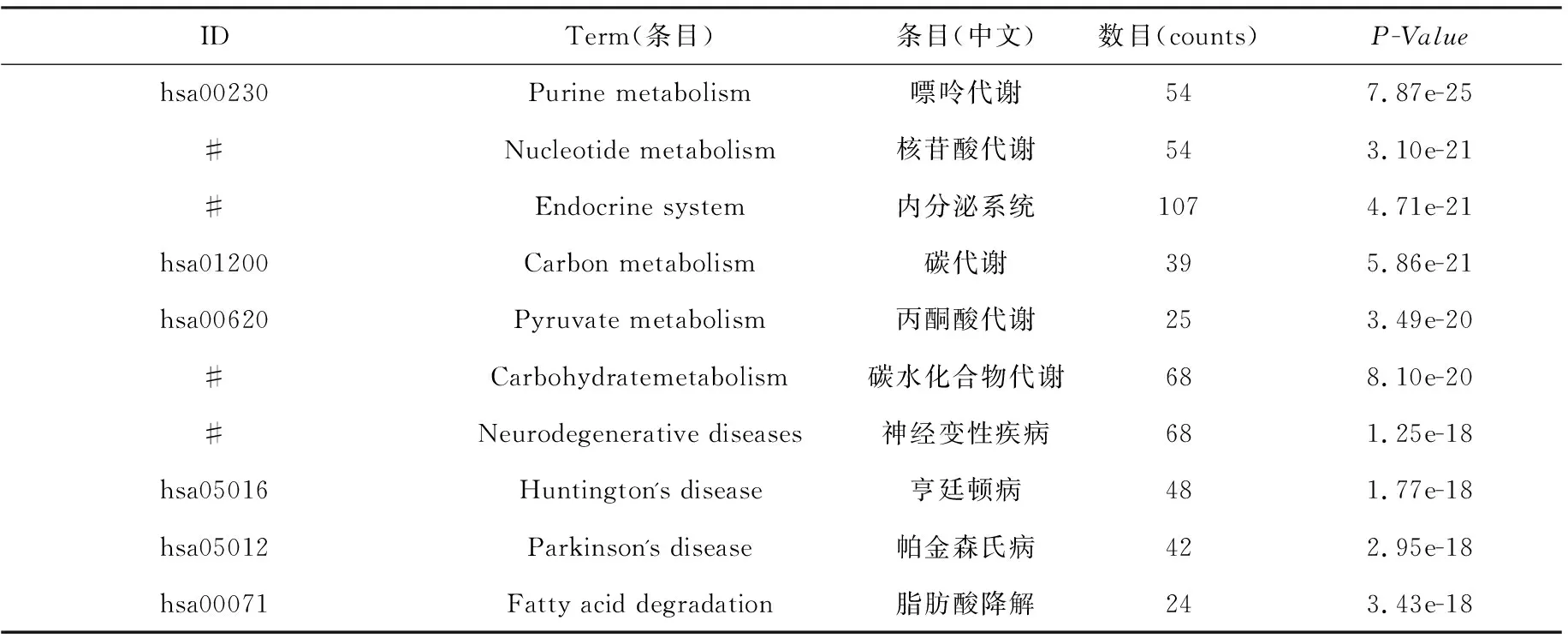
表3 人参、黄芪抗心脑疾病主要通路表(P-Value排名前十位)Tab.3 The main pathways of Ginseng and Astragalus membranaceus against cardio-cerebral diseases
3 讨论
人参、黄芪的主要成分多是小分子活性物质,人参皂苷类、多糖类、黄芪甲苷类等主要是能源物质和碳源物质,参与供能、供氧以及蛋白质、糖类、脂肪代谢等生物过程。人参皂苷、黄芪甲苷类均与ATP1A1有密切关系,人参皂苷类[8]、黄芪甲苷类[9]均具有保护心肌损伤、调节免疫、保护脑细胞、抗炎等作用,ATP1A1[10]是Na+/K+ATP酶的亚单位,研究表明通过调节Na+/K+ATP酶可以延长缺血性脑卒中的治疗窗口[11],减少心肌纤维化[12]。人参与黄芪治疗心脑疾病存在百余种共同靶标,其中HADHA、HADH、NSDHL、CROT、GCK、ADH1C、ENPP1、HSD17B10等具有较高的拓扑特征值,这些靶标都是参与线粒体活动、脂质代谢、氧化反应等过程的重要基因,线粒体[13]是负责能量产生、转化、传递以及氧化代谢过程重要的细胞器,心脏具有高容量的线粒体系统,线粒体会产生和消耗大量的能量(ATP)支持心肌功能,参与心脏肥大、心脏衰竭等病理过程。HADHA(hydroxyacyl-CoA dehydrogenas)是拓扑特征值最高的靶标(Degree值为135,Closeness值为0.55,Betweenness值为7.71),它是线粒体三功能蛋白(mitochondrial trifunctional protein,MTP)的一个亚基,研究表明HADHA参与脑星形胶质细胞的线粒体脂肪酸βCPT1氧化过程[14]。HADH(hydroxyacyl-CoA dehydrogenase)存在于肝、心、肾、脑等大部分组织中,参与线粒体脂肪酸氧化与能量转化,与低血糖脑病、高胰岛素低血糖、周围神经病变等有密切关系[15]。NSDHL基因则是参与神经元胆固醇、类固醇激素和脂类的合成过程,与心血管系统形态异常、脑畸形等疾病、再生障碍性贫血等疾病有关[16]。CROT(Carnitine O-Octanoyl transferase)是参与在脂质代谢和脂肪酸β-氧化的重要基因,心肌脂肪酸β氧化也是维持心脏能量平衡和收缩功能的关键[17]。GCK(Glucokinase,葡萄糖激酶)广泛存在于脑、心脏、肾脏、脂肪等组织,是胰岛β细胞或肝细胞糖代谢(葡萄糖磷酸化)的一个重要因素,参与促胰岛素分泌、降低血糖等过程[18];ADH1C(Alcohol dehydrogenase 1C,乙醇脱氢酶1C)是主要存在消化道和肝脏中的酒精代谢酶,参与氧化还原酶、乙醇脱氢酶(NAD)、视黄酸等的生物过程,研究表明其与酗酒、神经退行性疾病帕金森病、房颤等疾病有关[19]。
人参与黄芪属于不同科属,药性、成分、功效、药理作用等各有不同,在同一疾病、同一靶标等作用程度也不同。《金匮要略·中风历节病脉证并治第五》言:“缓则为虚,营缓则为亡血,卫缓则为中风……”,人参善补五脏之气,补气兼能养阴生津(营分),温养心气且补气作用迅速;黄芪善走卫分,补气兼能扶阳利水[20],人参、黄芪从《伤寒杂病论》中各司其职,到后世医家将其相须为用,体现了中医对药物“认识—实践—再认识”的发展过程。利用BATMAN-TCM数据分析工具(http://bionet.ncpsb.org/batman-tcm/)预测人参和黄芪的不同生物过程,人参参与糖酵解、柠檬酸循环、脂肪酸降解、组氨酸降解、赖氨酸合成、PPAR信号途径等生物过程,主要治疗疼痛、高血压、冠心病、心力衰竭、神经性疾病等疾病;黄芪参与苯丙氨酸、酪氨酸和色氨酸等生物合成、代谢过程,除了治疗心脑疾病外,黄芪也具有治疗呼吸系统疾病、性功能障碍等疾病的作用。《伤寒论》太阳、少阴、厥阴病描述皆有身痛症,分析发现人参的疾病靶标富集结果中多次出现“疼痛”的信息,研究表明[21]人参皂苷类具有诱导镇痛的作用。
通过网络药理学分析表明,人参、黄芪补气作用与线粒体代谢、氧化代谢、抗炎免疫有关,人参与黄芪在参与心脑疾病过程中,主要通过线粒体相关代谢通路,调节HADHA、HADH、NSDHL、ADH1A、ADH1C、ALDH3A2等关键靶标发挥氧化、产能等发挥共同作用,CROT、GCK、ENPP1等潜在药物靶标虽然不是心脑疾病的上游基因,却是心脑疾病主要致病因素及其并发症的重要活动因子,推测人参、黄芪补气作用与调控线粒体氧化供能有关,这些靶标可能为明确心脑疾病的直接致病原因提供佐证,也为阐释心脑疾病及其并发症发病机制提供重要的参考价值。
