分散固相萃取-高效液相色谱串联质谱法同时测定沉积物中氟喹诺酮类药物残留
2018-08-24钱卓真王丽娟汤水粉罗方方
钱卓真,梁 焱,王丽娟,汤水粉,罗方方,陈 思
(1.福建省水产研究所,福建省海洋生物增养殖与高值化利用重点实验室,福建 厦门 361013; 2.海南省环境科学研究院,海南 海口 570026)
氟喹诺酮类药物是一类人工合成的广谱类抗生素药物,被广泛应用于畜禽、水产养殖及医药行业。由于该类药物的大量及不恰当使用,大量药物被直接排入环境中,或通过人体、动物以间接方式进入环境[1-2]。据文献报道,氟喹诺酮类药物不仅在动物源性食品中广泛被检出,而且在环境水体[3-5]、沉积物[6-8]、土壤[9]中也普遍被检出。该类药物在沉积物和土壤中性质稳定,半衰期较长,不易降解[10-11],可对环境造成直接污染。且该药物还可能对土壤和沉积物中微生物的耐药性产生压力,诱导抗生素抗性基因和耐药性细菌的产生,从而产生严重的生态毒性[12-13]。因而氟喹诺酮类药物引起的环境污染问题已成为近年来国内外的研究热点[14]。
目前已报道的检测方法有电化学法、酶联免疫吸附法、高效液相色谱法、高效液相色谱串联质谱法、荧光偏振免疫分析法等。其中,高效液相色谱串联质谱法具有准确度高、重现性好等优势,已成为氟喹诺酮类药物残留测定的主要检测方法。与高效液相色谱串联质谱法结合的传统净化方法主要是固相萃取法,但其步骤繁琐、耗时,费用较高。虽然近几年基于固相萃取法衍生出一系列新的净化方法,如磁性氧化石墨烯固相萃取法[15]、分子印迹固相萃取法[16]等,但整体研究难度仍偏大。2003年美国农业部提出了一种快速、简单、成本低廉的新型分散固相萃取净化技术。该技术问世以来,已经成为了全球检测水果、蔬菜中农残的标准样品处理方法,近年来也涉及到越来越多的不同领域,比如肉类、血液、酒,但应用于沉积物中氟喹诺酮类药物残留测定的研究鲜有报道。
本研究考察了不同吸附剂净化效果,将优化后的分散固相萃取法应用于沉积物样品的前处理,拟建立沉积物中5种典型氟喹诺酮类药物同时被测定的高效液相色谱-串联质谱法,将为沉积物样品中氟喹诺酮类药物多残留量痕量快速检测和判断沉积物中氟喹诺酮类药物污染提供技术支持。
1 材料与方法
1.1 材料与试剂
标准品诺氟沙星(Norfloxacin,NOR)、环丙沙星(Ciprofloxacin,CIP)、恩诺沙星(Enrofloxacin,ENR)、沙拉沙星(Sarafloxacin,SAR)、氟罗沙星(Fleroxacin,FLE)购自Dr.Ehrensorfer公司(纯度>95%);氘代诺氟沙星(Norfloxacin-D5,NOR-D5)、氘代环丙沙星(Ciprofloxacin-D8,CIP-D8)、氘代恩诺沙星(Enrofloxacin-D5,ENR-D5)购自Witega公司(纯度>99%)。上述标准品用甲醇配制成100 μg/mL的标准储备液,于-18℃下避光保存,有效期为6个月;用甲醇配制成NOR、CIP、ENR、SAR、FLE的1 μg/mL混合标准溶液,于4℃下避光保存,有效期为1个月;用甲醇配制成NOR-D5、CIP-D8、ENR-D5的1 μg/mL混合标准溶液,于4℃下避光保存,有效期为1个月。
甲醇、乙腈、甲酸均为色谱纯,购自美国Tidea公司;乙酸铵、磷酸(H3PO4)、二水合磷酸二氢钾(KH2PO4·2H2O)、乙二胺四乙酸二钠(Na2EDTA)、氯化钠(NaCl)为化学纯,购自国药集团化学试剂有限公司;无水硫酸镁(MgSO4)、N-丙基乙二胺(PSA)、石墨化炭黑(GCB)、C18均购置天津博纳艾杰尔科技有限公司;0.22 μm尼龙微孔滤膜购自天津市津腾实验设备有限公司。磷酸盐缓冲溶液:2.72 g KH2PO4·2H2O与0.13 mL H3PO4,用超纯水定容至100 mL。
1.2 仪器与设备
TSQ QUANTUM ULTRA 高效液相色谱-串联质谱仪:美国Thermo-Fisher Scientific公司;AB204-E型、PL203型电子分析天平:Mettler Toledo公司;DT5-5型低速台式离心机、GT16-3高速台式离心机:北京时代北利离心机有限公司;TDL-80-2B低速离心机:上海安亭科学仪器厂;MS3型旋涡混合器:德国IKA公司;ZZDCH16水浴氮吹仪:广州智真生物科技有限公司;KQ3200E超声波清洗仪:昆山市超声仪器有限公司; Milli-Q型超纯水仪:美国Millipore公司。
1.3 仪器分析条件
色谱柱:Ultimate XB-C18色谱柱(2.1 mm×150 mm,5 μm);柱温:40℃;流动相A:4 mmol/L乙酸铵-0.1%甲酸水溶液,流动相B:0.1%甲酸甲醇;流速:0.3 mL/min;梯度洗脱程序见表1。电喷雾电离(ESI)正离子扫描模式,多反应监测模式(MRM),喷雾电压3 500 V,鞘气压力55 Arb,辅助气压力15 Arb,离子传输管温度320℃,雾化室加热温度220℃,碰撞气1.5 mtorr;母离子、子离子和碰撞能量见表2;Q1半峰宽为0.7 Da,Q3半峰宽为0.7 Da。

表1 梯度洗脱程序

表2 氟喹诺酮类药物质谱参数
注:*表示定量离子。
Note:*indicated quantitative ion.
1.4 样品前处理
称取(2.00±0.02)g试样于50 mL塑料离心管中,加入0.15 g Na2EDTA、20 mL乙腈-磷酸盐(1∶1,V/V)缓冲液,NOR-D5、CIP-D8、ENR-D5内标各50 ng,涡旋1 min,超声5 min,剧烈手摇2 min,再加入2 g NaCl继续手摇1 min,4 000 r/min离心5 min;移取7~8 mL上清液于15 mL含有分散固相萃取材料(0.25g MgSO4、0.05 g C18、0.12 g PSA、0.01 g GCB)的离心管中,涡旋1 min,手摇1 min,3 000 r/min离心3 min,移取5 mL上清液,50℃氮吹至干。加入流动相溶液(流动相A∶流动相B=7∶3,V/V)0.5 mL超声溶解,过0.22 μm滤膜后供高效液相色谱-串联质谱仪测定。
2 结果与分析
2.1 色谱及质谱条件的优化
氟喹诺酮类药物具有两性基团,属于酸碱两性化合物,在水溶液中通常以离子形式存在,易与色谱柱内硅胶残留的硅醇基作用,从而造成色谱峰拖尾、峰形异常和保留值不稳定。试验比较了不同品牌的色谱柱,最终选择了端基封尾较好的Ultimate XB-C18色谱柱。同时尝试了乙腈、甲酸、乙酸铵之间多种配比的流动相条件,经过多次比较优化,本试验采用含4 mmol/L乙酸铵的0.1 %甲酸水溶液-0.1%甲酸甲醇溶液,采用梯度洗脱程序,诺氟沙星、环丙沙星、恩诺沙星、沙拉沙星、氟罗沙星在10 min内被洗脱且分离良好,峰型尖锐对称。
用注射针吸1 μg/mL氟喹诺酮类药物混合标准溶液通过蠕动泵以5 μL/min的速度直接注入离子源,在正离子扫描方式下,分别进行一级质谱分析(Q1扫描)、二级质谱分析(Q3扫描)和多反应监测分析,接着分别再对碰撞气能量、电喷雾电压、鞘气压力、辅气压力、离子源温度、雾化室温度进行优化,使每种药物的分子离子与特征碎片离子(子离子)产生的离子对信号强度达到最大,从中选择每种药物的监测子离子对。LC/MS/MS标准品色谱图见图1。

2.2 样品前处理条件的优化
2.2.1 样品提取
提取溶液仍选用常用的土壤抗生素提取溶液——磷酸盐缓冲溶液与乙腈混合溶液。试验采用超声波辅助提取法[17],主要是利用超声波的空化、机械及热效应等来增强提取溶液分子的运动速度及穿透力,从而提高氟喹诺酮类药物的提取效率。且考察了1、2、5、7 min超声提取时间对氟喹诺酮类药物的提取效果。结果表明,随着提取液与目标物超声接触时间的延长,目标物提取效率随之增大。当超声时间增至5 min时,目标物平均回收率达到67.9%~112%。而当超声时间延长至7 min时,目标物回收率无受影响。为了保证提取效率,同时减少杂质干扰,试验最终选择5 min作为超声提取时间。试验中加入NaCl,有助于提取液的乙腈层和水层分开。
2.2.2 样品净化
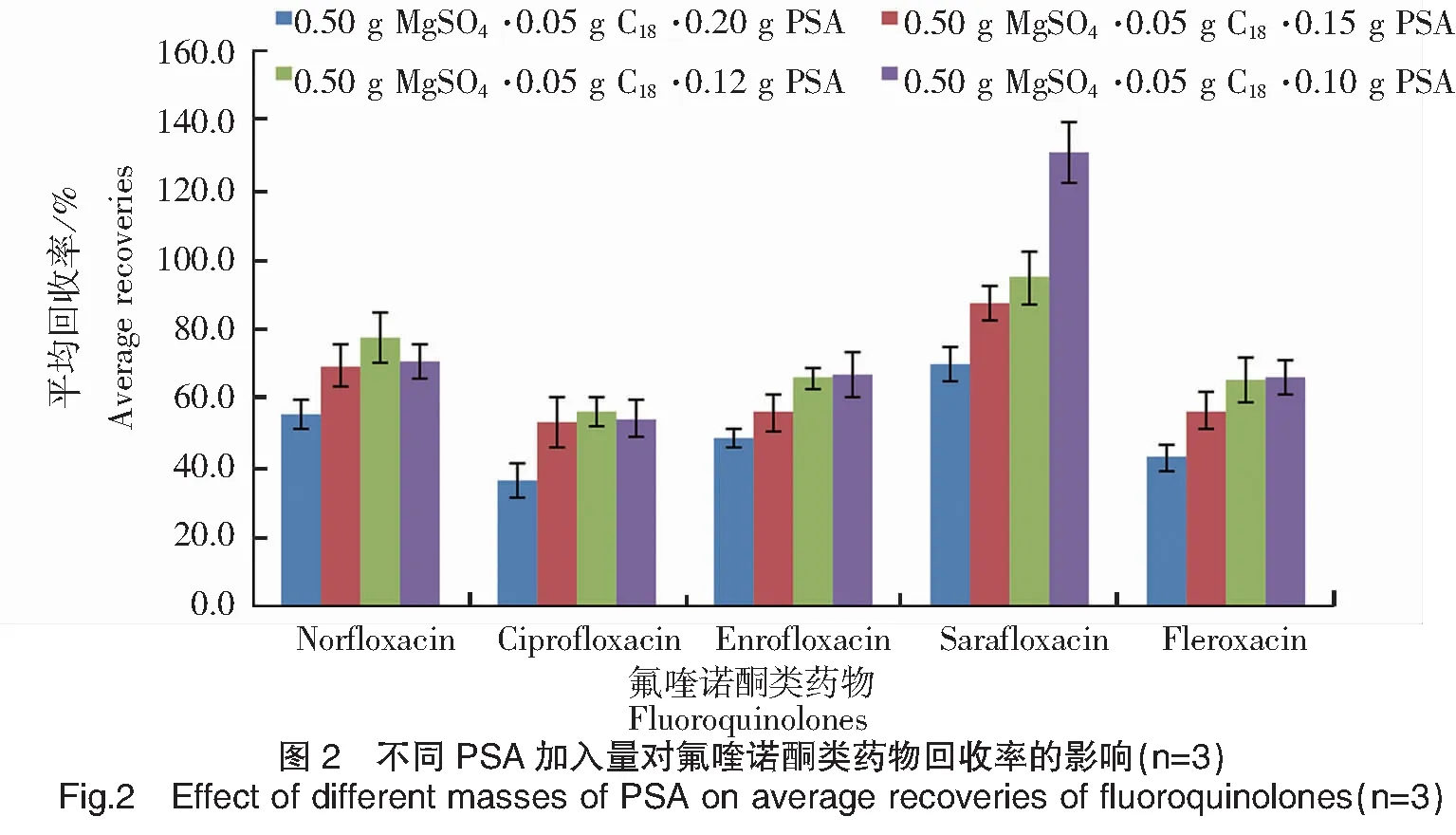
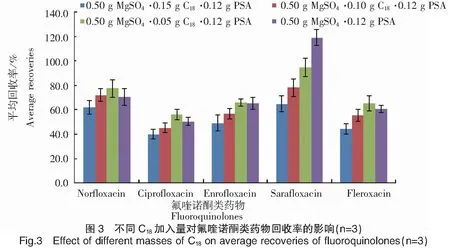
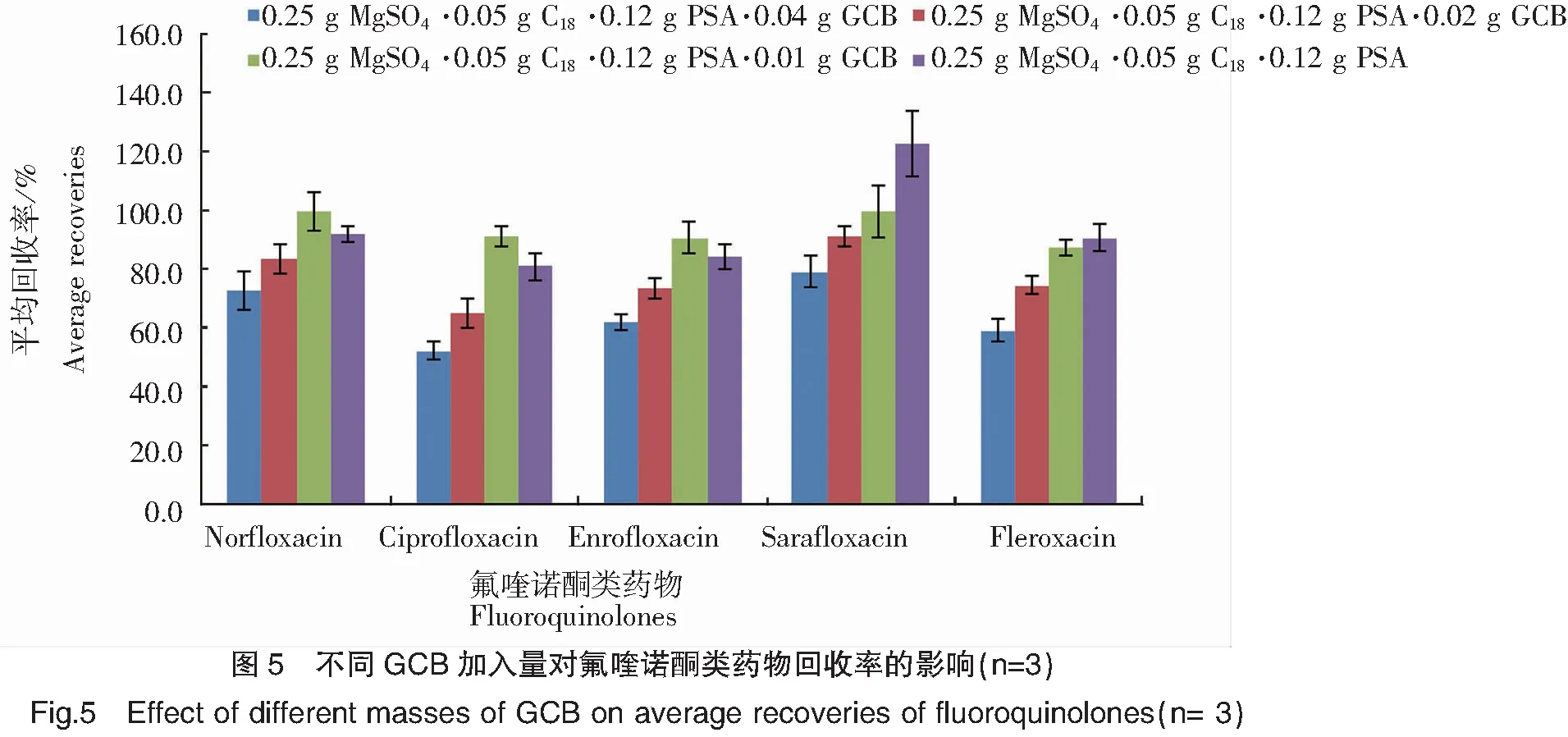
沉积物样品中存在脂肪、色素、甾醇等杂质,因而分散固相萃取法的关键是吸附剂的选择,既能有效除去沉积物中杂质,又不会吸附目标物。常见的分散固相萃取法的吸附材料有MgSO4、PSA、C18、GCB等。作为传统干燥剂,MgSO4用于去除有机溶剂残留的水,且吸水放热的过程可促进目标物的溶出[18]。PSA含有两个氨基,可有效吸附糖类、色素、脂肪酸和其他极性有机酸[19-21]。C18含有十八烷基官能团,属于非极性吸附剂,可以吸附脂肪和一些矿物质[22]。GCB保留特殊的层状结构,能够吸附色素、甾醇等杂质[23]。为了选择合适的吸附剂,试验考察了4种吸附剂量对目标物氟喹诺酮类药物回收率的影响,设计了4个水平:MgSO4(1.00、0.75、0.50、0.25 g),PSA(0.20、0.15、0.12、0.10 g),C18(0.15、0.10、0.05、0 g),GCB(0.04、0.02、0.01、0 g),见图2~图5。试验结果表明,添加浓度为25 μg/kg水平下,单独采用PSA、C18净化,净化效果不佳;因而选用MgSO4、PSA、C18、GCB作为混合净化吸附剂。随着PSA用量的增加,回收率降低(图2);随着C18用量的增加,回收率先升高随后降低(图3);随着MgSO4用量的增加,回收率急剧降低(图4);在保证回收率的基础上,少量GCB的加入,可有效除去提取液中的色素(图5)。经优化,综合考虑净化效果和方法回收率,最终确定0.25 g MgSO4、0.12 g PSA、0.05 g C18、0.01 g GCB作为净化吸附剂。
2.3 标准曲线、线性范围、检出限和定量限
在电喷雾有机质谱电离条件下,沉积物样品提取液具有明显的基质增强效应,这主要来源于沉积物样品中脂肪、色素、甾醇等杂质。为了消除基质效应带来的定量偏差[24],试验采用基质匹配标准曲线法,移取适量混合标准溶液,用空白沉积物样品提取液分别配制成不同质量浓度基质标准溶液,目标物浓度分别为2.5、5、10、50、100和200 ng/mL,内标的质量浓度均为100 ng/mL。以各目标物质量浓度为横坐标(X),各目标物与同位素内标峰面积比为纵坐标(Y)建立标准曲线,各组分浓度与其色谱峰面积比呈良好的线性关系,线性相关系数均大于0.99。以10倍信噪比(S/N)计算定量限,具体数值见表3。
2.4 方法准确度和精密度
以实际采集的养殖区泥质为研究对象,进行标准添加试验,分别以低、中、高三个添加水平进行加标回收试验,每个浓度水平做5个平行试验,考察方法的准确度及精密度。如表3所示,平均回收率在79.8%~112%,相对标准偏差3.2%~9.9%。30 d内25 μg/kg加标浓度下进行6次标准添加试验,考察方法日间精密度,相对标准偏差5.3%~8.6%(表3)。方法的精密度和准确度均能满足药物残留监测需求。选取3种类型的的沉积物——泥质、泥沙、沙质为检测对象,25 μg/kg加标浓度下考察方法适用性,回收率为87.1%~101%,相对标准偏差为3.2%~9.0%(表4)。该方法适用范围广。
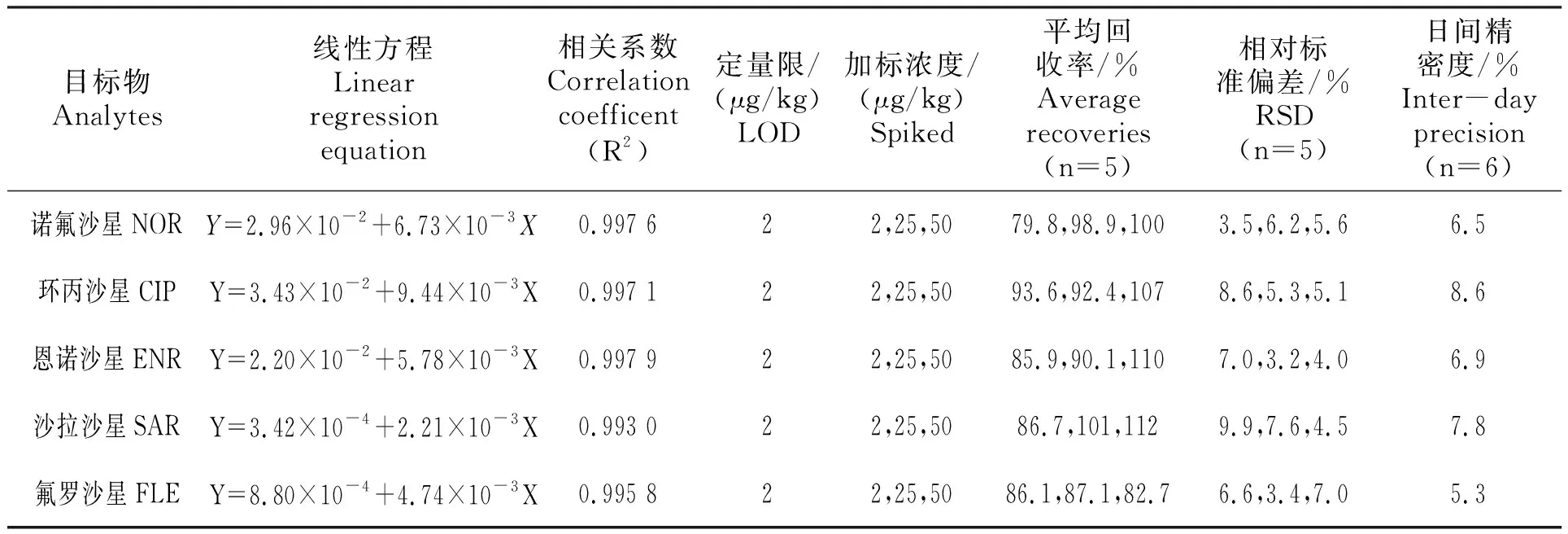
表3 方法准确度和精密度测定结果

表4 不同类型的沉积物样品加标回收率(n=5)
3 结论
本研究系统地建立了分散固相萃取-高效液相色谱-串联质谱法检测沉积物中诺氟沙星、环丙沙星、恩诺沙星、沙拉沙星、氟罗沙星残留的分析方法,并对色谱条件、质谱条件、样品提取净化方法进行了优化,方法简单、快速、灵敏度高,准确度、精密度和各项技术指标均满足国内外残留检测的相关要求。且该方法实用性强,适用于大批量样品的测定,可作为沉积物样品中氟喹诺酮类药物多残留量痕量快速检测的方法,并为沉积物中氟喹诺酮类药物污染的判定提供技术支持。
