工业碳酸钠中硫酸盐含量的分析
2018-08-21,,
, ,
(中盐昆山有限公司,江苏 昆山 215300)
1 试验部分
1.1 方法原理
将 Na2CO3用 HCl中和溶解并煮沸除去CO2,加入过量并且定量标准BaCl2溶液生成沉淀,在相应pH值下以钙镁特(CMG)为指示剂,用EDTA标准溶液滴定过量之BaCl2,反应终点到达时与钙镁特形成红色配合物的金属离子(过量的Ba、Na2CO3中含有的Ca和Mg)全部被EDTA螯合,显示钙镁特本身的蓝色,指示终点的到达,最终计算时将消耗总量减去Ca和Mg的消耗量才是实际过量Ba消耗的EDTA体积。反应如下:
Na2CO3+2HCl=2NaCl+H2O+CO2↑
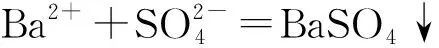
M+Y=MY
1.2 试剂仪器
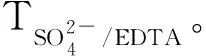
乙二胺四乙酸二钠镁(Mg-EDTA):0.04 mol/L溶液
氯化钡:0.02 mol/L溶液
盐酸:1+1溶液和1 mol/L溶液
氨水:1+1溶液
硝酸:1+1溶液
无水乙醇:分析纯
氨-氯化铵缓冲溶液:pH=10
钙镁特(CMG):1 g/L乙醇溶液
硫酸根标准溶液:3.255 mg/mL
封闭式半微量10 mL A级滴定管
1.3 分析步骤
定量称取Na2CO310 g(准确至0.0002 g)于250 mL烧杯中,加适量去离子水润湿,在搅拌下滴加35 mL (1+1) HCl溶液及1 mL (1+1) HNO3溶液,加热煮沸10 min(中间可适量添加去离子水)以赶尽CO2,冷却至室温,滴加(1+1) NH3·H2O溶液至pH≈8~9,再加热至微沸并冷却,以快速滤纸过滤并洗涤3次以上。将盛有过滤样液的烧杯加热煮沸,待样液体积约为60 mL左右时停止加热,冷却后滴加1 mol/L HCl 2~3滴至pH≈4~5。用移液管准确移取5 mL 0.02 mol/L BaCl2溶液加入样液,边滴加边震荡烧杯,滴加完继续震荡一会,放置40 min。加入5 mL 0.04 mol/L Mg-EDTA溶液,20 mL无水乙醇,滴加9~10滴(1+1) NH3·H2O溶液,加入10 mL氨-氯化铵缓冲溶液,8滴钙镁特指示剂,用0.02 mol/L EDTA标准溶液滴定至溶液由酒红色变为亮蓝色。消耗体积记为V3。
用去离子水做空白试验,消耗体积记为V1。
参照以上步骤另称一份样,在加HCl和HNO3后煮沸冷却,然后滴加(1+1) NH3·H2O溶液至pH≈8~9左右,加热至微沸并冷却,以快速滤纸过滤并洗涤3次以上。将盛有所有过滤样液的烧杯加热煮沸,待样液体积约为60 mL左右时停止加热,冷却后滴加4~5滴(1+1)NH3·H2O溶液,加入10 mL氨-氯化铵缓冲溶液,8滴钙镁特指示剂,用0.02 mol/L EDTA标准溶液滴定至溶液由酒红色变为亮蓝色。消耗体积记为V2。
1.4 结果计算
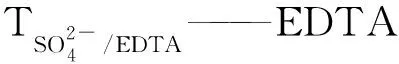
V1——滴定5.00 mL氯化钡溶液EDTA标液的用量,mL;
V2——滴定钙镁离子总量EDTA标液的用量,mL;
V3——滴定硫酸根EDTA标液的用量,mL;
W——所取样品质量,g。
2 结果与讨论
2.1 样品量确认及样品前期处理
2.1.1 BaCl2溶液的加量
2.1.2 加热煮沸驱CO2
准确称样并以少量水润湿后,必须用足够的HCl溶液使样品完全溶解,然后加热煮沸10 min,因为在酸溶纯碱的过程中会产生大量CO2气体,必须加热煮沸将其赶尽,否则会形成BaCO3沉淀造成结果偏高。
2.2 干扰离子消除
2.3 加氯化钡前溶液溶解度控制、沉淀时间、样液酸碱度的控制
2.3.1 溶解度控制
在加BaCl2前要将样品溶液调为弱酸性(pH≈4~5),是减少沉淀吸附杂质的机会,并促使BaSO4晶粒长大,但酸度过高,又会使沉淀溶解,使结果偏低。另外,BaSO4沉淀是离子型晶体,在有机溶剂中的溶解度比在纯水中要小,为了使BaSO4沉淀稳定,在滴定前加入样液体积30%的无水乙醇以降低其溶解度。
2.3.2 沉淀时间
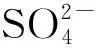
2.3.3 酸碱度控制
在样品滴定时,加入缓冲溶液前,加9~10滴(1+1) NH3·H2O溶液,使样液为中碱性,是确保加10 mL缓冲溶液后样液pH在10左右。
2.4 指示剂的选择
本试验滴定的过程,是EDTA滴定过量剩余的Ba的过程。样液中存在的Ca、Mg,其与EDTA的配合物稳定常数是10.69和8.69,均大于Ba的稳定常数7.86,滴定过程中Ba的反应最缓慢,除了控制滴定速度外,我们选择了钙镁特(CMG)指示剂替换常用的铬黑T指示剂,因为其颜色变化和铬黑T相似,但比铬黑T颜色鲜明,终点时在微量镁离子存在情况下变色更敏锐,并且很稳定,可以长期使用。
2.5 样品测定精确度
连续多天做平行样测定,数据见表1。各组平行样的相对平均偏差在0.3%~0.8%之间;标准偏差在0.0002左右;变异系数均小于1%。由此可见该方法精确度较高。
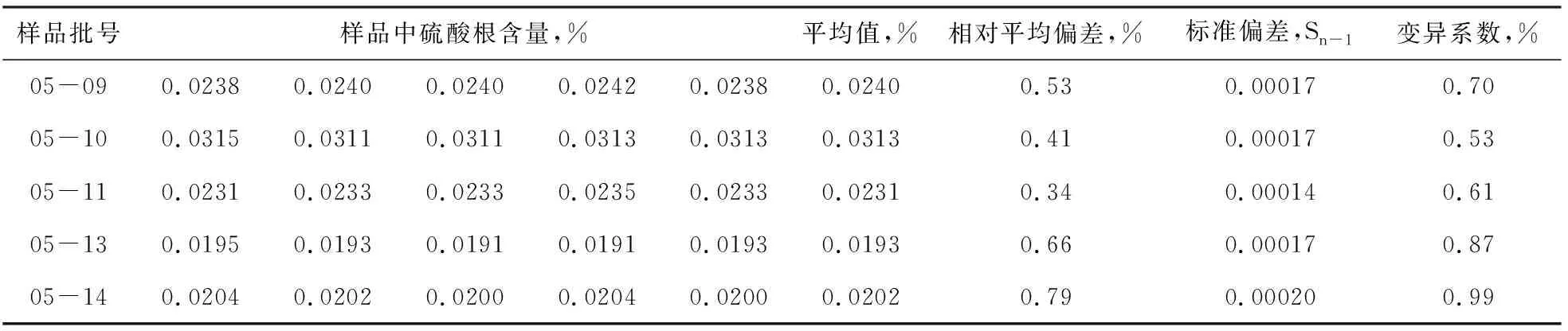
表1 平行样测定
2.6 加标回收试验
纯碱中硫酸根以平均含量0.0250%计算,称样10 g,滴定前溶液体积为60 mL左右,样液中硫酸根含量约为42 mg/L。表2是加标回收试验数据,由此可见,该方法的样品加标回收率令人满意。
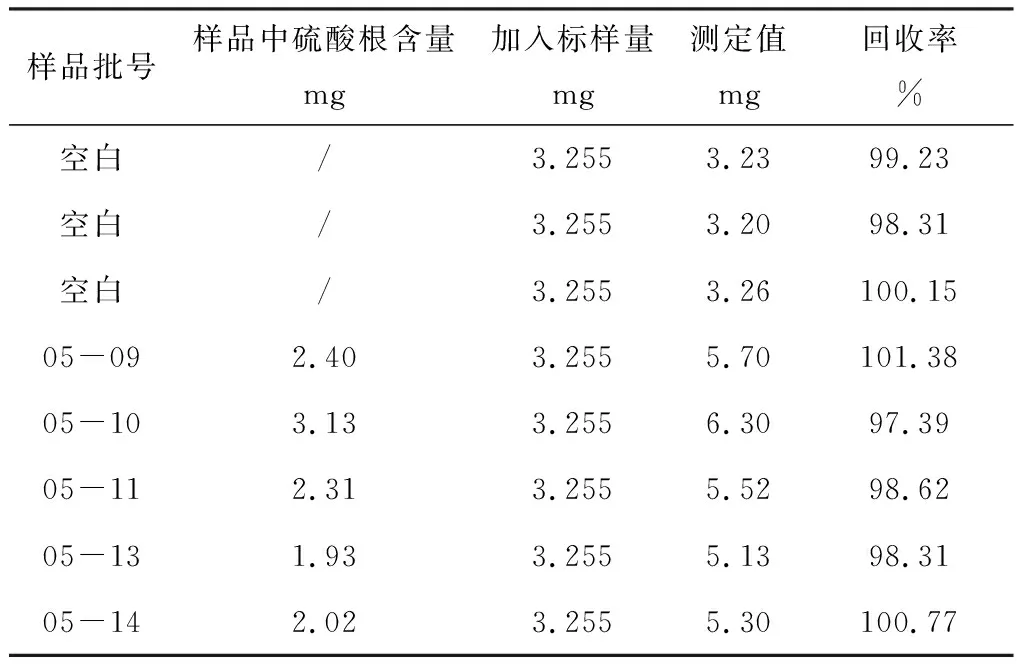
表2 加标回收率