非酒精类发酵食品中氨基甲酸乙酯的检测
2018-08-20
(浙江方圆检测集团股份有限公司,浙江 杭州 310018)
随着科学技术不断进步,大量的化学物品越来越多地出现在食品的生产加工中,这些原料一方面有利于提高生产效率,从而创造更高的经济效益,但是另一方面,过多接触这些化学原料也会给人们的身体带来一些伤害。本文中提到的氨基甲酸乙酯正是如此,它广泛用于农药、医药的中间合成体,但是它如果出现在食品中,则会带来巨大的危害,会严重威胁人类的健康。氨基甲酸乙酯(EC)又名尿烷,是发酵食物和酒精饮品在发酵或贮存过程中天然产生的污染物,酒精类物质及其分解物经发酵过程后极易产生EC。一些前体物质(如尿素、氰酸酯和瓜氨酸)与乙醇发生化学作用,易产生EC,而产生的数量取决于高温和光线。但是,本文中要研究的则是非酒精类发酵物质中的EC。众所周知,在食品发酵的过程中,不可避免地会产生酒精,加上EC对人们的身体健康是有潜在的致癌作用,世界卫生组织已经将EC列入致癌物名单。对此,更有必要对发酵食品中的EC进行检测,保障人们的饮食健康。本文采用气相色谱串联质谱方法检测非酒精类发酵食品中的EC,主要致力于研究非酒精类发酵食品中EC的含量以及对人们生活的影响,为后期的提取方法提供一定的理论依据,更好地促进企业的发展。
1 实验部分
1.1 主要仪器和装置
Clarus 500气相色谱-质谱联用仪,美国PE公司产品,配有电子轰击源(EI);R-210旋转蒸发仪,瑞士Buchi公司产品;Milli-Q超纯水器,美国Millipore公司产品;离心机,美国Thermo公司产品;MSl涡旋混合器,德国IKA公司产品。
1.2 主要材料和试剂
乙腈、甲醇、正己烷(色谱纯),美国TEDIA公司产品;乙酸乙酯、正己烷、二氯甲烷、乙醚(分析纯),国药集团化学试剂有限公司产品;无水硫酸钠,国药集团化学试剂有限公司产品,于500 ℃烘4 h以上,冷却后储存于干燥器中,备用。
氨基甲酸乙酯标准品(EC),纯度>99%;D5-氨基甲酸乙酯(D5-EC),纯度≥99.5%。
1.3 标准溶液配制
①D5-EC储备液。准确称取0.01 g(精确至0.1 mg)D5-EC标准品,用甲醇定容至10 mL,配成1.00 g/L。0~4 ℃下保存。②EC储备液。准确称取0.01 g(精确至0.1 mg)EC标准品,用甲醇定容至10 mL,配成1.00 g/L。0~4 ℃下保存3个月。③D5-EC使用液。准确称取1.0 g LD5-EC储备液0.1 mL,用甲醇定容至50 mL,配成2.00 mg/L。0~4 ℃下保存。④EC使用液。准确称取1.00 g LEC标准储备液1.0 mL,用甲醇定容至100 mL,配成10.00 mg/L。0~4 ℃下保存1个月。
1.4 样品前处理
1.4.1 醋、酱油类试样
称取约10.0 g至高速离心管中,加入适量的D5-氨基甲酸乙酯,加入适量的氯化钠,使其过饱和,然后加入10.0 mL的乙腈,剧烈振摇1 min,静置分层,取乙腈相,重复提取二次,合并提取液,浓缩至近干。
1.4.2 酱类试样称
取约10.0 g至高速离心管中,加入适量的D5-氨基甲酸乙酯,加入适量的水,摇匀,然后加入10.0 mL的乙腈,剧烈振摇1 min,高速离心,取乙腈相,重复提取2次,合并提取液,浓缩至近干。
1.4.3 茶饮料等试样
称取约10.0 g(茶叶试样称取约2.0 g,再加入10.0 mL水)至高速离心管中,加入适量的D5-氨基甲酸乙酯,加入适量的氯化钠,使其过饱和,然后加入等体积的二氯甲烷,剧烈振摇1 min,静置分层,取二氯甲烷相,重复提取2次,合并提取液,浓缩至近干。
1.4.4 面制品、发酵乳、酱腌菜、纳豆、腐乳
称取约10.0 g至高速离心管中,加入适量的D5-氨基甲酸乙酯,加入适量的水,摇匀,然后加入等体积的二氯甲烷,剧烈振摇1 min后,高速离心,取二氯甲烷相,重复提取2次,合并提取液,浓缩至近干。
1.4.5 肉制品试样
称取约10.0 g至高速离心管中,加入适量的D5-氨基甲酸乙酯,然后加入10.0 mL的乙腈,剧烈振摇1 min,高速离心,取乙腈相,重复提取2次,合并提取液,浓缩至近干。
1.5 净化
准确加入2.0 mL乙腈至浓缩瓶中,溶解残渣并转移到10 mL离心管中,加入2 mL正己烷,涡旋混合1 min,以5 000 r/min离心3 min,弃取正己烷相,再加入2 mL正己烷重复净化一次,在乙腈相中加入0.05 g PSA填料,涡旋混合1 min,过0.22 μm有机相滤膜,GC/MS测定。
1.6 分析条件
1.6.1 色谱条件
色谱柱,HP-Innowax毛细管柱(30 m×0.25 mm×0.25 μm);升温程序,50 ℃保持1 min,以8 ℃/min升至180 ℃,再以30 ℃/min升至240 ℃,保持5 min;载气(He)流速1.0 mL/min,进样量2.0 μL;不分流进样。1.6.2 质谱条件
电子轰击(EI)离子源;电子能量70 eV;传输线温度250 ℃;离子源温度230 ℃;选择性离子监测模式(SIM);EC定性离子(m/z)62、74、89,定量离子(m/z)62;EC-D5定性离子(m/z)44、64、76,定量离子(m/z)64;溶剂延迟6 min。
2 结果与分析
2.1 线性关系
准确吸取一定量的EC使用液配制含1.0 mg/L EC-d5 内标的 0.05、0.10、0.20、0.50、1.00、2.50 mg/L系列EC标准溶液,用内标定量法测定。在相同的条件下进行测定,以EC的浓度比为横坐标,以相应浓度的峰面积与内标峰面积比为纵坐标,绘制标准曲线,标准曲线如图1所示。EC在0.05~2.5 mg/L有良好的线性相关性,线形方程为y=0.632 78x-0.008 95,线形相关系数:r2=0.998 8。
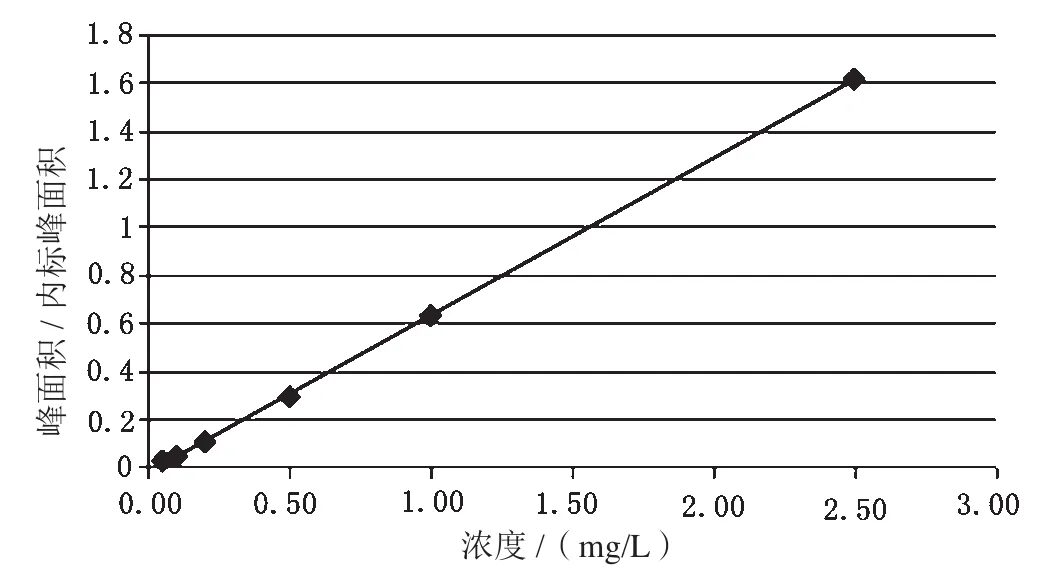
图1 EC标准曲线图
2.2 检出限、定量限、回收率及精密度
在未发现EC的样品中按照上述方法对样品进行处理和测定,进行回收率、精密度、检出限和定量限实验。在0.02、0.05、0.10 mg/kg 3个加标水平做6次平行实验。以3倍信噪比(S/N)计算EC的检出限为0.005 mg/kg,以10倍信噪比(S/N)计算EC的检出限为0.01 mg/kg,得到的结果,见表1。
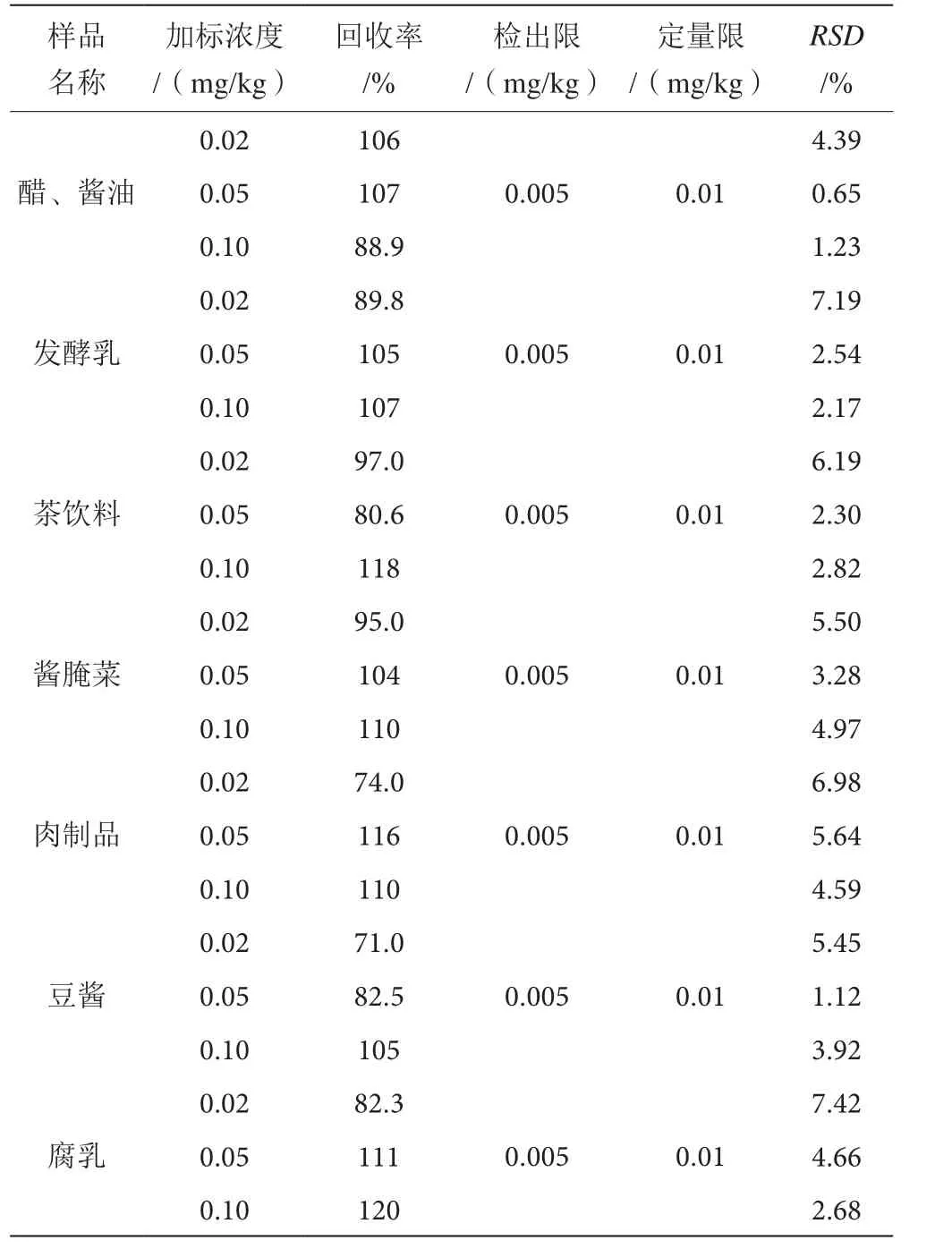
表1 样品中添加浓度、检出限、定量限、回收率及精密度实验数据表(n=6)
3 结语
经过实验研究以及技术人员之间的探讨,参照气相色谱-质谱法研究得出非酒精类发酵食品中的氨基甲酸乙酯含量的相关结论,通过不同物质之间的氨基甲酸乙酯含量进行对比,更加反映出非酒精类发酵食品中氨基甲酸乙酯的数据,检测提取或者降低食物中氨基甲酸乙酯,有利于保障人们的身体健康以及控制发酵食品行业领域中的安全问题。但是,此次研究也在一定程度上存在弊端,传统的实验检测方法虽然具有较高的可靠度,但是对其样本的预处理程序有很高的要求,过程比较复杂,因此可能存在检测成本较高、耗时较长的问题;而且,对于样本的检测,只能在具有专业仪器的实验室内进行,对于市场中大量的食品不具有普适性,具体操作起来比较困难,因此此类检测方法较适合于小范围的抽查。现在有许多企业已经研究出重组DNA技术、细胞融合技术、噬菌体技术等抗体制的设备,人们对于此类检测逐步转向了基因工程方面,对于非酒精类发酵食品中氨基甲酸乙酯的检测技术也是越来越具有检测优势并且在检测方法上也是渐渐趋于完善,将来必定在氨基甲酸乙酯的快速检测领域发挥越来越重要的作用。
