改性介孔二氧化硅对硫化氢的吸附研究
2018-07-26李灿马福秋葛春元莫杏梅
李灿,马福秋,葛春元,莫杏梅
(1.中国人民解放军92609部队,北京 100077;2.哈尔滨工程大学核科学与技术学院,哈尔滨 150001;3.中国环境保护产业协会,北京 100037)
硫化氢是一种无色、易燃易爆的酸性气体,低浓度时有一种特殊的臭鸡蛋气味(嗅觉阈值低至0.00041ppm)。其毒性极强,人在短时间内吸入少量的硫化氢便会导致死亡[1]。即使是低浓度的硫化氢,对眼、呼吸系统和中枢神经也会产生强烈影响,经常接触会对人员的身体健康造成较大损害[2]。对于舰艇舱室、国防指挥工程等密闭空间来说,其卫生间、污物桶、变质食品和人体胃肠道排气及排泄物、柴油机运转等会持续释放出一定量的硫化氢气体,危害内部人员的身体健康。针对密闭空间H2S废气污染,相应的化学吸收和物理吸附等净化方法有不同程度的应用,但这些方法也存在设备复杂、易产生二次污染等问题[3~5]。
介孔二氧化硅材料的比表面积较大,孔隙发达,孔道高度有序,均一性好,骨架结构稳定且易于掺杂,并具有较高的热稳定性和水热稳定性等优点[6],使得其在吸附、分离、催化、生物科技等多个领域有着广泛的应用[7~9]。本文以均匀沉淀法负载一定量的MgO、CuO、ZnO等金属氧化物改性介孔二氧化硅,并将其应用于H2S气体的吸附研究,旨在探索一种价廉、高效、操作简便的处理H2S废气的材料和方法。
1 实验部分
1.1 介孔二氧化硅的制备
量取9mL氨水,将其缓慢倒入124mL去离子水中。称取2.5g十六烷基三甲基溴化铵(CTMAB),在超声下缓慢加入到氨水混合液中,直至完全溶解。将混合液转移至水浴锅中,27℃恒温快速搅拌。量取10mL正硅酸乙酯,边搅拌边逐滴加入正硅酸乙酯(TEOS)。恒温持续搅拌2h。将反应物过滤、干燥、焙烧。焙烧温度由室温经30min升至为300℃,恒温30min,后经30min升至550℃,550℃恒温5h,得到介孔SiO2。
1.2 金属氧化物改性介孔二氧化硅的制备
利用均匀沉淀法合成金属氧化物改性二氧化硅(以制备20%的MgO/SiO2为例):取1.0g介孔二氧化硅,与一定量的去离子水混合,在超声的作用下充分分散。称取1.28gMg(NO3)2·6H2O和1.2g尿素,加入二氧化硅浊液中。待硝酸镁与尿素充分溶解,将烧杯转移至95℃的水浴锅中,用电动搅拌机不断搅拌4h后将烧杯中物质过滤,沉淀物在80℃干燥箱中干燥1h,研磨,在450℃马弗炉中焙烧4h,冷却后即得到20%的MgO/SiO2样品。
1.3 样品的分析测试方法
1.3.1 表面形貌观察及能谱分析
微观形貌在JSM-6480的扫描电镜上观察,样品未经喷金处理。同时利用扫描电镜的配件能谱仪(EDS)对样品进行能谱分析,得到其表面的元素组成和元素相对含量。
1.3.2 比表面积测定
比表面积和孔结构通过SSA-4200孔隙及表面积分析仪在77K下进行氮气等温吸附得到。比表面积由BET方程得出,总孔容由相对压力p/p0= 0.95时的氮气吸附量转换为液氮体积得到,微孔孔容由t图法得到[10]。
1.3.3 热重分析
吸附剂的热重分析在STA-409型号热重分析仪上进行,温度20℃~800℃,升温速率10K/min。
1.4 H2S气体穿透实验
通过气体穿透实验装置开展H2S气体穿透实验(如图1)。在缓冲瓶中的H2S浓度达到设定值后,将之通入吸附柱中进行吸附测试。当吸附后尾气中的H2S浓度达到1ppm时,定义为该吸附剂的穿透时间,结束穿透实验。以时间t(min)为横坐标,浓度C(ppm)为纵坐标,绘制H2S气体的穿透曲线。
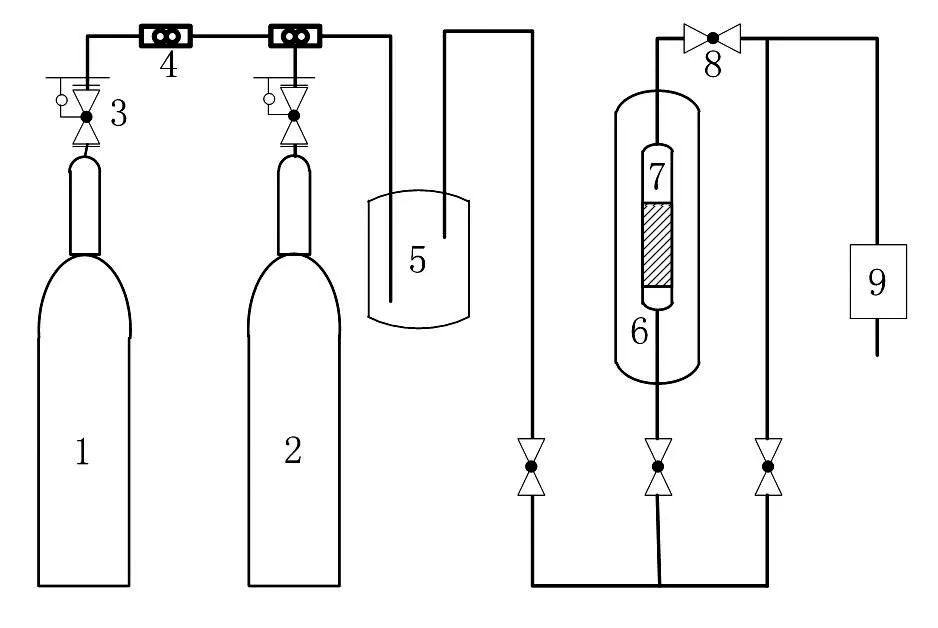
图1 气体穿透实验装置组成
按照以下公式计算吸附剂的吸附能力(δ)。

式中:
δ—吸附含硫气体的能力,mg/g;
M—含硫气体的相对分子质量,g/mol;
F—穿透实验中气体的流速,m3/min;
Cinlet—穿透实验中入口气体的浓度,ppm;
t—穿透时间,min;
m—穿透实验中吸附剂的质量,g;
VM—标准状态下的气体摩尔体积,cm3/mmol。
2 结果与讨论
2.1 不同金属氧化物改性介孔二氧化硅对H2S的穿透实验结果
在反应条件、烘干工艺、焙烧工艺一致的情况下,分别制备了负载量均为20%的MgO/SiO2、CuO/SiO2、ZnO/SiO2吸附剂。H2S气体穿透曲线(如图2)结果表明,与负载ZnO与MgO相比,负载CuO的吸附剂的脱硫效果更好。
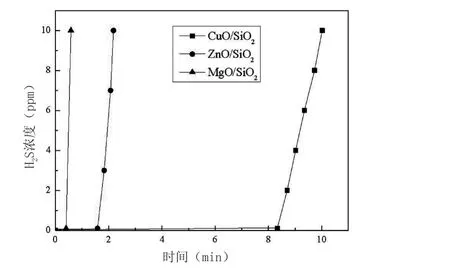
图2 不同金属氧化物改性介孔二氧化硅的H2S穿透曲线
2.2 不同CuO负载量改性介孔二氧化硅对H2S的穿透实验结果
分别制备了负载量为10%、30%、40%的CuO/SiO2吸附剂,并对其进行H2S穿透实验(见图3)。结果表明,CuO负载量为40%时,样品具有最佳的吸附性能,其H2S穿透时间为247.3min,穿透硫容达50.5mg/g。
2.3 不同焙烧温度制备的改性介孔二氧化硅对H2S的穿透实验结果
将负载40%CuO样品,分别在350℃、400℃、500℃下焙烧4h。对不同焙烧温度下制备的改性介孔二氧化硅进行H2S穿透实验(见图4)。结果表明,CuO负载量为40%,450℃的焙烧温度下制备的样品具有最佳的脱硫性能,其H2S穿透时间为247.3min,穿透硫容达50.5mg/g。
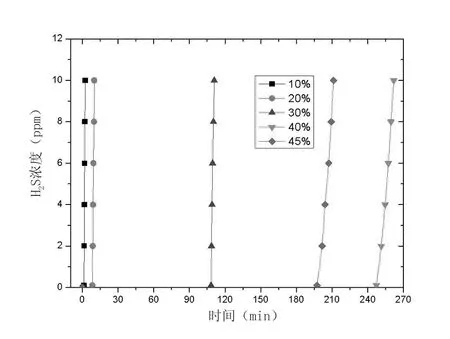
图3 不同CuO负载量的改性介孔二氧化硅的H2S穿透曲线
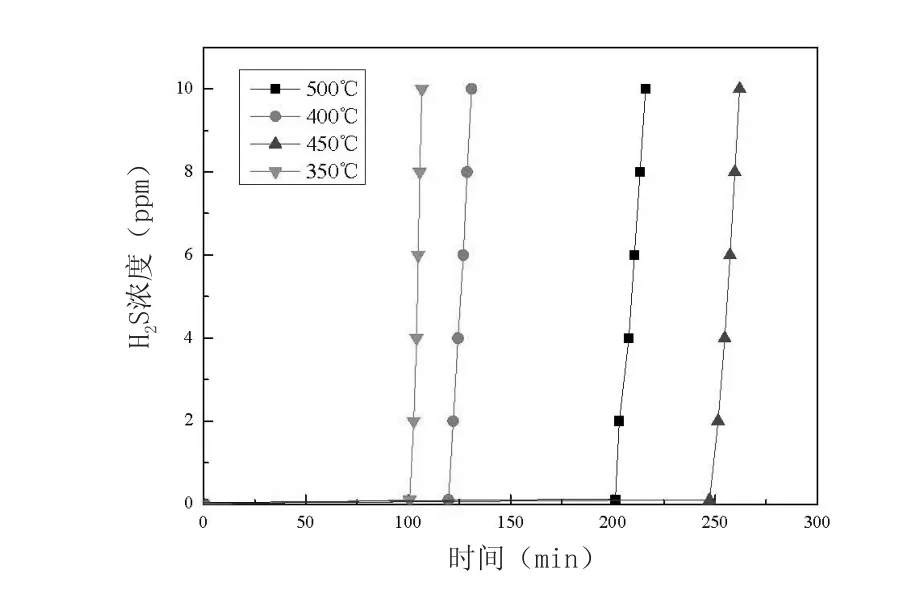
图4 不同焙烧温度、负载40%氧化铜的改性介孔二氧化硅的H2S穿透曲线
2.4 样品的表面形貌及能谱分析
为了更加直观地了解CuO/SiO2吸附剂的微观形貌及表面元素组成及含量,对CuO负载量为40%、450℃的焙烧温度下制备的化学吸附剂脱硫前后分别进行了扫描电子显微镜观察及能谱分析。
对比脱硫前后化学吸附剂的SEM图(见图5),其表面结构没有发生明显的变化;对应的EDS能谱图(见图6)可知,化学吸附剂在脱硫后表面元素出现了元素S的峰,其原子比例达到3.43%。
根据所得数据 ,排除导电胶C元素的影响后将元素含量重新整理,制成表面元素含量见表1。

图5 CuO/SiO2吸附剂吸附硫化氢前后的SEM图
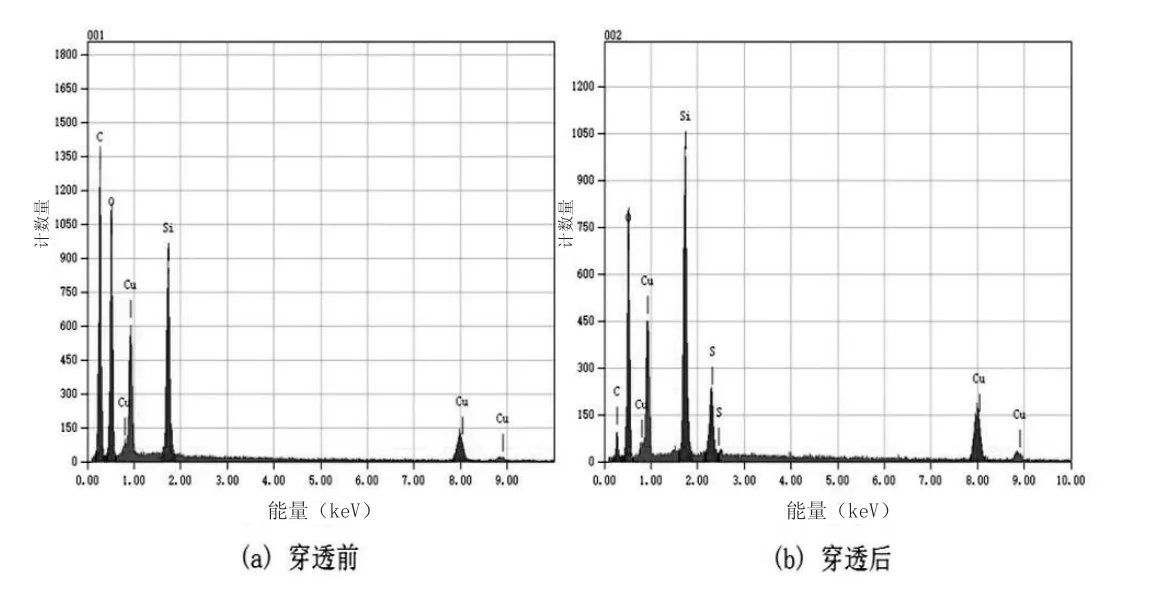
图6 CuO/SiO2吸附剂吸附H2S前后的能谱图
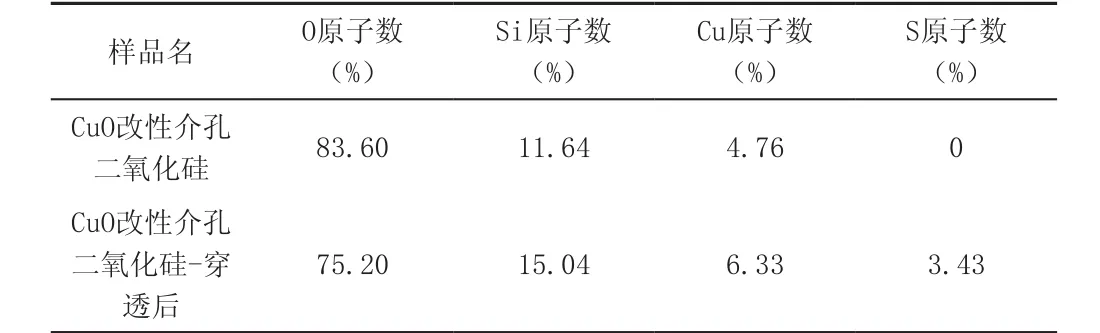
表1 CuO/SiO2吸附剂吸附H2S前后的表面元素含量对比表
根据以上图表可初步判断CuO改性介孔二氧化硅吸附H2S气体后,其中CuO与H2S发生了化学反应,使H2S气体中的S元素固化在吸附材料中而达到脱硫的目的。
2.5 样品的比表面积测试
对介孔二氧化硅及改性后的介孔二氧化硅样品进行N2吸附测试,结果见表2。
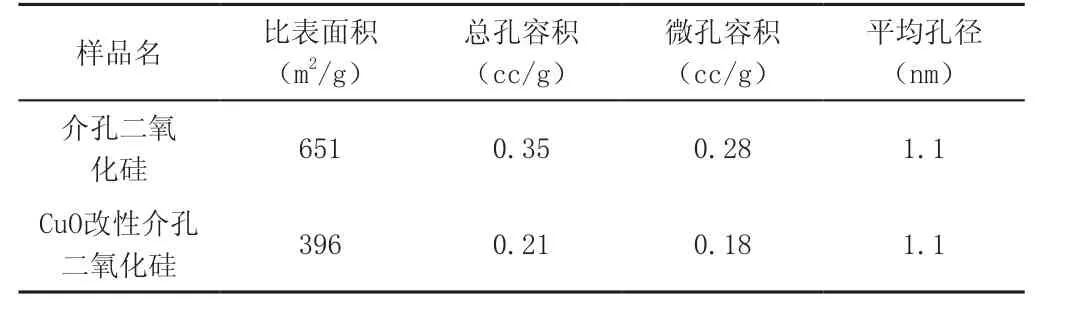
表2 介孔SiO2和CuO/SiO2吸附剂的N2吸附测试结果
由表2可看出,介孔二氧化硅的比表面积为651m2/g,在负载CuO后下降至396m2/g时,孔容也发生了下降,这是由于负载的CuO微粒分散在了SiO2的孔道之中,形成部分堵塞,导致了比表面积以及孔容的下降。
2.6 前驱体的热重分析
为了考察改性介孔二氧化硅制备过程中热分解过程,对其前驱体进行了热重分析(TG)和差热分析(DTA),图7是其热重-差热图谱。
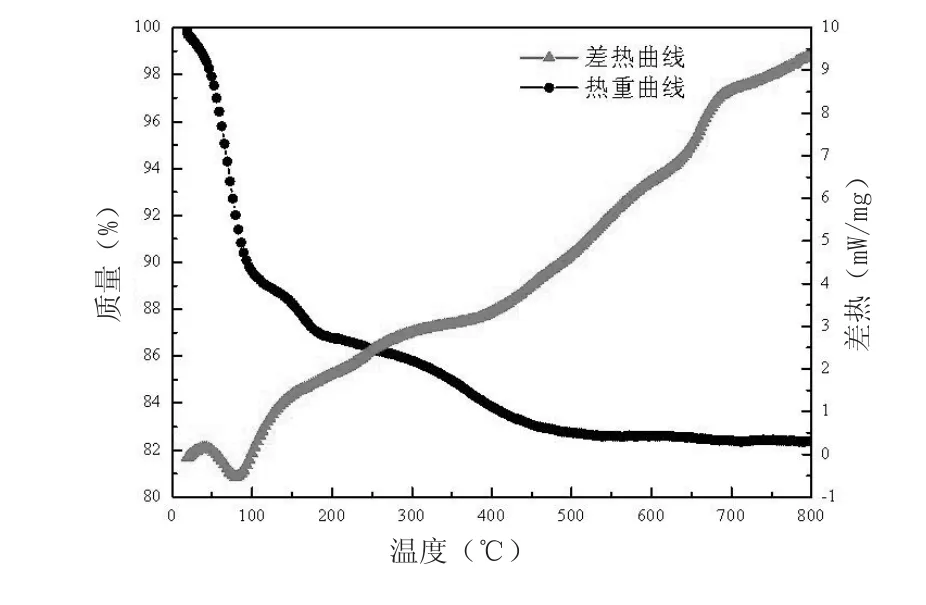
图7 改性介孔二氧化硅的前驱体在N2气氛下的TG-DTA谱图
从图7可看出,在温度上升至100℃的过程中有一段较为快速的失重,其主要原因是前驱物中水分的去除。碱式碳酸铜的分解温度约为220℃,200℃~400℃之间的碱式碳酸铜不断分解,造成失重。前驱物的质量在450℃之后接近恒定,说明此温度时基本已经分解完全,此图谱也表明450℃是制备CuO改性介孔二氧化硅的最佳焙烧温度。
3 结论
利用孔隙发达的介孔二氧化硅为载体,负载一定量的CuO后制备的复合型净化材料,对H2S气体具有吸附量大、不易解吸、成本低廉等特点,特别是在净化处理密闭舱室低浓度H2S气体方面有较大的优势,具有广阔的应用前景。
