花椒中麻味物质的呈味机理及制备方法研究进展
2018-07-23徐丹萍卓志航付本宁
徐丹萍,蒲 彪,,叶 萌,卓志航,付本宁
(1.四川农业大学食品学院,四川 雅安 625014;2.四川农业大学林学院,四川 成都 611130)
花椒是芸香科、花椒属落叶灌木或小乔木,种类有Zanthoxylum bungeanum、Zanthoxylum piperitum、Zanthoxylum schinifolium、Zanthoxylum armatum DC.等[1]。经人工和自然选择在全国形成的优良花椒品种及其中间类型大约有60 种[2]。通常所说的花椒指的是果实成熟后的花椒干果皮。花椒果皮(以下统称花椒)具有浓郁辛香,可作为调味品、香料、木本油料或入药[3]。花椒中化学成分主要有挥发油、酰胺、生物碱、黄酮等,引起麻味的主要成分是链状多不饱和脂肪酸酰胺[4],这些花椒中提取的引起人体辛麻感觉的酰胺类物质统称为麻味物质,麻味物质以山椒素为主要代表。麻味物质在空气中极易发生化学变化,目前国内外尚未建立花椒麻味评价及适用于工业生产的麻味物质提取的标准方法,这一现状阻碍了花椒的深加工及广泛的市场流通。不少学者对酰胺的制备方法及产生麻味的原因进行了分析,试图揭开麻味物质在人体中的响应机制并为花椒中麻味物质的快速检测构建有效方法。本文主要对花椒中麻味物质的主要种类、麻味物质呈味机理及制备方法的研究现状进行综述,为花椒麻味物质构效关系的深入探究和麻味物质检测标准方法的建立等提供支持。
1 麻味物质的主要种类
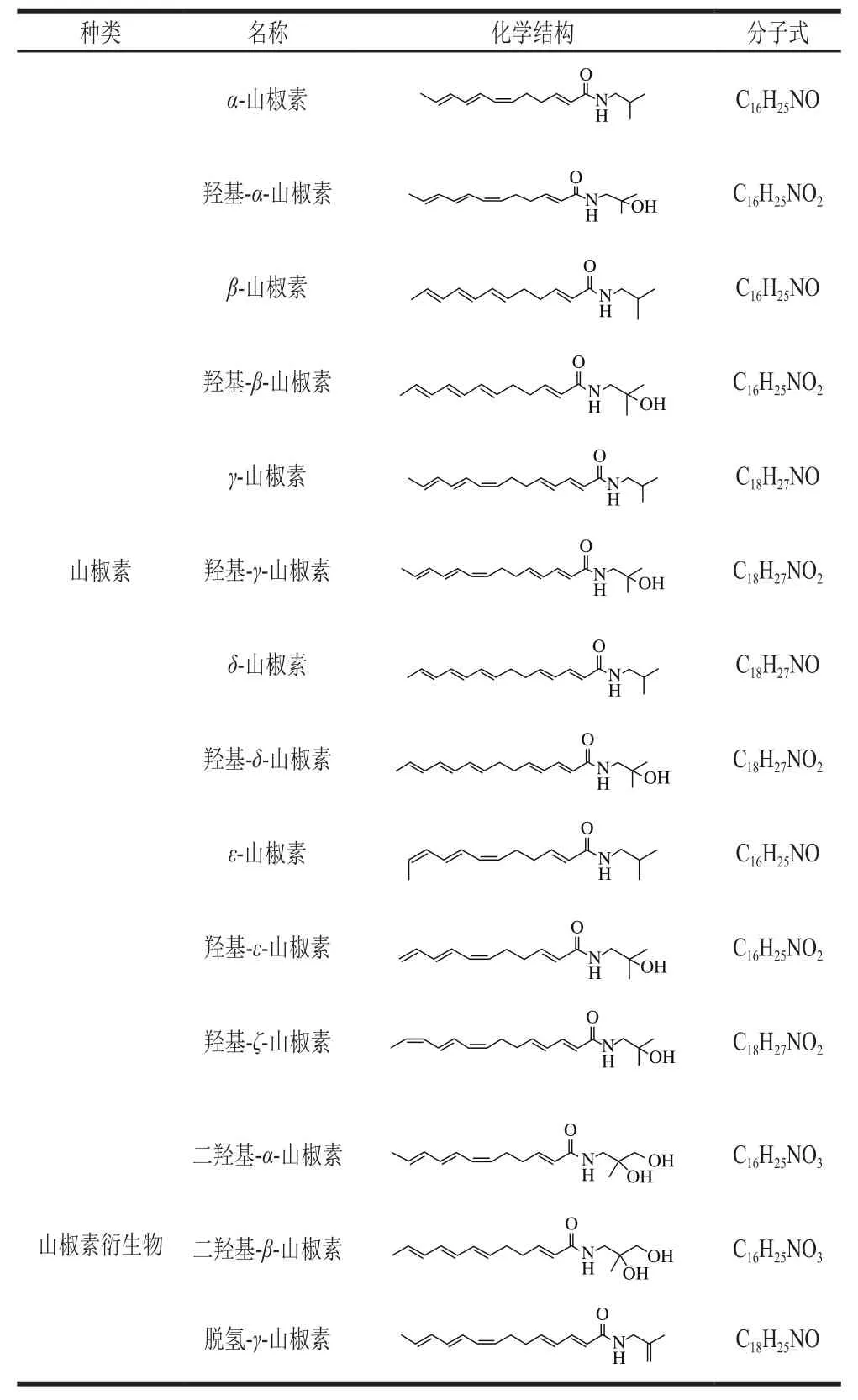
表1 山椒素及其衍生物结构Table1 Structures of sanshool and its derivatives in prickly ash
麻味物质分布于花椒的花、茎、叶、果皮、种子中,并在果皮中的含量最高[5-7]。大部分麻味物质为白色晶体,易溶于氯仿、乙酸乙酯等有机溶剂。结晶体在空气中易变色,一般在安瓿瓶中充氮气密封保存[5]。目前从花椒中分离鉴定出的天然不饱和脂肪酸酰胺有20多种[8-12],其中具有麻味的成分主要是以山椒素为代表的α-、β-、γ-、δ-山椒素等及其衍生物、结构如表1[8,13-14]。这些山椒素及其衍生物在结构上都有一个酰胺基团头部(N端)和一个链状多不饱和烷基尾部(C端),且C链末端都有3 个共轭双键;主要区别体现在C端烷基链长短、C端不饱和双键个数和位置及N端异丁基结构的变化。
2 麻味物质的呈味机理
2.1 麻味物质激发感觉神经
不同麻味物质对人体产生的具体感觉不同,例如羟基-α-山椒素主要产生刺痛的感觉,δ-、γ-和α-山椒素产生燃烧的感觉,而β-山椒素则主要产生麻木的感觉等[15-16]。麻味不是基本味觉,人体对麻味的感知主要与酰胺基团有关。一方面,酰胺基团N原子上的孤对电子不定域不易与其他原子形成共价键,脂烃基对氨基氮的斥电子效应使N原子上的电子云密度增大;另一方面,酰胺基团的C=O双键与脂肪链上的C=C双键形成π-π共轭,使电子云向氧原子方向移动,造成整个酰胺基团电子云密度增大,与质子结合力变强,刺激舌黏膜和触觉神经产生辛麻感[17]。
不少学者从生理机制角度提出了辛麻感产生的原因:
一种观点认为,麻味物质通过激活瞬时受体电位(transient receptor potential,TRP)V1和TRPA1离子通道来激活感觉神经。TRPV1离子通道除了可以被麻味物质激活外,还可以被热(43 ℃)和质子激活,TRPA1离子通道主要在感觉神经末梢中与TRPV1共表达[18]。TRPA1和TRPV1是非选择性阳离子通道,属于TRP家族[19]。TRP家族现在包括超过30 个阳离子通道,其中大多数可渗透二价和单价阳离子,包括Ca2+、Na+和Mg2+[20]。这些离子通道介导细胞对外部瞬时刺激(例如温度、光、机械力和渗透压)的“受体”诱导的响应。刺激作用可以增加或降低TRP通道对特定离子的选择性渗透性,随后改变细胞膜电位并导致去极化[21]。TRPV1和TRPA1在受到麻味物质的刺激后,使感觉神经元去极化,引起Ca2+内流,并诱发内向电流[22-23],使人体感受到麻味物质带来的辛麻感觉。
另外一种观点认为,麻味物质通过抑制两孔钾离子通道激发感觉神经元。两孔钾离子通道能够作为动作电位和兴奋性的主要调节器与感觉神经元相互作用[24]。对大鼠细胞外的三叉神经纤维研究表明羟基-α-山椒素能够激活三叉神经元引发刺激感受[25]。据报道,KCNK两孔钾离子通道家族的3 个成员KCNK3、KCNK9和KCNK18作为羟基-α-山椒素受体,与通过刺激物打开TRP通道相反,羟基-α-山椒素抑制两孔钾离子通道导致感觉神经元活化[26]。Beltrán[27]等通过使用非洲爪蟾卵母细胞的两电极电压钳实验评估几种刺激性化合物对野生型和突变型两孔钾离子通道的影响,发现几种刺激性化合物均能抑制两孔钾离子通道。
2.2 麻味物质的构效关系
电位离子通道TRPV1和TRPA1能被山椒素及其衍生物激活产生辛麻感,但是当刺激性物质的结构不同时,能刺激不同的受体产生刺激感受[28]。据报道,羟基-α-山椒素衍生物烷基链结构和极性酰胺结构在TRPA1激活中起作用,TRPA1的激活完全依赖烷基链部分,但是烷基结构的修饰和改变对TRPV1的激活却具有非常低的影响,意味着TRPA1对于山椒素的不饱和性表现出了选择性,而TRPV1没有表现出选择性[13]。虽然花椒中的刺激性感觉由TRPA1和TRPV1共同介导,但对于TRPA1激活,羟基-α-山椒素的多烯链中的顺式C6双键是关键的,而对于TRPV1的激活不需要结构特异性[29]。此外,麻味强度受到C链长短及N端结构的影响,C链长度越长麻味强度越低;同时,N端结构对麻味强度的影响,按照降序排列顺序依次是:异丁基酰胺、哌啶、乙醇胺和2-乙基己胺、吡咯烷、3-甲基丁胺、丁胺和甲基丁基酰胺[30-31]。
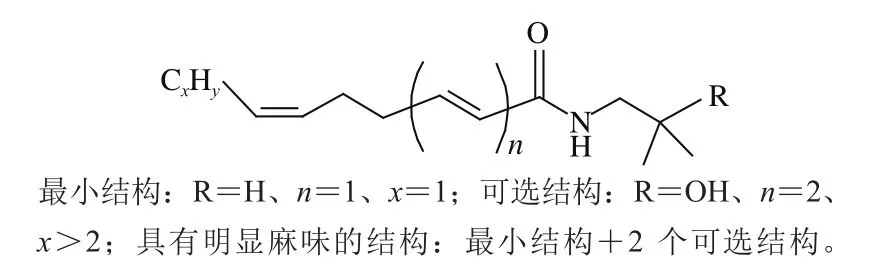
图1 麻味物质必需结构[32]Fig. 1 Structural requirements of numb-taste compounds[32]
据报道,N端酰胺最小结构N-(2-甲基-2-羟丙基)酰胺和C端烷基链基序CH=Z=CH—CH2—CH2—CH=E=CH是麻味物质引发辛麻感的必需结构,如图1所示。C链上的顺势双键结构是引发麻味的关键结构,且C链上不能有其它支链的存在。图1中x、y代表C端烷基链的长度,n代表双键的个数,R代表N端酰胺基团所连结构。当R=H、n=1、x=1时是产生辛麻感的最小结构;当N端R被—OH取代时,麻味强度提高;最小结构加两个可选结构可以产生明显的麻味,即在最小结构的基础上,同时满足可选结构3 个条件(R=OH、n=2、x>2)中的两个,产生明显麻味。
3 麻味物质的制备方法
对麻味物质激活感觉神经和构效关系的探索引发了学者对麻味物质制备的研究。花椒中麻味物质的制备方法主要有常规制备方法和化学合成的方法。常规制备方法即利用有机溶剂、超临界CO2萃取,通过系列柱层析、制备色谱等分离纯化进行制备;化学合成方法即借助易得到的化合物作为反应起始物,通过一系列化学反应合成具有特定结构的麻味物质。
3.1 常规制备方法
目前麻味物质的常规制备过程是:首先,利用有机溶剂或超临界CO2等对样品进行初步提取,初提后的样品进行硅胶、凝胶等色谱的梯度洗脱,收集不同洗脱条件下的馏分;其次,利用高效液相色谱(high performance liquid chromatography,HPLC)、气相色谱(gas chromatography,GC)、质谱(mass spectrometry,MS)等直接进行定性、定量,或者采用制备型薄层色谱(thin-layer chromatography,TLC)、制备/半制备型HPLC、高速逆流色谱(high-speed counter-current chromatography,HSCCC)、超高效液相色谱(ultra performance liquid chromatography,UPLC)等仪器进一步对样品分离纯化;最后结合核磁共振(nuclear magnetic resonance,NMR)、红外光谱(infrared spectrum,IR)、紫外光谱(ultraviolet spectrum,UV)、MS分析等,进行麻味物质结构的鉴定[8-11]。
3.1.1 麻味物质的提取和分离
常用的提取方法有有机溶剂提取、超临界CO2萃取等,主要的分离方法有硅胶色谱、制备/半制备型HPLC、HSCCC、UPLC等。
用于麻味物质初步提取的有机溶剂有甲醇、乙醇、氯仿、石油醚、乙醚、植物油等[9,11,23,33-34],其中甲醇、乙醇是最常使用的麻味物质粗提溶剂。单一的有机溶剂提取得到的麻味成分的含量较低,一般结合其他方法进行提纯。用石油醚作为索氏提取的溶剂,经甲醇溶液浸提后,采用逆流干柱层析法提取花椒油树脂中的麻味物质,不饱和酰胺在麻味物质纯品中的相对含量达到了95.50%[35]。有机溶剂提取法的缺点比较明显,易引入杂质,导致麻味物质变性,提取率较低,所得麻味成分质量不高等。超临界CO2萃取技术溶解度相对较高,并且可以有效避免萃取成分发生化学变化,能够与萃取成分完全分离,是花椒和辣椒刺激成分萃取的有效方法[36-37]。采用超临界CO2萃取花椒麻味成分,用半制备型HPLC分离提纯,得到的羟基-α-山椒素纯度达到98.2%[38]。
大孔树脂、硅胶、凝胶等配合使用,利用不同溶剂梯度洗脱,能够得到种类和质量不同的样品。用于麻味物质柱色谱分离中梯度洗脱的溶剂主要有正己烷、氯仿、乙酸乙酯、正丁醇等[11]。采用Toyopearl HW-40C、MCI-gel CHP-20P和YMC-gel ODS色谱分离,结合制备型HPLC纯化含有酰胺的级分,Hatano等[10]从花椒中成功分离出了6 种长链多不饱和酰胺类化合物(1)~(6),分别是(1):(6RS)-(2E,7E,9E)-6-羟基-N-(2-羟基-2-甲基丙基)-11-氧代-2,7,9-十二碳三烯酰胺、(2):(11RS)-(2E,7E,9E)-11-羟基-N-(2-羟基-2-甲基丙基)-6-氧代-2,7,9-十二碳三烯酰胺、(3):(10RS,11SR)-(2E,6Z,8E)-10,11-二羟基-N-(2-羟基-2-甲基丙基)-2,6,8-十二碳三烯酰胺、(4):(10RS,11RS)-(2E,6Z,8E)-10,11-二羟基-N-(2-羟基-2-甲基丙基)-2,6,8-十二碳三烯酰胺、(5):(6RS,11SR)-(2E,7E,9E)-6,11-二羟基-N-(2-羟基-2-甲基丙基)-2,7,9-十二碳三烯酰胺、(6):(6RS,11RS)-(2E,7E,9E)-6,11-二羟基-N-(2-羟基-2-甲基丙基)-2,7,9-十二碳三烯酰胺。Sugai等[39]利用硅胶色谱和半制备型HPLC对花椒不同部位的麻味物质进行了分析,认为麻味物质主要存在于其果实中,幼叶和花中的主要麻味成分是α-山椒素,果实中的主要麻味成分是羟基-α-山椒素。HSCCC是20世纪80年代发展起来的一种连续、高效的液-液分配色谱分离技术,因不需要任何固态支撑物或载体,避免了不可逆吸附引起的样品损失、失活、变性等问题,适于天然产物的分离,广泛应用在食品、医药、天然产物等领域[40-41]。Wang Shi等[42]采用HSCCC法在正己烷、乙酸乙酯、甲醇、水的体积比为7∶3∶5∶5,流速为1.5 mL/min,转速为850 r/min的条件下,得到纯度为98.0%的烷基酰氨0.19 g,所得物质纯度高、得率大。UPLC是基于小颗粒填料的液相色谱技术,可以实现样品的同时检测。Kumar等[43]采用超高效液相色谱-二极管阵列检测器结合串联电喷雾离子化质谱(ultra performance liquid chromatography-diode array detector-electrospray ionizationtandem mass spectrometry,UPLC-DAD-ESI-MS/MS)对青花椒中的酰胺、呋喃木酚木脂素、芝麻素等几种化合物进行了同时定量,并鉴定了16 种酰胺类化合物和呋喃丹木脂素类化合物,缩短了分析时间并减少了溶剂消耗。
3.1.2 麻味物质的结构鉴定
经分离提纯后的样品通过NMR、IR、UV、MS等进行综合分析,能够得到麻味物质的精确化学结构,为进一步研究麻味物质的构效关系及不同麻味物质间的相互作用提供了基础[42]。
NMR、IR、UV、MS能够提供化合物中原子的化学位移、耦合常数、积分曲线,分子中化学键、官能团的振动吸收频率,电子跃迁吸收波长,离子质荷比等方面的信息,是进行结构鉴定的常用方法。Bader等[8]将超临界流体萃取的四川花椒(Zanthoxylum piperitum)中的麻味物质进一步通过液相色谱-飞行时间质谱(liquid chromatography-time of flight- mass spectrometry,LC-TOF-MS)、LC-MS及1D/2D NMR分析,检测出了8 种不饱和脂肪酸酰胺,7 种麻味物质的结构得到了鉴定,其中1 种未经过文献报道。利用有机溶剂甲醇进行初提,正己烷、二氯甲烷、乙酸乙酯、正丁醇等进行硅胶色谱梯度洗脱,YMC色谱柱过滤,结合LC-Q-TOF-MS、NMR、傅里叶变换红外光谱进行分析,Yang等[11]从花椒(Zanthoxylum piperitum)中提取鉴定出了9 种化合物,其中化合物6,7,10,11-四羟基-N-(2-羟基-2-甲基丙基)-2E,8E-十二碳二烯酰胺是在花椒中新发现的物质。Tian Junmian等[9]将经过乙醇提取后的提取物在硅胶柱色谱上用CHCl3重复洗脱,并依次经过羟丙基葡聚糖凝胶(Sephadex LH-20)、反相柱色谱、制备型TLC、半制备型HPLC进行纯化,利用MS、IR、NMR进行结构鉴定,最终得到了8 种化合物,其中3 种是花椒中新鉴定出的长链不饱和酰胺。
3.2 麻味物质的化学合成
因麻味物质结构中不饱和双键的存在,使其在常规制备方法中容易产生异构化、氧化、聚合或光降解等反应,且常规制备方法操作繁琐、提取效率低,不适于大规模生产。因此,不少学者对麻味物质尤其是山椒素的化学合成方法进行了探索。
Wittig反应是合成双键、共轭双烯、醛、酮等结构的重要反应,也是麻味物质合成的常用方法。Sonnet[44]在1969年最先报道了合成β-山椒素的方法,利用Wittig反应采用市售山梨醛为起始反应物,经过5 步化学反应得到得率为72%白色针状麻味物质。以2,6,8,10-十二碳四烯酸作为合成反应的关键中间体,Wu Bo等[45]利用涉及6 个反应的Wittig反应得到了总产率为21%的羟基-α-山椒素。以2,6,8,10-十二碳四烯酸作为反应中间体不仅可以用于制备山椒素,而且可以制备酰胺类似物来丰富酰胺文库。
然而,Wittig反应作为一种低选择性合成方法,在所合成的山椒素结构中都缺少羟基,不能实现物质的空间结构的立体选择性。Igarashi等[46]在2012年首次报道了采用Suzuki-Miyaura偶联反应进行羟基-α-山椒素和羟基-β-山椒素全合成的方法,这种方法能够选择性合成具有羟基基团的顺式/反式结构的山椒素。Aoki等[47]探索了一种通过2,4-己二烯醛与Fe(CO)3络合合成羟基-α-、羟基-β-和γ-山椒素的方法,最终得到3 种山椒素的总产率分别是45%、26%和31%,这种方法能够体现立体选择性并得到具有羟基基团的特定化合物。此外,得到的中间产物2,6,8,10-十二碳四烯酸作为1 种固体羧酸可以用作麻味物质的替代保存品,并实现麻味物质的大规模生产。采用立体选择性Wittig反应、Corey-Fuchs反应,在合成过程中共享相同的中间体Z异构体2,4,8,10,12-十四碳五烯酸,并对上述Aoki的方法进行改进,可以得到更高产率的γ-山椒素和羟基-γ-山椒素[14]。除上述几种山椒素外,δ-山椒素因还可以用作I型糖尿病的潜在治疗药物,其化学合成方法也已经建立起来[48]。
麻味物质容易发生化学变化,分离纯化较复杂,提取率低,麻味物质标准品还未实现工业化生产。化学合成麻味物质采用市售化学物质作为反应起始物,能够在工业化生产中通过控制化学反应过程关键参数,以经济、可控、快速、规模化的标准实现批量生产。此外,以化学反应中间体作为麻味物质前体物质进行保存,能够有效实现麻味物质保存、运输等过程的稳定性[47]。化学合成麻味物质为麻味物质标准品制备、花椒中麻味物质含量检测、花椒分级及花椒油标准制定等领域提供了条件。
4 结 语
目前的研究表明山椒素是刺激口腔黏膜产生麻味的主要物质,通过研究刺激受体激活的山椒素基团或结构的类型,对探明酰胺产生麻味的必需结构具有一定意义。物质的麻味强度受分子结构的影响,通过将麻味物质结构数值化,量化麻味强度和分子结构的关系,有助于深入分析麻味物质的构效关系。花椒中物质种类复杂,麻味强度还受到挥发油、酮类等物质的影响,探究其他物质对麻味强度的相生相克作用,有助于明确人体对麻味的响应机制。
国内外还没有麻味评价或者麻味物质标准品制备的标准方法,亟待建立麻味物质快速、工业化制备方法。麻味物质在空气中易发生化学变化,常规提取制备过程繁琐,不适于大规模生产,通过探索化学合成、分子印迹、微萃取技术等麻味物质制备的新方法,是满足工业化和市场化的需求的一个努力方向。采用删除不必要的结构或分析用其他基团取代麻味物质部分结构(例如采用苯环替代C链末端的共轭结构等),稳定麻味物质的化学性质,来探索麻味物质新型保存方法。此外,改进现有方法,或借助感官评价、电子舌等方法,从整体上对花椒的麻味进行评价,建立不同产地、不同品种花椒的麻味评价体系,也将对花椒产业的发展具有重要意义。
在化学合成中,探索化学性质更稳定、选择性合成更有效、经济成本更低的反应中间体,麻味物质的保存可以转化为合成反应中间体的保存,实现批量、便捷、低成本运营。构建麻味物质及其类似物文库,能够为深入探究麻味物质结构对麻味强度的影响及麻味物质在人体中的响应机制提供丰富资源,也是今后麻味物质研究的一个方向。
