含酰氧基三嗪酮类化合物的合成及生物活性
2018-07-23崔培培
杨 岩,崔培培
(太原理工大学 a.艺术学院,山西 晋中 030600,b.化学化工学院,太原 030024)
吡蚜酮是瑞士先正达公司于1988年开发的新型吡啶类杀虫剂,具有高效、低毒、高选择性、对环境友好等特点,可用于大部分同翅目害虫的防治,适用于蔬菜、水稻、棉花、果树等多种作物[1-2]。三嗪酮(1,2,3-triazin-4(3H)-one)是吡蚜酮合成中重要的中间体。保留吡蚜酮中的三嗪酮部分,对吡蚜酮环中的亚胺部分及吡啶环进行改造而得到的三嗪酮类杀虫剂,显示出较高的生物活性,是近年来新型杀虫剂的重要研发方向之一[3-12]。
本文以三嗪酮为农药先导,将烷氧羰基引入到三嗪酮分子中,设计并合成了8种未见文献报道的含酰氧基三嗪酮类化合物。利用1H NMR、13C NMR和HRMS对其结构进行确证,并对其进行了生物活性测试研究。
1 实验
1.1 仪器与试剂
1H NMR,13C NMR谱使用Bruck-AV400核磁共振仪测定;高分辨质谱使用VG ZAB-HS高分辨质谱仪测定;熔点使用SWG X-4显微熔点仪测定;所有溶剂均以标准方法纯化处理;柱层析使用青岛化工厂生产的硅胶(100~200目)。
1.2 目标化合物3a-3h的合成方法
中间体1参照文献[3]方法制备。在100 mL单口瓶中,加入氨基三嗪酮1(5 mmol),二氯甲烷(40 mL)搅拌溶解。加入K2CO3(2.5 mmol),冰水降温至0 ℃.氯甲酸甲酯2a-2h(5 mmol)溶于二氯甲烷(10 mL),慢慢滴加到上述溶液中。滴加完毕后,在0 ℃继续搅拌0.5 h,然后加热回流8 h,TLC监测反应完毕。将反应液减压脱溶后,用V(二氯甲烷)/V(甲醇)=(100∶1~50∶1)进行硅胶柱层析,得到目标产物3a-3h(见图1、图2).

1 2a-2h 3a-3h图1 目标化合物3a-3h的合成路线Fig.1 Synthetic route of target compounds of 3a-3h

图2 目标化合物3a-3h的结构(图中%为产率)Fig.2 Structure of target compounds of 3a-3h
甲基(6-甲基-3-氧-2,3-二氢-1,2,4-三嗪-4(5H)-酰基)氨基甲酸酯(3a):白色固体,产率72%.m.p.169~170 ℃;1H NMR(400 MHz,DMSO-d6)δ9.83(s,1H,NH),9.47(s,1H,NH),4.05(s,2H,CH2),3.61(s,3H,CH3),1.85(s,3H,CH3);13C NMR(100 MHz,DMSO-d6)δ156.2,151.3,145.0,52.1,51.5,19.8.ESI-HRMS(m/z):Calcd.for C6H11N4O3[M+H]+187.083 1;found 187.082 8.
乙基(6-甲基-3-氧-2,3-二氢-1,2,4-三嗪-4(5H)-酰基)氨基甲酸酯(3b):白色固体,产率70%.m.p.127~128 ℃;1H NMR(400 MHz,DMSO-d6)δ9.81(s,1H,NH),9.41(s,1H,NH),4.06(q,J=7.2,2H,CH2CH3),4.05(s,2H,CH2),1.85(s,3H),1.19(t,J=7.2 Hz,3H,CH2CH3);13C NMR(100 MHz,DMSO-d6)δ155.8,151.4,145.0,60.8,51.6,19.8,14.8.ESI-HRMS(m/z):Calcd.for C7H13N4O3[M+H]+201.0982;found 201.098 3.
异丙基(6-甲基-3-氧-2,3-二氢-1,2,4-三嗪-4(5H)-酰基)氨基甲酸酯(3c):白色固体,产率55%.m.p.125~126 ℃;1H NMR(400 MHz,DMSO-d6)δ9.79(s,1H,NH),9.41(s,1H,NH),4.05(s,2H,CH2),3.81(d,J=6.4 Hz,2H,CH2CH(CH3)2),1.85(brs,4H,CH3,CH2CH(CH3)2),0.89(d,J=6.4 Hz,6H,CH2CH(CH3)2);13C NMR(100 MHz,DMSO-d6)δ156.0,151.5,145.2,70.7,51.7,27.7,19.9,18.9.ESI-HRMS(m/z):Calcd. for C9H17N4O3[M+H]+229.129 5;found 229.129 8.
烯丙基(6-甲基-3-氧-2,3-二氢-1,2,4-三嗪-4(5H)-酰基)氨基甲酸酯(3d):白色固体,产率63%.m.p.111~112 ℃;1H NMR(400 MHz,DMSO-d6)δ9.83(s,1H,NH),9.54(s,1H,NH),5.85(m,1H,=CH),5.32(d,J=16.2 Hz,1H,=CH2),5.22(d,J=10.8 Hz,1H,=CH2),4.55(d,J=5.1 Hz,2H,OCH2),4.06(s,2H,CH2),1.85(s,3H,CH3);13C NMR(100 MHz,DMSO-d6)δ155.5,151.4,145.0,132.9,117.7,65.2,51.6,19.8.ESI-HRMS(m/z):Calcd.for C8H13N4O3[M+H]+213.098 2;found 213.098 5.
2,2,2-三氯乙基(6-甲基-3-氧-2,3-二氢-1,2,4-三嗪-4(5H)-酰基)氨基甲酸酯(3e):白色固体,产率36%.m.p.207~208 ℃;1H NMR(300 MHz,DMSO-d6)δ10.5(s,1H,NH),9.90(s,1H,NH),4.88(s,2H,OCH2),4.09(s,2H,CH2),1.86(s,3H,CH3);13C NMR(100 MHz,DMSO-d6)δ154.3,151.2,145.2,95.6,73.9,51.5,19.9.ESI-HRMS(m/z):Calcd. for C7H10Cl3N4O3[M+H]+302.981 8;found 302.981 5.
苯基(6-甲基-3-氧-2,3-二氢-1,2,4-三嗪-4(5H)-酰基)氨基甲酸酯(3f):白色固体,产率91%.m.p.181~182 ℃;1H NMR(300 MHz,DMSO-d6)δ10.08(s,1H,NH),9.92(s,1H,NH),7.42(t,J=7.8 Hz,2H,Ar-H),7.25(t,J=7.2 Hz,1H,Ar-H),7.14(d,J=7.8 Hz,2H,Ar-H),4.15(s,2H,CH2),1.88(s,3H,CH3);13C NMR(100 MHz,DMSO-d6)δ154.0,151.2,150.5,145.2,129.5,125.6,121.5,51.5,19.9.ESI-HRMS(m/z):Calcd.for C11H13N4O3[M+H]+249.098 2;found 249.098 8.
4-氯苯基(6-甲基-3-氧-2,3-二氢-1,2,4-三嗪-4(5H)-酰基)氨基甲酸酯(3g):白色固体,产率59%.m.p.184~185 ℃;1H NMR(300 MHz,DMSO-d6)δ10.15(s,1H,NH),7.48(d,J=8.7 Hz,2H,Ar-H),7.19(d,J=8.7 Hz,2H,Ar-H),4.14(s,2H,CH2),1.87(s,3H,CH3);13C NMR(100 MHz,DMSO-d6)δ153.7,151.2,149.2,145.1,129.6,129.4,123.3,51.4,19.8.ESI-HRMS(m/z):Calcd. for C11H12ClN4O3[M+H]+283.059 8; found 283.059 8.
苄基(6-甲基-3-氧-2,3-二氢-1,2,4-三嗪-4(5H)-酰基)氨基甲酸酯(3h):白色固体,产率65%.m.p.126~127 ℃;1H NMR(300 MHz,DMSO-d6)δ9.84(s,1H,NH),9.58(s,1H,NH),7.37(brs,5H,Ar-H),5.10(s,2H,OCH2),4.07(s,2H,CH2),1.85(s,3H,CH3);13C NMR(100 MHz,MSO-d6)δ155.7,151.4,145.1,136.3,128.5,128.1,128.0,66.2,51.6,19.8.ESI-HRMS(m/z):Calcd. for C12H15N4O3[M+H]+263.113 9;found 263.114 3.
1.3 生物活性测试
1.3.1 棉铃虫、玉米螟、粘虫、蚊幼虫的生物活性测定
棉铃虫的实验方法:饲料混药法。从配置好的溶液中移取3 mL加入约27 g的刚配置好的饲料中,从而得到稀释10倍的所需浓度。药剂混匀后均匀地倒入干净的24孔板中,晾凉后接入24头3龄棉铃虫,观察3~4 d后检查结果。
玉米螟的试验方法:浸叶法。配置所需浓度后,把直径约为5~6 cm的叶片浸入药液中5~6 s,取出,放在吸水纸上晾干,放在指定的培养皿中,接入10头3龄幼虫,放入(27±1) ℃的养虫室中观察,3~4 d后检查结果。
粘虫的实验方法:浸叶法。配置所需浓度后,把直径约为5~6 cm的叶片浸入药液中5~6 s,取出,放在吸水纸上晾干,放在指定的培养皿中。接入10头3龄幼虫,放入(27±1) ℃的养虫室中观察,3~4 d后检查结果。
蚊幼虫的实验方法:尖音库蚊淡色亚种,室内饲养的正常群体。称取供试化合物约5 mg于盘尼西林药瓶中,加5 mL丙酮(或适宜溶剂),振荡溶解,即为1 000 mg/L母液。移取0.5 mL母液,加入盛有89.5 mL水的100 mL烧杯中,选取10头4龄初蚊子幼虫,连同10 mL饲养液一并倒入烧杯中,其药液的质量浓度即为5 mg/L.放入标准处理室内,24 h后检查结果。以含有0.5 mL实验溶剂的水溶液为空白对照。
1.3.2 抑制真菌活性的测定
以番茄早疫病菌(Alternariasolani)为例,其他病菌的测试方法相同。离体测试方法:将番茄早疫病菌接到PDA培养基上培养7 d,用打孔器在菌落边缘制取直径4 cm的菌碟接种到含有50 μg/mL和不含药剂的PDA培养基上培养4 d,量取菌落直径,与对照比较计算出药剂的抑制百分率。抑菌率(%)的计算公式为:
杀菌活性=[(对照菌落直径-处理菌落直径)/(对照菌落直径-菌碟直径)]×100% .
1.3.3 除草活性的测定
盆栽法:在直径8 cm的塑料小杯中放入一定量的土,加入一些清水,播种后覆盖一定厚度的土壤,于花房中培养,幼苗出土前以塑料覆盖。每天加一定量的清水以保持正常生长。测试试材:油菜、反枝苋、稗草、马唐。处理19 d后检查结果,测定地上部鲜重,以鲜重抑制百分数来表示药效。
2 结果与讨论
2.1 化合物的核磁共振谱解析
以目标化合物3a的核磁氢谱和碳谱数据为例对其结构进行说明。δ9.83处的单峰为侧链上氮上连接的氢的吸收峰;δ9.47处的单峰为三嗪酮环氮上氢的吸收峰;δ4.05处的单峰为三嗪酮环上亚甲基的吸收峰;δ3.61处的单峰为酯的甲基氢的吸收峰;δ1.85处的单峰为三嗪酮环上甲基的吸收峰。δ156.2处的峰为支链上羰基碳的吸收峰;δ151.3处的峰为三嗪酮环上的亚胺碳的吸收峰;δ145.0处的峰为三嗪酮环上羰基碳的吸收峰;δ52.1处的峰为三嗪酮环上亚甲基碳的吸收峰;δ51.5处的峰为酯的甲基碳的吸收峰;δ19.8处的峰为三嗪酮环上甲基碳的吸收峰。
2.2 杀虫活性测试
2.2.1 化合物3a-3h在添加量600 mg/kg时对棉铃虫、玉米螟和粘虫的杀虫活性
本文对化合物3a-3h在添加量为600 mg/kg时对棉铃虫、玉米螟和粘虫的杀虫活性进行了测试,结果见表1.测试表明,化合物3b,3f的杀棉铃虫、玉米螟和粘虫活性均为100%,高于对照药吡蚜酮的杀虫活性(20%,35%,50%);化合物3a,3g的杀棉铃虫活性(25%、30%)高于吡蚜酮(20%),杀玉米螟和粘虫活性(15%,20%;20%,25%)低于吡蚜酮(35%,50%);化合物3e的杀棉铃虫活性(20%)与吡蚜酮(20%)相当,杀玉米螟和粘虫活性(15%,25%)低于吡蚜酮(35%,50%).其余化合物对棉铃虫、玉米螟和粘虫的杀虫活性均低于对照药吡蚜酮。因此,化合物3b,3f在添加量为600 mg/kg时表现出优于吡蚜酮的杀棉铃虫、玉米螟和粘虫活性。

表1 目标化合物3a-3h在添加量为600 mg/kg时对棉铃虫、玉米螟和粘虫的杀虫活性Table 1 Insecticidal activity of compounds 3a-3h against cotton bollworm, corn borer, oriental armyworm at 600 mg/kg
2.2.2 化合物3a-3h在添加量200 mg/kg时对棉铃虫、玉米螟和粘虫的杀虫活性
鉴于化合物3b,3f的在添加量为600 mg/kg时表现出比吡蚜酮优异的杀棉铃虫、玉米螟和粘虫活性,本文对化合物3b,3f在添加量为200 mg/kg时的杀棉铃虫、玉米螟和粘虫活性进行了测试,结果见表2.测试表明,化合物3b在添加量为200 mg/kg时的杀棉铃虫、玉米螟和粘虫活性分别为30%,30%,40%,化合物3f在添加量为200 mg/kg时的杀棉铃虫、玉米螟和粘虫活性分别为30%,20%,60%,而吡蚜酮在此含量时没有活性。因此,化合物3b,3f在添加量为200 mg/kg时的杀棉铃虫、玉米螟和粘虫活性高于吡蚜酮。
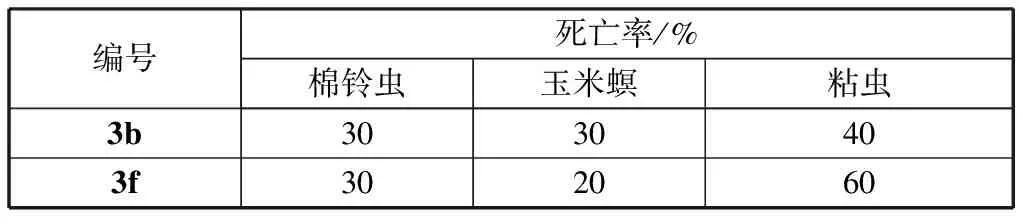
表2 目标化合物3b,3f在200 mg/kg时对棉铃虫、玉米螟和粘虫的杀虫活性Table 2 Insecticidal activity of compounds 3b, 3f against cotton bollworm, corn borer, oriental armyworm at 200 mg/kg
2.2.3 化合物3a-3h对蚊幼虫的杀虫活性
本文对化合物3a-3h的杀蚊幼虫活性进行测试,结果见表3.在含量为10 mg/kg时,除化合物3e活性较低(40%)外,其余化合物的杀蚊幼虫活性均为100%.在添加量为5 mg/kg时,仅化合物3b,3f的杀蚊幼虫活性为100%,高于对照药吡蚜酮的杀蚊幼虫活性(40%).当添加量降低到2 mg/kg时,化合物3b,3f的杀蚊幼虫活性仍为100%,此时对照药吡蚜酮不具有杀蚊幼虫活性。当添加量降低至1 mg/kg,化合物3b,3f杀蚊幼虫活性仍达到100%,40%.当添加量降低至0.5 mg/kg,化合物3b杀蚊幼虫活性仍达到40%,而化合物3f不具有杀虫活性。因此,化合物3b的杀蚊幼虫活性最高。

表3 目标化合物3a-3h对蚊幼虫的杀虫活性Table 3 Insecticidal activity of compounds 3a-3h against mosquito
2.2.4 化合物的抑制真菌活性
本文对化合物3a-3h的抑菌活性进行测试,结果见表4.在添加量为50 mg/kg时,化合物2d,3h的抑制番茄早疫菌活性(29.4%,29.4%)高于吡蚜酮(23.8%),其它化合物的活性低于吡蚜酮;化合物3f,3g,3h的抑制小麦赤霉病菌(FusariumgraminearumSehw.)活性(20.0%,22.9%,20.0%)高于吡蚜酮(13.3%),其它化合物的活性低于吡蚜酮;化合物3a-3h的抑制马铃薯晚疫病菌(Phytophthorainfestans(Mont.)deBary)、辣椒疫霉病菌(Phytophthoracapsici)、油菜菌核病菌(Sclerotiniasclerotiorum(Lib.)deBary)活性低于吡蚜酮(22.2%,36.7%,31.7%);化合物3g的抑制黄瓜灰霉病菌(Botrytiscinerea)、水稻纹枯病菌(Rhizotoniasolani)活性(63.2%,62.8%)高于吡蚜酮(47.5%,19.0%),其他化合物的活性低于吡蚜酮;化合物3a-3h的抑制黄瓜枯萎病菌(Fusariumoxysporum)、花生褐斑病菌(CercosporaarachidicolaHori)、苹果轮纹病菌(Physalosporapiricola)、小麦纹枯病菌(Rhizoctoniacerealis)、玉米小斑病菌(Bipolarismaydis)、西瓜炭疽病菌(Watermelonanthracnose)活性高于吡蚜酮(5.0%,15.8%,27.6%,63.6%,16.7%,16.7%);化合物3e,3f的抑制水稻恶苗病菌(Fusariummoniliformesheld)活性(25.8%,32.3%)高于吡蚜酮(19.0%),其他化合物的活性低于吡蚜酮。因此,所有化合物均有一定的抑菌活性,其中化合物3g,3h表现出较为优异的抑菌活性。

表4 目标化合物3a-3h的抑菌活性(添加量为50 mg/kg)Table 4 Insecticidal activity of compounds 3a-3h against mosquito
2.2.5 化合物的除草活性
本文对化合物3a-3h的除草活性进行测试,结果见表5.在1 500 g/公顷时,化合物3d,3f对土壤处理过的油菜除草活性(10.0%,5.0%)高于吡蚜酮(0),其他化合物没有活性;化合物3b对土壤处理过的反枝苋除草活性(10.0%)高于吡蚜酮(0),其他化合物没有活性;化合物3a-3h对土壤处理过的稗草、马唐没有除草活性;化合物3a,3b,3c对茎叶处理过的油菜除草活性(5.0%,5.0%,10.0%)高于吡蚜酮(0),其他化合物没有活性;化合物3b,3f,3h对茎叶处理过的反枝苋除草活性(20.0%,10.0%,5.0%)高于吡蚜酮(0),其他化合物没有活性;化合物3a,3b对茎叶处理过的稗草没有除草活性,其他化合物的除草活性高于吡蚜酮(0);化合物3g,3h对茎叶处理过的马唐除草活性(10.0%,10.0%)高于吡蚜酮(0),其他化合物没有活性。因此,大部分化合物没有除草活性,仅有部分化合物具有微弱的除草活性。

表5 目标化合物3a-3h的除草活性Table 5 Insecticidal activity of compounds 3a-3h against mosquito
3 结 论
本文设计合成了8种含羰基氧的三嗪酮类化合物,经1H NMR、13C NMR和HRMS确证了其结构,并测试了其杀虫活性、抑菌活性及除草活性。
1) 杀虫活性测试表明,在添加量为200 mg/kg和600 mg/kg时,化合物3b,3f的杀棉铃虫、玉米螟和粘虫活性优于吡蚜酮。当添加量降低至0.5 mg/kg,化合物3b杀蚊幼虫活性仍达到40%,优于吡蚜酮。
2) 本文测试了8种化合物对14种病菌的抑菌活性,实验表明,所有化合物均有一定的抑菌活性,其中化合物3g,3h的抑菌活性较为优异。化合物3a-3h仅有微弱的除草活性。相关化合物的合成及生物活性研究还在进行中。
