高锰酸钾溶液制备方法的优化研究
2018-07-20何吉焕
何吉焕
(云南磷化集团有限公司,云南 昆明 650600)
高锰酸钾是一种运用广泛的强氧化剂[1],呈深紫色,有金属光泽,粒状或针状结晶,在强酸溶液、弱酸和碱性溶液中都与还原剂反应:
MnO4-+8H++5e=Mn2++4H2O (常用)
MnO4-+2H2O+3e=MnO2↓+4OH-(很少用)
在酸性溶液中的反应常用硫酸酸化,不用硝酸及盐酸,因为它们可能与被测物和高锰酸钾反应。
1 影响高锰酸钾标准溶液稳定性的因素
市售高锰酸钾纯度在99%左右,常含有少量的MnO2及其它杂质,同时蒸馏水中也常含有还原性物质,如尘埃,有机物等,因此高锰酸钾只能用间接法来配制标准溶液。
1.1 酸度的影响
在酸性溶液中高锰酸钾不稳定,会缦慢的但很明显的分解, 4MnO4+4H+=MnO2↓+3O2+2H2O;在中性或微碱性溶液中分解速度更慢[3]。
1.2 水的影响
高锰酸钾会氧化水而放出氧气,使浓度变低。中性溶液中高锰酸钾与水反应放出氧气比酸性溶液时更困难。
1.3 光照的影响
高锰酸钾见光会分解。
1.4 还原性物质的影响
水中还原性物质与高锰酸钾会反应。
1.5 有机物的影响
高锰酸钾会氧化有机物,有些有机物会使高锰酸钾裉色。
2 配制
按照国标GB/T601-2002中规定的方法配制高锰酸钾标准溶液。
称取3.3g高锰酸钾,溶于1050 mL水中,缓缓煮沸15min,于暗处放置两周,用已处理过的4﹟玻璃滤埚过滤。贮存于棕色瓶中[2]。
3 标定
称取0.25 g于105~110℃电烘箱中干燥至恒重的工作基准试剂草酸钠,溶于100mL硫酸溶液(8+92)中,用配制好的高锰酸钾溶液滴定,近终点时加热至约65℃,继续滴定至溶液呈粉红色,并保持30s。同时做空白试验。
4 结果与讨论
4.1 煮沸时间和放置时间对高锰酸钾溶液稳定性的影响
同时配制两份高锰酸钾标准溶液,一份按照国标方法煮沸15min,暗处放置两周,过滤后进行标定,另一份煮沸1h,用煮沸30min以上的蒸馏水稀释至原体积,放置过夜,过滤后进行标定,结果如下表1和表2。

表1 煮沸15min、放置两周对高锰酸钾溶液稳定性的影响
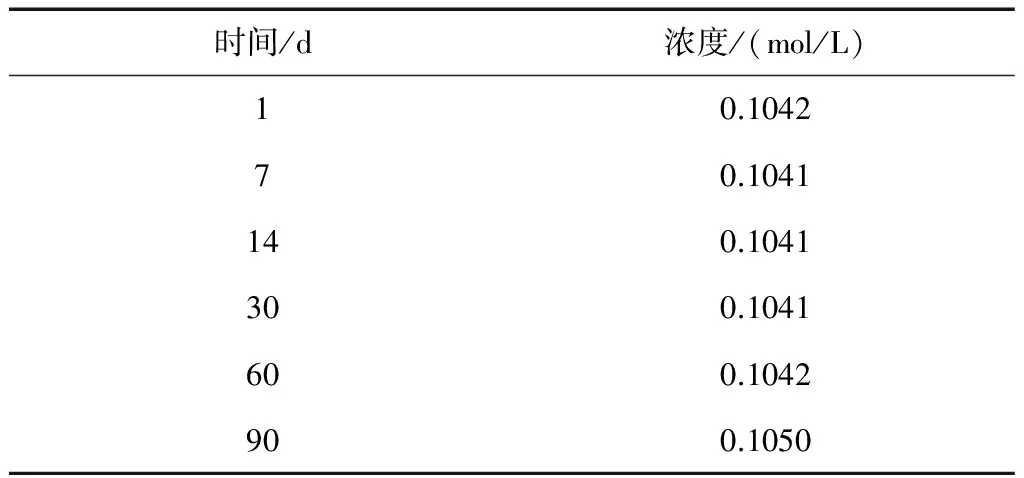
表2 煮沸1h、放置过夜对高锰酸钾溶液稳定性的影响
由表1和表2可知,两种配制方法得到的高锰酸钾溶液,在三个月内分别测试其浓度,浓度变化不大,说明水中的还原性物质很少,在不同煮沸时间和放置时间下都已反应完全。
4.2 酸度对高锰酸钾溶液稳定性的影响
两种配制方法得到的高锰酸钾溶液,测定pH值结果如表3。
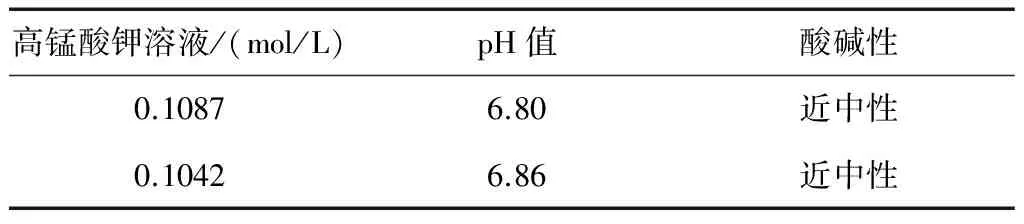
表3 高锰酸钾溶液pH值
由表3看出,它们的pH值接近中性,再结合表1和表2的标定结果可知,配制得到的高锰酸钾溶液,很稳定,说明在中性环境,高锰酸钾的分解速度很慢,氧化水的能力也很低。
4.3 有机物质对高锰酸钾溶液稳定性的影响
按国标配制高锰酸钾溶液,用4﹟玻璃滤埚过滤,抽滤过程出现真空泵水少量倒吸,溶液标定结果如表4。

表4 有机物质对高锰酸钾溶液稳定性的影响
表4中数据显示各次标定结果相差很大,溶液极不稳定,浓度一直在变化,且标定过程中变色不明显,没有高锰酸钾明显的紫色,溶液已被真空泵和管子里残留的有机物污染,不能再用,可见有机物对高锰酸钾溶液的稳定性影响很大。
4.4 不同浓度高锰酸钾溶液标定硫酸亚铁铵
用两种配制方法得到的高锰酸钾溶液,分别标定同一硫酸亚铁铵,标定结果如表5。
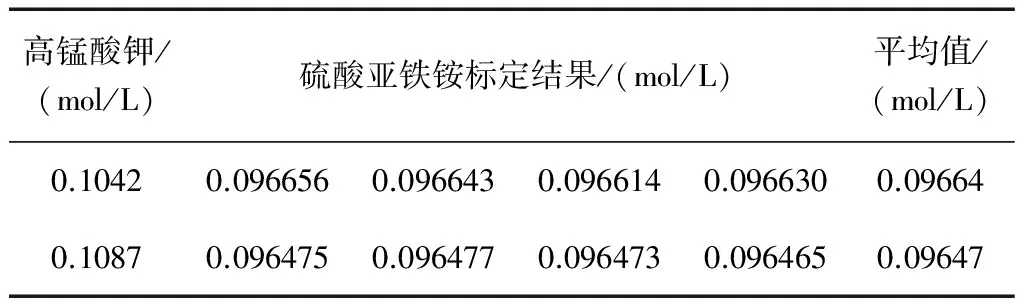
表5 不同浓度高锰酸钾溶液标定硫酸亚铁铵
两个浓度的高锰酸钾溶液标定同一硫酸亚铁铵溶液,测得的浓度值相对极差为0.18%,说明两种方法配制的溶液都可行,有效。高锰酸钾本身的氧化性及试样性质是影响测定结果的最主要因素[4]。
用标定后得到的两个硫酸亚铁铵标准溶液0.09664 mol/L和0.09647 mol/L分别测定黄磷中的P2O3,结果为0.0017%和0.0021%。
4.5 同浓度高锰酸钾溶液测定水中COD(Mn)
将两个不同浓度高锰酸钾溶液稀释10倍后,测定水中的耗氧量,结果如表6。

表6 同浓度高锰酸钾溶液测定水中COD(Mn)
说明两种方法配制的高锰酸钾溶液都可行,有效。
5 注意事项
在高锰酸钾溶液配制和标定过程中,应该注意:
(1)玻璃滤埚在抽滤前应在同浓度的高锰酸钾溶液缓缓煮沸5min。抽滤切不能出现倒吸。
(2)滴定开始要先慢后快。
(3)近终点时,要加热到65℃再进行滴定,不能超过85℃。
6 小结
配制高锰酸钾溶液时,煮沸溶液1 h,并用煮沸30min以上的蒸馏水稀释至原体积,放置一夜后经抽滤,标定,得到的高锰酸钾标准溶液浓度稳定。实验证明和GB/T601-2002的配置方法相比,大大缩短了放置时间,且浓度有较高的准确性。
