响应面优化人参花黄酮 提取工艺及活性研究
2018-07-11都宏霞陶劲强刘宴秀
都宏霞,陶劲强,2,王 翔,刘宴秀,俞 轩
(1.南京科技职业学院化工与材料学院,江苏南京 210048;2.南京工业大学材料科学与工程学院,江苏南京 211800)
人参花是珍贵草药五加科植物人参的花蕾[1],在我国主要生长在河北北部、黑龙江、辽宁、吉林等地[2]。人参是我国的瑰宝,近年来,国内外学者先后对人参的根、根茎、茎、叶及果实的化学成分做了较为系统的研究,但对人参花资源的研究报道甚少。
人参花作为一种具有潜在药用和食用价值的植物,也在逐渐受到大家的关注[3-4],虽然研究的不多,但也取得了一定进展,研究主要集中在花蕾发育的细胞学特征[5]、皂苷[6-7]、多糖[8]及挥发油等其他化学成分上[9-11],刘淑莹等通过甲醇作为萃取溶剂,经RRLC-Q-TOF-MS/MS分析得到14种人参皂苷[6],而徐斐等通过70%的乙醇提取,得到11种人参皂苷[7],回瑞华等通过超声波提取得到人参花多糖提取最佳工艺[8],徐斐等通过水蒸气回流法提取并鉴定出33种人参花挥发性成分[10]。关于人参花黄酮(Ginseng Flower Flavonoids,简称GFF)的研究只见一篇报道,采用8种不同方法对人参花进行炮制,比较其人参皂苷含量、黄酮、多糖的含量[11]。
黄酮类化合物是天然药用植物的主要活性成分之一,具有多种生理功能[12-13],迄今为止还未有对GFF的提取工艺和抗氧化活性的系统研究,本文在单因素分析的基础上,通过响应面法优化,初步确定GFF提取的最优工艺,并对三种自由基的抗氧化活性进行了测定,为GFF的研究奠定了重要的基础,为进一步开发人参花资源提供了坚实的理论依据。
1 材料与方法
1.1 材料与仪器
新鲜人参花 六年生大花,吉林省长白山土特产公司;芦丁标准样品 北京恒元启天化工技术研究所;1,1-二苯基-2-三硝基苯肼、邻苯三酚 Sigma公司;乙醇、三氯化铝、醋酸钾、FeSO4·7H2O、水杨酸、H2O2、三羟甲基氨基甲烷、浓盐酸均为分析纯。
ME204E-02型电子天平 梅特勒-托利多仪器(上海)有限公司;7600型紫外分光光度计 上海菁华科学仪器制造有限公司;TDL-50B型低速台式离心机 上海安亭科学仪器厂。
1.2 实验方法
1.2.1 GFF的提取及测定 以新鲜人参花为原料,经过洗涤、阴干等预处理,经超微粉碎至40目、乙醇浸泡、微波提取,转速3000~4000 r/min,时间20~30 min进行离心分离,取出上清液,过0.45 μm滤膜,对D101大孔树脂进行预处理后,上样,待吸附平衡后,用去离子水、分别用质量浓度为30%、50%、70%、90%的乙醇溶液洗脱,每个浓度均洗脱3柱体积(BV),流速为1 BV/h,收集90%乙醇浓度的洗脱液,于45 ℃旋转蒸发进行浓缩后[14],再用50%的乙醇溶液进行稀释得到人参花黄酮样品(GFF)。
人参花黄酮提取量的测量按文献方法[15-16]并稍微修改。用质量分数为50%的乙醇溶液定容5.0 mg芦丁标准品至25.0 mL。
称取芦丁标准品(0.2 mg/mL)0.5、1.0、2.0、3.0、4.0、5.0 mL分别置于6只比色管中,分别用质量分数50%的乙醇溶液至5.0 mL,0.1 mol/L三氯化铝溶液3.0 mL和1 mol/L醋酸钾溶液5.0 mL,摇匀,同法制成空白对照:静待40 min后于415 nm波长处测其吸光度值,并通过originpro 2017软件绘出标准曲线。
人参花中黄酮提取量的测定:吸取2 mLGFF提取液,按上述标准曲线步骤反应后,在415 nm处测定吸光度值,结果以人参花中含有相当于芦丁的毫克数表示,单位为mg/g。
式中:X表示标准曲线计算出的质量浓度(mg/mL);v表示提取液的总体积(mL);N表示稀释倍数;m表示人参花粉末的质量(g)。
1.2.2 微波提取GFF的单因素实验
1.2.2.1 微波功率对GFF提取量的影响 料液比1∶10,乙醇质量分数60%,微波时间30 s,再分别取80、240、400、640、800 W的微波功率作为变量,观察微波功率对其提取量的影响。
1.2.2.2 乙醇质量分数对GFF提取量的影响 料液比1∶10,在微波时间30 s和微波功率为800 W的条件下,乙醇质量分数分别为40%、50%、60%、70%、80%,制备出提取液,比较该变量对其提取量的影响。
1.2.2.3 料液比对GFF提取量的影响 在50%的乙醇质量分数,微波功率800 W,时间30 s的条件下,分别取料液比1∶10、1∶15、1∶20、1∶25、1∶30制备出提取液,比较此变量对其提取量的影响。
1.2.2.4 微波时间对GFF提取量的影响 在50%乙醇质量分数,800 W微波功率,1∶20料液比的条件下,分别取微波时间20、30、40、50、60 s,比较该变量对其提取量的影响。
1.2.3 响应面法优化GFF最优提取工艺条件 使用Design-Expert.V8.0.6软件中Box-Behnken组合设计来确定实验最优工艺,从单因素实验基础上,选择液料比、乙醇质量分数、微波时间作为3因素,每个因素选择三个对GFF提取量影响较大的水平,进行3因素3水平的响应面实验,并以GFF提取量作为响应值,各因素的三个水平分别采取-1、0、1作为编码,如表1。
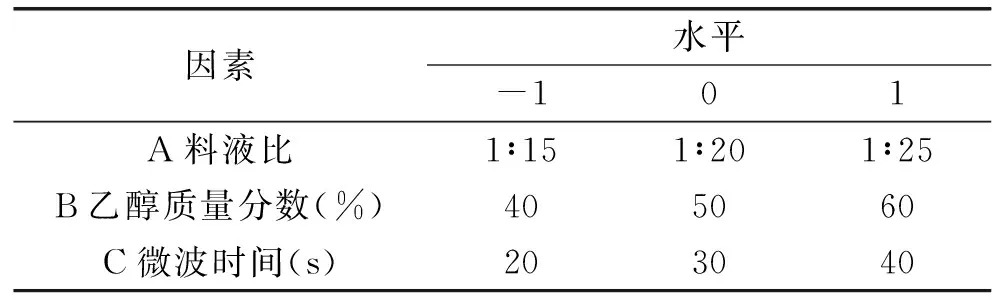
表1 响应面实验分析因素水平表Table 1 Factors and levels of response surface methodology
1.2.4 GFF对DPPH自由基的清除能力测定 依据Brandwilliams[17-19]等人的实验步骤,制定实验方案。配制0.1 mmol/L的DPPH乙醇溶液备用。精确吸取0、0.4、0.8、1.2、1.6、2.0、2.0 mL经D101大孔树脂纯化过的提取液,精确吸取2.0、1.6、1.2、0.8、0.4、0.6、0 mL和6.0 mL新配制的DPPH溶液于试剂中,避光静待30 min后,再用分光光度法在517 nm处测定吸光度值,并用VC做阳性对照。GFF提取液对DPPH自由基的清除能力依据公式计算:
式中,I1表示对DPPH自由基的清除率(%);Ai表示GFF和DPPH溶液混合液吸光度;Aj表示无DPPH溶液吸光度;A0表示无样品时DPPH溶液的吸光度。
1.2.5 GFF对羟自由基的清除能力测定 采用Fenton反应来测定GFF的羟自由基清除率[20-22]。于比色管中分别加入1 mL的9 mol/L FeSO4溶液、1 mL的9 mmol/L水杨酸-乙醇溶液,不同浓度用D101树脂纯化过的待测GFF提取液1 mL(空白对照以蒸馏水代替GFF提取液),最后加1 mL的8.8 mol/L H2O2溶液,水浴35 min,温度恒定35 ℃,测其吸光度的波长为510 nm,检测液本身有吸光度,因此测其本底值需用蒸馏水代替H2O2,并用VC做阳性对照。并根据此公式计算其清除率:
式中,I2表示对羟自由基的清除率(%):A0是空白对照实验(蒸馏水代替GFF提取液)的吸光度;AX是加入提取液后的吸光度;AX0是检测液本底的吸光度(蒸馏水代替过氧化氢)。
1.2.6 GFF对超氧阴离子自由基的清除能力测定 采用邻苯三酚自氧化法[22-25]进行测定超氧阴离子自由基清除能力,分别取4.5 mL pH8.2的Tris-HCl缓冲液于若干比色管中,20 ℃水浴25 min。每管中分别加入不同浓度经D101树脂纯化过的待测GFF样品溶液0.1 mL及0.3 mL 在30 ℃预热条件下3 mmol/L的邻苯三酚(用10 mmol/L的HCl配制),振荡后恒温20 ℃水浴6 min,随滴2滴8 mol/LHCl反应终止,空白对照选用蒸馏水,测吸光度波长为320 nm,并用VC做阳性对照。提取液对超氧自由基的清除率按公式计算。
式中,I3表示对超氧自由基的清除率(%),A0为空白对照的吸光度;An为加入GFF后的吸光度。
1.3 数据处理
使用Microsoft office excel 2013、Originpro 2017和Design-Expert.V8.0.6进行数据处理、图表制作及数据分析。
2 结果与分析
2.1 芦丁标准曲线的结果分析
经测定,由图1得其回归方程为Y=16.43412X+0.06882,其系数R2=0.99938,在0~0.08 mg/mL范围内线性关系良好。

图1 芦丁标准曲线Fig.1 Standard curve of Rutin
2.2 单因素实验
2.2.1 微波功率对GFF提取量的影响 结果如图2所示:微波功率在80~240 W之间,随着功率的增大,GFF提取量呈上升趋势;在240~400 W范围内,随着功率的增大,GFF提取量呈下降趋势;在400~800W范围内,随着功率的增大,GFF提取量呈上升趋势。GFF的提取量在800 W时最大。而在240~400 W之间下降,可能是在微波的交变电磁场作用下,引发黄酮强烈振荡,导致分子间氢键断裂,使得有少量黄酮受热分解[26],加速了乙醇溶液的热运动,使得一些醇溶性杂质,脂溶性成分溶出量增加,使溶液黏度变大,增大了传质过程中溶剂的阻力,减慢了GFF向溶剂扩散,减少了粉末表面与溶剂之间GFF浓度差,从而导致GFF的提取量减少[27]。微波功率在小于800 W时,分子热运动较慢,微波对细胞膜破坏作用较小,因此提取量不高。最高值为3.604 mg/g。

图2 微波功率对GFF提取量的影响Fig.2 Effect of microwave power on extraction yield of GFF
2.2.2 乙醇质量分数对GFF提取量的影响 结果如图3所示:乙醇质量分数在50%时GFF的提取量最大,而在40%~50%时,GFF的提取量呈上升趋势,当50%~80%时,GFF的提取量呈下降趋势。许辉[28],刘俊[29]等人在研究中发现黄酮提取量随着乙醇浓度的增加而呈现与本文同样的趋势,推测是加入乙醇溶液之后引入了羟基,乙醇分子与水分子间和其自身间均相互结合形成氢键,体系极性降低,故黄酮的提取量在升高,但随着乙醇质量分数增加,其极性下降,导致了黄酮的溶解能力减弱,因此最佳乙醇质量分数为50%。此时提取量最高,提取量为3.628 mg/g。
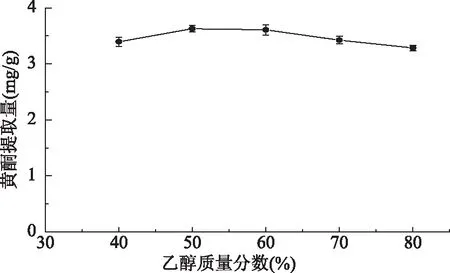
图3 乙醇质量分数对GFF提取量的影响Fig.3 Effect of ethanol concentration on extraction yield of GFF
2.1.3 料液比对GFF提取量的影响 结果如图4所示:GFF的提取量先高后低,此时料液比在不断增加,料液比1∶20时人参花黄酮的提取量最大。料液比1∶20,当料液比大于1∶20时,人参花黄酮的提取量下降。大体积的溶剂量减小了黄酮吸收的能力导致其溶解量减小。GFF提取量随着料液比的升高而升高,但当料液比达到1∶20后,提取量呈现下降趋势。因为料液比的增加可以使体系的溶解度升高,促进人参花细胞破壁,使内容物溢出率增加,但当溶解度大到一定程度时,可能会发生饱和的现象,导致部分黄酮无法溶解。因此最佳料液比为1∶20。提取量为5.313 mg/g。

图4 料液比对GFF提取量的影响Fig.4 Effect of liquid-material ration on extraction yield of GFF
2.2.4 微波时间对GFF提取量的影响 结果如图5所示:在20~30 s时提取量呈上升趋势,此时黄酮的溶出主要受温度控制,因此提取量随着温度升高而提高。但在30~60 s时反而呈下降趋势,可能是微波加热有升温过程。但在30~60 s阶段温度已经稳定,大部分细胞膜已经破坏,黄酮的溶出速度受分子扩散速度,因此提取量随着时间增加而降低,最大条件为30 s。此时提取量最高为5.359 mg/g。
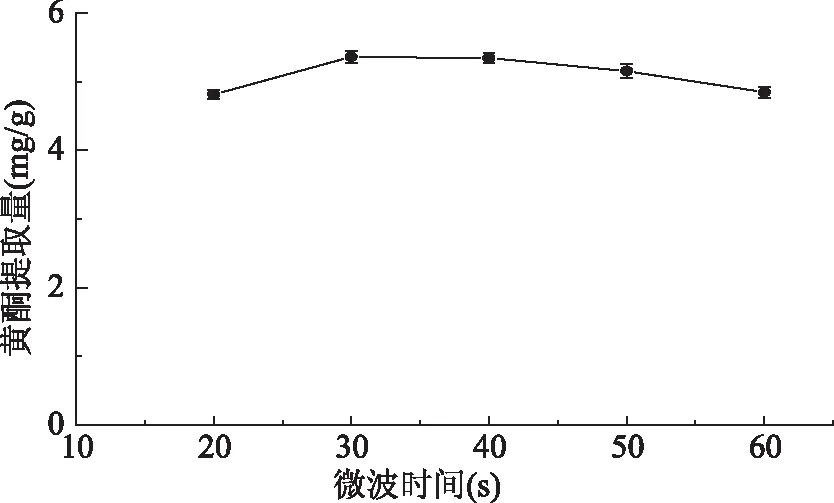
图5 微波时间对GFF提取量的影响Fig.5 Effect of extraction time on extraction yield of GFF
2.3 响应面实验结果与优化分析
2.3.1 响应模型的建立与分析 Box-Behnken实验结果:根据单因素实验结果,选取响应面实验因素为A料液比、B乙醇质量分数(%)、C微波时间(s),GFF为响应值(Y),采用Design-expert软件按照Box-Benhnken实验设计了15组实验,12组为析因点实验,3组为重复零点实验,结果见表2对人参花黄酮提取量的影响进行响应面优化需对3个自变量进行编码,以GFF提取量作为响应值。实验设计方案及响应面数据结果分析见表2,方差与误差统计分析见表3。

表2 响应面Box-Benhnken 实验设计及结果Table 2 Design and results of the response surface methodology(RSM)and Box-Behnken
在表2中进行分析并建立如下二次回归方程(编码方程):Y(黄酮提取量)=4.83+0.12A-(1.250E-003)B+0.055C-0.046AB-0.069AC-0.010BC-0.62A2-0.12B2-0.40C2
表3的数据可知:模型的p值为0.0037,模型显著(p<0.05);失拟项p值为0.1260,结果不显著(p>0.05),表明拟合状况良好。方程决定系数R2=0.9656,CV为6.64%<10%,能真实的反映本模型,可用此模型分析响应面的变化。信噪比(Adeq Precision)为11.396大于4,表示模型合理[30]。
由方差F值可知,各因素对GFF提取量影响为:B(乙醇质量分数)>C(微波时间)>A(料液比)。由表3还可知,因素中B的影响显著,而A,C,AB,AC,BC的影响不显著,该方程可适用。
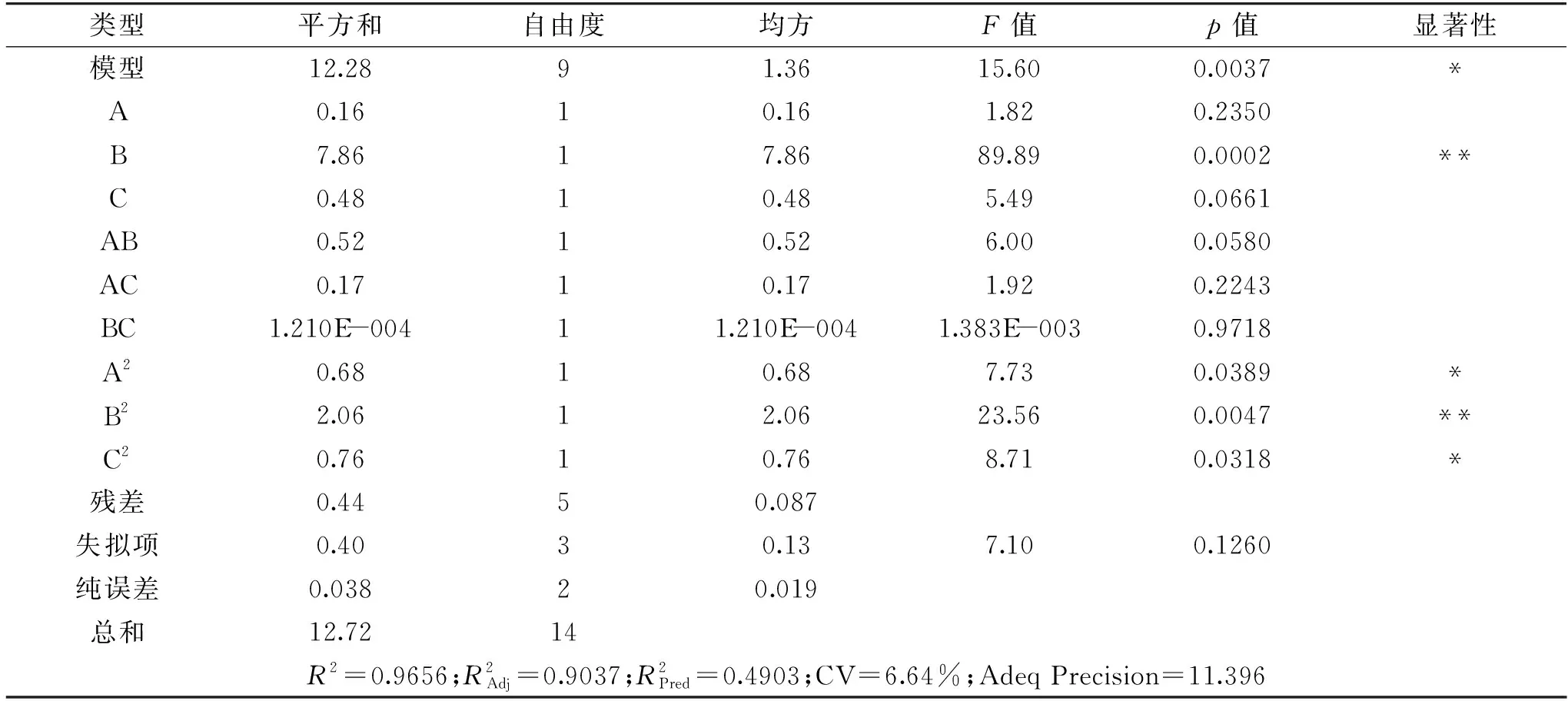
表3 回归模型的方差分析Table 3 Variance analysis of regression model
2.3.2 响应面交互作用分析与优化 各因素间交互作用得到响应面曲线图。图6~图8分别显示3个结果分析,并绘制响应面曲线图。当黄酮的提取量相同时等高线图在同一曲线上[31-32]。在密闭区域内,GFF值从中心向四周下降。当等高线排列紧密,表明操作条件与响应值改变较为明显。等高线图直观表示2变量之间交互作用,此时椭圆形则为显著[30]。

图6 料液比与乙醇质量分数响应面图Fig.6 Response Surface of Y=f(A,B)

图7 微波时间与料液比响应面图Fig.7 Response Surface of Y=f(A,C)
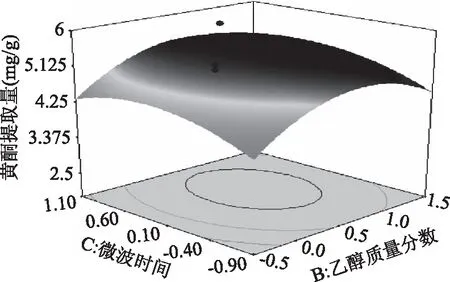
图8 微波时间与乙醇质量分数响应面图Fig.8 Response Surface of Y=f(B,C)
分析图6三维曲面图可以看出,料液比曲面比乙醇质量分数曲面坡度陡峭,固定另一因素不变,即表明料液比对人参花黄酮提取量的影响比乙醇质量分数的影响大。同理再分析图7三维曲面图可以得出料液比比微波时间对人参花黄酮提取量的影响大,这与二元回归方程系数相符合,图8中微波时间与乙醇质量分数的曲面坡度均陡峭,交互作用明显,这与方差分析表一致。
可从各响应面立体图观测出响应面有最值。通过软件得出理论最佳提取工艺:微波功率800 W,微波时间29.69 s,乙醇质量分数为54.21%,料液比1∶21.43,理论黄酮提取量为5.6502 mg/g,结合实验室条件修正为800 W,微波时间30 s,54%的乙醇质量分数,料液比1∶21,最终实验结果为5.624 mg/g,与理论值相差0.03%,说明模型与实际情况拟合较好,验证了所预测模型的正确性。因此,响应面法对微波辅助人参花黄酮提取的参数优化是可行的,得到的工艺条件具有实际应用价值。
2.4 GFF对自由基的清除能力结果分析
2.4.1 GFF对DPPH自由基的清除能力结果分析 不同浓度的人参花黄酮提取液与VC溶液对DPPH自由基清除能力如图9所示。从图中可以看出,VC在1 mg/g左右达到最大值,且在之后基本不变。GFF对DPPH自由基的清除能力比VC差。DPPH自由基清除率随着GFF提取量的增加,也在不断升高,当人参花黄酮浓度是0.24 mg/mL时,清除率最大为71.47%,人参花黄酮和VC的IC50值分别为0.17 mg/mL和0.09 mg/mL。

图9 GFF对DPPH自由基清除能力Fig.9 Scavenging effect of GFF on DPPH radical
2.4.2 人参花黄酮对羟自由基的清除能力结果分析 不同浓度的人参花黄酮提取液与VC溶液对羟自由基清除能力如图10所示,从图中可以看出,GFF对羟自由基具有一定的抑制能力但不如VC显著,羟自由基与GFF提取量有量效关系,呈正相关,当人参花黄酮浓度在0.24 mg/mL时,清除率最大为49.91%,人参花黄酮和VC溶液的IC50为0.24 mg/mL和0.30 mg/mL。

图10 GFF对羟自由基清除能力Fig.10 Scavenging effect of GFF on hydroxyl free radicals
2.4.3 GFF对超氧阴离子自由基的清除能力结果分析 不同浓度的人参花黄酮提取液与VC溶液对超氧阴离子自由基清除能力如图11所示。从图11中可以明显看出GFF和VC溶液对超氧自由基都有一定的抑制能力,抑制率与浓度呈良好的量效关系,且GFF比VC溶液对超氧自由基的抑制能力要好,当人参花黄酮浓度是0.24 mg/mL时,有最大清除率72.32%,人参花黄酮和VC溶液的IC50分别为1.73 mg/mL和0.14 mg/mL。
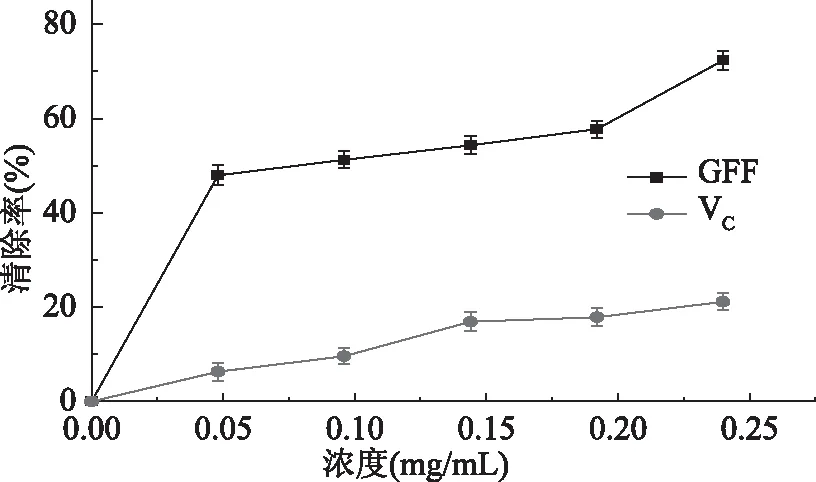
图11 GFF对超氧自由基的清除能力Fig.11 Scavenging effect of GFF on superoxide anion free radical
2.4.4 GFF对3种自由基清除率的比较 通过实验比较发现,GFF对3种自由基均具有清除能力,且抑制率与GFF提取量成正比,72.32%(超氧自由基清除率)>71.47%(DPPH自由基清除率)>49.91%(羟自由基清除率),且超氧自由基和DPPH自由基的活性相似。羟自由基是已知最活泼的氧化剂且反应范围广[33],因此GFF对其清除率最低。
3 结论
通过单因素实验得出响应面优化条件,在使用Design-Expert软件中的设计方法上建立数学模型。方差分析结果表明人参花黄酮提取量与乙醇质量分数呈正相关,与微波时间,液料比有一定影响,结合响应面交互作用分析结果和实际情况预测最佳条件,并验证后得出人参花黄酮提取最佳条件为微波功率为800 W,微波时间30 s,54%的乙醇质量分数,料液比1∶21。
人参花中黄酮的研究鲜有报道,这不仅不利于对中国传统中医药领域的研究,还不利于对中国自然资源的再利用。通过对人参花黄酮的研究,测量人参花黄酮的活性,有助于了解其成分功效,开发其潜在价值,研发出新的产品,将其工业化,扩大人参花这一潜在市场,并以此带动传统农产品和中药材的附加价值再利用。
