离子液体对CO2捕集及电转化的研究
2018-07-07成丽苹郝永超王秀玲马晓刚
成丽苹,郝永超,李 敏,王秀玲,赵 哲,马晓刚,王 月
(邢台学院 化学工程与生物技术学院,河北 邢台 054001)
CO2是温室效应的主要因素,温室效应愈演愈烈,已造成气候变暖等极其严重的问题,引起了全世界的重视。如何缓解温室效应造成的环境问题,一方面减少CO2的排放量,另一方面收集利用CO2也是解决问题的途径之一。CO2可作为碳资源,将其转化成燃料,那么对于解决能源危机是非常有帮助的[1]。所以从能源和环境两个方面来看,CO2的捕集和利用都是非常有意义的。目前吸收固定CO2的方法有物理法、化学法、生物法等固定方法,物理固定是通过将CO2封存于海底,但是这种方法易导致海水酸化;生物法固定是通过植物的光合作用固定二氧化碳,但是近年来植被的破坏,光合作用也严重受限,无法与人类生产活动释放的二氧化碳总量持平;化学法固定是实现二氧化碳循环利用最有效的途径[2],工业上普遍使用的是以醇胺法固定二氧化碳的化学吸附,但是因其具有挥发性和腐蚀性,对仪器设备破坏性大[3],因此,开发绿色无污染的方法是目前亟待解决的。
离子液体(Ionic Liquids)在室温下呈液态,是由特定阴、阳离子构成,被称为新型“绿色溶剂”、“软”功能材料[4-6],也被称作室温离子液体、低温熔融盐、有机离子液体等。目前尚无统一的名称,但倾向于简称离子液体。它不挥发、不可燃,具有良好的化学稳定性,液体稳定范围和电化学窗口都较宽,循环使用性能较好[7]。
离子液体的制备方法有微波合成法和其他辅助波法,微波法是在磁场中将交变电磁能转化为介质内能的一种加热方法,该方法具有加热速度快、均匀、节能高效等优点。本文采用微波法合成咪唑氨基酸([Amim]Gly)、咪唑四氟硼酸盐([Bmim]BF4)和咪唑六氟磷酸盐([Bmim]PF6)离子液体,并对不同类型离子液体吸附CO2特性进行考察,并以咪唑氨基酸类离子液体作为电解质,对二氧化碳进行电化学还原,探究其对CO2电转化甲醇的催化效能。
1 实验部分
1.1 仪器与试剂
仪器:XH-100B电脑微波催化合成/萃取仪,RE-52AA 旋转蒸发仪,HDY-I 恒电位仪,Agilent 789A气相色谱仪。
试剂:1-甲基咪唑,氯丙烯,四氟硼酸钠,六氟磷酸钾,溴代正丁烷,二氯甲烷,甘氨酸,丙酮,环己烷,乙酸乙酯,无水乙醇,无水硫酸钠,氯化钠,盐酸,氢氧化钠,无水碳酸钠,浓硫酸,无水乙醚,甲醇(除甲醇为色谱纯外均为分析纯),去离子水。
1.2 功能化离子液体的制备
[Amim]Gly离子液体的制备。采用微波-动态离子交换法合成。先合成氯化1-甲基-3-烯丙基咪唑,取0.1 mol 1-甲基咪唑加入10 mL氯丙烯,磁力搅拌10min。设置微波参数功率:500 W,温度:55 ℃,在微波条件下反应120min。用20 mL的环己烷萃取三次,等体积的乙酸乙酯萃取两次[8]。除去溶剂,得到中间体氯化1-甲基-3-烯丙基咪唑。将中间体用乙醇稀释加入活化后的离子交换树脂层析柱中,控制液滴速率(10s/滴),直至液滴pH为中性,产物蒸发一半溶剂。再加入等物质的量的甘氨酸,室温搅拌12 h,加入无水硫酸钠干燥,减压抽滤,抽滤所得液体经减压蒸馏后,恒温干燥24 h。
[Bmim]BF4离子液体的制备。称取0.3 mol 1-甲基咪唑,0.33 mol(稍过量)溴代正丁烷于微波专用反应瓶中,设置参数进行反应,产物用乙酸乙酯进行洗涤,再蒸去乙酸乙酯,得到中间体溴代1-丁基-3-甲基咪唑。称取0.1 mol溴化1-丁基-3-甲基咪唑和11 g四氟硼酸钠于锥形瓶中,加入150 mL丙酮,磁力搅拌5 h,除去不溶物,蒸出丙酮,加入200 mL二氯甲烷,每次用15 mL水洗涤,直到水层用AgNO3溶液检测不到溴离子为止,下层加入过量无水MgSO4,除去不溶物,蒸去二氯甲烷溶剂得到离子液体,烘干,备用。
[Bmim]PF6离子液体的制备。先用少量水溶解0.1 mol上述中间体,称取18.4 g六氟磷酸钾于烧杯中,溶解并逐滴滴入中间体溶液中,室温磁力搅拌2 h,静置分层,有机层溶液加入去离子水洗涤,直到水层用AgNO3溶液检验无沉淀为止。烘干,备用。
1.3 离子液捕集CO2
碳酸钠和盐酸溶液反应制备CO2,经过饱和碳酸钠溶液吸收氯化氢气体,浓硫酸吸收水蒸气后通入装有离子液的小试管中。通过称重计算CO2吸附量。
准确称量H型电解槽的质量,将样品的水溶液(样品与水的体积体比为7∶3)50 mL加入H型电解槽中,铂电极为阳极,银电极为阴极,甘汞电极为参比电极,还原之前,向电解槽内通入CO210 min,进行CO2饱和捕获,再次称取电解槽,计算捕获CO2的质量。在外加-0.5 V过电位下,电化学还原25min,用无水乙醚萃取得到还原产物[1],还原产物用气相检测CO2转化甲醇的含量。
1.4 检测条件
气相色谱条件:HP-INNOWAX毛细管柱(30 m×320 μm×0.25 μm);载气:N2,流量:1.3 mL/min;进样口温度180 ℃;程序升温:27 ℃保持10min,然后以25 ℃/min升到220 ℃,保持10min;检测器温度:230 ℃;分流比:50∶1;进样量1 μm[9]。
标准曲线:精密量取0.1、0.2、0.3、0.4、0.5 mL甲醇分别置于10 mL容量瓶中,用无水乙醇稀释至刻度,制成体积分数分别为0.1%、0.2%、0.3%、0.4%、0.5%的甲醇溶液。进行气相检测,得到标准曲线方程为y = 0.948x + 0.0019,R2=0.9989。
2 结果与讨论
2.1 离子液体的FT-IR分析
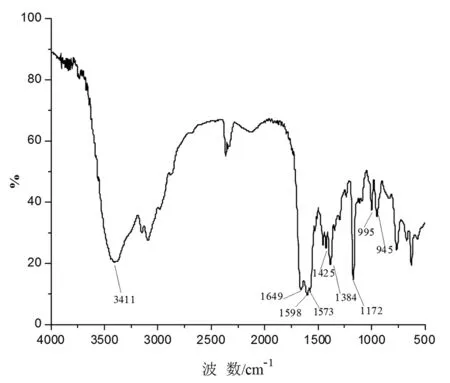
图1 [Amim]Gly的红外谱图
图1是[Amim]Gly的红外谱图。波数为1573 cm-1是咪唑环特征振动峰,1172 cm-1是咪唑环C-H面内弯曲振动峰。1649 cm-1和1425 cm-1分别是烯丙基上C=C伸缩振动峰和双建上的C-H弯曲振动峰。3411 cm-1是N-H伸缩振动峰,1598 cm-1和1384 cm-1是甘氨酸中C=O伸缩振动峰。995 cm-1是-CH=CH2的C-H面外弯曲振动峰,945 cm-1是-CH=CH2的C-H面内摇摆振动峰。

图2 [Bmim]BF4的红外谱图
图2是[Bmim]BF4的红外谱图。波数为3160cm-1和3122cm-1是咪唑环上的C-H伸缩振动峰,波数为2964 cm-1和2877 cm-1是CH3-和CH2-的伸缩振动峰,波数为1573 cm-1和1469 cm-1咪唑环振动峰,波数为1176 cm-1是咪唑环C-H面内弯曲振动峰,波数为1066 cm-1是B-F伸缩振动峰,波谱特征与文献一致[10]。

图3 [Bmim]PF6的红外谱图
图3是[Bmim]PF6的红外谱图。波数为3168 cm-1和3129 cm-1是咪唑环上的C-H伸缩振动峰,波数为2969 cm-1和2875 cm-1是CH3-和CH2-的伸缩振动峰,波数为1572 cm-1和1463 cm-1是咪唑环振动峰,波数为1172 cm-1是咪唑环C-H面内弯曲振动峰,波数为846 cm-1是P-F伸缩振动峰,波谱特征与文献一致[10]。
2.2 离子液体对CO2吸附量的研究
在常温下,考察CO2吸附量随时间的变化,分别称取相同质量[Amim]Gly、[Bmim]BF4和[Bmim]PF6离子液体置于小试管中,将纯净的CO2以鼓泡形式通入离子液体中,控制鼓入速度,每隔5 min称重,计算二氧化碳的质量变化,如表1。由表1可知,开始时CO2吸附量增加较快,当吸附10 min后产物CO2的吸附量变化不大,20 min达到饱和,最大吸附量为每摩尔离子液吸收0.24 mol CO2。[Bmim]BF4开始时吸附CO2的量增加较快,当通入20 min之后,吸附CO2的量变化较缓慢,当通入30 min之后则不再发生变化,最大吸附量经过计算为每摩尔离子液吸收0.024 mol的CO2。[Bmim]PF6开始吸附CO2的量上升较快,当通入15min之后,吸附CO2的量变化不明显,当通入20 min之后则不再发生变化,最大吸附量经过计算为每摩尔离子液吸收0.015 mol CO2。
经过比较,[Amim]Gly离子液体对CO2的吸附量效果较好,选择[Amim]Gly离子液体进行电催化还原的研究。

表1 离子液体吸附CO2量随时间的变化
2.3 CO2电转化甲醇含量的测定
使用新鲜的吸附了CO2的离子液体进行电化学还原,萃取后取样于小试管,并编号为1;用萃取后的离子液体重新吸附CO2进行电催化还原,萃取后取样于小试管,并编号为2;以此类推重复五次。上述五种电化学还原产物进行气相检测,在检测标准溶液的条件下分别检测待测试样,记录检测数据,然后将数据带入上述方程求得甲醇的浓度,计算转化率,结果如表2所示。

表2 CO2的转化率
由表2可知,[Amim]Gly离子液重复使用,CO2转化率在64.1%~77.4%之间变化。在重复使用的离子液体中CO2转化率比在新鲜的离子液体的转化率高,可能是由于在电还原条件下,离子液体形成了聚合离子液体,这种聚合离子液体提高了CO2转化率。
3 结论
本文采用微波法合成了[Amim]Gly、[Bmim]BF4和[Bmim]PF6功能型离子液体,考察吸附CO2性能,最大吸附量分别为每摩尔离子液吸收0.24 mol、0.023 mol、0.015 mol的CO2,[Amim]Gly离子液体对于CO2具有良好的捕获性。室温条件下,并以[Amim]Gly离子液体为电解质,当吸附20 min时CO2达到饱和,外加-0.5 V过电位下,通电25 min,转化率即可达到64.1%~77.4%。[Amim]Gly离子液体在使用后只需简单处理即可重复使用。与以往的甲醇工业生产相比,此方法成本低、无污染、反应时间短,为工业生产甲醇提供了一种新方法。
[1]朱家艺,贺军辉.二氧化碳的捕集、存储及转化[J].影像科学与光化学,2011,29(3):170-172.
[2]刘芙蓉.基于离子液体的二氧化碳电催化还原研究[D].长沙:湖南大学,2014:1-28.
[3]范 薇,孙晓霞,苏 岩.基于离子液体固定二氧化碳的研究进展[J].化学研究,2009,20(3):101-102.
[4]文启忠,乔玉楼.爱护地球从自己做起—纪念第38个世界地球日[J].今日科苑,2007(9):41-43.
[5]张 慧,陆建刚,嵇 艳,等.离子液分离/固定二氧化碳的研究进展[J].现代化工,2009,29(11):32-36.
[6]邓友全.离子液体:性质、制备和应用[M].北京:中国石化出版社,2006.
[7]张星辰.离子液体--从理论基础到研究进展[M].北京:化学工业出版社,2009.
[8]赵卫星,姜洪波,张来新.咪唑类离子液体的制备与合成[J].贵州化工,2010,35(4):9-11.
[9]王化同,王洪莹.毛细管气相色谱法测定白酒中甲醇含量的研究[J].中国社区医师,2014,30(22):136.
[10]黄一波.咪唑类离子液体的合成与表征[J].天津化工,2007,21(6):28-29.
