Nec-1对模拟缺氧条件下骨骼肌细胞损伤修复的作用研究
2018-07-02周珊瑶陈睿谭夕佘燕玲雷斯
周珊瑶 陈睿 谭夕 佘燕玲 雷斯
氧在细胞呼吸和能量代谢中起着重要的作用。临床上,运动性损伤、缺血缺氧性疾病或组织炎症性改变常伴随氧灌注不足或摄氧障碍,低氧环境可使组织功能进一步下降、甚至发生萎缩或变性坏死[1-2]。近年来,程序性坏死(Necroptosis)作为非凋亡的细胞死亡信号途径成为缺血缺氧性损伤研究的新热点,越来越多研究者发现,程序性坏死在多系统缺血缺氧性损伤后的炎症反应、损伤修复过程中发挥重要作用[3]。相关研究表明,受体交互作用蛋白激酶1(RIP1)特异性抑制剂——坏死性凋亡抑制剂Necrostatin-1(Nec-1)能显著改善缺血缺氧性损伤,对细胞、组织的增殖分化、损伤修复功能有保护作用[4-6]。但笔者见Nec-1在骨骼肌缺氧损伤修复中作用的相关报道很少,故利用小鼠骨骼肌C2C12成肌细胞构建缺氧细胞模型,观察缺氧对肌细胞的影响及Nec-1的保护作用。
材料与方法
一、主要仪器与试剂
二氧化碳培养箱(美国Thermo Fisher Scientific公司),光学电子显微镜(美国Life Technologies公司),流式细胞仪(美国Beckman Coulter公司),电泳转印系统(北京凯元信瑞仪器有限公司),化学发光成像系统(上海天能科技有限公司)。C2C12小鼠骨骼肌细胞系购于中国科学院干细胞库,高糖DMEM培养基(美国Gibco公司),胎牛血清、马血清(美国Hyclone公司)。二氯化钴(CoCl2)、Nec-1(德国Sigma公司)。细胞周期检测试剂盒、电化学发光(ECL)试剂盒(江苏凯基生物技术有限公司)。肌细胞生成素(Myogenin,Myog)一抗(德国Merck-Millipore公司)。肌细胞增强因子2A(MEF2A)一抗(美国CST公司)。Tubulin一抗、辣根过氧化物酶标记山羊抗兔(美国ABclonal公司)。
二、实验方法
1.细胞培养
将C2C12小鼠骨骼肌细胞系置于含10%胎牛血清的高糖DMEM培养基中,于37 ℃、5%二氧化碳的培养箱中进行培养,隔日换液,观察细胞形态和生长情况。当细胞达到90%~100%融合时吸去完全培养液,使用含2%马血清的高糖DMEM培养基进行诱导分化,隔日换液。分化72 h后将细胞分为4组,分别加入等量培养基(Control组)、200 μM CoCl2(CoCl2组)、150 μM Nec-1(Nec-1组)、200 μM CoCl2+150 μM Nec-1(CoCl2+Nec-1组)。48 h后收集细胞,进行后续实验。
2.光学显微镜下观察肌管融合情况
加入CoCl2、Nec-1处理48 h后,在40倍光学显微镜下观察细胞形态、肌管融合情况。
3.细胞划痕实验
采用Maeker笔在培养板底部均匀划线做标记,控制细胞数为5×105个,待细胞生长至90%时,用200 μl枪头沿标记线垂直划痕,用磷酸盐缓冲液(PBS)冲洗3次,去除划痕损伤后不贴壁的细胞,重新加入相应培养基进行培养,采用显微镜拍照记录不同时间段划痕面积,使用Image J软件统计划痕面积。
4.细胞周期
用2%胰酶消化、离心、收集细胞,用PBS洗涤2次,调整细胞浓度为1×106/ml,制成单细胞悬液。加入70%冷乙醇500 μl固定2 h,用PBS洗去固定液,加入500 μl碘化丙啶/核糖核酸酶A(PI/RNase A)染色工作液,避光室温孵育60 min。应用PI染色法流式细胞分析不同处理下的C2C12细胞周期变化。
5.蛋白免疫印迹检测
细胞培养板中加入含蛋白酶抑制剂、磷酸蛋白酶抑制剂的细胞组织(RIPA)裂解液,于冰上裂解30 min,4℃,12 000转/分离心10 min。用二喹啉甲酸(BCA)法检测蛋白含量。取30 μg蛋白,进行电泳,再将蛋白电转移至聚偏二氟乙烯(PVDF)膜上,室温封闭1 h。加入一抗于4℃孵育过夜。洗膜5次后于室温孵育二抗。洗膜5次后,使用ECL液显色,用天能系列全自动化学发光成像分析系统扫描成像。以Tubulin作为内参,目的蛋白条带与内参比较作为条带的相对表达值。
三、统计学处理
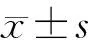
结 果
一、Nec-1、CoCl2对C2C12细胞肌管形成的影响
实验中,Control组、Nec-1组肌细胞分化情况良好,可见大量长条状肌管形成。经CoCl2处理后,分化停滞,肌管萎缩、断裂,少见长条状肌管形成。而加入CoCl2+Nec-1处理后,可见细胞分化情况较CoCl2组改善,肌管形成增多,见图1。
二、Nec-1、CoCl2对Myog、MEF2A表达水平的影响
CoCl2处理可诱导肌生成、分化标志基因Myog、MEF2A蛋白表达下降(P均<0.01),加入Nec-1处理后,可逆转CoCl2的抑制作用,上调Myog(P<0.05)及MEF2A的表达(P<0.001),见图2、表1。
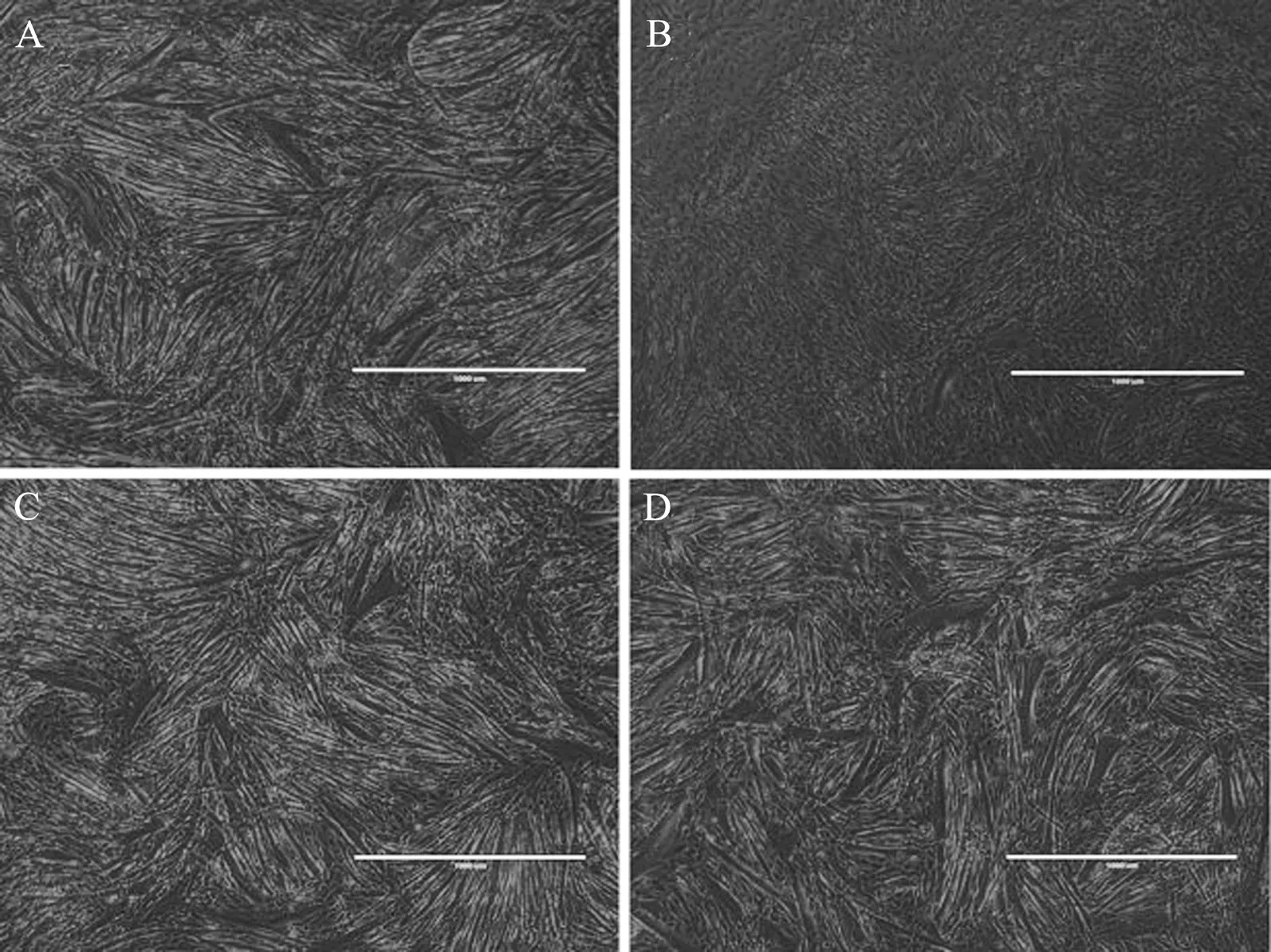
图1 处理48 h后于光学显微镜下观察各组肌细胞分化情况(×40,标尺=1 000 μm)
A:Control组;B:CoCl2组;C:Nec-1组;D:CoCl2+Nec-1组
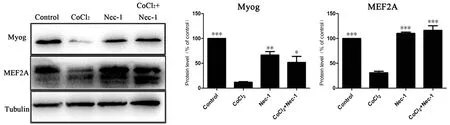
图2 Nec-1对CoCl2抑制Myog、MEF2A表达的保护作用
与CoCl2组比较,*P<0.05,**P<0.01,***P<0.001
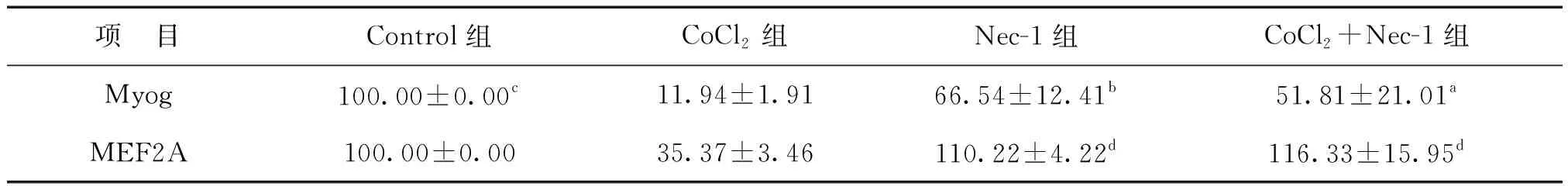
表1 Myog、MEF2A蛋白的相对表达量 %
注:各组Myog总体比较F=26.673,P<0.001,与CoCl2组比较,aP=0.017,bP=0.003,cP<0.001;各组MEF2A总体比较F=58.927,P<0.001,与CoCl2组比较,dP<0.001
三、Nec-1、CoCl2对细胞周期的影响
结果显示,CoCl2组[(12.47±1.06)%]和CoCl2+Nec-1组[18.89±3.52 )%]S期细胞比例均较Control组[(35.69±2.67)%]少(P均<0.001),但CoCl2+Nec-1组较CoCl2组多(P=0.039),见图3。
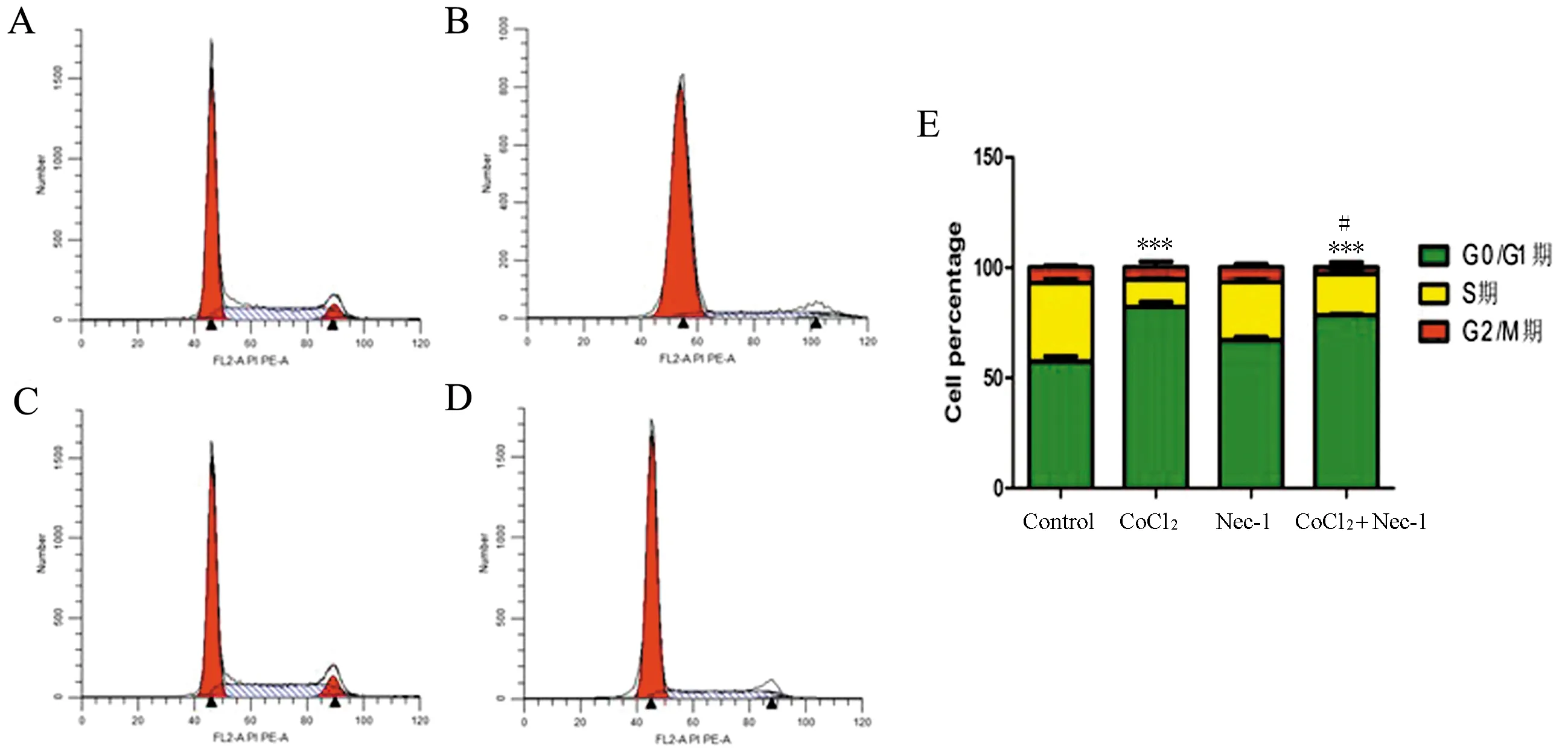
图3 不同处理组的细胞周期
A:Control组;B:CoCl2组;C:Nec-1组;D:CoCl2+Nec-1组;与Control组比较,**P<0.01;与CoCl2组比较,#P<0.05
四、Nec-1、CoCl2对C2C12细胞划痕愈合的影响
实验结果显示,不同处理组的划痕愈合程度不同,见图4。随时间推移,划痕面积逐渐缩小,Control组、Nec-1组及CoCl2+Nec-1组愈合速度较快,在72 h时几乎完全愈合,而CoCl2组愈合速度相对较慢。
实验结果采用单因素方差分析,对比各个时间点不同处理组之间的变化差异。在0 h时,各处理组比较差异无统计学意义(P>0.05);在24、48、72 h时,CoCl2组细胞划痕损伤面积均大于Control组、Nec-1组(P均<0.001);而加入Nec-1处理逆转了CoCl2引起的细胞损伤,CoCl2+Nec-1组划痕损伤面积减小,划痕愈合程度较CoCl2组高(P<0.001),见表2、图5。
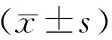
表2 各处理组在不同时间点的划痕损伤面积 μm2

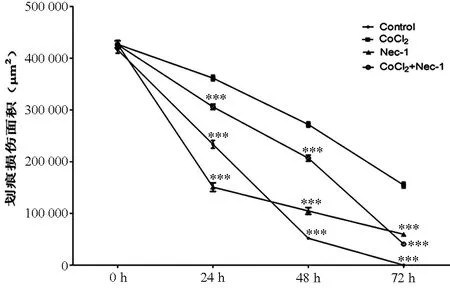
图5 各处理组划痕损伤面积在不同时间的变化
同一时间点与CoCl2组比较, ***P<0.001
讨 论
本研究采用CoCl2模拟低氧环境,观察小鼠C2C12成肌细胞的变化。CoCl2是常用的缺氧模拟化合物,在组织中通过钴离子竞争血红蛋白卟啉环中的铁离子,抑制氧合血红蛋白的形成而丧失与氧结合的能力,在细胞中通过抑制脯氨酰羟化酶的羟化作用,从而诱发一系列类似缺氧反应,在细胞增殖、分化以及损伤应激研究中被广泛应用[7-8]。
通过CoCl2模拟缺氧后,可观察到肌细胞形态学异常,肌细胞的分化标志物Myog和MEF2A表达下调。Myog属于生肌调节因子(MRF)家族成员,具有控制成肌细胞融合的起始,促使成肌细胞增殖,促进单核成肌细胞转变为多核肌纤维的作用,是肌细胞终末分化的决定因素[9]。本课题组的前期研究也显示,MRF的表达对肌细胞的分化、融合有重要的作用[10]。Myog具有碱性螺旋-环-螺旋 (bHLH)结构,MEF2的MADS-box区域可与bHLH相互作用,从而激活Myog的表达,进而实现对骨骼肌发育的调控。本研究结果提示,CoCl2模拟缺氧可抑制肌细胞的分化。
缺氧可使多种细胞生长停滞,并使其代谢、功能和形态结构发生异常变化,并出现凋亡、坏死、自噬、程序性坏死等[7-8, 11]。本研究结果显示,CoCl2诱导可导致细胞周期阻滞,划痕损伤修复能力减弱,推测缺氧对细胞增殖有抑制作用。此外,亦有文献报道,短时间或低剂量的缺氧环境可激活细胞应激保护机制,上调血管内皮生长因子(VEGF)、转化生长因子-β1(TGF-β1)等因子的表达量,减少细胞凋亡、加速细胞增殖分化,促进修复[12-13]。
近年来,程序性坏死是细胞死亡领域新的研究热点,具有坏死的细胞形态特点和自噬的活化,主动耗损能量,且能被一系列信号传导通路高度调控[14]。有研究表明,CoCl2诱导缺氧能使程序性坏死活化[15-16]。Nec-1是程序性坏死的特异性抑制剂,文献报道Nec-1可改善缺血缺氧损伤,通过抑制程序性坏死对缺血缺氧模型的脑、肝、心肌组织具有保护作用,减少病理损伤,促进组织的损伤修复,对临床治疗指导意义重大[14, 17-19]。本研究结果显示,与CoCl2处理组相比,加入Nec-1干预能使细胞形态恢复正常,Myog、MEF2A蛋白表达水平上调,S期细胞比例上升,划痕实验后的损伤面积修复能力改善,说明Nec-1在缺氧条件下对骨骼肌细胞增殖分化有保护作用。由此推测,Nec-1可能通过抑制肌细胞程序性坏死的发生,从而逆转缺氧状态对细胞增殖分化的损害。
综上所述,CoCl2模拟缺氧可诱导肌细胞损伤,抑制其增殖、分化功能,Nec-1对缺氧条件下的肌细胞损伤修复有保护作用,可能通过抑制程序性坏死来促进肌细胞的损伤修复。然而,本研究仅验证了Nec-1对化学诱导缺氧下的骨骼肌细胞具有保护作用,缺乏对物理缺氧模型的研究,未来将在后续的研究中进一步探讨其在物理缺氧的体内外模型的作用,研究Nec-1的药理作用及机制,为肌组织缺氧损伤相关疾病的治疗提供理论依据。
[1] Kawamura I, Takemura G, Kanamori H, Takeyama T, Kawaguchi T, Tsujimoto A, Goto K, Maruyama R, Watanabe T, Shiraki T, Aoyama T, Fujiwara T, Fujiwara H, Minatoguchi S. Repeated phlebotomy augments angiogenesis to improve blood flow in murine ischemic legs. Am J Physiol Heart Circ Physiol, 2010,299(2):H372-H378.
[2] 叶伟凤, 陈亮, 熊敏, 付晓燕, 汪建. 不同缺氧方式对大鼠缺氧诱导因子-1α及脑源性神经营养因子的表达和认知功能影响. 医学研究生学报, 2017,30(6):569-573.
[3] Degterev A, Huang Z, Boyce M, Li Y, Jagtap P, Mizushima N, Cuny GD, Mitchison TJ, Moskowitz MA, Yuan J. Chemical inhibitor of nonapoptotic cell death with therapeutic potential for ischemic brain injury. Nat Chem Biol, 2005,1(2):112-119.
[4] 米明珊, 鲍剑峰, 许勇, 张伟波, 杜鹏, 彭兴国, 任磊. 程序性坏死特异性抑制剂-1促进大鼠脊髓损伤修复的研究. 中华实验外科杂志, 2015,32(9):2214-2216.
[5] 支中文,杨龙,杜波,周延龙,耿德勤,程言博. Necrostatin-1对大鼠脑缺血再灌注损伤后小胶质细胞和炎症因子的影响. 中华神经医学杂志, 2015,14(8):757-763.
[6] 欧阳资章, 刘晓萍, 江晟, 钟志华, 肖诚胤, 邓惠容. Nec-1对于环孢素A导致的细胞毒性的保护作用与机制研究. 中国生化药物杂志, 2017,11(7):1005-1678.
[7] Mohamed AS, Hanafi NI, Sheikh Abdul Kadir SH, Md Noor J, Abdul Hamid Hasani N, Ab Rahim S, Siran R. Ursodeoxycholic acid protects cardiomyocytes against cobalt chloride induced hypoxia by regulating transcriptional mediator of cells stress hypoxia inducible factor 1α and p53 protein. Cell Biochem Funct, 2017,35(7):453-463.
[8] He F, Wu Q, Xu B, Wang X, Wu J, Huang L, Cheng J. Suppression of Stim1 reduced intracellular calcium concentration and attenuated hypoxia/reoxygenation induced apoptosis in H9C2 cells. Biosci Rep, 2017,37(6):R20171249.
[9] 李硕, 郝斐, 吴海青, 毕兆伟, 张志鹏, 刘东军, 仓明. 山羊MyoG启动子的克隆和活性检测. 中国农业科学, 2014,47(5):984-994.
[10] 陈睿, 佘燕玲, 周珊瑶, 史华彩, 黎程. TNF-α与ERK1/2在心脏毒素诱导的肌损伤再生修复中的作用研究. 新医学, 2016,47(4):231-236.
[11] Chen R, Jiang T, She Y, Xu J, Li C, Zhou S, Shen H, Shi H, Liu S. Effects of cobalt chloride, a hypoxia-mimetic agent, on autophagy and atrophy in skeletal C2C12 myotubes. Biomed Res Int, 2017,2017:7097580.
[12] Akeno N, Czyzyk-Krzeska MF, Gross TS, Clemens TL. Hypoxia induces vascular endothelial growth factor gene transcription in human osteoblast-like cells through the hypoxia-inducible factor-2alpha. Endocrinology, 2001,142(2):959-962.
[13] 孙崇毅, 姚猛, 刘庆鹏, 吉光荣, 王岩松. 缺氧培养对大鼠神经干细胞体外增殖影响及其机制的研究. 现代生物医学进展, 2006,6(11):18-19.
[14] Yang R, Hu K, Chen J, Zhu S, Li L, Lu H, Li P, Dong R. Necrostatin-1 protects hippocampal neurons against ischemia/reperfusion injury via the RIP3/DAXX signaling pathway in rats. Neurosci Lett, 2017,651:207-215.
[15] Wang HY, Zhang B. Cobalt chloride induces necroptosis in human colon cancer HT-29 cells. Asian Pac J Cancer Prev, 2015,16(6):2569-2574.
[16] Rovetta F, Stacchiotti A, Faggi F, Catalani S, Apostoli P, Fanzani A, Aleo MF. Cobalt triggers necrotic cell death and atrophy in skeletal C2C12 myotubes. Toxicol Appl Pharmacol, 2013,271(2):196-205.
[17] Ito K, Eguchi Y, Imagawa Y, Akai S, Mochizuki H, Tsujimoto Y. MPP+ induces necrostatin-1- and ferrostatin-1-sensitive necrotic death of neuronal SH-SY5Y cells. Cell Death Discov, 2017,3:17013.
[18] Kim SJ, Lee SM. Necrostatin-1 protects against D-galactosamine and lipopolysaccharide-induced hepatic injury by preventing TLR4 and RAGE signaling. Inflammation,2017,40(6):1912-1923.
[19] Geng F, Yin H, Li Z, Li Q, He C, Wang Z, Yu J. Quantitative analysis of necrostatin-1, a necroptosis inhibitor by LC-MS/MS and the study of its pharmacokinetics and bioavailability. Biomed Pharmacother,2017,95:1479-1485.
