我院612例药物不良反应不同民族分析
2018-06-26
云南省玉溪市人民医院药学部,云南 玉溪 653100
我国自2001年12月1日开始按照《药品管理法》实行的不良反应(ADR)报告制度,使ADR检测工作在我国逐渐深入开展,引起普遍关注。药物不良反应的发生受多种因素影响,研究显示,不同的种族背景,是导致药物不良反应事件的一个重要因素。云南省玉溪市为多民族聚集地区,分布有汉、彝、哈尼、傣、回等多个民族。目前我国有关ADR在不同种族人群的研究较少。本文拟就我院2017年度612例包含不同民族的ADR进行回顾性分析,以为不同民族患者的临床合理用药提供参考。
1 资料与方法
收集我院2014年1月至2017年12月发现的ADR 612例,分别依据患者的民族将ADR类型、患者的性别与年龄、给药途径、药品种类以及ADR所累积部位的进程统计分析,数据以(n/x%)形式表示,n代表ADR的绝对人数,x%代表ADR人数占本民族总ADR人数的百分比。
2 结果
2.1各民族ADR患者的性别年龄分布 612例ADR中,汉、彝、哈尼、傣、回和其他民族ADR人数分别为410、113、30、24、25和11例。其中汉族占总ADR人数的67.0%,居于主要地位。各民族发生ADR的性别年龄分布见表1。整个ADR人群男性略多于女性,比例为1.10∶1,但是各民族的亚组分析显示彝族和回族的ADR发生率却是女性高于男性,男女比例分别为0.95∶1与0.78∶1。ADR人群的年龄从8个月至92岁不等,从总ADR人群的统计结果看,年龄在18~60岁的ADR发生率比较高,占58.6%,各民族亚组的统计结果也显示18~60岁为ADR高发的年龄段。
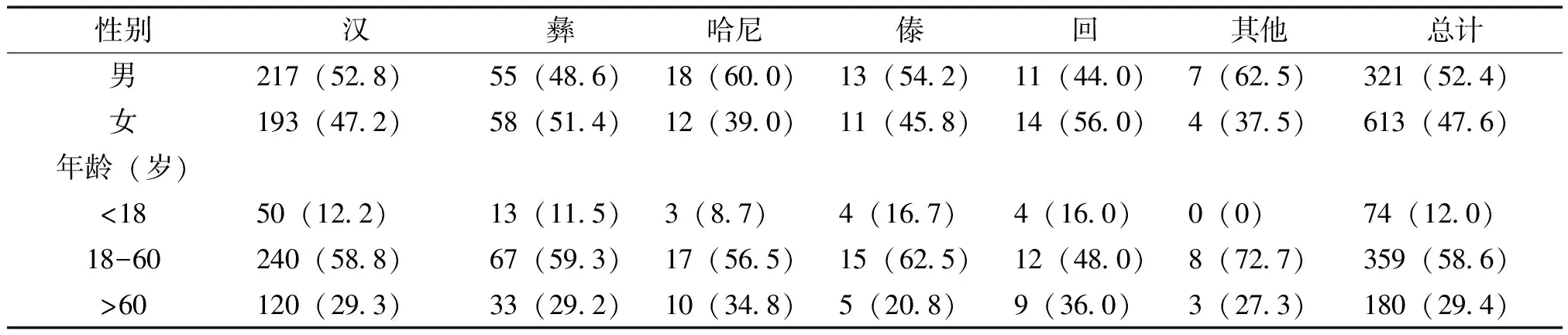
表1 各民族发生ADR的性别和年龄分布 [例(%)]
2.2 各民族ADR患者用药情况
2.2.1 用药途径:在612例ADR患者中静脉给药(包括静脉滴注和静脉推注)方式引发的ADR最多,达332例(占54.2%);其次为口服给药,为135例(占22.0%)[1],亚组分析则显示静脉给药所致ADR的发生率在汉、哈尼、傣、回和其他名族分别为52.4%、54.8%、65.2%、66.7%、52.0%和87.5%,均占据主要地位。引发ADR的给药途径分布见表2。
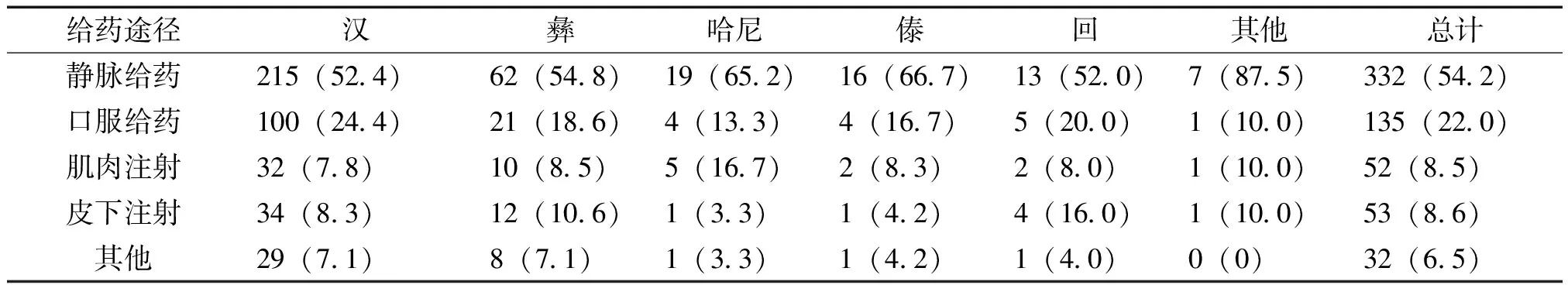
表2 各民族引发ADR的给药途径分布
2.2.2 ADR涉及的药品种类:612例ADR共涉及药品17大类近350个品种,其中抗感染药所占比例最大,达到50.4%,其次是抗肿瘤药,占18.9%[2]。亚组分析的结果则显示各民族所致ADR的药物占比首位的均是抗感染药物,在汉、彝、哈尼、傣、回和其他名族所致的ADR比例分别为49.0%、57.5%、43.3%、66.7%、44.0%和40.0%,引发ADR的药品种类及发生率见表3。

表3 各民族引发ADR的药物种类途径分布
2.3 各民族ADR所累及器官的分布 612例ADR涉及的器官或系统主要临床表现为皮肤及其附件、消化系统、循环系统等方面,其中皮肤及其附件损害最为常见[3],占总例数的46.2%,其在汉、彝、哈尼、傣、回和其他各民族ADR所累及器官中均占首位,比例分别为42.7%、55.8%、56.7%、37.5%、48.0%和75%,ADR涉及的器官或系统分类及临床表现见表4.
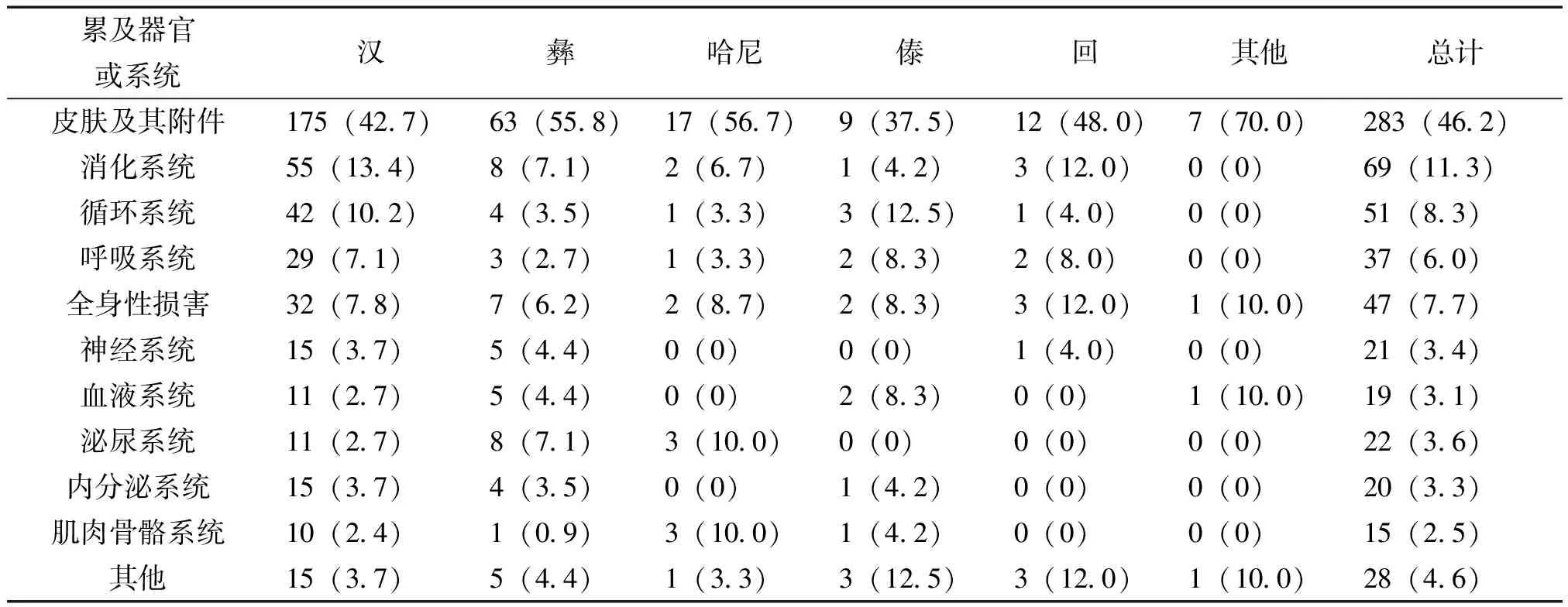
表4 各民族ADR涉及的器官或系统分类
2.4 各民族ADR的分级 ADR级别分为一般和严重,本组资料中,比较严重的病例有30例(占4.9%),其中汉族20例(占4.9%),彝族7例(占6.2%),回族3例(占12.0%),其他民族则未见严重ADR病例;引起较严重ADR的药物主要是抗感染药物;一般的有582例,占95.1%。引起严重ADR的临床表现主要为过敏性休克、大疱性表皮坏死性松懈型药疹和药物性肝损害等。各民族ADR的程度分级情况见表5。

表5 各民族ADR程度分级
3 讨论
由表1可知,ADR发生于汉族人群的比例较大,占67.0%,其次分别为彝族、哈尼族、回族与傣族,ADR人群的民族构成比与本地区的各民族的人口构成具有相关性,云南省玉溪市汉族人口占69.3%,占据主体地位,其余人口较多的民族分别是彝族占17.6%,哈尼族占4.7%,傣族占4.0%,回族占3.7%,其余民族共占0.7%。612例ADR中,除彝族和回族的ADR发生率女性高于男性外,其他各民族均是男性略多于女性,具体原因有待于进一步的研究。在ADR发生的年龄段分布方面,无论总体还是在各民族亚组均表现为18~60岁年龄段ADR发生率最高[4],大于60岁的发生率则紧随其次,18~60岁的高发率可能与该年龄段人群压力较大、处于亚健康状态比例较高,而导致患病率增加,用药机会加大。而老年患者则一般由于身患多种疾病,生理机能衰老退化,用药种类多,易影响药动学及药效学,因此用药不良反应发生率上升[5]。
在总的ADR群体中,静脉给药引发的ADR最高(占54.2%),其次是口服给药(占22.0%),其他给药途径引发的ADR较少。在给药途径所致的ADR方面,给民族亚组的分析未见明显与总体的差别,静脉给药与口服给药所致ADR均占主导地位。其原因在于静脉给药使药物直接进入血液循环,血药浓度较高,易发生ADR;其次药液的PH值、不溶性微粒、输液器的环氧乙烷残留等因素都可能成为发生ADR的诱因[6]。因此,临床上应按照世界卫生组织(WHO)倡导的合理用药原则,根据患者的病情选择适宜的给药方式,能够口服的不注射;或者采用抗菌药物的“序贯疗法”,当患者病情一旦改善,迅速由静脉给药改为口服给药,尽量减少静脉给药的机会和次数,避免严重ADR的发生。口服给药所致ADR发生率较高,因此在选择口服药物的时候一定要遵循安全有效的原则,根据患者自身的病理和生理情况,选择合理的药物及给药途径[7-8]。
本组612例ADR共涉及药品17大类近350个品种,其中抗感染药所占比例最大(占50.4%),各民族亚组分析显示在彝族和傣族抗感染药所致ADR均超过一半[9-10],分别达到57.5%和66.7%,而在汉族则占49.0%,其余各民族也均占主要地位。该情况可能与临床上在抗感染药的使用中存在一些不合理用药情况有关,进而造成抗感染药的ADR增多,因此,应加强抗菌药物管理,遵循《抗菌药物临床应用指导原则》[11],提高合理用药水平,以减少抗菌药物ADR的发生。在总ADR人群与各民族亚组ADR人群中,其他导致ADR的药物主要为抗肿瘤药(占总ADR人数的18.9%)与中药制剂(占总人数的10.8%)。抗肿瘤药由于本身存在的细胞毒作用,因此其不良反应基本无法避免,近年随着肿瘤发病率的上升,其不良反应也呈现上升的趋势。中药制剂绝大多数为复方制剂,成分复杂,少数杂质难以去除。中药制剂尤其是注射剂的质量难以控制,与其它药物配伍后极易发生ADR[12]。
在总的ADR研究人群中,ADR最常累及的器官是皮肤及其附件,其发生率达到46.2%,其中哈尼族患者的累及率最高,达56.7%,其次为彝族和回族,分别为55.8%和48.0%,汉族则占42.7%,皮肤反应发生率较高的原因可能是皮肤反应的临床表现易于观察和诊断,且不易与其他疾病相混淆,而且临床上的一些常见药物如抗感染药等抗原性较强,易引起这类反应。其他最常累及器官分别为消化系统(占总ADR人数的11.3%)与循环系统(占总ADR人数的8.3%)[2]。各民族ADR的严重程度均以一般为主,严重的ADR事件占总人数的4.9%,与国内外的报道基本一致。各民族亚组分析显示除回族外,各民族亚组的ADR事件均在6%以下,而回族则有10.5%,其原因有待进一步分析。
总之,ADR的发生与药物自身特性、患者体质、临床给药途径等多种因素有关,而中老年患者ADR发生率较高,患者的民族因素影响较小,但回族人群的ADR事件发生率较高。基于以上情况,对于中老年ADR发生率较高的患者,临床应作为重点监测对象,应加强抗感染药、抗肿瘤药和中药制剂的合理使用。对于ADR发生率较高的回族人群,也应建立重点检测,由于此次研究中回族人群的样本量偏小,呼吁其它医疗机构也重视对回族ADR事件的关注,以减少ADR事件发生率。
开展ADR监测工作是医疗机构的一项重要任务,尤其是医务人员在其中起着举足轻重的作用,必须加大ADR监测力度,促进其全面开展,确保临床用药安全、有效、经济。
[1]乔逸,恽艳琴,徐焕春,等.我院2012-2015年997例药品不良反应报告分析[J].中国药物应用与监测,2017,14(1):34-36.
[2]缴万里,王云松,刘海净.药品不良反应报告分析与预防措施研究[J].中华医院感学杂志,2015,25(2):357-359.
[3]曲彩红,张永明,朱洁明,等.76例严重药品不良反应报告分析[J].中国医院药学杂志,2014,34(12):1031-1034.
[4]李梅,曹玉莹,张华吉,等.基于本体的国内抗感染药物不良反应报告分析[J].药物流行病学杂志,2017,26(2):115-119.
[5]杜望春,杨涛,高宁周,等.老年人药品不良反应的监测和预防[J].药物流行病学杂志,2014,23(6):385-388.
[6] 雍小兰,曾仁杰,张勤.静脉输液相关的不良反应及其原因[J].药物不良反应杂志,2004,6(3):161-163.
[7] 张燕荣,甑健存.依据《药品不良反应信息通报》探讨避免药品不良反应发生的措施[J].中国医院药学杂志,2015,35(2):612-160.
[8]吴国海,郭蓉,陈璐,等.药物不良反应326例报告分析[J].解放军药学学报,2017,33(1):99-101.
[9]李梅,曹玉莹,张华吉,等.基于本体的国内抗感染药物不良反应报告分析[J].药物流行病学杂志,2017,26(2):115-119.
[10]董迪,崔蔚,陈宁,等.我院头孢菌素相关用药安全问题分析[J].中国药师,2017,20(1):121-123.
[11]《抗菌药物临床应用指导原则》修订工作组.抗菌药物临床应用指导原则[M].2015年版.北京:人民卫生出版社,2015:26.
[12]赵启邹,王青,聂彩霞,等.124例中药注射液致不良反应报告[J].中国医院用药评价与分析,2017,17(1):114-118.
