经颅直流电刺激治疗卒中后吞咽困难的系统评价
2018-06-22陈亮陈洁张茹芳李兴贵展群岭
陈亮,陈洁,张茹芳,李兴贵,展群岭
1.重庆市第五人民医院,a.神经内科;b.医务科;c.检验科,重庆市400062
吞咽困难是卒中后常见的并发症,在脑卒中患者中的发生率达20%~81%[1]。卒中后吞咽困难可导致严重并发症,如脱水、营养不良和吸入性肺炎,从而造成脑卒中患者病死率增加[2]。对于卒中后吞咽困难的治疗缺乏有效药物,而传统康复训练的疗效亦有限[3]。
经颅直流电刺激(transcranial direct current stimulation,tDCS)是一种通过阳性和阴性电极在头皮特定位点施加微弱电流,调节大脑皮质兴奋性的非侵袭性技术,具有便携、易用和低成本的特点[4]。2009年,Jefferson等[5]发现阳极tDCS能够刺激咽运动皮质,以增加强度的方式增加咽部的兴奋性。2011年,Kumar等[6]发现阳极tDCS能够显著改善亚急性脑卒中患者的吞咽功能。最近的一项关于tDCS的系统评价[7]分析表明,tDCS能够改善卒中后吞咽困难患者的吞咽功能,但是该研究并没有进行定量分析。
本研究通过Meta分析的方法,对运用tDCS治疗卒中后吞咽困难的随机对照试验进行系统评价,为临床治疗卒中后吞咽困难提供新的证据。
1 资料与方法
1.1 一般资料
1.1.1 纳入标准
①tDCS治疗脑卒中后吞咽困难的随机对照试验(randomized controlled trials,RCTs);②研究对象为缺血性或出血性脑卒中并发吞咽困难,并经CT或MRI证实,吞咽困难符合电视透视吞咽功能检查(video fluoroscopy swallowing study,VFSS)及洼田饮水试验评分判断标准。
1.1.2 排除标准
①非随机对照试验;②受试者的吞咽困难是其他神经肌肉疾病所致,如帕金森病等;③非公开发表的文献,如会议论文等;④非英文或中文发表的文献;⑤重复发表的文献。
1.1.3 干预措施
试验组为tDCS治疗;对照组为假刺激或其他康复治疗方案(如电针等)。
1.1.4 结局指标
吞咽功能改善程度指标:①吞咽困难的疗效和严重程度量表(Dysphagia Outcome Severity Scale,DOSS),共7分,1分最严重,7分正常;②功能性吞咽困难量表(Functional Dysphagia Scale,FDS),共100分,0分正常,100分最严重;③改良曼恩吞咽能力评分(modified Mann Assessment of Swallowing Ability,MMASA),共100分,0分最严重,100分正常;④纤维光学内镜吞咽评估量表(Fiberoptic Endoscopic Dysphagia Severity Scale,FEDSS),共6分,1分正常,6分最严重;⑤才藤氏7级评估法,共6分,0分最严重,6分正常。
安全性指标:不良事件。
1.2 检索策略
选择计算机检索Medline、EMΒASE、Cochrane Library(CENTRAL)、中国生物医学文献数据库(CΒMdisc)、维普中文科技期刊数据库(VIP)、中国知网(CNKI)以及万方数字化期刊全文数据库。检索时间为建库至2018年2月,纳入文献语种限制为英文和中文。
以CΒMdisc为例,中文检索策略为:
#1脑血管病OR脑卒中OR脑梗死OR卒中OR脑出血OR蛛网膜下腔出血
#2直流电刺激OR经颅直流电刺激ORDCS
#3吞咽障碍OR吞咽困难OR吞咽功能障碍
#4(#1)AND(#2)AND(#3)
以CENTRAL数据库为例,英文检索策略为:
#1 cerebrovascular disorders/or exp basal ganglia cerebrovascular disease/or exp brain ischemia/or exp carotid artery diseases/or exp intracranial arterial diseases/or exp"intracranial embolism and thrombosis"/or exp intracranial hemorrhages/or stroke/or exp brain infarction/or vertebral artery dissection/
#2(stroke or poststroke or post-stroke or cerebrovasc$or brain vasc$or cerebral vasc$or cva$or apoplex$or SAH).tw.
#3((brain$or cerebr$or cerebell$or intracran$or intracerebral)adj5(isch?emi$or infarct$or thrombo$or emboli$or occlus$)).tw.
#4((brain$or cerebr$or cerebell$or intracerebral or intracranial or subarachnoid)adj5(haemorrhage$or hemorrhage$or haematoma$or hematoma$or bleed$)).tw.
#5 hemiplegia/or exp paresis/
#6(hemipleg$or hemipar$or paresis or paretic or hemineglect or hemi-neglect or((unilateral or spatial or hemi?spatial or visual)adj5 neglect)).tw.
#7 or/1-6
#8(transcranial adj5 direct current adj5 stimulation).tw.
#9(transcranial adj5 DCadj5 stimulation).tw.
#10(transcranial adj5 electric$adj5 stimulation).tw.
#11(tDCSor A-tDCSor C-tDCSor S-tDCS).tw.
#12 Transcranial direct current stimulation/
#13 8 or 9 or 10 or 11 or 12
#14 exp deglutition disorders/
#15(Dysphagi$or(swallow$or deglutition$)).tw.
#16 14 or 15
#17 7 and 13 and 16
1.3 文献筛选、资料提取以及质量评价
由2名评价员独立进行文献筛选和资料提取,然后交叉核对结果,如有分歧由第三位研究者协助解决。资料提取内容包括研究作者、研究发表时间、发表国家、偏倚风险评价的关键要素、纳入样本的基本信息(年龄、性别)、干预措施、tDCS治疗的要素(刺激电流、时间以及部位)、相关结局指标信息等。采用改良Jadad量表对纳入文献进行质量评价,主要评估内容包括随机序列的产生、随机化隐藏、盲法、撤出与退出,评分1~3分为低质量,评分4~7分为高质量,如有分歧则由第三位研究者协助解决。
1.4 偏倚风险评价
采用Cochrane协作网推荐的系统评价员手册对纳入研究进行偏倚风险检测,主要内容包括:①随机序列的产生;②隐蔽分组;③对研究对象及干预实施者采取盲法;④对结果测评者采取盲法;⑤对结局指标数据的完整性(失访情况)报告偏倚;⑥选择性报告研究结果的可能性;⑦其他方面的偏倚(基线可比性等)。
偏倚风险程度分为低偏倚风险、高偏倚风险及风险程度不明(文献未提供足以进行分析的信息)。
1.5 统计学分析
采用RevMan5.3软件进行统计分析。由于纳入研究结局指标不是相同量表,因此采用标准化均数差(standard mean difference,SMD)作为合并效应量进行Meta分析。采用χ2检验分析各研究之间的异质性,同时结合I2定量判断异质性的大小,I2≤25%提示异质性小,25%<~50%,考虑存在中等程度异质性,I2>50%提示异质性程度高。若各研究异质性小,则采用固定效应模型进行Meta分析;若各研究间存在中等程度以上异质性,则采用随机效应模型进行Meta分析,并分析异质性来源,必要时采用亚组分析或敏感性分析等方法进行处理。Meta分析的检验水准设为α=0.05。
2 结果
2.1 文献检索流程与结果
共检索出文献78篇,通过除去重复文献和阅读标题摘要后获得文献23篇,阅读全文后最终纳入文献8篇[6,8-14]。各数据库文献检索结果和筛选流程结果见图1。
2.2 纳入文献特征
纳入的8篇文献中,中国研究3项,韩国研究2项,美国、日本和德国的研究各1项;纳入研究发表的时间为2011年至2018年,共225例患者。3项研究[6,9-10]纳入病例全部为缺血性脑卒中,4项研究[8,11-13]纳入病例为脑出血和脑梗死,1项研究[14]未报道纳入研究的具体诊断;2项研究[6,9]纳入病例的卒中发病时间<1个月,6项研究[8,10-14]纳入病例的卒中发病时间≥1个月;6项研究[6,8-11,13]的对照组采用假刺激,2项研究[12,14]未采用假刺激;3项研究[6,9,11]tDCS刺激部位为健侧,3项研究[8,10,14]tDCS的刺激部位为患侧,1项研究[12]既报道健侧刺激的结果,也报道患侧刺激研究的结果;1项研究[13]采用双侧刺激(纳入卒中类型为小脑卒中)。
所有纳入研究均采用阳极tDCS。纳入研究详细一般特征见表1。采用改良Jadad量表对纳入研究进行评价,所有纳入研究的改良Jadad量表评分≥4分,均为高质量研究。纳入研究详细质量评价见表2。
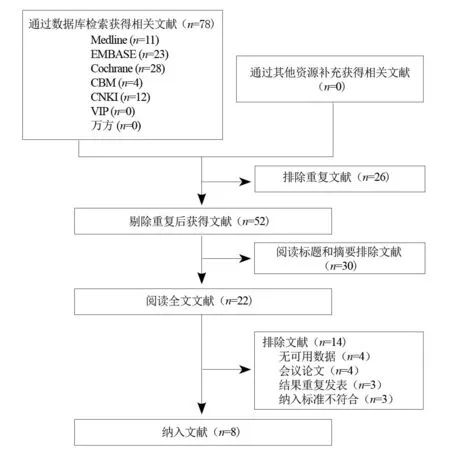
图1 文献检索以及筛选流程与结果
2.3 偏倚风险检测
所有纳入研究中,7项研究[6,8-11,13-14]采用随机数字表法,1项研究[12]采用抽签法;1项研究[9]采用隐蔽分组,其他研究均没有报道使用隐蔽分组情况;5项研究[6,8-11]采用盲法,其中3项研究[6,9,11]采用双盲,2项研究[8,10]采用单盲,3项研究[12-14]未报道盲法使用情况;所有研究均对结局数据的完整性进行说明;所有纳入研究均没有出现选择性报道情况;所有纳入研究的病例入组时基线水平基本一致。纳入研究的偏倚风险研究结果和各偏倚所占百分比分别见图2和图3。
2.4 tDCS治疗卒中后吞咽障碍的效果评价
2.4.1 DOSS
3项研究[6,8,11]运用DOSS评价吞咽功能,异质性检验显示纳入研究异质性小(I2=0%,P=0.62),采用固定效应模型,合并效应量SMD=0.61,95%CI:0.09~1.13,P=0.02,差异有统计学意义;同时采用随机效应模型进行敏感性分析,合并效应量为SMD=0.61,95%CI:0.09~1.13,P=0.02。森林图中菱形表示合并SMD的95%CI,位于无效线的右侧(图4),提示tDCS改善DOSS评分优于对照组。
2.4.2 MMASA
2项研究[12-13]运用MMASA评价吞咽功能,其中一项研究为三臂研究,异质性检验提示纳入研究存在中等程度异质性(I2=48%,P=0.14),采用随机效应模型,合 并 效 应 量 SMD=0.70, 95%CI:-0.08~1.48, P=0.08,差异无统计学意义,森林图中菱形与无效线相交(图4),提示tDCS改善MMASA评分与对照组无差异。
2.4.3 FEDSS
1项研究[9]运用FEDSS评价吞咽功能,效应量SMD=0.99,95%CI:0.44~1.53,P=0.0004,差异有统计学意义,森林图中菱形位于无效线的右侧(图4),提示tDCS改善FEDSS优于对照组。
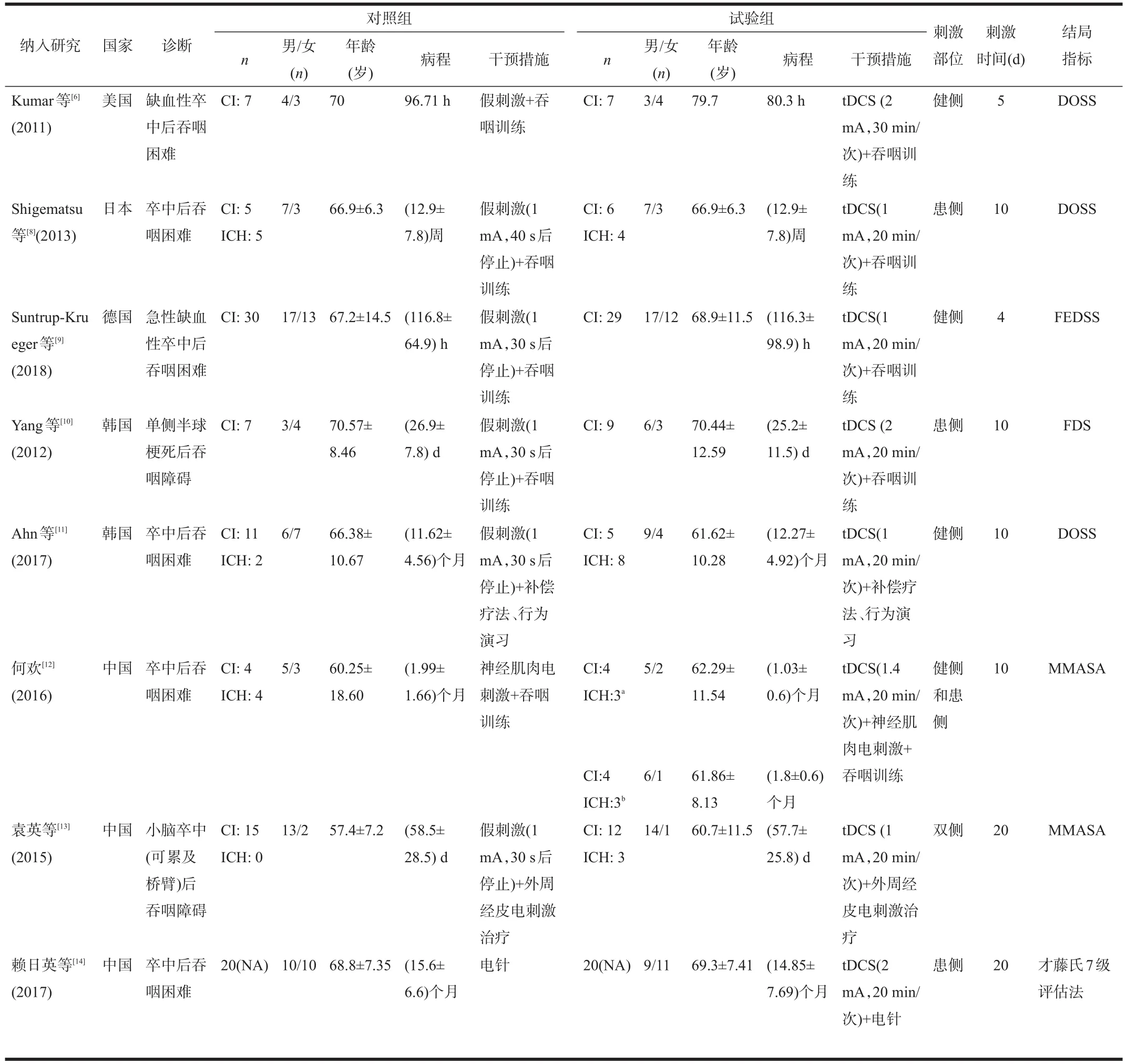
表1 纳入研究基本特征和质量评价
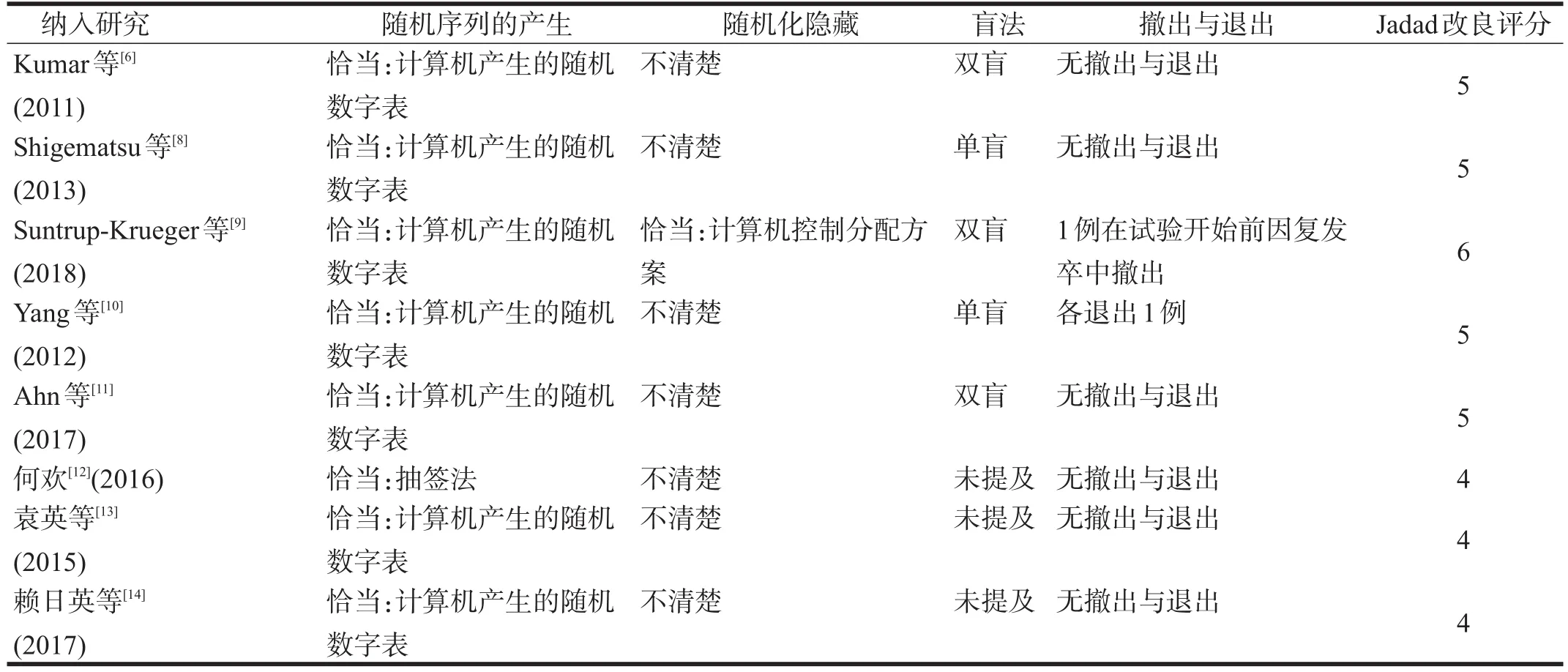
表2 纳入研究质量评估结果
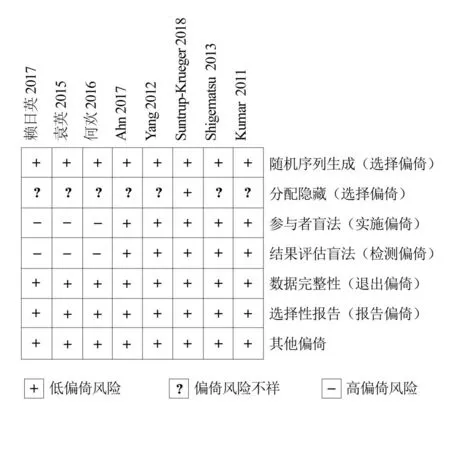
图2 纳入研究的偏倚风险项目判断
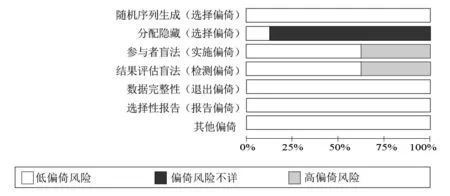
图3 纳入研究偏倚风险项目百分比
2.4.4 FDS
1项研究[10]运用FDS评价吞咽功能,效应量SMD=-0.59,95%CI:-1.68~0.50,P=0.29,差异无统计学意义,森林图中菱形与无效线相交(图4),提示tDCS改善FDS评分与对照组无差异。
2.4.5 才藤氏7级评估法
1项研究[14]运用才藤氏7级评估法评价吞咽功能,效应量 SMD=0.70,95%CI:-0.08~1.48,P<0.0001,差异有统计学意义,森林图中菱形在无效线右侧(图4),提示tDCS改善该评估法评分优于对照组。
2.4.6 总效应量
对所有纳入研究的结局指标做合并分析,异质性检验显示纳入研究存在中等程度异质性(I2=47%,P=0.06),采用随机效应模型,合并效应量SMD=0.71,95%CI:0.32~1.10,P=0.0004,差异有统计学意义,森林图中菱形位于无效线右侧(图4),提示tDCS改善卒中后吞咽障碍患者的吞咽功能优于对照组。
2.5 亚组分析
由于纳入研究间存在中等程度异质性(I2=47%,P=0.06),并且结局指标的效应量与总效应量不一致,故对纳入研究按照卒中发病时间和tDCS刺激部位分别进行亚组分析。
2.5.1 根据卒中发病时间分析
2项研究[6,9]纳入病例的卒中发病时间<1月,采用随机效应模型,合并效应量SMD=0.96,95%CI:0.47~1.45,P=0.0001,差异有统计学意义,森林图中菱形位于无效线的右侧(图5),提示tDCS改善急性卒中后吞咽障碍患者的吞咽功能优于对照组。6项研究[8,10-14]纳入病例的卒中发病≥1个月,采用随机效应模型,合并效应量 SMD=0.63,95%CI:0.11~1.14,P=0.02,差异有统计学意义,森林图中菱形位于无效线的右侧(图5),提示tDCS改善卒中恢复期患者的吞咽功能优于对照组。
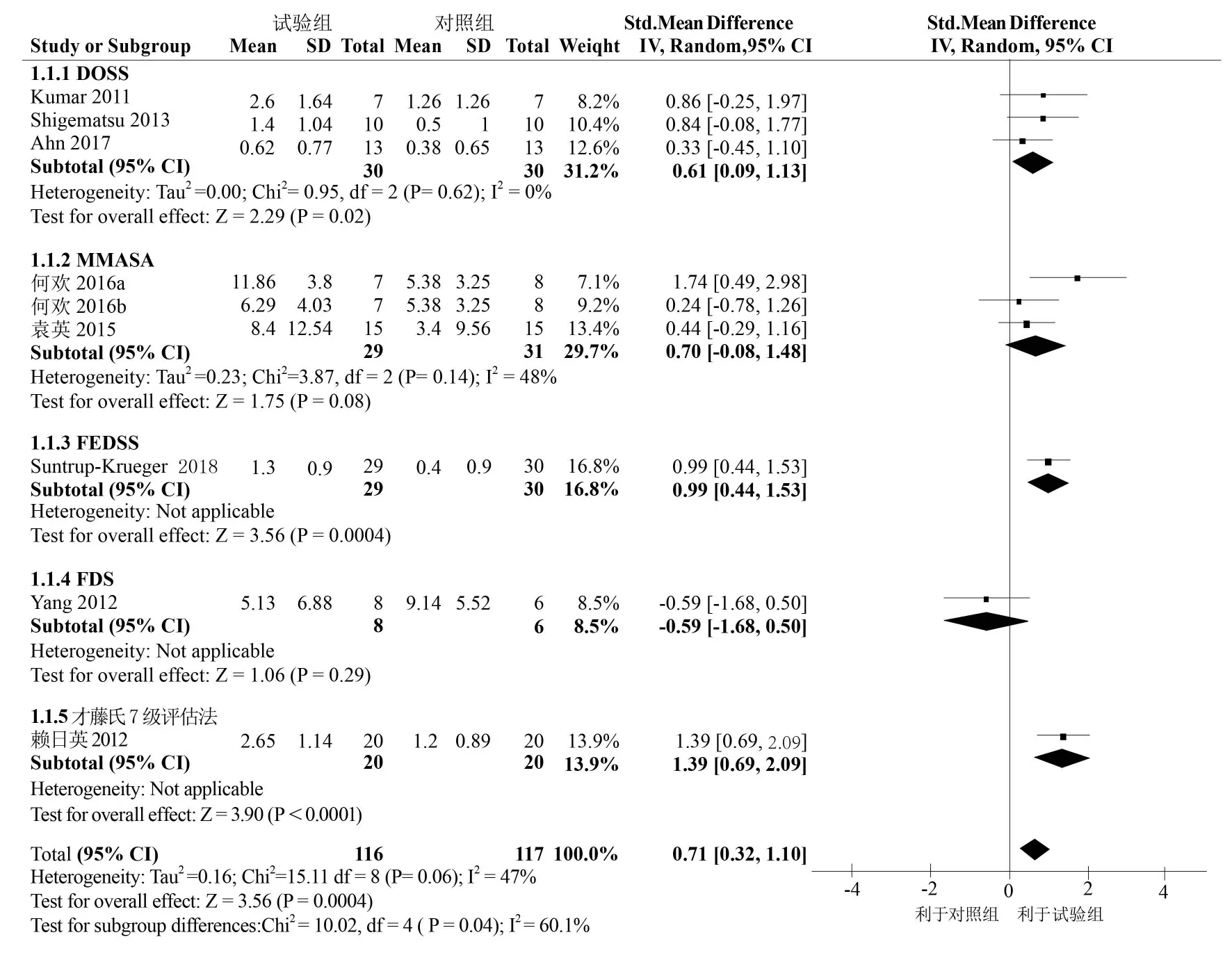
图4 两组治疗后吞咽功能评分改善的Meta分析森林图
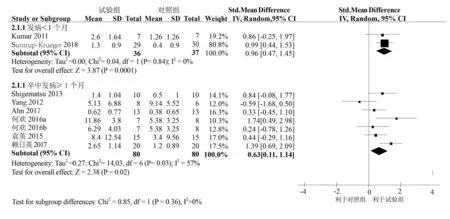
图5 根据卒中发病时间的亚组分析森林图
2.5.2 根据tDCS刺激部位分析
4项研究[6,9,11-12]tDCS刺激部位为健侧,采用随机效应模型,合并效应量SMD=0.88,95%CI:0.40~1.36,P=0.0003,差异有统计学意义,森林图中菱形位于无效线的右侧(图6),提示tDCS健侧刺激的吞咽功能改善程度优于对照组。4项研究[8,10,12,14]tDCS刺激部位为患侧,采用随机效应模型,合并效应量SMD=0.54,95%CI:-0.30~1.38,P=0.21,差异无统计学意义,森林图中菱形位与无效线相交(图6),提示tDCS健侧刺激的吞咽功能改善与对照组无差异。
2.6 安全性
2项研究[6,12]报道tDCS治疗开始时电极放置位置有轻微刺痛,但是均无严重不良事件发生。所有研究均没有因tDCS治疗出现的脱落病例,详细见表3。
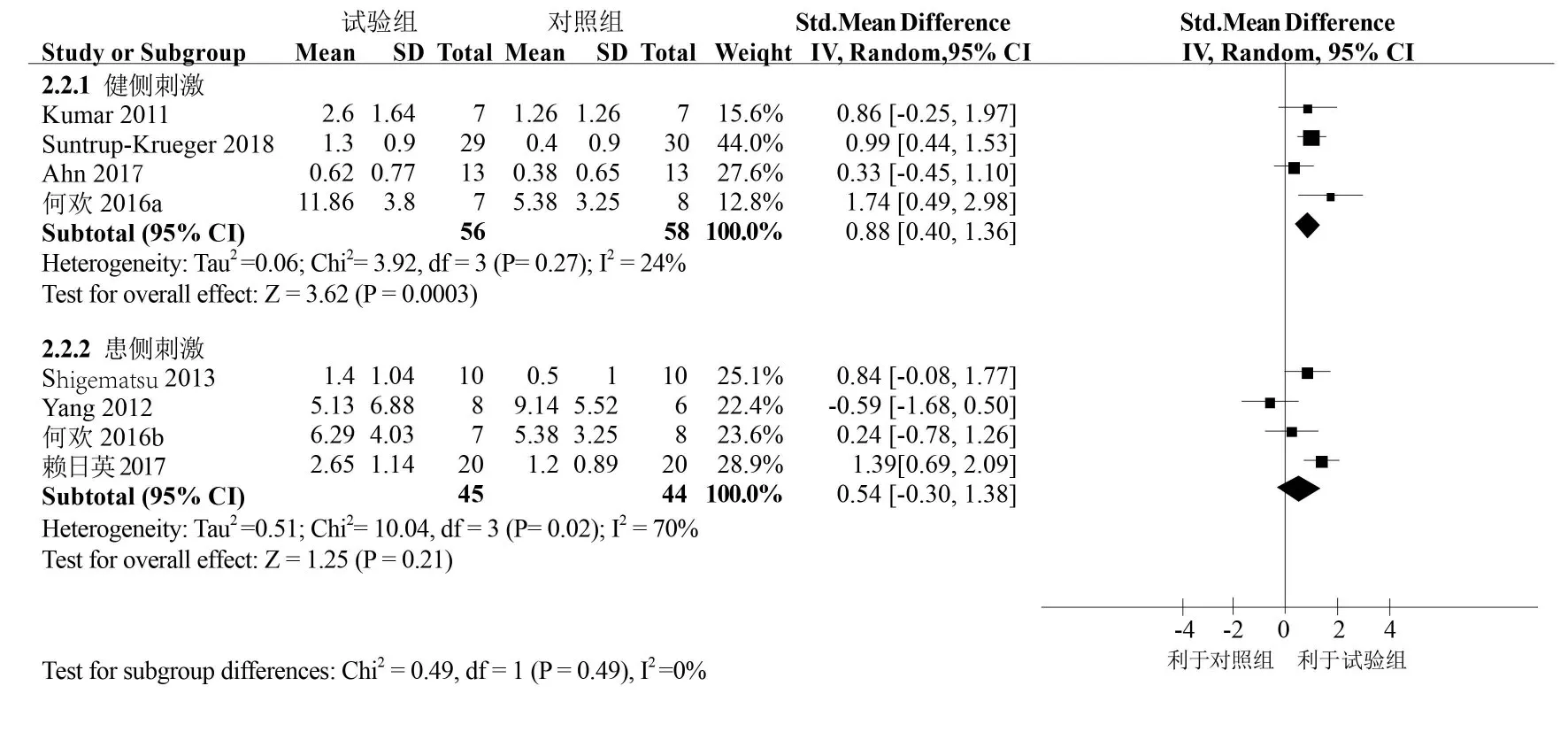
图6 根据刺激部位的亚组分析森林图

表3 纳入研究安全性统计
2.7 敏感性分析以及发表偏倚检测
采用变更分析模型的方法对敏感性进行分析。对总效应量采用固定效应模型分析,结果提示,SMD=0.75,95%CI:0.48~1.02,P<0.00001,与当前所得结果一致,表明分析结果稳健。采用倒漏斗图进行发表偏倚分析(图6),所选的文献在图中分布不对称,并且文献筛选时发现有会议文献报道,但是因为无法提取数据而剔除,因此可能存在一定的发表偏倚。
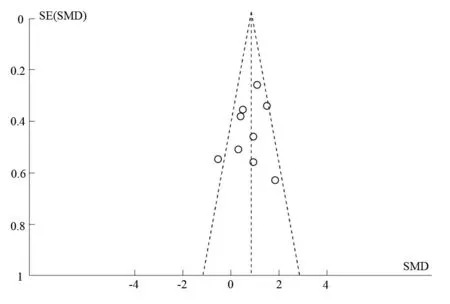
图7 两组治疗后吞咽功能评分改善改善的倒漏斗图
3 讨论
本研究共纳入8项研究,其中5项研究[6,8-11]存在偏倚风险低,3项研究[12-14]偏倚风险较高;本研究纳入的脑卒中病例包括脑梗死和脑出血;所有纳入研究均采用阳极tDCS,没有检索到关于阴极tDCS的RCTs。在本研究中,采用SMD对各个量表的变化结果进行合并分析,结果提示,阳极tDCS能够改善卒中后吞咽困难患者的吞咽功能,并且具有较好的安全性,无不良事件发生。
在本研究中,由于各个具体结局指标结果的不一致性,且所有纳入研究间存在中等程度的异质性,因此通过亚组分析来分析异质性来源。①病例卒中发病时间:纳入病例的卒中发病时间为发病80 h~15个月,两个亚组分析结果提示tDCS能够改善急性脑卒中和脑卒中恢复期的患者的吞咽功能。本研究没有检索到卒中发病72 h内和卒中发病1年半后的临床试验,而卒中后吞咽困难患者在卒中发病后何时进行tDCS治疗的在国际上尚无定论[15],也有研究表明[16],过早使用tDCS可能会加重病情,而在慢性卒中期治疗效果同样不显著。②刺激部位:本研究表明,健侧刺激能够明显改善患侧吞咽功能,而患侧刺激对于吞咽功能的改善与对照组差异无统计学意义。研究表明tDCS能够改善脑皮质功能可塑性[17],而吞咽功能受双侧大脑半球支配[18],因此刺激健侧比刺激患侧对吞咽功能的改善更加明显。而这与Pisegna等[19]的研究一致。
所有纳入研究均报道tDCS具有良好的安全性,部分病例在刺激开始时出现刺激部位皮肤的轻微疼痛,无严重不良事件发生,未出现脱落病例。而关于tDCS的其他证据也表明,tDCS具有良好的安全性[20]。
本研究共纳入8项RCTs,在检索时发现有会议论文报道了结果,但是未公开发表,因此可能存在一定的发表偏倚,对本研究结果可能造成一定的影响;本研究纳入研究的tDCS刺激电流、刺激时间不一致,总治疗时间不一致等因素降低了本研究所得到证据的质量;而且受研究规模的限制,每一项研究纳入的病例数较少,也降低了证据的质量。
综上所述,本次系统评价结果表明,阳极tDCS能够改善卒中后吞咽困难患者的吞咽功能,并且健侧刺激疗效较好。然而本次研究的规模以及异质性,我们仍需要大样本高质量的RCTs加以验证和评价。
[1]Arnold M,Liesirova K,Βroeg-Morvay A,et al.Dysphagia in acute stroke:incidence,burden and impact on clinical outcome[J].PLoSOne,2016,11(2):e0148424.
[2]张婧.卒中后吞咽困难的识别和管理指南[J].中国卒中杂志,2007,2(3):242-255.
[3]Geeganage C,Βeavan J,Ellender S,et al.Interventionsfor dysphagia and nutritional support in acute and subacute stroke[J].Cochrane Database Syst Rev,2012,10(10):CD000323.
[4]Βikson M,Grossman P,Thomas C,et al.Safety of Transcranial Direct Current Stimulation:EvidenceΒased Update 2016[J].Βrain Stimulation,2016,9(5):641-661.
[5]Jefferson S,Mistry S,Singh S,et al.Characterizing the application of transcranial direct current stimulation in human pharyngeal motor cortex[J].Am JPhysiol Gastrointest Liver Physiol,2009,297(6):G1035-G1040.
[6]Kumar S,Wagner CW,Frayne C,et al.Noninvasive brain stimulation may improve stroke-related dysphagia:a pilot study[J].Stroke,2011,42(4):1035-1040.
[7]Ghandehari KEM,Kiadarbandsari EPM.Transcranial direct current stimulation in post-stroke dysphagia:a systematic review of randomized controlled trials[J].Rev Clin Med,2016,3(3):117-121.
[8]Shigematsu T,Fujishima I,Ohno K.Transcranial direct current stimulation improves swallowing function in stroke patients[J].Neurorehabil Neural Repair,2013,27(4):363-369.
[9]Suntrup-Krueger S,Ringmaier C,Muhle P,et al.Randomized trial of transcranial direct current stimulation for poststroke dysphagia[J].Ann Neurol,2018,83(2):328-340.
[10]Yang EJ,Βaek SR,Shin J,et al.Effects of transcranial direct current stimulation(tDCS)on post-stroke dysphagia[J].Restor Neurol Neurosci,2012,30(4):303-311.
[11]Ahn YH,Sohn H,Park J,et al.Effect of bihemispheric anodal transcranial direct current stimulation for dysphagia in chronic stroke patients:a randomized clinical trial[J].J Rehabil Med,2017,49(1):30-35.
[12]何欢.经颅直流电刺激治疗卒中后吞咽障碍的疗效研究[D].昆明:昆明医科大学,2016.
[13]袁英,汪洁,吴东宇,等.经颅直流电刺激改善卒中后共济失调型吞咽障碍的疗效观察[J].中国康复医学杂志,2015,30(8):765-770.
[14]赖日英.电针结合经颅直流电刺激对脑卒中后吞咽障碍的疗效观察[D].广州:广州中医药大学,2017.
[15]Simons A,Hamdy S.The use of brain stimulation in dysphagia management[J].Dysphagia,2017,32(2):209-215.
[16]Fregni F,Pascual-Leone A.Technology insight:noninvasive brain stimulation in neurology-perspectives on the therapeutic potential of rTMSand tDCS[J].Nat Clin Pract Neurol,2007,3(7):383-393.
[17]Vasant DH,Mistry S,Michou E,et al.Transcranial direct current stimulation reverses neurophysiological and behavioural effects of focal inhibition of human pharyngeal motor cortex on swallowing[J].JPhysiol,2014,592(4):695-709.
[18]Suntrup S,Teismann I,Wollbrink A,et al.Altered cortical swallowing processing in patients with functional dysphagia:a preliminary study[J].PLoSOne,2014,9(2):e89665.
[19]Pisegna JM,Kaneoka A,Pearson WG,et al.Effects of non-invasive brain stimulation on post-stroke dysphagia:A systematic review and meta-analysis of randomized controlled trials[J].Clin Neurophysiol,2016,127(1):956-968.
[20]Godinho MM,Junqueira DR,Castro ML,et al.Safety of transcranial direct current stimulation:evidence based update 2016[J].Βrain Stimul,2017,10(5):983-985.
