PVC涂膜Ce(Ⅳ)离子选择性电极的制备与性能
2018-06-19张冬恒
张冬恒,姜 鹏,李 勇
(东北大学 冶金学院,沈阳 110004)
稀土元素在磁性、光学、电学方面具有优异的性质,含有稀土元素的永磁、荧光、抛光、储氢、磁光、超导、功能陶瓷等新材料在众多高科技领域中起着至关重要的作用,因此稀土有“工业味精”“和“新材料宝库”之称[1-5].氟碳铈矿(RE2(CO3)3REF3)是具有高开采价值的稀土矿物类型,在世界稀土资源中占有相当大的比重,大约70%的稀土产品来自于氟碳铈型稀土矿[6-8].矿物中所含稀土以轻稀土为主,稀土元素主要为镧、铈、镨、钕,其中铈含量约占50%[9-11].通常,处理氟碳铈矿主要采用湿法冶金工艺[12-13],而稀土Ce(Ⅳ)存在于氟碳铈矿氧化焙烧-稀硫酸浸出-萃取法提取稀土工艺流程的各个阶段中,因此Ce(Ⅳ)浓度的测定在稀土冶炼提取的整个工艺流程中具有重要意义.
目前,对于Ce(Ⅳ)浓度的测定主要可分为仪器分析法和化学分析法,仪器分析法包括分光光度法、原子吸收法、电感耦合离子体原子发射光谱法等[14-17],化学分析法包括滴定分析法和重量分析法等.其中,仪器分析法需要对待测样进行预处理,过程繁琐,且不能有效保证准确度,不适用于稀土离子的快速测定,化学分析法的灵敏度不高.综上所述,目前测定稀土Ce(Ⅳ)的方法普遍存在着繁琐、耗时、离线等不足;开一种实时在线测定Ce(Ⅳ)浓度的新方法很有必要.电化学方法具有简便、准确的优点,其中离子选择性电极是一种具有潜在应用价值的测定稀土离子浓度的方法[18].已有将离子选择性电极应用于稀土分析的研究报道[19],进一步揭示了选择性电极应用于稀土研究的可能性,但对于高价态稀土Ce(Ⅳ)离子的选择性电极的实验探究还未见报道.
本文针对Ce(Ⅳ)浓度的测定存在繁琐与离线的问题,采用涂膜的方式制备了PVC涂膜Ce(Ⅳ) 离子选择性电极,为开发新的Ce(Ⅳ)浓度的测定方法进行了实验探索.
1 材料和方法
1.1 实验材料
聚氯乙烯(PVC),分析纯,aladdin试剂公司;二甲苯胺蓝(II),分析纯,上海刘氏医药科技公司;邻苯二甲酸二丁酯(DBP)、油酸(OA)、四氢呋喃(THF)、硫酸、硫酸钠、硫酸铁和氯化钙都为分析纯,国药化学试剂有限公司.实验所用水为二次去离子水.
1.2 分析测试仪器和设备
PXSJ-216型离子活度计、312-01铂电极和217型饱和甘汞电极:上海雷磁仪器厂;DF-101S型集热式恒温加热磁力搅拌器,巩义市予华仪器有限公司;FA2104型电子分析天平,上海民桥精密科学仪器公司;螺旋测微仪:河北新创制量具有限公司.
1.3 PVC涂膜电极的制备
称取一定比例的聚氯乙烯粉(PVC)、活性剂、增塑剂、适量添加剂于烧杯中,用约4 ml的四氢呋喃(THF)溶解,持续搅拌约10 min至混合液有一定黏度,取洁净的铂电极放入混合液中使铂电极前端铂片完全浸没于液体中,停留5 s后取出铂电极,待其风干将其浸入混合液中反复数次制备出适宜厚度的涂膜电极.
1.4 电极的响应性能测试
1.4.1 活化
将制备的PVC涂膜电极放入0.001 mol/L的Ce(SO4)2溶液中,稳定保存12 h.
1.4.2 测试
配制各种稀土离子(Ce、La、Pr、Nd、Sm)对应的硫酸盐溶液、硫酸铁和氯化钙溶液,浓度C分别为10-1~10-5mol/L五组,酸度均为0.5 mol/L(用H2SO4调节离子酸度,Na2SO4调节离子强度).另外加一组不加酸的Ce(SO4)2溶液.将所制备的Ce(Ⅳ)离子选择性电极与甘汞参比电极连接到离子计,按照浓度从低到高的顺序记录各组待测液的稳定电位示数,并绘制E-lgC曲线.考察PVC膜组成、溶液酸度、温度等对电极响应性能的影响,并考察了PVC涂膜电极的稳定性、重现性、电极的寿命以及稀土相伴杂离子对电极响应性能的影响等.
1.4.3 保存
将使用后的电极浸泡在0.001 mol/L的待测溶液中.
2 结果与讨论
2.1 PVC敏感膜的组成
本文选择铂电极作为基底电极,二甲苯胺蓝(II)为活性剂,DBP为增塑剂,油酸为离子添加剂,采用涂膜法制备了PVC涂膜Ce(Ⅳ)离子选择性电极,考察了各组分含量对电极电位响应的影响.
2.1.1 膜厚度对电极响应性能的影响
考虑到敏感膜厚度可能与膜电极对待测离子的敏感程度有关,本文对敏感膜的厚度做了研究图1中电极1~3中膜厚度分别为0.21、0.33和0.435 mm.从图中可以看出,厚度为0.21 mm的电极电位示数波动很大,膜厚度0.33 mm以后电极示数趋于稳定,随着电极厚度的增加,电极的稳定时间变短.厚度为0.33 mm和0.435 mm的电极电位差距不大,有较稳定的电位,本文选择厚度为0.435 mm的电极进行后续研究.

图1 涂膜厚度对电极响应的影响Fig.1 Effect of film thickness on the electrode response
2.1.2 增塑剂的含量及影响
增塑剂用于调节电极膜的塑性、韧性和黏稠度,利于离子的迁移和通过,邻苯二甲酸二丁酯(DBP)是聚氯乙烯最常用的增塑剂,本文考察DBP用量为100 mg、150 mg、200 mg时对电极响应性能的影响,绘制如图2所示E-lgC曲线.

图2 增塑剂用量对电极响应的影响Fig.2 Effect of plasticizer on the electrode response
从图2中可以看出,随着待测离子浓度的增加,电动势逐渐增大,在DBP用量为200 mg时电动势偏大,电极响应性能一般,在DBP用量为100 mg、150 mg时在待测离子浓度范围内都有线性响应,通过比较相关系数R2值,得出在DBP含量为100 mg时有好的电极响应性能.
2.1.3 离子添加剂的含量及影响
离子添加剂用来优化PVC膜中性载体或核电载体电极的电位响应性能,判断电极载体对被测离子产生电位响应时的相应机理.本文考察了添加量分别为5 mg、10 mg、20 mg的油酸对电极响应性能的影响.

图3 离子添加剂用量对电极响应的影响Fig.3 Effect of ion addition on the electrode response
从图中可以看出,电位值随着离子添加剂油酸用量的改变而发生变化,在油酸用量为20 mg时,电位明显发生了漂移,对添加量为5 mg、10 mg的油酸在线性范围内进行拟合,在油酸10 mg时有较高的R2值,为0.987,因此,加入10 mg的油酸时PVC涂膜电极的电位响应效果好.
2.2 Ce(Ⅳ)离子选择性电极的性能测定
2.2.1 Ce(Ⅳ)离子选择性电极的选择性分析
离子选择性是制备离子选择性电极最重要的特点,本文测试了电极对常见阳离子三价镧(La)、钕(Nd)、钐(Sm)、镨(Pr)、铈(三价和四价)的相应效果,其E-lgC如图4所示.

图4 Ce(Ⅳ)离子选择性电极的选择性Fig.4 Selectivity of Ce(Ⅳ) ion selective electrode
从图中可以看出,离子选择性电极对于无酸的Ce(Ⅳ)离子和Nd离子基本无选择性,Ce (Ⅲ)离子在电位600 mV上下浮动,La(Ⅲ) 离子在浓度10-5~10-2范围内变化不大,在10-2浓度后略有上升.对于Sm(Ⅲ)离子在浓度为10-4~10-3时电位略有升高,之后随着浓度的增大上升到600 mV后维持不变,可见Ce(Ⅳ)离子选择性电极对三价Ce(Ⅲ)、Nd(Ⅲ)、La(Ⅲ)、Sm(Ⅲ)离子基本无选择性.Pr离子的电位值随着浓度的增大而增大,但是增长缓慢,而对Ce(Ⅳ)离子,随着其浓度的增大,电位值增大,表现出很好的线性关系,其线性范围为1.0×10-5~1.0×10-1mol/L,表明了所制备的电极对于Ce(Ⅳ)具有很好的选择性.
2.2.2 重现性及稳定性分析
电极的重现性是指从一种浓度的溶液换到另一浓度的溶液进行多次胶体测量时,电极电势的重现程度.电极的稳定性是指常温条件下,一段时间内进行连续测量某一浓度待测液时,其电位波动范围.根据电极的稳定性加之分析测量中所要求的准确度,可以确定用标准溶液校准电极的时间周期.实验将所制备的Ce(Ⅳ)离子选择性电极在1.0×10-2mol/L浓度的硫酸铈溶液中测定稳定后记示数,再放入浓度为1.0×10-3mol/L的硫酸铈溶液中稳定后记示数.

图5 电极的稳定性与重现性Fig.5 Electrode stability and reproducibility
从图5中可以看出在2 h内,每隔5 min测定的电极数据波动很小,在0.01 mol/L和0.001 mol/L 的Ce(SO4)2溶液中电极电位的标准偏差(SD)分别为2.1196 mV、4.0645 mV,表明制备的Ce(Ⅳ)选择性电极有优异的稳定性和重现性.
2.2.3 酸度对电极电位响应性能的影响
酸度即待测液中H+的浓度,酸度对电极性能的影响其实质是指待测溶液中的H+电极测量时电位的影响.通过考察电极在不同酸度溶液中电位的变化,从而确定电位响应稳定的酸度范围.
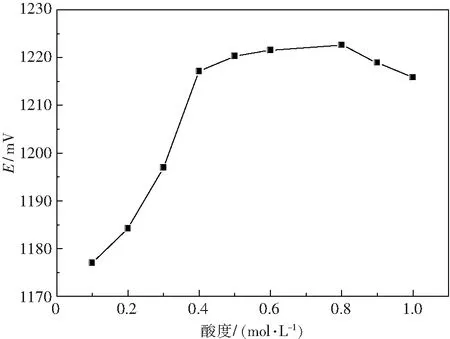
图6 酸度对Ce(Ⅳ)离子选择性电极性能的影响Fig.6 Effect of acidity on performance of the Ce (Ⅳ) ion-selective electrode
由图6可知电极在酸度为0.4~0.8 mol/L溶液中呈现出稳定的电位值,但是当溶液酸度值低于0.4 mol/L和高于0.8 mol/L时,电极就表现出不稳定的电位值.当溶液酸度低于0.4 mol/L时候,可能是由于溶液Ce(Ⅳ)在低酸度下发生水解,而当溶液酸度高于0.8 mol/L时电极的电位产生漂移,可能是由于H+影响了活性剂的活性,载体分子的质子化而不能够与Ce(Ⅳ)配位所致.因此,测试液对电极的适宜酸度是0.4~0.8 mol/L.
2.3.4 电极的使用寿命
本实验将制备的Ce(Ⅳ)离子选择性膜电极在180d内测定3次(参见图7),电极对待测液各个浓度所响应的电位值相差不大,且并未发现电极的灵敏度、线性范围及检测下限等电位响应性能有明显的降低,表明电极的使用寿命高于 180 d.

图7 使用时间对Ce(Ⅳ)离子选择性电极电位的影响Fig.7 Effect of operating time on potential of the Ce(Ⅳ) ion-selective electrode
2.3.5 Ce(Ⅳ)离子选择性电极的应用研
根据上述实验结果,在选择性电极中加入100 mgDBP增塑剂,10 mg离子添加剂,涂膜厚度为0.435 mm,调节溶液酸度为0.6 mol/L,观测电极对不同浓度的待测液的响应电位,绘制如图8所示标准曲线.

图8 待测液浓度与电极响应电位的关系Fig.8 Relationship between concentration of tested solution and electrode response potential
从图中可以看出Ce4+选择性电极的线性响应范围为1.0×10-5~1.0×10-1,并且在1.0×10-2~1.0×10-1范围内响应效果较好,因此分别配置浓度为0.1 mol/L、0.01 mol/L的CeSO4溶液,0.1 mol/L CeSO4和0.01 mol/L的FeCl2溶液,0.1 mol/L CeSO4和0.01CaCl2溶液,使用制备的Ce4+选择性电极对水溶液浓度进行测定,并与传统滴定法的结果进行比较如表1所示.
观测Ce(Ⅳ)离子选择性电极的测定效果和稀土常伴杂离子Fe2+、Ca2+对电极响应性能的影响.
通过表中数据可以计算出用离子选择电极法和滴定法测得的水溶液浓度相差小于 0.003 mol/L,若以滴定数据为真值标准,则测定相对误差小于3%,所以制备的离子选择性电极可用于水溶液中Ce4+浓度的测定.同时在有杂离子Fe2+、Ca2+的干扰下,通过选择性电极测得Ce4+浓度并未有较大的变化,说明稀土相伴杂离子对电极的响应性能造成影响较小.

表1 Ce4+选择性电极对水相浓度进行测定结果Table 1 Results of determination of aqueous phase concentration by the Ce4+ selective electrode
3 结 论
(1)本实验制备了PVC涂膜Ce(Ⅳ)离子选择性电极,确定了Ce(Ⅳ)离子选择电极的最佳涂膜厚度约为0.43 mm.并确定了膜组分材料的添加量,以100 mg的DBP为增塑剂,10 mg油酸为离子添加剂时电极有较好的电位响应效果.
(2)测试了制备的PVC涂膜Ce(Ⅳ)离子选择性电极的各项响应性能,其线性范围为1.0×10-5~1.0×10-1mol/L.通过膜电极的选择性测试表明所制备的离子选择性电极对Ce(Ⅳ)有很好的选择性,可以应用于Ce(Ⅳ)浓度的测定,研究结果表明Ce(Ⅳ)离子选择性电极对待测液合适的酸度范围为0.3~0.8 mol/L.
(3)研究结果表明制备的PVC涂膜Ce(Ⅳ)离子选择性电极的稳定性和重现性都较好,电极使用寿命大于180 d,Fe2+、Ca2+等稀土相伴杂离子对电极的响应性能影响较小.
参考文献:
[1] 李国玲, 李兴国.稀土金属及其金属间化合物的研究与应用[J].中国稀土学报, 2016, 34(06):748-763.
(Li Guoling, Li Xingguo.Research and application of rare earth metal and intermetallic.[J].The Chinese Society of Rare Earths, 2016, 34(06):748-763.)
[2] 王珺之.中国稀土保卫战[M].北京:中国经济出版社, 2010:25-160.
(Wang Junzhi.China rare earth defense war[M].Beijing:The Publisher of China Econmic, 2010:25-160.)
[3] 吴文远.稀土冶金学[M].北京:化学工业出版社, 2005:13-165.
(Wu Wenyuan.Rare earth metallurgy[M].Beijing:The Publisher of Chemical industries, 2005:13-165.)
[4] 许振亮, 刘冬潇, 刘喜美.国际稀土研究的科学知识图谱分析[J].有色金属科学与工程, 2016, 7(05):144-152.
(Xu Zhenliang, Lu Dongxiao, Liu Ximei.Analysis of scientific knowledge mapping in research area of international rare earth[J].Nonferous Metals Science and Engineering, 2 016, 7(05):144-152.)
[5] Wang L S, Huang X W, Yu Y,etal.Towards cleaner production of rare earth elements from bastnaesite in China[J].Cleaner Production , 2017, 165:231-242.
[6] 马莹, 李娜, 王其伟, 等.白云鄂博矿稀土资源的特点及研究开发现状[J].中国稀土学报, 2016, 34(06):641-649.
(Ma Yi, Li Na, Wang Qiwei,etal.Characteristics and current research situation of rarearth resources in bayan obo ore[J].The Chinese Society of Rare Earths, 2016, 34(06):641-649.)
[7] Marino Gergoric, Christian Ekberg, Britt-Marie,etal.Separation of heavy rare-earth elements from light rare-earth elements via solvent extraction from a neodymium magnet leachate and the effects of diluents[J].Sustainable Metallurgy, 2017, 3(03):601-610.
[8] 杜晓慧.全球稀土矿产资源分布、开发现状以及未来发展格局[J].资源与产业, 2014, 16(06):21-28.
(Du Xiaohui.Resource distribution、development situation and future development of gl-obal ree[J].Resources and Industries, 2014, 16(06):21-28.)
[9] 张臻悦, 何正艳, 徐志高, 等.中国稀土矿稀土配分特征[J].稀土, 2016, 37(01):121-127.
(Zhang Zhenyue, He Zhengyan, Xu Zhigao,etal.Rare earth partitioning characteristics of china rare earth ore[J].China Rare Earth, 2014, 16(06)21-28.)
[10] 杜梅, 许涛, 吴文琪.稀土标准分析方法中稀土元素分析谱线的述评[J].稀土, 2014, 35(06):99-105.
(Du Tao, Xu Tao, Wu Wenqi.Review of the analytical lines of rare earth elements in rare earth standard analysis methods[J].China Rare Earth, 2014, 35(06)99-105.)
[11] 刘文华.稀土元素分析[J].分析试验室, 2012, 31(07):111-123.
(Lu Wenhua.Review of rare earth analysis[J].Chinese Journal of Analysis Laboratory, 2012, 31(07):111-123.)
[12] 张晓伟, 李梅, 柳召刚, 等.HNO3-Al(NO3)3溶液分离包头混合稀土精矿的研究[J].中国稀土学报, 2013, 31(05):588-596.
(Zhang Xiaowei, Li Wei, Liu Zhaogang.Separation of baotou mixed rare earth concentrate by HNO3-Al(NO3)3solution[J].The Chinese Society of Rare Earths, 2013, 31(05):588-596.)
[13] 陈涛, 李宁, 晏波, 等.稀土湿法冶炼废水污染治理技术与对策[J].化工进展, 2014, 33(05):1306-1311+1355.
(Chen Tao, Li Ning, Yan Bo,etal.Pollution control technologies and measures of rare earths hydrometallurgy wastewater[J].Chemical Industry and Engineering Progress, 2014, 33(05):1306-1311+1355.)
[14] 吴健生, 宋静, 郑茂坤, 等.土壤重金属全量监测方法研究进展[J].东北农业大学学报, 2011, 42(05):133-139.
(Wu Jiansheng, Song Jing, Zheng Maokun,etal.Review of methods for monitoring soil heavy metal concentrations[J].Journal of Northeast Agric:Ultural University, 2011, 42(05):133-139.)
[15] 刘子森, 肖恩荣, 张丽萍, 等.EPS及其测定方法分析[J].膜科学与技术, 2015, 35(04):103-109+122.
(Liu Zisen, Xiao Enrong, Zhang Liping,etal.The preparation and modification of hemodialysis membrane materials and hemodialyzer[J].Membrane Science and Technology, 2015, 35(04):103-109+122.)
[16] Singh A K, Saxena P.A PVC-based membrane electrode for nickel (II) ions incorporate-ng a tetraazamacrocycle as an ionophore[J].Sens Actu B, 2007, 121(2):349-355.
[17] Shamsipur M, Soleymanpour A, Akhond M.Highly selective chromium(Ⅲ) PVC-membrane electrodes based on some recently synthesized Schiffs bases[J].Electroanalysis, 2005, 17(9):776-782.
[18] 李冰, 周剑雄, 詹秀春.无机多元素现代仪器分析技术[J].地质学报, 2011, 85(11):1878-1916.
(Li Bing, Zhou Jianxiong, Zhan Xiuchun.Modern instrumental analysis of inorganic multi elements[J].Acta geologica sinica, 2011, 85(11):1878-1916.)
[19] 王玫玫,张晓,李梅珍, 等.PVC液膜稀土离子选择性电极的研究[J].福建师范大学学报(自然科学版), 1993 (04):56-60.
(Wang Meimei, Zhang Xiao, Li Meizhen,etal.Study on rare earth ion-selective electrodes with rare earth active material-containing PVC membrane[J].Fuijian Normal University (Natural Science), 1993 (04):56-60.)
