添加氧化镁和铵明矾对菜田高磷土壤活性磷的影响
2018-06-06樊秉乾郜斌斌
朱 謇,樊秉乾,郜斌斌,陈 清
(农田土壤污染防控与修复北京市重点实验室 中国农业大学资源与环境学院,北京 100193)
蔬菜根系发育弱,对土壤磷素供应要求很高,尤其是设施菜田生产中,加强有机肥和磷肥的施用是保障磷素供应的关键[1]。由于蔬菜对磷素的吸收数量远远低于投入的数量,因此菜田土壤磷素累积问题十分突出,如2015年京郊设施菜田每季作物生产的P2O5平均投入量为637 kg·hm-2,是作物磷素吸收量的7~32倍[2]。考虑作物对磷的吸收能力,采用耗竭方法大约需要9~22年才能利用20-50%的土壤残留磷[3],对于菜田土壤来说需要时间很长,不能快速降低磷素淋失风险。而农田土壤磷素中有机磷所占的比例一般低于20%[4-5],大多数是以吸附态、铁铝结合态和钙镁结合态存在的无机磷。因此随着土壤中外源不断施入的可溶性磷酸盐的增加,超出矿物吸附和结合能力以后,磷素的有效性迅速提高,甚至超过了土壤的固持吸附能力,从而导致其在土壤中的移动性增加,流失到水体中的风险也迅速上升[6-8]。
发达国家早在十多年前就面临土壤磷素累积到“饱和”状态的问题,从而不得不采取向土壤中加入黏土矿物、铁铝结合物和钙镁结合物等矿物质的措施,来快速有效固定土壤中的活性磷,从而减少土壤磷素移动[9-11]。研究发现铝盐能有效固定土壤活性磷[12-13],Novak等[14]在不同类型高磷土壤中添加6.0%的含铝废水,土壤M3浸提磷下降了145~471 mg·kg-1,但是土壤pH也显著下降。而钙镁化合物也有较强的吸附性,但其一般呈碱性,对土壤pH的影响较大。Michael等[15]的研究发现在土壤中添加2.0%的氧化镁培养4周后能减少78.6%可溶性磷,但土壤pH也增加到了9.43。因此不同种类的矿物钝化剂对土壤磷素的钝化机制不同,由此所引发的问题是所钝化的土壤磷素在减少环境污染风险的情况下是否对作物依然有效?是否可以通过不同钝化剂混合施用来固定土壤活性磷,同时减少对土壤pH和其他养分有效性的影响。
本试验以北京市房山区高磷设施菜田土壤为研究对象,采用室内培养试验,向土壤中加入土壤干重0.5%和2.0%的铵明矾、氧化镁及二者混合物,探究氧化镁、铵明矾及其混合物在培养45 d内对土壤磷素固定效果的影响,以期回答上述科学问题。
1 材料与方法
1.1 试验材料
(1)供试土壤:供试石灰性土壤取自北京市房山区西场村设施菜田0~30 cm土层。土样自然风干,去除作物根茎、石块等杂物后过2 mm筛,备用,其部分理化性质见表1。
(2)钝化材料:试验所用的氧化镁(MgO)(饱和水溶液的pH值10.30)和铵明矾[NH4Al(SO4)2·12H2O](饱和水溶液的pH值3.04)都是来自国药集团的分析纯试剂。钝化材料过100目筛,并按照铵明矾∶氧化镁=1∶5、1∶2、1∶1、2∶1、5∶1 的比例混合形成混合物,备用。

表1 供试土壤理化性质Table 1 Physical and chemical properties of test soil

表2 试验设计Table 2 Design of soil incubation experiment
1.2 试验处理及方法
在田间试验中,一般一次性添加土壤干重2.0%的土壤调理剂[16],但是氧化镁和铵明矾一次性添加会造成土壤pH剧烈变化。本研究的培养试验共设置风干土壤干重的0.5%和2.0%(m/m)的添加水平,7种添加材料配比,加上不添加钝化材料的空白处理(CK)共15个处理,每个处理设置三个重复(表2)。
培养试验的方法如下:称取300 g风干土壤和每个处理所需的钝化材料(表2),在牛皮纸上混匀,装入直径8.0 cm、高8.8 cm的广口瓶中,加水调节湿度至田间持水量的60%[该土壤的田间持水量为29.2%(m/m)],再用带小孔的塑料膜封口后放入温度25℃、湿度70%的遮光培养箱内进行培养,培养过程中,每3~4 d添加去离子水至田间持水量的60%。在培养第1、15、45 d分别进行破坏性取样,将土壤自然风干后测定相关指标。
为了进一步探究土壤磷素形态转化,根据Hedley磷分组方法研究减少的水浸提磷和碳酸氢钠浸提磷的去向,试验选取添加梯度为2.0%氧化镁、铵明矾及其混合物处理下培养45 d后的土壤,利用修正的Hedley磷素分组方法[17-19]测定土壤不同磷素形态,具体如下:称0.5g过2mm筛的风干样品置于50mL的离心管中,依次采用 30mL 去离子水(H2O-P)、0.5mol·L-1NaHCO3溶液(NaHCO3-P)、0.1 mol·L-1NaOH 溶液(NaOH-P)和1 mol·L-1HCl溶液(HCl-P)浸提。每一步加入浸提液后,振荡 16 h(25 ℃,200 r·min-1),离心(25 000g,10 min,0℃),之后收集上清液并过0.45μm滤膜。无机磷Pi含量采用钼锑抗比色法测定,全磷Pt含量采用过硫酸铵氧化-钼锑抗比色法测定。
1.3 测定项目与方法
(1)土壤pH的测定:采用去二氧化碳超纯水提取土壤溶液(土水比1∶2.5),用pH计测定pH。
(2)土壤EC的测定:采用去二氧化碳超纯水提取土壤溶液(土水比1∶5),用EC计测定EC。
(3)土壤速效磷测定:0.5 mol·L-1的碳酸氢钠按土液比1∶20浸提后,采用钼锑抗比色法测定[20]。
(4)土壤水溶性磷测定:0.01 mol·L-1的 CaCl2按土液比1∶5浸提后,采用钼锑抗比色法测定[21]。
(5)无机磷Pi含量采用钼锑抗比色法测定,全磷Pt含量采用过硫酸铵氧化-钼锑抗比色法测定[17-19]。
1.4 统计分析
数据统计、作图采用Microsoft Excel 2010软件和Sigmaplot 10.0,方差分析采用IBMSPSSStatistics20,所有数据结果均以3次重复的平均值表示。显著性差异分析采用Duncan法,显著性水平设定为α=0.05(*)。
2 结果与分析
2.1 土壤pH值变化
向土壤中添加不同种类和比例的钝化材料后,土壤pH值的变化见表3。培养1 d后,添加铵明矾的处理土壤pH值降低,添加氧化镁的处理土壤pH值显著增加。仅添加土壤干重0.5%的氧化镁,土壤pH值就从7.36升高到9.47,添加梯度增加到2.0%时,土壤pH值进一步增大到9.81。将铵明矾和氧化镁按不同比例混合添加到土壤中后,土壤pH值介于空白处理(pH7.36)和MgO处理(pH9.47)之间。
随着培养时间的延长,土壤pH存在动态变化。空白处理的土壤pH值变化很小。添加铵明矾和氧化镁处理的土壤pH值均随着培养时间的延长而下降。相比于培养1 d,培养45 d后A-L和A-H处理的土壤pH值分别降低了0.29和0.5个单位;M-L和MH处理的土壤pH值分别下降了0.83和0.29个单位。混合物处理中土壤pH值下降最多的为AM15-L处理,下降1.25个单位;下降最少的为AM15-H处理,下降0.18个单位,这和混合物中铵明矾和氧化镁的含量有关。AM15-H和AM12-H处理中的氧化镁含量较多,中和H+的能力较强,土壤pH值下降效果不明显。而其他处理中的铵明矾含量较多,土壤pH值下降较为明显。
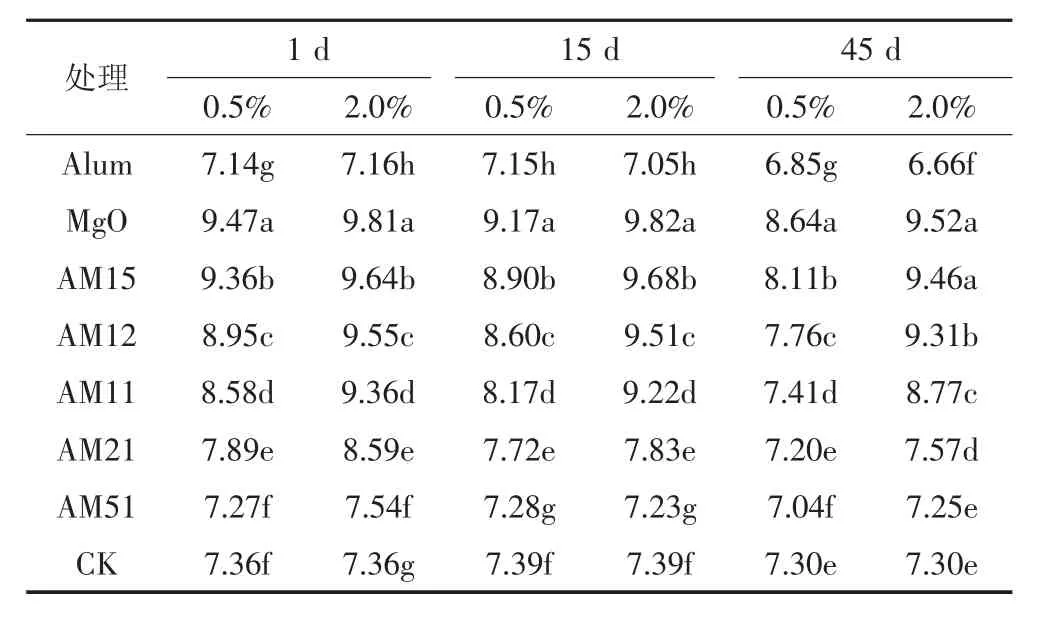
表3 添加氧化镁、铵明矾及其混合物后不同培养时间的土壤pH值变化Table 3 Effectsof adding MgO,alumand their mixtures on soil pH at different incubating days
2.2 土壤EC值变化
向土壤中添加不同种类和比例的钝化材料后,土壤EC值的变化见表4。添加铵明矾和氧化镁培养1 d后土壤EC值显著增加。添加土壤干重0.5%和2.0%的氧化镁分别使土壤EC从0.78 mS·cm-1增加到了1.12 mS·cm-1和 1.37 mS·cm-1。添加 0.5%和 2.0%的铵明矾分别使土壤EC从0.78 mS·cm-1增加到了2.20 mS·cm-1和 3.44 mS·cm-1。在混合物处理中,土壤 EC随着铵明矾占比增加而增加。在2.0%添加梯度下,当铵明矾∶氧化镁=5∶1时,铵明矾所占比例较大,培养1 d、15 d和45 d后土壤的EC值均高于A-H处理。
2.3 土壤CaCl2-P含量变化
添加0.5%的不同钝化材料后土壤CaCl2-P含量变化见图1(A)。在0.5%添加梯度下,所有处理都能显著降低土壤CaCl2-P含量。与对照相比,M-L处理降低土壤CaCl2-P效果最显著,在培养1 d、15 d和45 d后,土壤CaCl2-P分别下降了97.1%、94.0%和87.8%。而在混合物中,降低土壤CaCl2-P效果最显著的是AM15-L处理,并且随着氧化镁在混合物中所占比例逐渐减小,混合物降低土壤CaCl2-P效果减弱,但混合物降低土壤CaCl2-P的效果仍然优于添加土壤干重0.5%的铵明矾。
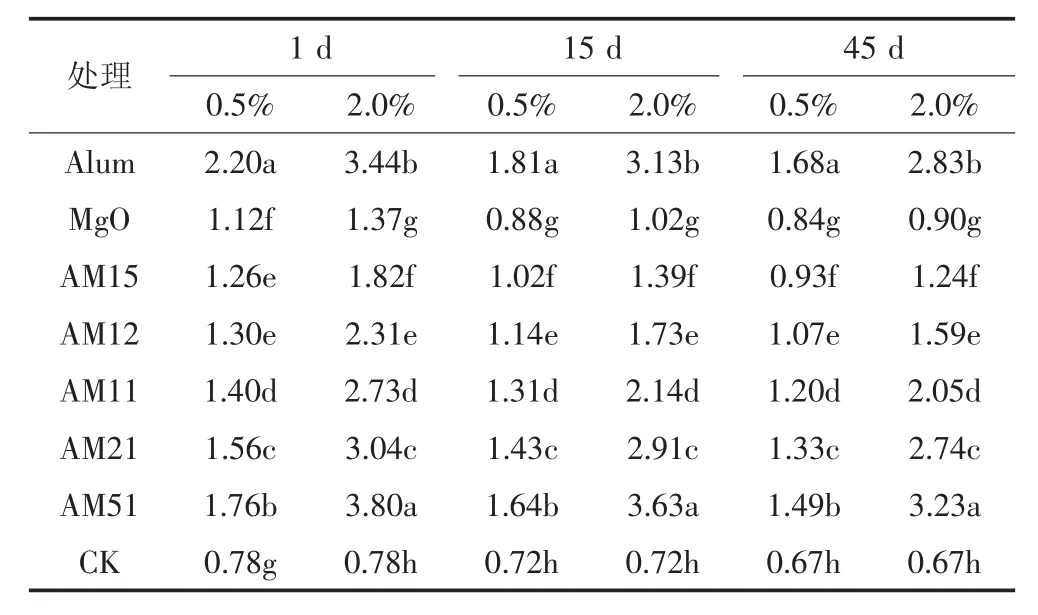
表4 添加氧化镁、铵明矾及其混合物后不同培养时间下土壤 EC 值变化(mS·cm-1)Table 4 Effectsof adding MgO,alumand their mixtures on soil ECat different incubating days(mS·cm-1)
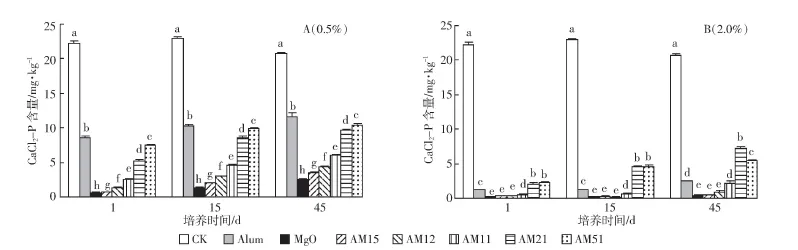
图1 不同钝化剂对不同培养时间下土壤CaCl2-P含量的影响Figure 1 Effect of different amendment on the contents of CaCl2-Pin soil at different incubating days
添加2.0%的不同钝化材料后土壤CaCl2-P含量变化见图1(B)。在2.0%添加梯度下,所有处理都能显著降低土壤CaCl2-P含量,并且降低土壤CaCl2-P的效果优于0.5%添加梯度。与未钝化的对照相比,降低CaCl2-P效果最显著的是M-H、AM15-H、AM12-H处理,在培养1、15、45 d后,土壤CaCl2-P分别降低了99.1%、98.3%和 98.2%;99.0%、98.8%和 99.4%;98.0%、97.5%和95.7%。不同于0.5%添加梯度,2.0%梯度下随着混合物中氧化镁占比逐渐减小,当铵明矾∶氧化镁=2∶1 和 5∶1 时,钝化剂降低土壤 CaCl2-P 效果却不如添加土壤干重2.0%的铵明矾,甚至降低效果弱于0.5%添加梯度下的M-L、AM15-L和AM12-L处理。而且,在2.0%添加梯度下,培养1 d、15 d和45 d后,AM15-H处理、AM12-H处理和A-H处理之间对降低土壤CaCl2-P的效果无显著性差异。培养45 d后,AM11-H处理和M-H处理之间也无显著性差异。
在0.5%添加梯度和2.0%添加梯度下,随着培养时间的延长,土壤CaCl2-P含量都出现了缓慢增加的现象。而2.0%添加梯度下CaCl2-P平均增量少于0.5%添加梯度。在0.5%添加梯度和2.0%添加梯度下增量最多的处理都为AM21处理,土壤CaCl2-P含量分别增加了 4.43 mg·kg-1和 5.18 mg·kg-1。
2.4 土壤Olsen-P含量变化
添加土壤干重0.5%的不同钝化材料后土壤Olsen-P含量变化见图2(A)。在培养1 d后,所有处理都能显著降低土壤Olsen-P含量,其中效果最显著的是A-L、M-L和AM51-L处理,分别降低了27.7%、23.6%和25.1%的Olsen-P。但随着培养时间的延长,M-L、AM15-L、AM12-L 和AM11-L 处理中土壤Olsen-P含量显著增加。在培养15 d后,AM11-L处理和空白处理之间不存在显著性差异;在培养45 d后,M-L、AM15-L、AM12-L和AM11-L处理与空白处理之间差异均不显著。而A-L和AM51-L处理中土壤Olsen-P含量并没有随着培养时间延长而增加。
添加土壤干重2.0%的不同钝化剂后土壤Olsen-P含量变化见图2(B)。在2.0%添加梯度下,所有处理都能显著降低土壤Olsen-P含量,并且降低土壤Olsen-P效果优于0.5%添加梯度,其中效果最显著的是A-H处理和AM51-H处理,分别降低了51.2%和45.4%的土壤Olsen-P含量。而且,类似于0.5%添加梯度,A-H处理和AM51-H处理中的土壤Olsen-P含量也没有随着培养时间延长而增加。而M-H、AM15-H、AM12-H、AM11-H和AM21-H处理,相比于培养1 d,培养45 d后,土壤Olsen-P含量分别增加了32.8%、40.5%、53.3%、45.3%和15.3%。但是,所有处理在培养45 d后,土壤Olsen-P含量均显著小于未添加钝化材料的对照处理。
铵明矾降低土壤Olsen-P的效果强于MgO,但在0.5%添加梯度下,培养1、15 d和45 d后,随着铵明矾在混合物中所占比例逐渐增加,钝化剂降低土壤Olsen-P有先减弱再增强的趋势。在2.0%添加梯度下培养45 d后也出现这样的趋势,这可能与土壤pH值的变化有关。
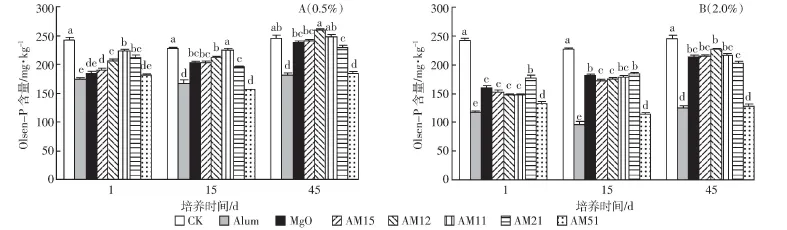
图2 不同钝化剂对不同培养时间下土壤Olsen-P含量的影响Figure 2 Effect of different amendment on the contentsof Olsen-Pin soil at different incubating days
2.5 土壤磷素组分变化
利用修正的Hedley磷素分组方法测定的土壤磷素形态见图3。2.0%添加梯度下,培养45 d后,添加钝化材料处理的土壤H2O-Pt含量都显著低于未添加钝化材料的空白处理,这与培养了45 d的0.01 mol·L-1氯化钙浸提的结果相一致。与未添加钝化材料的对照相比,培养 45 d后,A-H、M-H、AM21-H 和AM51-H处理都能显著降低土壤NaHCO3-Pt含量,其中效果最好的是A-H处理,降低了60.0%,并且随着混合物中铵明矾占比的增加,降低土壤NaHCO3-Pt的效果呈现逐渐增强的趋势。与对照相比,A-H和AM51-H处理都显著增加了土壤NaOH-Pt含量,分别增加了289%和137%,而其他处理对土壤NaOHPt含量的影响不显著。与对照相比,各处理对土壤HCl-Pi含量的影响均不显著。

图3 培养45 d后不同钝化剂对土壤各组分磷含量变化的影响Figure 3 Thechangesof Pfractionsin the soilswith different amendments addition after 45 d incubation
3 讨论
3.1 添加氧化镁和铵明矾对土壤CaCl2-P的影响
添加氧化镁、铵明矾或二者不同比例的混合物均能显著降低土壤CaCl2-P含量。磷素组分结果(图3)表明,添加铵明矾后CaCl2-P向以化学吸附作用吸附于含铝化合物的磷素(NaOH-P)转化。但是,等质量添加条件下,添加氧化镁处理的CaCl2-P值显著低于添加铵明矾的处理(图1),说明氧化镁降低土壤CaCl2-P的能力更强。该结果可能与等质量条件下,氧化镁的比表面积更大有关,氧化镁表面较多的活泼基团为吸附磷素提供了位点[22-23],导致活性磷难以被0.01 mol·L-1的 CaCl2溶液浸提出来。
培养1 d后,0.5%添加梯度下氧化镁含量和土壤CaCl2-P的减少量(0.961**)之间的相关性比2.0%(0.782*)添加梯度显著。这表明2.0%添加梯度下氧化镁对土壤CaCl2-P的固定能力减弱。同时,2.0%添加梯度下的AM51-H处理(1 g MgO+5 g Alum)土壤CaCl2-P含量低于0.5%添加梯度下的AM12-L处理(1 g MgO+0.5 g Alum)也证明了这一现象。这是因为在高添加梯度下混合物中铵明矾量较多,铵明矾水解生成的H+可能溶解了部分氧化镁,从而降低了氧化镁的吸附作用。
同时,本实验结果表明除了0.5%添加梯度下的AM51-L处理,随着培养时间的延长,其他处理的土壤CaCl2-P含量和土壤pH值之间呈现出显著的负相关性(表5),即出现了随着土壤pH值降低,土壤CaCl2-P含量增加的现象。这可能是因为随着pH的升高,H2PO-4会向HPO2-4转化,而HPO2-4的溶解性低于H2PO-4,从而导致活性磷更难以被CaCl2溶液浸提出来[24]。而AM51-L处理中铵明矾含量较多,其土壤pH值随着时间的延长变化幅度较小,对土壤CaCl2-P含量影响也较弱。
以上结果表明,土壤CaCl2-P含量既与氧化镁和铵明矾的性质有关,也和土壤pH值有关。土壤中的PO3-4、HPO2-4、H2PO-4能和氧化镁表面提供的-OH发生配位反应从而被吸附固定,但是Al3+水解产生的H+会导致OH-被消耗,从而破坏氧化镁吸附位点[25]。
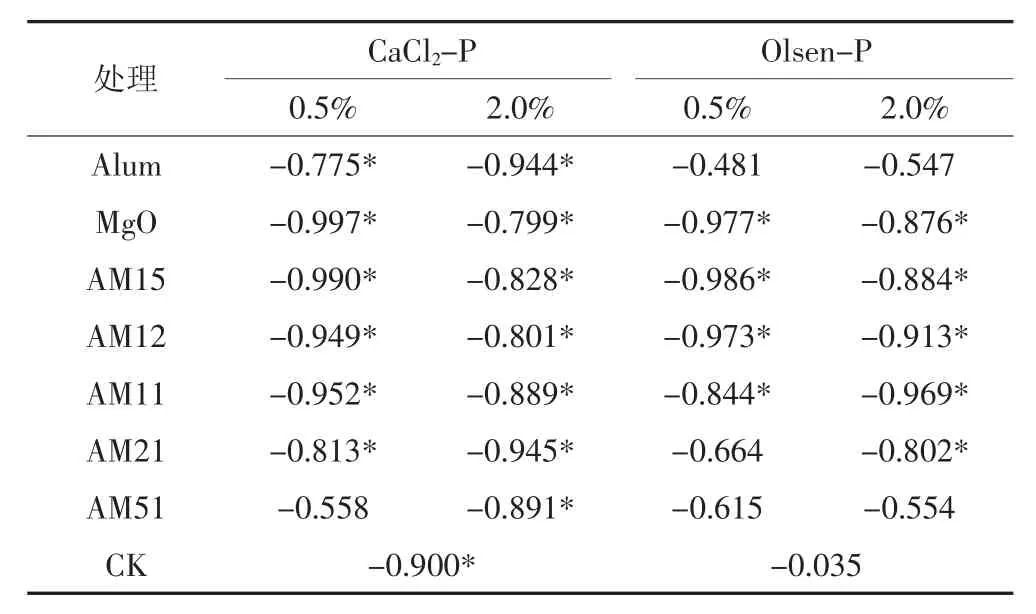
表5 培养不同时间的土壤CaCl2-P和Olsen-P含量与pH间的Pearson系数和显著性检验Table 5 Pearson coefficient and significance test of CaCl2-P content,Olsen-Pcontent and soil pH value in soil with thesame treatment at different incubatingdays
3.2 添加氧化镁和铵明矾对土壤Olsen-P的影响
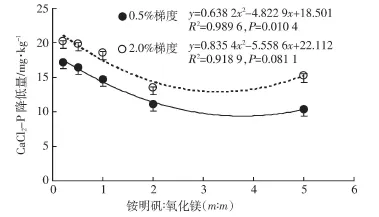
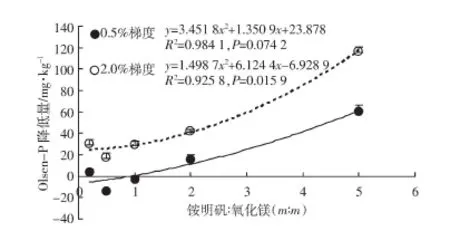
添加氧化镁、铵明矾或二者不同比例的混合物都能降低土壤Olsen-P含量。氧化镁降低土壤Olsen-P含量的原因可能是形成稳定态的镁磷,也有可能是土壤pH升高,与氧化镁表面-OH发生配位吸附的磷酸根由不稳定的单基配位向稳定的双基配位转化[26-27],从而难以被NaHCO3溶液浸提出来。而铵明矾降低石灰性土壤活性磷的原因主要是氢氧化铝胶体的吸附作用,磷素组分结果(图3)中NaHCO3-P的减少和NaOH-P含量的增加也说明活性态的磷向中稳定态的磷的转化。这与Moore等[28]结果一致,6 不同于CaCl2-P的结果,培养45 d后,添加铵明矾处理的土壤Olsen-P含量显著低于添加氧化镁的处理(图2)。该原因可能是氧化镁吸附的磷酸盐绝大部分存在于氧化镁的表面,碳酸氢钠溶液能够将其浸提出来。 从培养1 d到培养45 d,添加铵明矾处理Olsen-P含量基本维持不变。而添加氧化镁的处理的Olsen-P含量由 160 mg·kg-1回升到 213 mg·kg-1。 土壤pH与土壤Olsen-P含量间的Pearson系数和显著性检验(表5)说明施入钝化剂1 d后pH>8.0的处理,随着培养时间的延长,土壤中的Olsen-P含量与土壤pH值之间也呈现出了显著的负相关性。pH值的降低一方面使稳定态的镁磷释放,另一方面减弱氧化镁对于磷素的双基配位吸附,因此,活性磷被释放。 氧化镁和铵明矾在降低石灰性土壤CaCl2-P和Olsen-P含量的同时都会带来土壤pH的变化。将氧化镁和铵明矾按照不同比例混合后,可以有效缓解其对土壤pH的影响(表1)。 在0.5%添加梯度下培养45 d后,随着混合物中氧化镁比例的减少,降低土壤CaCl2-P的效果逐渐减弱。铵明矾与氧化镁的质量比与CaCl2-P降低量的回归分析表明(图4),随着混合物中铵明矾比例的增加,CaCl2-P降低量整体呈现二次非线性显著降低(P=0.010 4),但是有逐渐上升的趋势。在2.0%添加梯度下培养45 d后,随着混合物中铵明矾比例的增加,CaCl2-P的降低量先下降后升高(P=0.081,图4)。不同于0.5%添加梯度,2.0%添加梯度下,AM21处理降低CaCl2-P量最低,然后逐渐升高。等质量添加条件下,所有混合物处理对CaCl2-P的降低量均低于MgO处理,但是高于Alum处理,说明氧化镁和铵明矾混合后互相影响。图1结果表明,MgO降低CaCl2-P含量显著强于Alum,但是0.5%的添加梯度下,铵明矾添加量较少,对土壤pH影响不明显。因此,随着混合物中氧化镁的含量下降,CaCl2-P降低量逐渐减少。而在2.0%添加梯度下,AM21处理和AM51处理中铵明矾含量较多,土壤pH显著低于其他混合物处理,较低的pH破坏了氧化镁的结构,降低了氧化镁的吸附作用。土壤EC值的结果显示AM51处理的EC值高于Alum处理,也说明铵明矾溶解后产生的H+能够溶解一部分氧化镁。因此,AM21-H和AM51-H处理的CaCl2-P含量高于其他处理。氧化镁的结构被破坏后,铵明矾的作用就会凸显,因此AM51-H处理降低CaCl2-P的能力强于AM21-H处理。 对于土壤Olsen-P而言,图2结果表明铵明矾降低土壤Olsen-P的作用显著强于氧化镁。铵明矾与氧化镁的质量比与Olsen-P降低量的回归分析表明(图5),在0.5%和2.0%添加梯度下速效磷降低量整体随铵明矾和氧化镁比例的升高而显著增加,但是在2.0%梯度下相关性显著(P=0.016),而在0.5%梯度下二者相关性并不显著(P=0.074 2)。这主要是因为2.0%添加梯度氧化镁添加量较高,土壤pH较大。pH增大可能会导致OH-和Al(OH)3反应生成Al(OH)-4[15],减弱了对Olsen-P的固定能力。因此,在0.5%添加梯度和2.0%添加梯度下,土壤Olsen-P降低量出现了类似的规律,AM12处理降低土壤Olsen-P的效果最差。AM12和AM15、AM11处理的土壤pH值都超过了8.0,氢氧化铝胶体可能发生碱性电离[29-30],其吸附土壤活性磷的能力下降,AM15-H、AM12-H和AM11-H处理之间差异不显著。 尽管混合物处理降低土壤CaCl2-P和Olsen-P的能力弱于单一添加氧化镁或者铵明矾,但是合适配比的混合物不仅能显著降低土壤CaCl2-P和Olsen-P含量,而且能够有效缓解土壤pH的剧烈变化(表1)。 图4 土壤CaCl2-P的降低数量与添加的铵明矾与氧化镁质量比之间的回归分析Figure4 Regression analysisbetween thereduced amount of soil CaCl2 extracted Plevel and theadded ratiosof alum to MgOintosoil 图5 土壤Olsen-P降低数量与添加的铵明矾与氧化镁质量比之间的回归分析Figure5 Regression analysisbetween thereduced amount of soil Olsen-Plevel and theadded ratio of alumto MgOinto soil (1)氧化镁和铵明矾都能显著降低土壤CaCl2-P含量。培养45 d后,0.5%添加梯度的氧化镁和铵明矾分别降低了87.8%和44.4%的土壤CaCl2-P含量。而2.0%添加梯度固定Olsen-P的效果强于0.5%添加梯度。两种物质混合降低土壤CaCl2-P含量的能力弱于单施氧化镁。 (2)铵明矾固定土壤Olsen-P的能力强于氧化镁,培养45 d后,0.5%添加梯度的氧化镁和铵明矾分别降低了3.2%和13.2%的土壤Olsen-P含量。2.0%添加梯度固定Olsen-P的效果强于0.5%添加梯度。培养45 d后,AM12处理维持土壤Olsen-P的能力最强。 (3)氧化镁是一种既能显著降低土壤水溶性磷含量,又不影响土壤活性磷含量的物质。 [1]Zhang XS,Liao H,Chen Q,et al.Responseof tomatoon calcareoussoils to different seedbed phosphorus application rates[J].Pedosphere,2007,17(1):70-76. [2]郭金花.典型设施蔬菜生产系统水肥、农药投入及环境影响的生命周期评价[D].北京:中国农业大学,2016.GUOJin-hua.Inputsof irrigation water,fertilizer,pesticide and lifecycle assessment of environmental impacts in the typical greenhouse vegetablefieldsin China[D].Beijing:China Agricultural University,2016. [3]Rowe H,Withers PJA,Baas P,et al.Integratinglegacy soil phosphorus intosustainablenutrient management strategiesfor future food,bioenergy and water security[J].Nutrient Cyclingin Agroecosystems,2015,104(3):393-412. [4]鲁如坤.土壤磷素水平和水体环境保护[J].磷肥与复肥,2003,18(1):4-6.LURu-kun.The phosphorus level of soil and environmental protection of water body[J].Phosphate&Compound Fertilizer,2003,18(1):4-6. [5]赵少华,宇万太,张 璐,等.土壤有机磷研究进展[J].应用生态学报,2004,15(11):2189-2194.ZHAOShao-hua,YUWan-tai,ZHANGLu,et al.Research advance in soil organic phosphorus[J].Chinese Journal of Applied Ecology,2004,15(11):2189-2194. [6]Pautler M.Relationships between soil test phosphor us and soluble phosphorus saturation in Delaware soils[J].Soil Science Society of America Journal,2000,64(2):765-773. [7]刘建玲,廖文华,张作新,等.磷肥和有机肥的产量效应与土壤积累磷的环境风险评价[J].中国农业科学,2007,40(5):959-965.LIUJian-ling,LIAOWen-hua,ZHANGZuo-xin,et al.The responseof vegetable yield to phosphate fertilizer and organic manure and environmental risk assessment of phosphorus accumulated in soil[J].Scientia Agricultura Sinica,2007,40(5):959-965. [8]Dou ZX,Ramberg CF,Toth JD,et al.Phosphorusspeciation and sorption-desorption characteristicsin heavily manured soils[J].Soil Science Society of America Journal,2009,73(1):93-101. [9]Gérard F.Clay minerals,iron/aluminumoxides,and their contribution to phosphate sorption in soils:A myth revisited[J].Geoderma,2016,262:213-226. [10]梁玉英.城市菜地土壤磷的固定机制研究[D].北京:中国农业大学,2005.LIANG Yu-ying.Studies on the mechanism of phosphorus fixation in urban kailyard soil[D].Beijing:China Agricultural University,2005. [11]麻万诸,章明奎.改良剂降低富磷蔬菜地土壤磷和氮流失的作用[J].水土保持学报,2012,26(5):22-27.MA Wang-zhu,ZHANG Ming-kui.Effects of amendments to reduce runoff loss of phosphorus and nitrogen from a vegetable soil with high test phosphorus[J].Journal of Soil and Water Conservation,2012,26(5):22-27. [12]Liu W,Ji H,Kerr P,et al.The application of soil amendmentsbenefits tothereduction of phosphorusdepletion and thegrowth of cabbage and corn[J].Environmental Science&Pollution Research,2015,22(21):16772-16780. [13]姬红利,颜 蓉,李运东,等.施用土壤改良剂对磷素流失的影响研究[J].土壤,2011,43(2):203-209.JIHong-li,YAN Rong,LIYun-dong,et al.Effects of soil ameliorants on phosphorusloss[J].Soil,2011,43(2):203-209. [14]Novak JM,Watts D W.An alum-based water treatment residual can reduceextractablephosphorusconcentrations in threephosphorus-enriched coastal plain soils[J].Journal of Environmental Quality,2005,34(5):1820-1827. [15]Michael K M,Craig D S,Cheryl M,et al.Developing a remediation strategy for phosphorus immobilization:Effect of co-blending,Alresidual and Ca-Mg amendments in a manure-impacted spodosol[J].Soil&Sediment Contamination An International Journal,2011,20(4):337-352. [16]Rastija D,Zebec V,Rastija M.Impacts of liming with dolomite on soil reaction and availabilities of phosphorus and potassium[J].N觟vénytermelés,2014,63(Suppl):193-196. [17]Hedley MJ,Stewart JWB,Chauhan BS.Changesin inorganic and organic soil-phosphorusfractionsinduced by cultivation practicesand by laboratoryincubations[J].Soil Science Society of America Journal,1982,46(5):970-976. [18]Condron L M,Newman S.Revisiting the fundamentals of phosphorus fractionation of sediments and soils[J].Journal of Soils and Sediments,2011,11(5):830-840. [19]Negassa W,Leinweber P.How does the Hedley sequential phosphorus fractionation reflect impactsof land use and management on soil phosphorus:A review[J].Journal of Plant Nutrition and Soil Science,2010,172(3):305-325. [20]Olsen SR,Cole CV,Watanabe FS,et al.Estimation of availablephosphorus in soils by extraction with sodium bicarbonate[J].USDA Circular,1954,939,1-19. [21]Schofield R.Can a precise meaning be given to"available"soil phosphorus[J].Soilsand Fertilizers,1955,18:373-375. [22]赖胜强,林亲铁,项江欣,等.氧化镁基固化剂对铅离子的吸附作用及其影响因素[J].环境工程学报,2016,10(7):3859-3865.LAISheng-qiang,LINQin-tie,XIANGJiang-xin,et al.Adsorption of Pb2+on a magnesia-based curing agent and its influencing factors[J].Chinese Journal of Environmental Engineering,2016,10(7):3859-3865. [23]王素平.高活性氧化镁的制备与吸附性能的研究[D].天津:天津大学,2015.WANG Su-ping.Study on the synthesis and adsorption properties of high active MgO[D].Tianjin:Tianjin University,2015. [24]赵玉萍.土壤化学[M].北京:中国农业大学出版社,1991:283-285.ZHAO Yu-ping.Soil chemistry[M].Beijing:China Agricultural University Press,1991:283-285. [25]Wang WD,Ma C,Zhang Y T,et al.Phosphateadsorption performance of a novel filter substrate made fromdrinking water treatment residuals[J].Journal of Environmental Sciences,2016,45(7):191-199. [26]夏汉平,高子勤.磷酸盐在白浆土中的吸附与解吸特性[J].土壤通报,1992,23:283-287.XIA Han-ping,GAOZi-qin.Adsorption-desorption behaviorsof phosphate in Baijiang soil[J].Chinese Journal of Soil Science,1992,23:283-287. [27]刘 凡,介晓磊,贺纪正,等.不同pH条件下针铁矿表面磷的配位形式及转化特点[J].土壤学报,1997(4):367-374.LIU Fan,JIE Xiao-lei,HE Ji-zheng,et al.Coordination forms and transformations of phosphate adsorbed by goethite surface on different pH[J].Acta Pedologica Sinica,1997(4):367-374. [28]Moore P A,Miller D M.Decreasing phosphorus solubility in poultry litter with aluminum,calciumand iron amendments[J].Journal of Environmental Quality,1994,23(2):325-330. [29]Hsu P H. Comparison of iron(Ⅲ)and aluminum in precipitation of phosphate from solution[J]. Water Research, 1976, 10(10):903-907. [30]Hsu P H. Comparison of iron(Ⅲ)and aluminum in precipitation of phosphate from solution[J]. Water Research, 1976, 10(10):903-907.[30] Lewandowski J, Schauser I, Hupfer M. Long-term effects of phosphorus precipitations with alum in hypereutrophic Lake Süsser See(Germany)[J]. Water Research, 2003, 37(13):3194-3204.3.3 氧化镁和铵明矾不同配比的混合物对于土壤CaCl2-P和Olsen-P的影响
4 结论
