五种氮杂查尔酮的1H-NMR波谱分析
2018-05-28王新兵赵文彬吴林文王俊淇王航宇
王新兵,赵文彬*,吴林文,王俊淇,王航宇
(石河子大学药学院,新疆 石河子 832002)
查尔酮(chalcone),具有 1,3-二苯基丙烯酮的结构,是黄酮类化合物中的重要类型,有关查尔酮的提取、合成、谱图分析及药理活性研究的报道[1-3]非常多。本文讨论的氮杂查尔酮,为查尔酮B环杂合了两个氮原子的系列衍生物,查尔酮和氮杂查尔酮类化合物的结构、编号如图1所示。

图1 查尔酮、氮杂查尔酮结构及其编号Fig.1 The structure of chalcones and azachalcones,and their numbering and naming
按之前研究的合成方法[4],丰富了相应化合物的品种;由于所合成的化合物与已有文献中报道的查尔酮类化合物在母核中增加了杂环并合的结构特征,希望将结构改造后相应的核磁共振图谱特性进行研究。
将合成出的氮杂查尔酮所测得的氢核磁共振的化学位移与文献值、计算机结构绘制和图谱分析软件(Chemoffice 2006)模拟分析结果对比,用以比较和研究该类化合物的核磁共振图谱特征,前文[5]已将该类化合物的碳核磁共振数据及规律进行了报道,本文主要研究其氢谱出峰位置、顺序和规律,进一步确证所合成化合物的结构,并丰富该类化合物的波谱数据。
1 材料与方法
1.1 材料
NMR使用Bruker 400 Uhrashield型核磁共振仪,测定溶剂为色谱纯的氘代二甲基亚砜,TMS为内标;巴比妥酸购自Aldrich公司,其余试剂为国产分析纯试剂。
1.2 方法
1.2.1 合成及NMR测定
见文献[5],增补化合物V的合成及相应数据在2017年补足。
1.2.2 文献值
依据文献[6-7],实测氮杂查尔酮中A环及中间三碳链中α-H、β-H的1H-NMR化学位移可与之对应进行分析;B环数据可用电脑模拟数据比较分析。
1.2.3 电脑模拟计算
在电脑中安装office 2010及chemoffice2006程序,使用chemoffice2006程序组中的chemdraw ultra 10.0程序,将相关化合物结构绘制后,模拟分析出各化合物氢核磁共振图谱和数据,并将模拟图和数据拷贝到office 2010中的word2010程序。
2 结果
2.1 氮杂查尔酮
根据设计的合成路线,得到了以下结构的5个化合物(表 1)。
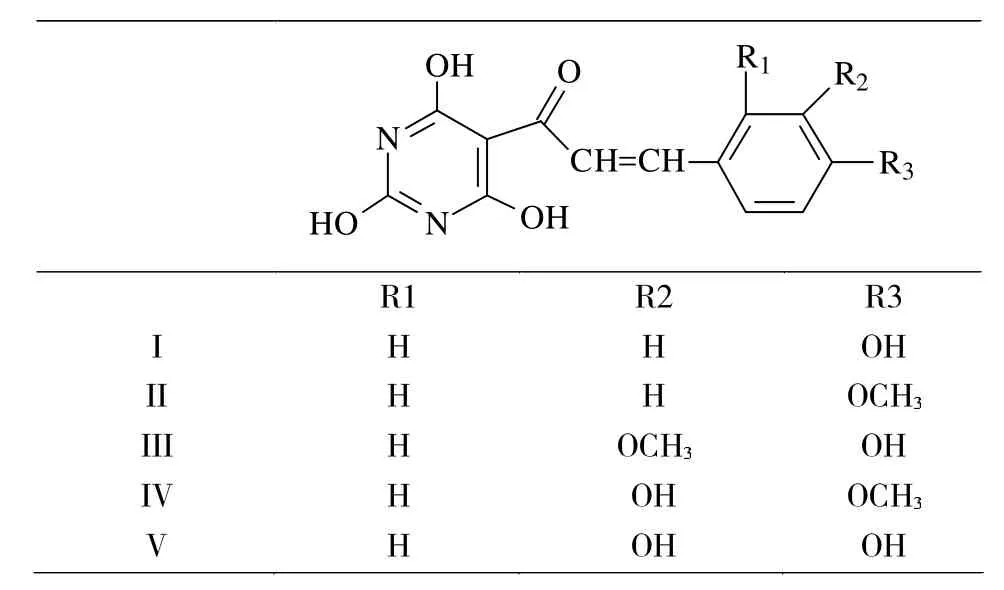
表1 化合物结构 I-VTab.1 The structure of compound I-V
2.2 所合成氮杂查尔酮氢核磁共振数据
将合成所得化合物实测氢谱汇总(表2)。

表2 合成氮杂查尔酮氢核磁共振化学位移 ppmTab.2 the1H-NMR chemical shift of azachalcones
2.3 计算机模拟氮杂查尔酮和查尔酮氢核磁共振数据

图2 五种氮杂查尔酮的计算机模拟化学位移值Fig.2 the granted 1H-NMR chemical shift of five azachalcones emulated by computer estimation(ppm)
将合成所得化合物用chemdraw ultra 10.0程序绘制,并得出如下图谱数据(图2)。将五种对应查尔酮用chemdraw ultra 10.0程序 绘制,并得出下图(图3)图谱数据
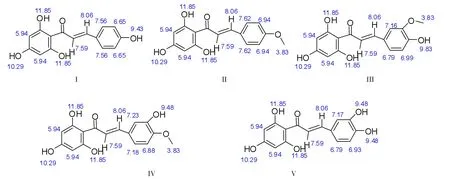
图3 五种查尔酮的计算机模拟化学位移值(ppm)Fig.3 The granted1H-NMR chemical shift of five chalcones emulated by computer estimation
3 讨论
从实测图谱(表2)的数据可以看出,合成出化合物的核磁共振氢谱的出峰位置、积分关系和偶合情况与设计得目标化合物结构一一对应,基本可以确证化合物的结构。将所测得数据分别与文献[6-7]中的不含氮杂结构查尔酮数据、计算机模拟所得数据对比分析,可以分中间三碳链、A环和B环出峰情况三部分讨论如下。
3.1 中间三碳链
根据文献中的对应查尔酮的数据[6]可知,α-H在 6.7-7.4 ppm,β-H在7.3-7.7 ppm,与图 2中计算机模拟数据(α-H在6.7 ppm,β-H在7.7 ppm)相符却比杂合了氮原子之后所测得化合物的数据(α-H在 7.82-7.93 ppm,β-H在 8.22-8.31 ppm)相比较小,差值约为0.5-1ppm,说明杂合了氮原子后对中间三碳链的化学环境有了一定影响;将所测化合物数据与计算机模拟结果(图3)α-H在7.59 ppm,β-H在8.06 ppm比较,实测结果的出峰位置又偏小,但偏离程度明显较小(约0.2-0.3 ppm),且偶合常数情况与化合物原本的结构情况相符,为16 Hz左右。
综合以上的分析,说明所合成的化合物中间三碳链的结果与预测目标化合物的氮杂查尔酮更匹配,B环的氮杂合对该部分结构化学环境有一定影响。
3.2 A环
文献[6]中,A环与合成化合物的情况近似,有以下两种情况。
3.2.1 4-氧取代查尔酮(对应化合物I和化合物II)
文献中:对应查尔酮的2,6-H在7.4-7.6 ppm,3,5-H在6.5-7.1 ppm,与模拟图谱对照数据相符;与 所 测 得 的 2,6-H 在 7.58-7.69ppm,3,5-H 在6.87-7.06 ppm也相符,且偶合常数大小也适合。
3.2.2 3,4-二氧取代查尔酮(对应化合物III-V)
文献中,对应查尔酮的5-H在6.7-7.1 ppm(J=8.5 Hz),2和 6-H信号重叠,在 7.2-7.9 ppm之间,与图2中计算机模拟数据基本相符,但6-H(模拟数为6.79-7.18 ppm)略有出入;与所测得的2-H为 7.18-7.26ppm,6-H 在 7.06-7.23ppm,5-H 在6.83-7.02 ppm情况相符,且偶合常数大小也适合。
考虑到早期文献数据都是由100MHz的核磁共振仪所采集的相对复杂的图谱分析而来,且使用的溶剂也有区别。基本可以认定3种方式采集的数据在A环方面具有很好的一致性,说明在B环有杂合结构,对于A环的化学环境几乎没有影响,亦可以通过图2和图3中A环中相应化合物数据完全一致说明这种情况。
3.3 B环
因所合成化合物B环杂合了两个氮原子,和文献情况不符,故这里只能与计算机模拟数值进行比较。
与图2的计算机模拟结果对比说明,不管A环上如何取代变化,四个化合物B环上2′,6′-OH均在11.40 ppm,4′-OH均在 11.34 ppm(相应不含氮杂图 3 的相应数据为 2′,6′-OH 均在 11.85 ppm,4′-OH均在 10.29 ppm);而实测数据显示,2′或 6′-OH 在 11.69-11.74 ppm,4′-OH 在 11.05-11.08 ppm,出峰位置2′,6′-OH比模拟分析结果大了约0.3ppm,而 4′-OH比模拟分析结果小了约0.3ppm。综合比较来看,实测结果与图2相应结果更接近,且2′或6′-OH总是结构的情况少一个-OH的峰的积分,进而与前文[5]对应碳谱的数据对照分析和讨论,认为可能是发生了如下的互变异构,仅显示出 2′-OH 的峰,6′-OH转化为羰基(图 4)。

图4 氮杂查尔酮的互变异构分析Fig.4 Analysis the tautomerization of azachalcone
4 结论
通过五种合成化合物所测得的核磁共振氢谱与文献和计算机程序chemdraw模拟结果比照,确证了相应目标化合物结构,明确了该类化合物在发生芳环氮原子杂合后出现的核磁共振氢谱的规律性变化。通过数据的比较,发现实测所得数据在B环被氮原子杂合后,A环氢核磁共振数据呈现了与不杂合相应化合物有很好的一致性;而中间三碳链中α-H和β-H的化学环境受到了一定程度的影响;B环则会因互变异构的因素少一个OH的峰的积分,且与已有文献不含杂原子相应查尔酮数据有了一定差距,出峰位置比对应氮杂化合物模拟分析结果也分别变化了0.2-0.3 ppm。
通过用实测数据和文献及用电脑程序模拟结果印证的方式,用来研究和推测新的或未知化合物的核磁共振图谱及相关规律,可以相对较为清晰的明确其中的细节,便于研究的开展。
但是这种研究方式对于复杂未知化合物(如生物大分子、多环并合或具有不常见重金属离子络合的有机化合物等),可能存在研究的盲点,毕竟文献及计算机模拟的方式还有未涉及没有预见到的死角,另外随着研究的深入和数据的丰富,并伴随着计算机程序的更新,这些相应的缺陷会有所弥补。而通过相应化合物氢核磁共振谱图和碳核磁共振谱图的协同研究或进而研究其二维核磁共振图谱,可以补足相应化合物的谱图数据和早期已报道文献的一些数据,为研究类似化合物的图谱规律及结构确证,提供线索和经验。
[1]廖头根,汪秋安,方伟琴,等.新型查尔酮类化合物的合成及其生物活性研究[J].有机化学,2006,26(5):685-689.Liao T G,Wang Q A,Fang W Q,et al.Studies on the synthesis of novel chalcone and biological activity[J].Organic Chemistry,2006,26(5):685-689.
[2]胡志国,刘军,李工安,等.SOC12-EtOH催化查尔酮的合成Ⅲ[J].化学研究与应用,2004,16(4):583-584.Hu Z G,Liu J,Li G A et al.Synthesis of chalcone Catalyzed by SOC12-EtOHⅢ[J].Chemical research and application,2004,16(4):583-584.
[3]陈欣华.明日叶中查尔酮提取方法的探讨及营养成分的分析[D].2014,河北:河北联合大学.
[4]王新兵.噢哢类化合物的合成及结构鉴定[D].2003,西安交通大学,药物分析:29-30.
[5]王新兵,邓喜玲,王航宇等.四种氮杂查尔酮的13C-NMR波谱分析[J].石河子大学学报(自然科学版),2016,34(6):752-755.Wang X B,Deng X L,Wang H Y etc.Spectrum analysis of 13C-NMR chemical shift of the four aza-aurones[J].Journal of Shihezi University(Nature Science),2016,34(6):752-755.
[6]中国科学院上海药物研究所植物化学研究室编译.黄酮体化合物鉴定手册[M].上海:科学出版社,1981.
[7]关丽萍,尹秀梅,全红梅,等.羟基查尔酮类衍生物的合成[J].有机化学,2004,24(10):1274-1277.Guan L P,Yin X M,Quan H M et al.Synthesis of hydroxy chalcone derivatives[J].Organic Chemistry,2004,24(10):1274-1277.
