一测多评法测定牛黄上清系列制剂中7种成分的含量
2018-05-23吕佳佳周昌艳韦恋祝
吕佳佳,王 莎,周昌艳,韦恋祝
(遵义医学院 药学院药剂学教研室,贵州 遵义 563099)
牛黄上清系列制剂是中医治疗实热证的经典方剂,由人工牛黄、薄荷、菊花、荆芥穗、白芷、川芎、栀子、黄连、黄柏、黄芩、大黄、赤芍等19味药材组成,具有清热泻火,祛风止痛等功效[1-4]。临床上常用于热毒内盛、风火上攻所致的头痛眩晕、目赤耳鸣、咽喉肿痛和大便燥结等。牛黄上清系列制剂质量标准收载于《中国药典》2015版第一部[5]。现行药典仅对栀子苷、黄芩苷和大黄素进行含量测定,由于复方中药药效的发挥通常是多成分共同作用的结果,决定了单一成分或少数成分难以表达整个复方的内在质量。因此,应选择多成分、多指标进行同时测定,对与功效相关的成分进行综合评价。本复方中川芎、当归、黄连、黄柏、赤芍、地黄等同为重要药味,应该对其主要活性成分进行检测,为全面控制牛黄上清系列制剂的质量提供科学依据。
由于多指标的质量控制模式对对照品的种类以及数量需求较大,同时存在部分对照品不易获得且检测成本高等问题。王智民等[6]提出一测多评的多指标质控模式,在多指标质量评价时,以样品中价廉易得的对照品为内标,建立该成分和其他成分之间的相对校正因子,通过相对校正因子计算其他成分的含量。目前已成功应用于三七、虎杖、枳实、银翘解毒系列制剂等的质量控制[7~11],且黄连药材的一测多评法被《中国药典》2010版收录。因此本实验使用一测多评法,以栀子苷为内参物,计算芍药苷、毛蕊花糖苷、阿魏酸、黄芩苷、盐酸小檗碱和大黄素的相对校正因子,建立牛黄上清系列制剂的一测多评法,为其质量控制提供新的评价模式。
1 材料与方法
1.1 药品与试剂 芍药苷(批号151120,质量分数98%)、毛蕊花糖苷(批号160526,质量分数98%)、阿魏酸(批号16011402,质量分数98%)、盐酸小檗碱(批号131128,质量分数98%)、栀子苷(批号16121202,质量分数98%)、黄芩苷(批号16092401,质量分数98%)、大黄素(批号17042501,质量分数98%),均购于成都普菲德生物技术有限公司。牛黄上清片(批号20161111,密之康药业有限公司),牛黄上清片(批号161201,百泉制药有限公司),牛黄上清片(批号170146,佐今明制药有限公司),牛黄上清片(批号170118,巢湖今辰药业有限公司),牛黄上清胶囊(批号170204,天施康弋阳制药有限公司),牛黄上清丸(批号160132,御生堂集团石家庄制药有限公司),牛黄上清丸(批号160218,中新药业股份有限公司),牛黄上清丸(批号16015329,同仁堂股份有限公司)。甲醇、乙睛为色谱纯,水为超纯水,其余试剂均为分析纯。
1.2 仪器 Agilent 1260型高效液相色谱系统,Agilent Chemstation工作站(美国Agilent公司),Thermo Scitific Ultimate 3 000高效液相色谱系统,Xcalibur工作站(美国Thermo公司),Waters 2695-2996型高效液相色谱系统,Empower工作站(美国Waters公司);色谱柱:Agilent Eclipse C18色谱柱(250 mm×4.6 mm,5 μm),Diamonsil Plus C18色谱柱(250 mm×4.6 mm,5 μm),Thermo Hypersil C18色谱柱(250 mm×4.6 mm,5 μm),Unitary C18色谱柱(250 mm×4.6 mm,5 μm),Hedera C18色谱柱(250 mm×4.6 mm,5 μm);BT125D型分析天平[赛多利斯科学仪器(北京)有限公司]; DL-820D型智能超声波清洗器(上海之信仪器有限公司);DURA12纯水机(上海和泰仪器有限公司)。
1.3 方法
1.3.1 色谱条件 采用Diamonsil Plus C18色谱柱(250 mm×4.6 mm,5 μm),流动相为乙腈-0.1%磷酸水溶液,梯度洗脱程序为0~4 min,5%~20%乙腈;4~25 min,20%~40%乙腈;25~33 min,40%~85%乙腈;33~41 min,85%~5%乙腈;流速为1.0 mL/min;分段变波长测定,0~11 min为230 nm(栀子苷和芍药苷),11~14 min为 334 nm(毛蕊花糖苷和阿魏酸),14~25 min为280 nm(黄芩苷和盐酸小檗碱),25~35 min为254 nm(大黄素);柱温37 ℃;进样量10 μL。
1.3.2 对照品的制备 精密称取栀子苷、芍药苷、毛蕊花糖苷、阿魏酸、黄芩苷、盐酸小檗碱、大黄素对照品适量,分别置于25 mL容量瓶中,加甲醇溶解并定容至刻度,制备成质量浓度分别为栀子苷0.420 mg/mL、芍药苷0.540 mg/mL、毛蕊花糖苷0.416 mg/mL、阿魏酸0.448 mg/mL、黄芩苷0.392 mg/mL、盐酸小檗碱0.408 mg/mL、大黄素0.408 mg/mL的对照品储备液,备用。再精密吸取毛蕊花糖苷、阿魏酸、盐酸小檗碱储备液各4 mL,其余各对照品储备液3 mL于25 mL量瓶中,加甲醇定容至刻度,制得混合对照品溶液,4 ℃避光保存,备用。
1.3.3 供试品溶液的制备 将牛黄上清片剂去糖衣,研细(过40目筛),取约0.5 g,胶囊剂取10粒内容物混匀后取约0.5 g,置具塞锥形瓶中,精密加入70%甲醇50 mL,称定重量,超声处理(功率500 W,频率40 kHz)30 min,放冷称定重量,用70%甲醇补足减失重量,摇匀过滤,滤液定容至50 mL容量瓶中。丸剂剪碎后,取约1.0 g,精密称定后置圆底烧瓶中,精密加入70%甲醇50 mL,称定重量,加热回流1 h,放冷称定重量,用70%甲醇补足减失重量,摇匀过滤,滤液定容至50 mL容量瓶中。
1.3.4 阴性对照溶液的制备 按照牛黄上清片的处方比例和制备工艺,制备缺少川芎、当归、黄连、黄柏、赤芍、地黄药材的阴性对照样品溶液,并按照“1.3.1”项下色谱条件进行测定。
1.3.5 专属性实验 分别精密吸取“1.3.2”项下混合对照品溶液、“1.3.3”项下供试品溶液、“1.3.4”项下阴性对照品溶液,按照“1.3.1”项下色谱条件进行分析。
1.3.6 线性关系的考察 精密吸取上述混合对照品溶液0.5、1.0、1.5、2.0、3.0、5.0、7.0 mL于10 mL容量瓶中,加甲醇定容至刻度,摇匀,得系列混合对照品溶液,按照“1.3.1”项下色谱条件进行测定。
1.3.7 精密度试验 精密吸取混合对照品溶液10 μL,在“1.3.1”项下色谱条件下连续进样6次,测得栀子苷、芍药苷、毛蕊花糖苷、阿魏酸、黄芩苷、盐酸小檗碱和大黄素的峰面积,计算各组峰面积的RSD值。
1.3.8 重复性试验 取今辰药业生产的牛黄上清片粉末0.5 g,平行6份,精密称定后按“1.3.3”项下供试品溶液制备方法进行制备,精密吸取各供试品溶液10 μL,依法测定,计算栀子苷、芍药苷、毛蕊花糖苷、阿魏酸、黄芩苷、盐酸小檗碱和大黄素质量分数的RSD值。
1.3.9 稳定性试验 精密吸取同一供试品溶液10 μL,分别于配制后的0、4、8、12、24、36 h测定各成分的峰面积,计算栀子苷、芍药苷、毛蕊花糖苷、阿魏酸、黄芩苷、盐酸小檗碱和大黄素峰面积的RSD值。
1.3.10 加样回收率试验 取同一批已知含量的今辰牛黄上清片粉末(过40目筛)约0.5 g,平行6份,精密称定,分别加入一定量的对照品溶液,按“1.3.3”项下供试品溶液制备方法进行制备,精密吸取上述供试品溶液10 μL,依法测定,计算各成分的回收率。
1.3.11 相对校正因子的确定
1.3.11.1 牛黄上清制剂中待测成分相对校正因子的计算 在牛黄上清制剂的多指标质量评价时,以制剂中栀子苷为内标物,建立栀子苷与芍药苷、毛蕊花糖苷、阿魏酸、黄芩苷、盐酸小檗碱、大黄素之间的相对校正因子,根据相对校正因子计算公式 (Ck、Ak分别为内参物对照品的质量分数和峰面积,Cm、Am分别为待测成分对照品的质量分数和峰面积),计算栀子苷对芍药苷、毛蕊花糖苷、阿魏酸、黄芩苷、盐酸小檗碱、大黄素的相对校正因子。
1.3.11.2 相对校正因子重现性考察 在“1.3.1”项色谱条件下,精密吸取混合对照品溶液10 μL,采用Agilent 1260液相色谱系统,分别考察5种不同品牌的色谱柱Agilent Eclipse C18、Diamonsil Plus C18、Unitary C18、Hypersil C18、Hedera C18色谱柱;同时采用Agilent Eclipse C18色谱柱,分别考察Agilent 1260、Waters 2695-2996和Thermo Scitific Ultimate 3000 高效液相色谱仪对相对校正因子的影响。
1.3.12 待测组分色谱峰的定位 利用相对保留时间Rm/k进行色谱峰定位,(m为待测组分,k为内参物),通过计算在不同液相色谱系统和不同色谱柱中各待测成分色谱峰和栀子苷色谱峰的相对保留时间,对各种待测成分进行定位。
1.3.13 一测多评法和外标法结果比较研究 为验证一测多评法的准确性,考察使用外标法和一测多评法分别测定牛黄上清片(密之康、百泉、佐今明、巢湖今辰药业有限公司),牛黄上清胶囊(天施康弋阳制药有限公司),牛黄上清丸(御生堂、中新、同仁堂股份有限公司)中栀子苷、芍药苷、毛蕊花糖苷、阿魏酸、黄芩苷、盐酸小檗碱、大黄素的含量。
2 结果
2.1 专属性试验 测得色谱图如图1所示,供试品溶液中各待测成分色谱峰的分离度均大于1.5,峰形良好,阴性样品溶液在7个目标成分的色谱峰位置均无吸收,表明方法专属性良好。


1:栀子苷;2:芍药苷;3:毛蕊花糖苷;4:阿魏酸;5:黄芩苷;6:盐酸小檗碱;7:大黄素。A:对照品溶液;B:供试品溶液;C:阳性样品溶液。图1 4种样品溶液的HPLC色谱图
2.2 线性关系的考察 将系列混合对照品溶液按照“1.3.1”项下色谱条件进行测定,以对照品质量浓度为横坐标(X),峰面积为纵坐标(Y)进行线性回归,得到7个成分的标准曲线方程,相关系数(r)和线性范围,结果(见表1)。
表1牛黄上清系列制剂中7种成分的线性方程及范围
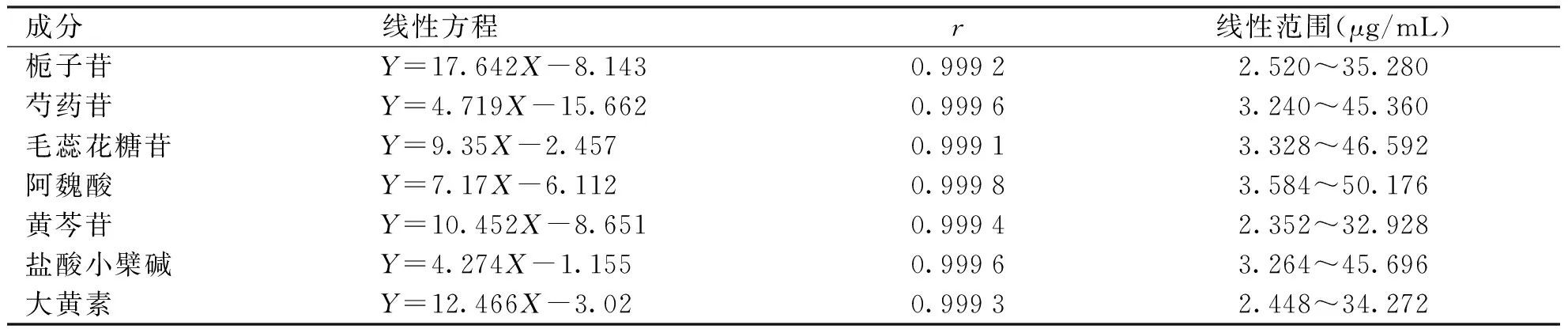
成分线性方程r线性范围(μg/mL)栀子苷Y=17.642X-8.1430.99922.520~35.280芍药苷Y=4.719X-15.6620.99963.240~45.360毛蕊花糖苷Y=9.35X-2.4570.99913.328~46.592阿魏酸Y=7.17X-6.1120.99983.584~50.176黄芩苷Y=10.452X-8.6510.99942.352~32.928盐酸小檗碱Y=4.274X-1.1550.99963.264~45.696大黄素Y=12.466X-3.020.99932.448~34.272
2.3 精密度、重复性、稳定性试验 根据各测定结果计算栀子苷、芍药苷、毛蕊花糖苷、阿魏酸、黄芩苷、盐酸小檗碱和大黄素的RSD(n=6)值。结果见表2,表明仪器精密度良好,同时供试品溶液在36 h内稳定性良好,该方法的重复性良好。
表2精密度、重复性、稳定性试验结果(%,n=6)
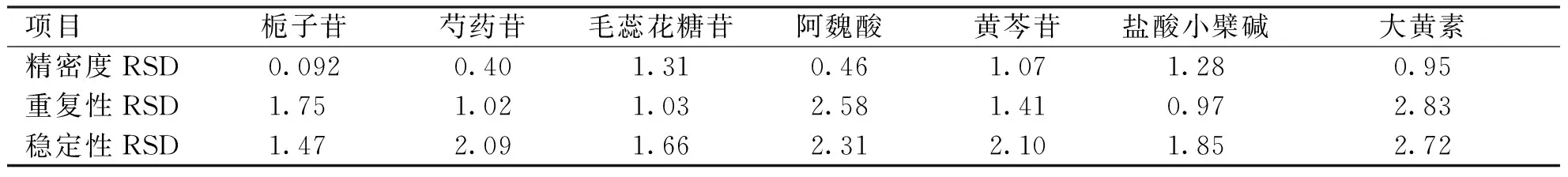
项目栀子苷芍药苷毛蕊花糖苷阿魏酸黄芩苷盐酸小檗碱大黄素精密度RSD0.0920.401.310.461.071.280.95重复性RSD1.751.021.032.581.410.972.83稳定性RSD1.472.091.662.312.101.852.72
2.4 加样回收率试验 将制备的加样回收供试品溶液按照“1.3.1”项下色谱条件进行测定,计算栀子苷、芍药苷、毛蕊花糖苷、阿魏酸、黄芩苷、盐酸小檗碱和大黄素的加样回收率分别为98.14%、96.68%、95.35%、99.24%、97.03%、101.29%、95.88%,RSD分别为1.94%、2.33%、2.09%、1.86%、2.51%、1.92%、2.75%,表明方法的准确性良好。
2.5 相对校正因子的确定

表3芍药苷、毛蕊花糖苷、阿魏酸、黄芩苷、盐酸小檗碱、大黄素的相对校正因子
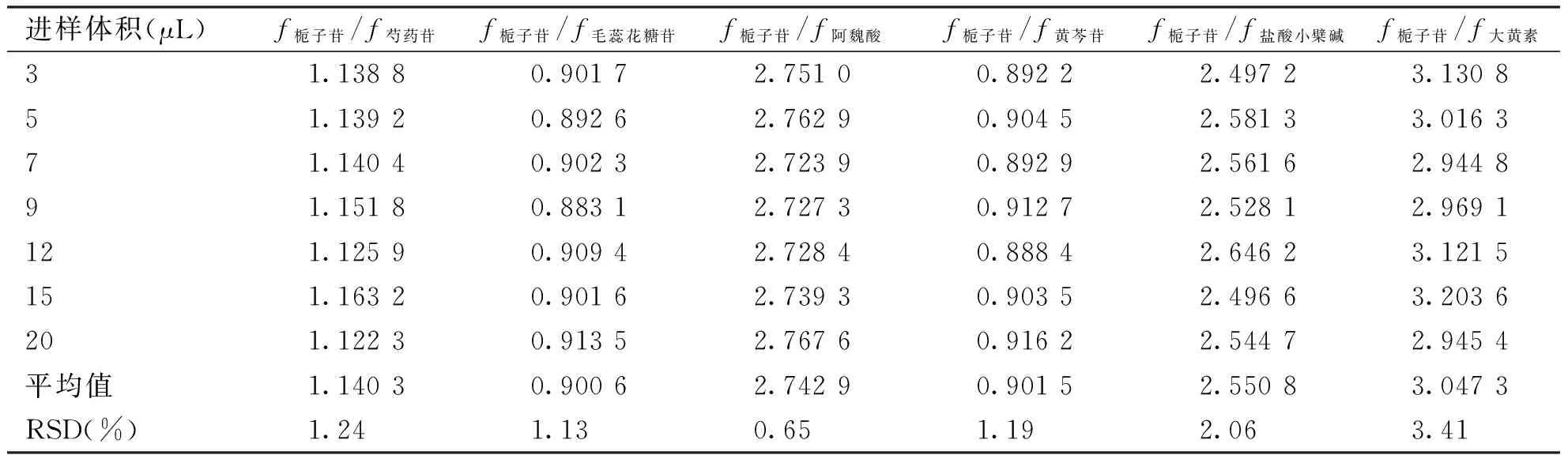
进样体积(μL)f栀子苷/f芍药苷f栀子苷/f毛蕊花糖苷f栀子苷/f阿魏酸f栀子苷/f黄芩苷f栀子苷/f盐酸小檗碱f栀子苷/f大黄素31.13880.90172.75100.89222.49723.130851.13920.89262.76290.90452.58133.016371.14040.90232.72390.89292.56162.944891.15180.88312.72730.91272.52812.9691121.12590.90942.72840.88842.64623.1215151.16320.90162.73930.90352.49663.2036201.12230.91352.76760.91622.54472.9454平均值1.14030.90062.74290.90152.55083.0473RSD(%)1.241.130.651.192.063.41
2.5.2 相对校正因子重现性考察 不同色谱柱和高效液相色谱仪相对校正因子重现性考察结果见表4,表明各成分相对校正因子重现性良好(RSD<5%)。
表4相对校正因子重现性考察

仪器色谱柱f栀子苷/f芍药苷f栀子苷/f毛蕊花糖苷f栀子苷/f阿魏酸f栀子苷/f黄芩苷f栀子苷/f盐酸小檗碱f栀子苷/f大黄素AgilentDiamonsilC181.16290.91722.72450.91392.54033.1474UnitaryC181.13590.89622.70450.90422.58423.1381HypersilC181.14830.92282.75880.90492.59022.9563HederaC181.15070.90392.70160.88772.62143.2047AgilentC181.13290.87962.76030.92372.50012.9198WatersAgilentC181.12140.91052.74860.91442.53242.9945DionexAgilentC181.13560.88612.72440.89832.47673.0932平均值1.14110.90232.73180.90672.54933.0649RSD(%)1.201.770.901.312.033.53
2.6 待测组分色谱峰的定位 各种待测组分色谱峰的定位结果(见表5),表明相对保留时间的波动较小(RSD≤5%)。
表5不同色谱仪和色谱柱测得的相对保留时间

仪器色谱柱f栀子苷/f芍药苷f栀子苷/f毛蕊花糖苷f栀子苷/f阿魏酸f栀子苷/f黄芩苷f栀子苷/f盐酸小檗碱f栀子苷/f大黄素AgilentDiamonsilC181.17271.35041.46612.11232.15554.2632UnitaryC181.16301.32111.47351.94792.18504.1040HypersilC181.17201.31981.50041.98212.15494.1960HederaC181.14711.25551.40891.93352.27394.1744AgilentC181.14561.30641.41021.94942.21564.0459 WatersAgilentC181.13621.25561.44841.99842.26304.1593DionexAgilentC181.12521.24611.47781.95792.27114.0026平均值1.15171.29361.45501.98312.21704.1351RSD(%)1.583.152.383.082.402.18
2.7 一测多评法和外标法结果比较研究 外标法和一测多评法测定不同来源牛黄上清系列制剂中7种成分的含量比较结果(见表6),表明两种方法在牛黄上清系列制剂中测得各成分的含量基本一致。因此,一测多评法可以成功应用于牛黄上清系列制剂的含量测定。
表6不同来源牛黄上清系列制剂中7种成分的含量比较(mg/g)

来源栀子苷a芍药苷ab毛蕊花糖苷ab阿魏酸ab黄芩苷ab盐酸小檗碱ab大黄素ab同仁堂上清丸3.8270.4270.4282.8662.8410.5060.4965.8735.6582.1682.2050.1950.187御生堂上清丸3.5190.3900.3922.6302.6070.3920.3845.4135.2141.9842.0180.1830.175中新上清丸3.8390.4310.4322.9412.9150.3850.3775.9515.7332.3372.3770.1940.185百泉上清片3.8270.4270.4292.9442.9180.3770.3705.8955.6792.1922.2290.1930.185密之康上清片3.8860.4360.4382.9752.9490.3730.3655.8305.6162.2232.2600.2030.194今辰上清片3.7480.4630.4653.0062.9800.3950.3865.9475.7292.2942.3330.2020.193佐今明上清片3.8570.4400.4422.9282.9030.4580.4495.9415.7232.2282.2660.1980.189天施康上清胶囊3.8160.4540.4562.9932.9670.3790.3715.8925.6762.1592.1960.1950.187
a为外标法,b为一测多评法。
3 讨论
牛黄上清系列制剂属于中药复方制剂,含有十九味中药,成分十分复杂并且不同剂型间生产工艺以及辅料的不同导致采用一测多评法比测定单一药材的难度大。本研究首先考察了甲醇-水、甲醇-0.1%冰醋酸水、甲醇-0.1%磷酸水、乙腈-水、乙腈-0.1%冰醋酸水、乙腈-0.1%磷酸水等流动相洗脱系统,综合考察分离度、峰形、基线噪音等因素,结果表明,在乙腈-0.1%磷酸水的色谱条件下,牛黄上清系列制剂具有良好的色谱行为。
栀子苷、芍药苷、毛蕊花糖苷、阿魏酸、黄芩苷、盐酸小檗碱和大黄素是牛黄上清系列制剂的主要活性成分,与牛黄上清系列制剂的功效具有相关性,是评价牛黄上清系列制剂质量的适宜指标。其中栀子苷化学性质稳定并且价廉易得,在制剂中含量相对较高,对照品的制备工艺也较为成熟,因此选择其为内参物,便于降低检测成本。
预实验时,通过查阅文献初步拟定7个成分采用同一检测波长254 nm,结果发现芍药苷的灵敏度极低。为使各个成分都在其最大吸收波长下进行检测,对混合对照品溶液中各个成分进行紫外扫描以获得最大吸收峰。采用分段变波长的检测方式对7种化学成分进行测定,结合各成分出峰时间的差异,在0~11 min设定检测波长为230 nm,以测定栀子苷和芍药苷,11~14 min设定检测波长为334 nm,以测定毛蕊花糖苷和阿魏酸,14~25 min设定检测波长为280 nm,以测定黄芩苷和盐酸小檗碱,25~35 min设定检测波长为254 nm以测定大黄素。
文献报道采用一测多评法应满足相对校正因子接近1 的要求,而本研究中阿魏酸、盐酸小檗碱和大黄素的相对校正因子分别为2.74、2.55、3.05,上述3个成分的含量在外标法和一测多评法间的相对平均偏差分别是1.04%、0.84%、2.22%,两种方法的含量测定结果具有相似性。结果表明相对校正因子与1相差较大时,仍可采用一测多评法进行检测。
本实验建立的一测多评法可以成功用于药味繁多、成分复杂、剂型工艺和辅料不同的牛黄上清系列制剂的质量控制,为该系列制剂的质量标准统一奠定基础。
[参考文献]
[1] 李芳,陈显雄,秦裕辉,等. 牛黄上清胶囊及其丸剂药理作用的比较研究[J].中药药理与临床,1993,6(2):3-5.
[2] 杨长琴.HPLC法测定牛黄上清胶囊中栀子苷含量[J].2014,26(4):18-19.
[3] 师永清,师永花.双波长RP-HPLC法同时测定牛黄上清片中栀子苷和黄芩苷的含量[J].药物分析杂志,2011,31(8):1586-1588.
[4] 陶利,王玉娟,梁竹,等.HPLC法测定牛黄上清片中5种成分的含量[J].解放军药学学报,2014,30(2):138-141.
[5] 国家药典委员会.中华人民共和国药典(一部)[S].北京:中国医药科技出版社,2015:641-645.
[6] 王智民,高慧敏,付雪涛,等.“一测多评”法中药质量评价模式方法学研究[J].中国中药杂志,2006,31(23):1925-1928.
[7] 王超群,贾秀虹,陈季,等.中药三七“一测多评”质量控制方法的系统研究[J].中国中药杂志,2012,37(22):3438-3444.
[8] 范玲,严冬,李爽,等.一测多评法测定虎杖中虎杖苷、白藜芦醇、大黄素及大黄素甲醚的含量[J].中国实验方剂学杂志,2013,19(7):103-107.
[9] 陈建维,刘圆,刘晟楠,等.一测多评法测定枳实中4种黄酮类成分[J].中草药,2015,46(9):1374-1377.
[10]王俊俊,张俐,郭青,等.一测多评法测定8个银翘解毒系列制剂中的7种酚酸类成分的含量[J].药学学报,2015,50(4):480-485.
[11]何兵,刘艳,杨世艳,等.HPLC一测多评法同时测定双青咽喉片中10种成分[J].中草药,2013,44(8):974-981.
猜你喜欢
杂志排行
遵义医科大学学报的其它文章
- 纳米铜硅胶膜厚度对MAS-IUS控释效果影响的实验研究
- 宫颈套扎术在IB2/IIA2期局部晚期宫颈癌先期处理中的运用
- 白及蔗糖合酶基因结构与功能的生物信息学分析
- Asymmetric reduction of chroman-4-one and its derivate by whole cell of Pseudomonas plecoglossicida
- 金钗石斛在SD大鼠体内的药代动力学研究
- Effects of morroniside on oxidative stress and cardiomyocyte apoptosis in rats with acute myocardial infarction
