Fe2O3/硅藻土催化剂同时脱除煤气中气态Hg0和H2S
2018-05-22刘善和沈园园吴李瑞王乐强
刘善和,沈园园,吴李瑞,王 佳,王乐强
(安徽国星生物化学有限公司,安徽省杂环化学重点实验室,安徽 马鞍山 243100)
煤气化是煤洁净、高效利用的重要技术,其中煤气化过程中不可避免会产生Hg0和H2S等有毒有害污染物,严重污染环境,危害人体健康,因此必须加以处理。
汞在自然界中主要以三种形态存在,其中固态汞(Hgp)和二价汞(Hg2+)可用除尘装置脱除,而气态汞(Hg0)由于其低熔点、低水溶性和易迁移等特点,较难用现有的装置脱除[1-2]。活性炭吸附法是人们研究较多的吸附剂吸附法[3]。其中经过改性后的活性炭吸附剂大大提高了其脱除Hg0的能力[4-7]。H2S是一种无色、酸性、有臭鸡蛋气味的有毒气体,在湿热的条件下对管道和设备造成严重腐蚀。目前,对煤气化过程中Hg0和H2S的脱除技术主要采用吸附剂吸附法,其中包括活性炭、金属氧化物、新型吸附剂等[8]。Wang J C等[9]研究了三种商业铁基催化剂对气态Hg0和H2S的脱除影响,结果发现,气态Hg0和H2S在脱除的同时,H2S又对Hg0的脱除起到了一定的促进作用。
本文主要是采用等体积浸渍法,结合硅藻土资源丰富、廉价易得和三氧化二铁氧化活性高等特点,制备了一种新型的催化剂,并考查了Fe2O3的负载量、反应温度、气氛、空速以及气态汞浓度对活性的影响。
1 实验部分
1.1 催化剂的制备
硅藻土主要来源于吉林长白山地区,主要成分为SiO2,其中含有少量的 Al2O3、Fe2O3、CaO、MgO 等物质。本实验主要是将硅藻土等体积浸渍在一定浓度Fe(NO3)2溶液中,搅拌,在室温下静置2h,55℃下干燥7h,110℃下干燥7h,接着在煅烧温度为300℃的Ar气氛下煅烧4h,制得所需要的Fe2O3/硅藻土催化剂。
1.2 同时脱除Hg0和H2S的实验
本实验主要是在固定床反应装置上进行。如图1所示,将催化剂紧密装填在石英管的中间,两端用石英棉固定,放在电阻炉的中间。由程序升温仪控制反应温度。实验气氛为模拟煤气:15%CO,8%H2,500mg/L H2S,N2(平衡气),O2。其中,气态Hg0由汞渗透管(美国VICI公司)产生,通过控制水浴温度和载气N2流量,可以产生不同浓度的气态Hg0。将混合后的载有气态Hg0的模拟煤气通入装有催化剂的石英管,出口气体通入测汞仪,测汞仪末端连有电脑,直接读出数据,其中尾气经活性炭床吸收后排空。
催化剂对气态Hg0的脱除效率为η,表示在一定时间内催化剂对Hg0的吸附量与气态Hg0的初始浓度的百分比。
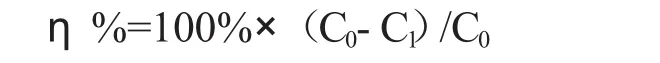
其中,C0表示气态Hg0的初始浓度,C1表示气态Hg0的经催化剂吸附后的浓度。
2 结果与讨论
2.1 Fe2O3负载量的影响
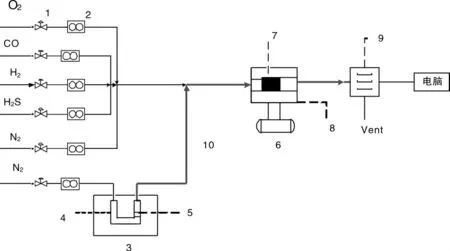
图1 固定床反应装置
图2表示了不同Fe2O3负载量下的催化剂对煤气中Hg0的吸附脱除的影响。可以看出,纯的硅藻土对Hg0的脱除效率在20%~30%之间,随着反应时间持续增加至12h,硅藻土对Hg0的吸附脱除能力有所下降。这主要是由于Fe2O3的负载量不同,催化剂表现出不同的吸附脱除Hg0的能力,且随着负载量由2%增加至8%,反应6h,催化剂脱除Hg0的效率由42%增加至89%;而当负载量持续增加至12%时,脱除Hg0的效率由89%降至72%。其中,Fe2O3/硅藻土催化剂的吸附脱除Hg0的能力始终强于纯硅藻土,这主要是由于Fe2O3催化氧化和硅藻土吸附能力协同作用的结果[9]。

图2 Fe2O3负载量对气态Hg0脱除的影响
2.2 反应温度的影响
图3表示反应温度对催化剂脱除Hg0和H2S的影响。可以看出,随着反应温度的增加,催化剂对Hg0和H2S的脱除能力先增加后减小。在低温区50℃时,催化剂脱除Hg0和H2S的能力较差,当温度高于200℃时,催化剂对Hg0和H2S的脱除能力迅速下降。从图3可以看出,在相同的反应温度和反应时间下,催化剂脱除H2S的能力始终强于脱除Hg0的能力。在反应温度为150℃,反应6h时,催化剂脱除H2S和Hg0的效率分别为95%、87%。

图3 反应温度对气态Hg0和H2S脱除的影响
2.3 气氛的影响
图4表示在不同反应气氛下,催化剂对Hg0脱除能力的影响。可以看出,在纯N2气氛中,催化剂脱除Hg0的效率在40%~50%之间,在CO+H2气氛中,催化剂脱除Hg0的效率比纯N2气氛中略高。而通入H2S气氛,催化剂脱除Hg0的能力明显增强,在反应6h时,脱除Hg0的效率为79%。当同时通入H2S和O2气氛时,催化剂脱除Hg0的能力比只通入H2S平均高出10%左右,在反应6h时,脱除Hg0的效率为85%。当通入模拟煤气(N2+CO+H2+H2S+O2)时,催化剂脱除Hg0的效率稍高于H2S+O2,在反应6h时,脱除Hg0的效率为89%。这表明CO和H2对催化剂脱除Hg0的效果影响不大,H2S和O2促进了反应的进行,这与文献中描述的一致[9-10]。

图4 气氛对气态Hg0脱除的影响
2.4 空速的影响
图5表示在不同的空速条件下,催化剂对Hg0和H2S的脱除影响。可以看出,在低空速的条件下,催化剂脱除Hg0和H2S的能力较高,其中,催化剂具有良好的脱除H2S的能力。在空速为2000h-1时,催化剂反应6h脱除Hg0和H2S的效率分别为94%、96%。随着空速增加至6000h-1时,脱除Hg0和H2S的效率降低到78%、89%,分别降低了16%、7%。这主要是由于低空速增加了Hg0和H2S与催化剂表面接触时间,从而提高了Fe2O3在催化剂表面的利用率,进而提高了Fe2O3/硅藻土催化剂脱除Hg0和H2S的能力[11]。

图5 空速对气态Hg0和H2S脱除的影响
2.5 气相Hg0浓度的影响
图6表示在不同Hg0浓度下,催化剂对Hg0的脱除效果。可以看出,低Hg0浓度的条件下,催化剂对Hg0的脱除能力较好,反应12h时脱除效率仍能保持在80%左右。当Hg0浓度增加到300μg/m3,反应6h时,催化剂脱除Hg0的效率为68%,反应12h时,催化剂脱除Hg0的效率仍能保持在60%左右。
3 结论

图6 Hg0的初始浓度对气态Hg0脱除的影响
自制Fe2O3/硅藻土催化剂具有良好的脱除Hg0和H2S的能力。具体为:①Fe2O3/硅藻土催化剂对Hg0脱除的能力随着Fe2O3负载量的变化而变化。当Fe2O3负载量为0%~12%时,催化剂脱除Hg0的效率先增加后减小,在8%的负载量下脱汞效率最佳,为89%;②在反应温度为50℃~300℃时,催化剂脱除Hg0和H2S的能力先增加后减小,在150℃时,脱除Hg0和H2S的能力最好;③H2S和O2促进了脱除Hg0的效率;④低空速、低汞浓度下催化剂脱除Hg0的能力较好;⑤随着反应时间的增加,催化剂脱Hg0和H2S的能力有所降低,但反应12h时,仍具有良好的吸附脱除能力。
[1]WANG J,WANG W H,XU W,et al.Mercury Removals by Existing Pollutants Control Devices of Four Coal-fired Power Plants in China [J].Journal of Environmental Sciences,2011,23(11):1839-1844.
[2]ZHOU Z J,LIU X W,ZHAO B,et al.Effects of Existing Energy Saving and Air Pollution Control Devices on Mercury Removal in Coal-fired Power Plants [J].Fuel Processing Technology,2015,131:99-108.
[3]UDDIN M A,OZAKI M,SASAOKA E,et al.Temperature-programmed Decomposition Desorption of Mercury Species over Activated Carbon Sorbents for Mercury Removal from Coal-derived Fuel Gas[J].Energy Fuels,2009,23(10):4710-4716.
[4]VIDIC R D,SILER D P.Vapor-phase Elemental Mercury Adsorption by Activated Carbon Impregnated with Chloride and Chelating Agents[J].Carbon,2001(1):3-14.
[5]LEE S S,LEE J Y,KEENER T C.Novel Sorbents for Mercury Emissions Control from Coal-fired Power Plants[J].J Chin Inst Chem Eng,2008,39(2):137-142.
[6]SUN W,YAN N-Q,JIA J-P. Removal of Elemental Mercury in Flue Gas by Brominated Activated Carbon[J].China Environmental Science,2006,26(3):257-261.
[7]LIU W,VIDIC R,BROWN T.Impact of Flue Gas Conditions on Mercury Uptake by Sulfur-impregnated Activated Carbon[J].Environ Sci Technol,2000,34(1):154-159.
[8]韩粉女,钟秦.燃煤烟气脱汞技术的研究进展 [J].化工进展,2011,30(4):878-885.
[9]WANG J C,ZHANG Y P,HAN L,et al.Simultaneous Removal of Hydrogen Sulfide and Mercury from Simulated Syngas by Iron-based Sorbents[J].Fuel,2012,103(1):73-79.
[10]张郃,赵建涛,房倚天,等.活性炭催化氧化脱除单质汞的研究[J].燃料化学学报,2011,39(5):373-377.
[11]王钧伟,陈培,刘瑞卿,等.粉煤灰负载Fe2O3脱除气态单质汞的试验研究[J].环境科学学报,2014,34(12):3152-3157.□
