降脂宁有效部位提取纯化工艺研究
2018-05-18李丽华杨瑞静姜艳艳
李丽华,杨瑞静,姜艳艳,刘 斌
(北京中医药大学中药学院,北京 102488)
降脂宁颗粒收载于《中华人民共和国卫生部药品标准:中药成方制剂》[1],由山楂、荷叶、制何首乌和决明子4味药组成,具有降血脂和软化血管的功能,用于增强冠状动脉血液循环,治疗心律不齐及高脂血症。山楂为方中君药,主要有效成分为黄酮类和三萜类[2-3],荷叶为臣药,主要有效成分为黄酮类和生物碱类[4],具有抗氧化、降压降血脂、抗心律不齐、增加冠状动脉流和保护心血管等作用[3-7]。制何首乌和决明子为佐使药,主要有效成分分别为二苯乙烯苷类[8]、蒽醌类[9-10]及萘并吡喃酮类[11],具有抗氧化、降压降脂和保肝等作用[9-12]。
本课题组前期对降脂宁降血脂药效及其作用机制开展了研究,结果显示,其作用机制是通过调节胆固醇吸收、合成和转化实现的[13-15]。同时,课题组也对降脂宁有效部位开展了药效研究,发现其亦有降血脂作用,且在药效作用上与降脂宁提取物具有等效性[16]。因此,本实验以总黄酮、总蒽醌、总生物碱和2,3,5,4′-四羟基二苯乙烯-2-O-β-D-葡萄糖苷为考察指标,采用正交实验和单因素实验筛选适用于工业化生产的降脂宁有效部位提取纯化工艺,以实现降脂宁的二次开发应用。
1 仪器与试药
1.1仪器 Waters 1525高效液相色谱仪,Empower色谱工作站(美国沃特公司);Sartorious BT 25S型十万分之一电子分析天平(北京赛多利斯仪器有限公司);KQ-500DE型超声波清洗器(昆山超声仪器有限公司);Hitachi U-2000型紫外-可见分光光度计(日本日立公司);UJS离心机(德国大陆集团);BUCHI Rotavapor R-220 旋转蒸发仪(瑞士布奇有限公司)。
1.2试药 制何首乌(产地湖北,批号601100089),荷叶(产地河北,批号601000998),山楂(产地河北,批号1601000906),决明子(产地安徽,批号70025002),均购自北京同仁堂医药集团北城批发部,经北京中医药大学中药资源与鉴定系张媛副教授鉴定。芦丁(批号MUST-16111111)和2,3,5,4′-四羟基二苯乙烯-2-O-β-D-葡萄糖苷(SBGC)(批号MUST-16021005),均购自成都曼斯特生物科技有限公司;1,8-二羟基蒽醌(批号110829-9702)和荷叶碱(批号111566-201304),均购自中国食品药品检定研究院。AB-8、S-8、NKA-9、X-5和D4020型大孔吸附树脂均购自天津南开大学化工厂。乙腈和甲醇(色谱纯,德国Sigma-Aldrich公司);乙醇、环己烷、盐酸、氨水和氯仿均为分析纯,均购自北京化工厂;水为屈臣氏蒸馏水。
2 方法与结果
2.1含量测定方法
2.1.1Al(NO3)3-NaNO2-NaOH比色法测定总黄酮含量 取降脂宁有效部位5 mg,精密称定,置于25 mL量瓶中,加体积分数为70%的乙醇溶解,定容至刻度,摇匀。分别精密吸取上述溶液2 mL、芦丁对照品溶液(取芦丁对照品10 mg,精密称定,置于25 mL量瓶中,加体积分数为70%的乙醇溶解,定容至刻度,摇匀)0.5和1.0 mL,分别置于10 mL试管中,加入质量浓度为50 g·L-1的亚硝酸钠0.3 mL,放置6 min,加入质量浓度为100 g·L-1硝酸铝0.3 mL,放置6 min,再加入质量浓度为40 g·L-1氢氧化钠4 mL,加水定容至刻度,摇匀,放置15 min,于510 nm处测定吸光度值,计算总黄酮的含量。
2.1.2醋酸镁比色法测定总蒽醌的含量 取降脂宁有效部位6 mg,精密称定,置于100 mL锥形瓶中,加环己烷30 mL以及216 mL·L-1的盐酸15 mL,回流水解2 h,静置分层,残渣用环己烷洗涤3次,合并滤液及洗液,回收溶剂,残留物用质量浓度为50 g·L-1的氢氧化钠 5 mL溶解,过滤,滤液用108 mL·L-1的盐酸7 mL酸化,静置15 min,过滤,沉淀用甲醇转溶至10 mL量瓶中,摇匀。分别精密吸取上述溶液2 mL、1,8-二羟基蒽醌对照品溶液(取对照品6 mg,精密称定,置于100 mL量瓶中,加甲醇溶解,稀释至刻度,摇匀)0.5和1.0 mL,分别置于10 mL试管中,加入质量浓度为60 g·L-1的醋酸镁甲醇溶液定容至刻度,摇匀。于510 nm处测定吸光度值,计算总蒽醌含量。
2.1.3溴甲酚绿比色法测定总生物碱含量 取降脂宁有效部位15 mg,精密称定,置于50 mL锥形瓶中,加入氨水0.5 mL,氯仿25 mL,超声提取(30 min,功率250 W,100 kHz),放冷,滤过,滤渣用少量溶剂洗涤3次,合并滤液及洗液,回收溶剂,残留物用甲醇转溶至10 mL量瓶中,定容至刻度,摇匀。分别精密吸取上述溶液2 mL,荷叶碱对照品溶液(取荷叶碱对照品8 mg,精密称定,置于10 mL量瓶中,加甲醇溶解,稀释至刻度,摇匀,精密量取1 mL,置于25 mL量瓶中,加甲醇定容至刻度,摇匀)0.4和0.8 mL,分别置于10 mL试管中,加入氯仿6 mL,密塞,剧烈振摇2 min,移至分液漏斗中,精密加入pH值为5.0的溴甲酚绿溶液4 mL,摇匀,静置。取澄清的氯仿溶液,于414 nm处测定吸光度值,计算总生物碱含量。
2.1.4HPLC法测定SBGC的含量 色谱柱:Agilent TC-C18色谱柱(250 mm×4.6 mm,5 μm);流动相:乙腈-水(18∶82);流速:1.0 mL·min-1;检测波长:320 nm;柱温:室温。
精密吸取SBGC对照品溶液(质量浓度为0.011 34 mg·mL-1)4,8,12,16和20 μL,注入液相色谱仪,测定色谱峰峰面积,以SBGC对照品的进样量对色谱峰峰面积进行回归,得回归方程:y=4 106 268.58x+5 908.81,r=0.999 1。
取降脂宁有效部位9 mg,精密称定,置于50 mL锥形瓶中,加入体积分数为50%的乙醇溶液25 mL,超声提取(30 min,功率250 W,100 kHz),放冷,滤过,滤渣用少量溶剂洗涤3次,合并滤液及洗液,回收溶剂,残留物用甲醇转溶至10 mL量瓶中,定容至刻度,摇匀。分别精密吸取SBGC对照品溶液和样品溶液各10 μL,注入高效液相色谱仪,测定,计算含量。
2.2降脂宁有效部位提取工艺 分别以Al(NO3)3-NaNO2-NaOH比色法测定总黄酮含量、醋酸镁比色法测定总蒽醌含量、溴甲酚绿比色法测定总生物碱含量和HPLC法测定SBGC含量,在单因素实验基础上,选择L9(34)正交表,以总黄酮、总蒽醌、总生物碱以及SBGC的提取率为评价指标,考察提取溶剂、溶剂用量、提取时间和提取次数对提取效果的影响,优选降脂宁有效部位最佳提取工艺。综合分析结果表明,提取溶剂、溶剂用量、提取时间和提取次数均有显著性影响,结合生产实际情况与节约成本综合考虑,确定降脂宁有效部位的最佳提取工艺为:按照处方比例称取药材,加10倍量体积分数为70%的乙醇提取3次,每次1.5 h,各评价指标的提取率均达到90%左右。
2.3降脂宁有效部位纯化工艺 分别以Al(NO3)3-NaNO2-NaOH比色法测定总黄酮含量、醋酸镁比色法测定总蒽醌含量、溴甲酚绿比色法测定总生物碱含量和HPLC法测定SBGC含量,通过单因素实验,以总黄酮、总蒽醌、总生物碱以及SBGC的吸附量、吸附-解吸率及其在洗脱物中的含量作为评价指标,筛选降脂宁有效部位的最佳纯化工艺。
2.3.1大孔树脂预处理 分别取适量AB-8、S-8、NKA-9、X-5和D4020型大孔吸附树脂在乙醇中浸泡12 h,湿法装柱后乙醇冲洗至流出液与水混合(1∶5)不呈现白色混浊;再用蒸馏水冲洗至流出液无醇味,备用。
2.3.2上样液的制备 按照正交实验结果得到的最佳提取工艺操作,即按照处方比例称取山楂500 g,决明子25 g,荷叶75 g,制何首乌25 g,加10倍量体积分数为70%的乙醇提取3次,每次1.5 h,过滤,减压回收溶剂至无醇味,得降脂宁提取物,加10倍量水超声分散溶解,以降脂宁药材计,溶液质量浓度为0.1 g·mL-1,离心,取上清液,即得。
2.3.3大孔树脂的筛选 取已处理好的5种大孔树脂各30 mL,分别装柱(径高比为1∶11),将上样液以2 BV· h-1的流速分别通过树脂床,间隔10 mL收集流出液,分别监测总黄酮(Al(NO3)3-NaNO2-NaOH显色反应)、总蒽醌(醋酸镁显色反应)、总生物碱(点于硅胶G板,碘化铋钾显色)以及SBGC(点于硅胶G板,硫酸乙醇显色)的泄漏点。吸附完成后,先用蒸馏水洗脱5 BV除杂,再用体积分数为50%的乙醇洗脱,至洗脱液近无色为止,收集洗脱液,回收溶剂,得洗脱物。取洗脱物适量,按照2.1项下方法操作,计算各评价指标,筛选树脂类型。结果见表1。
表1不同型号大孔吸附树脂筛选
Tab.1 Screening of different types of micro-porous resins

指标 树脂类型AB⁃8S⁃8NKA⁃9X⁃5D⁃4020总黄酮吸附量/mg451.31481.40210.61361.05191.16吸附⁃解析率/%95.9526.0569.2083.8196.09含量/%41.4843.3783.9661.8320.30总蒽醌吸附量/mg19.8421.179.2615.875.29吸附⁃解析率/%75.7634.4268.8084.3085.05含量/%1.442.523.673.000.79总生物碱吸附量/mg3.723.971.742.980.99吸附⁃解析率/%36.1327.8247.7593.5857.25含量/%0.130.380.480.630.10SBGC吸附量/mg7.247.733.385.791.93吸附⁃解析率/%46.3444.8638.3780.2344.15含量/%0.321.200.751.040.15
由表1中最大吸附量可知,D-4020和NKA-9型树脂吸附性较差;由吸附-解吸率可知,AB-8型树脂对总黄酮的吸附-解析率最高,X-5型树脂对总生物碱以及SBGC的吸附-解析率最高,X-5和D-4020型树脂对总蒽醌的吸附-解析率相差不大且优于其他树脂,结合洗脱物中总黄酮、总蒽醌、总生物碱以及SBGC的含量综合考虑,确定X-5型大孔吸附树脂作为降脂宁有效部位纯化用树脂。
2.3.4上样液浓度考察 取已处理好的X-5型大孔树脂30 mL,装柱(径高比为1∶11),取一系列相同体积不同质量浓度(0.05,0.1和0.15 g·mL-1)的上样液,以相同流速2 BV·h-1分别通过树脂柱,进行动态吸附。以Al(NO3)3-NaNO2-NaOH显色反应监测泄漏点(通过检识,发现总蒽醌、总生物碱以及SBGC在总黄酮泄漏后开始泄露,故以总黄酮的泄露点进行监测),记录上样量,计算总黄酮、总蒽醌、总生物碱以及SBGC的吸附量。结果显示,上样液质量浓度为0.1 g·mL-1时,X-5型树大孔脂对降脂宁总黄酮、总蒽醌、总生物碱以及SBGC的吸附量较大,故最佳上样液质量浓度为0.1 g·mL-1。
2.3.5吸附流速的考察 取已处理好的X-5型大孔树脂30 mL,装柱(径高比为1∶11),取上样液,分别以2,4和6 BV·h-1的流速通过树脂柱,以Al(NO3)3-NaNO2-NaOH显色反应监测泄漏点,记录上样量,计算总黄酮、总蒽醌、总生物碱以及SBGC的被吸附量,结果发现,随着吸附流速的增加,树脂对降脂宁总黄酮、总蒽醌、总生物碱以及SBGC的吸附量明显减少,当吸附流速增加到6 BV·h-1时,降脂宁有效成分与树脂之间的吸附力较差,吸附流速为2和4 BV·h-1时,吸附能力无明显差别,故确定吸附流速以4 BV·h-1为宜。
2.3.6树脂柱径高比考察 分别取已处理好的X-5型大孔树脂19,24.5和30 mL,装柱,径高比分别为 1∶7,1∶9和1∶11,取上样液,以4 BV·h-1的流速通过树脂柱,以Al(NO3)3-NaNO2-NaOH显色反应监测泄漏点,记录上样量,计算总黄酮、总蒽醌、总生物碱以及SBGC的吸附量。待吸附完成后,按照2.3.3项下操作,计算各评价指标。结果发现,从被吸附量和吸附-解吸率两方面考虑,径高比1∶9组和1∶11组(各指标吸附-解吸率在80%以上)均优于径高比1∶7组(各指标吸附-解吸率在65%左右),径高比1∶9组略优于1∶11组,但差异不显著;从洗脱物含量考虑,径高比1∶9组较好,故确定树脂柱径高比为1∶9。
2.3.7泄露曲线考察 取已处理好的X-5型大孔树脂24.5 mL,装柱(径高比1∶9),取上样液,以4 BV·h-1的流速连续通过树脂柱,每10 mL接收一次流出液,Al(NO3)3-NaNO2-NaOH比色法测定每份流出液总黄酮的质量浓度,以流份份数与总黄酮质量浓度(mg·mL-1)作图,结果见图1。
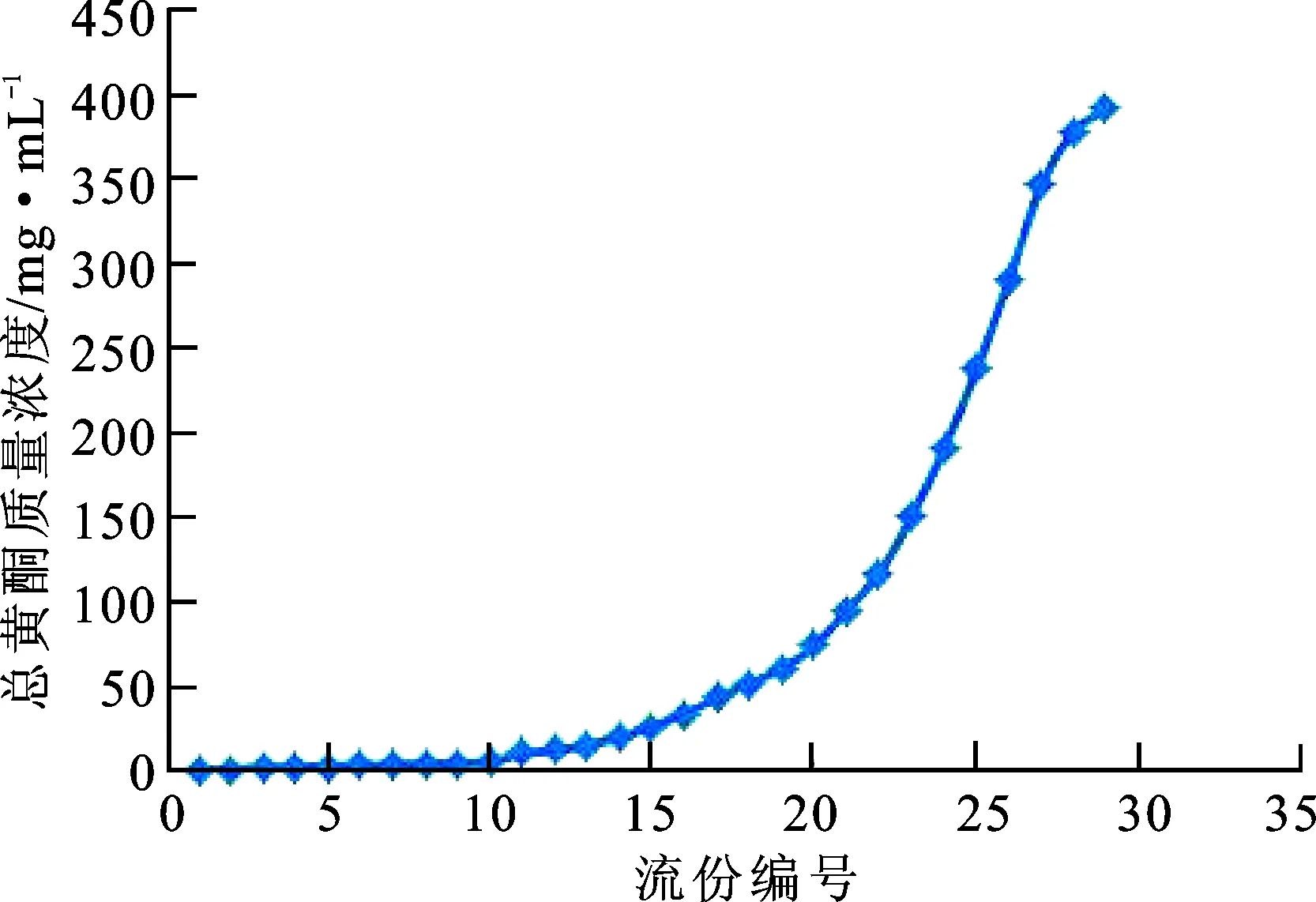
图1X-5大孔吸附树脂吸附总黄酮的动态曲线
Fig.1 Dynamic absorption curve of total flavoneson X-5 macro-porous resin
由图1可知,在上述吸附条件下,第10个流份,即上样量为100 mL时,总黄酮开始泄漏,但在总黄酮吸附-解析率达到一定要求的前提下,为提高树脂利用率,需要对树脂最大上样量进行进一步考察。
2.3.8最大上样量考察 取已处理好的X-5型大孔树脂24.5 mL,装柱(径高比1∶9),分别取上样液100,110,130和150 mL,以4 BV·h-1的流速通过树脂柱,待吸附完成,按照2.3.3项下操作,测定总黄酮含量,计算总黄酮吸附-解析率。结果见表2。
表2不同体积上样液经大孔处理结果
Tab.2 The purification effect of different valumes of sample
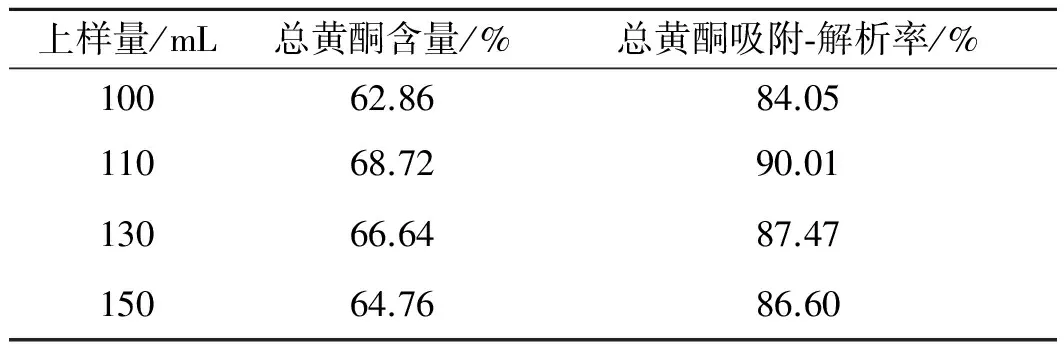
上样量/mL总黄酮含量/%总黄酮吸附⁃解析率/%10062.8684.0511068.7290.0113066.6487.4715064.7686.60
由表2可知,上样量为110 mL时总黄酮吸附-解析率最高,洗脱物中总黄酮含量也较高,随着上样量继续增加,总黄酮含量及其吸附-解析率也随之下降。因此,确定最大上样量为110 mL(4.5 BV),即树脂比吸附量(以总黄酮计)为13.51 mg·mL-1。
2.3.9水除杂体积考察 取已处理好的X-5型大孔树脂24.5 mL,装柱(径高比1∶9),取上样液110 mL,以4 BV·h-1的流速通过树脂柱,待吸附完成后,树脂柱分别用蒸馏水洗脱3,5和7 BV后,按照2.3.3项下操作,计算各评价指标。结果显示,当采用5 BV水体积进行洗脱时,各指标成分吸附-解吸率和含量均较优。即采用5倍量树脂柱体积水清洗树脂床既有利于有效地去除杂质,又能较好地保留有效物质。
2.3.10洗脱溶剂的考察 取已处理好的X-5型大孔树脂24.5 mL,装柱(径高比1∶9),取上样液110 mL,以4 BV·h-1的流速通过树脂柱,待吸附完成后,树脂柱用蒸馏水洗脱5 BV后,再分别用体积分数为50%,70%和90%的乙醇洗脱至洗脱液近无色,洗脱流速为2 BV·h-1,分别收集洗脱液后,按照2.3.3项下操作,计算各评价指标。结果发现,采用体积分数为50%的乙醇洗脱时,洗脱物中各指标的吸附-解析率均在80%以上,含量高于体积分数为70%和90%的乙醇洗脱,故确定采用体积分数为50%的乙醇作为洗脱溶剂。
2.3.11洗脱流速的考察 取已处理好的X-5型大孔树脂24.5 mL,装柱(径高比1∶9),取上样液110 mL,以4 BV·h-1的流速通过树脂柱,待吸附完成后,树脂柱先用蒸馏水洗脱5 BV进行除杂,再用体积分数为50%的乙醇洗脱至洗脱液近无色,洗脱流速分别控制为2,4和6 BV·h-1,分别收集洗脱液,按照2.3.3项下操作,计算各成分吸附-解吸率。结果显示,洗脱流速为4和6 BV·h-1时,各成分含量及吸附-解析率差异无统计学意义,且均优于2 BV·h-1。因此,结合生产实际情况与节约成本综合考虑,确定洗脱流速为4 BV·h-1。
2.3.12洗脱曲线考察 取已处理好的X-5型大孔树脂24.5 mL,装柱(径高比1∶9),取上样液110 mL,以4 BV·h-1的流速通过树脂柱,待吸附完成后,树脂柱先用蒸馏水洗脱5 BV进行除杂,再用体积分数为50%的乙醇洗脱,洗脱流速为4 BV·h-1。每20 mL收集1份洗脱液,回收溶剂后,按照2.1项下方法测定各成分质量浓度。以洗脱液体积(mL)与质量浓度(mg·mL-1)绘制洗脱曲线,结果见图2。
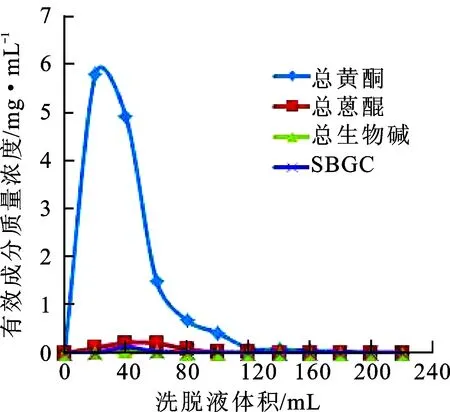
图2总黄酮、总蒽醌和总生物碱及2,3,5,4′-四羟基二苯乙烯-2-O-β-D-葡萄糖苷(SBGC)洗脱曲线
Fig.2 Elution curves of total flavones,total anthraquinones,total alkaloids and 2,3,5,4′-hydroxyphenyl-vinyl-2-O-β-D-glucoside
由图2可知,当体积分数为50%的乙醇洗脱7 BV时,已基本将总黄酮、总蒽醌、总生物碱和SBGC洗脱完全,故确定洗脱剂用量为7 BV。
2.4工艺验证 采用已确定的降脂宁有效部位最佳提取纯化工艺条件,进行3批中试验证,取降脂宁有效部位干浸膏适量,测定总黄酮、总蒽醌、总生物碱以及SBGC的含量。结果见表3。以各成分含量的可重复性评价工艺的适用性。结果表明,该提取纯化工艺合理、稳定。
表3不同批次样品经大孔树脂处理结果
Tab.3 The purification effect of different batches of samples
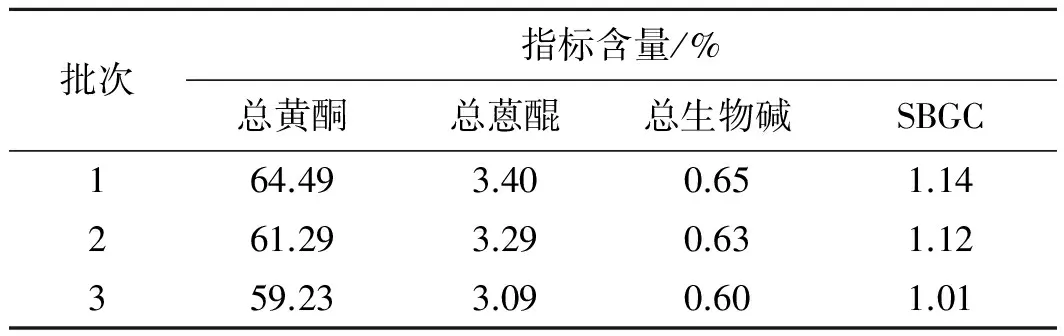
批次指标含量/%总黄酮总蒽醌总生物碱SBGC164.493.400.651.14261.293.290.631.12359.233.090.601.01
3 讨论
降脂宁由4味中药组成,其化学成分类型复杂、数量众多,为了更全面地评价其有效部位的提取纯化工艺,在指标的选择上应尽量考虑各药材的有效成分。根据课题组前期研究结果表明[16],该实验选择以总黄酮、总蒽醌、总生物碱及SBGC为指标成分。
本实验以各指标成分的提取率作为评价指标,对降脂宁有效部位的提取工艺进行研究,在单因素实验基础上结合正交实验确定了最佳提取工艺:加10倍量体积分数为70%的乙醇提取3次,每次1.5 h。该提取工艺较原来相比简化了工艺步骤,节约了时间,且各指标成分的提取率均有所提高。
近年来,随着对中药及天然药物活性成分及有效部位相关研究的增多,大孔吸附树脂在分离、纯化中的应用也越来越多[17],并取得了较理想的效果,尤其是在黄酮类[18-19]、生物碱类[19-20]和皂苷类[20]的纯化应用方面。本实验对降脂宁有效部位的纯化工艺进行了研究,经过筛选发现X-5型大孔树脂的综合吸附性能较好,其最佳纯化工艺为:上样液质量浓度为0.1 g·mL-1,吸附流速为4 BV·h-1,上样量以总黄酮计为13.51 mg·mL-1,树脂径高比为1∶9,蒸馏水5 BV洗脱除杂,体积分数为50%的乙醇7 BV洗脱富集降脂宁有效部位,洗脱流速为4 BV·h-1。在纯化工艺考察过程中,为避免上样液中的不溶物堵塞树脂,对上样液采用了离心操作。
按照最佳提取纯化工艺富集纯化后,降脂宁有效部位中总黄酮类成分的含量能达到60%左右,总蒽醌含量能达到3%以上,总生物碱含量能达到0.6%以上,SBGC含量能达到1%以上。经验证,该工艺稳定、可行,重复性较好。另外,实验中所用大孔吸附树脂可重复使用,成本低且快速、高效、低毒,适合实际生产,为降脂宁的进一步开发应用奠定了实验基础。
参考文献:
[1] 国家药典委员会.中华人民共和国卫生部药品标准:中药成方制剂:第十三册[S].北京:人民卫生出版社,1997:116.
[2] 王玲,吴军林,吴清平,等.山楂降血脂作用和机理研究进展[J].食品科学,2015,36(15):245-248.
[3] 詹琤琤,段时振,李杰.中药山楂的化学成分与药理作用研究概况[J].湖北中医杂志,2012,34(12):77-79.
[4] 王福刚,曹娟,刘斌,等.荷叶的化学成分及其药理作用研究进展[J].时珍国医国药,2010,21(9):2339-2340.
[5] 陈曦,戚进.荷叶中黄酮和生物碱的研究进展[J].中国实验方剂学杂志,2015,21(18):211-214.
[6] 肖桂青,卢向阳,田云,等.荷叶生物碱药理作用的研究进展[J].湖南农业科学,2006,(2):80-81,88.
[7] 朱秀萍,徐翔.荷叶生物碱研究进展[J].中国药房,2008,19(6):459-461.
[8] 孙康悦,李颖,李悦琪,等.国内降血脂药物研究进展[J].西北药学杂志,2017,32(1):122-124.
[9] 高淑红,苏珍枝,肖学凤.制首乌化学成分及药理作用研究进展[J].山西中医学院学报,2012,13(2):74-77.
[10]石亮,黄娜娜,孙蓉.血脂宁药理毒理学研究进展[J].中国药物警戒,2016,13(6):347-350.
[11]耿丹丹,刘灵娣,欧阳艳飞,等.决明子中萘并-吡喃酮类化学成分及其生物活性研究进展[J].特产研究,2017,(3):64-67.
[12]刘斌,巩鸿霞,肖学凤,等.决明子化学成分及药理作用研究进展[J].药物评价研究,2010,33(4):312-315.
[13]肖世凤.降脂宁提取物及其有效部位对高脂血症大鼠调脂作用的实验研究[D].呼和浩特:内蒙古医学院,2009:25-27.
[14]李晋生.降脂宁调节胆固醇代谢及抗动脉粥样硬化效应机制的研究[D].北京:北京中医药大学,2006:107-109.
[15]Chen J,Zhao H,Yang Y,et al.Lipid-lowering and antioxidant activities of Jiang-Zhi-Ning in traditional Chinese medicine[J].J Ethnopharmacol,2011,134(3):919-930.
[16]杨英,刘斌,毕力夫,等.降脂宁调血脂及抗脂质过氧化作用的实验研究[J].中华中医药杂志,2009,24(5):647-649.
[17]杨培民,代龙,魏永利.大孔吸附树脂分离纯化白花蛇舌草总黄酮的研究[J].北京中医药大学学报,2010,33(6):417-420,424.
[18]葛淑兰,陈龙华,李中文.大孔吸附树脂及其在黄酮类成分分离纯化中的应用进展[J].中国药师,2008,11(6):702-705.
[19]吴涓,田璐璐,祝德秋.大孔树脂在中药分离纯化中的应用进展[J].上海医药,2013,34(19):46-49.
[20]季慧,陈斌斌,黄越燕.大孔吸附树脂分离纯化生物碱类化合物研究进展[J].亚太传统医药,2017,13(1):72-75.
