后路经皮椎弓根钉内固定术与经肌间隙椎弓根钉内固定术治疗胸腰椎骨折的比较
2018-05-17涂洪波赵建华
涂洪波,柳 峰,赵建华
近年来,脊柱损伤的发病率不断上升,脊柱创伤愈发常见,其中胸腰椎骨折约占脊柱骨折的59%,且往往需要通过手术固定重建[1]。脊柱后路椎弓根螺钉内固定术复位固定胸腰椎骨折是手术治疗的主要方法,效果良好。目前常用的手术入路主要有传统的后正中开放入路、微创经皮入路以及经肌间隙入路三种。后正中开放入路作为传统术式,与后两种手术入路相比较,存在创伤大、剥离广泛,易出现背部僵硬、腰背痛等不足,已逐渐被后两种手术入路取代[2-3]。经皮入路和经肌间隙入路是目前临床上主要的微创手段。相较于传统的开放性手术,它们不但减少了对椎旁肌的剥离损伤,而且取得了满意的临床效果[4-5]。目前的研究主要集中在经皮入路和经肌间隙入路这两种微创手术与传统的后正中开放入路手术的比较,两种微创手术之间的优劣未见报道。笔者回顾分析2014年1月—2016年1月期间的79例经两种微创手术治疗的无神经损伤的单节段胸腰段骨折患者,比较其优缺点及临床效果。
临床资料
1一般资料
2014年1月—2016年1月期间共有79例无神经损伤的单节段胸腰段椎体骨折患者在笔者科室接受手术治疗,其中男性47例,女性32例;年龄17~65岁,平均46.3岁。高处坠落伤59例,道路交通伤20例。根据最新的AO胸腰椎损伤分型系统分型[6]:A1型47例,A2型7例, A3型14例,A4型11例。载荷分享(Load-sharing)评分[7]:3~6(平均4.5)分;受伤至手术时间2~9(平均3.6)d。所有骨折均采用后路椎弓根螺钉短节段固定伤椎,分别采用微创经皮入路(微创经皮组35例)和经肌间隙入路(经肌间隙组44例),两组间性别、年龄、骨折分型、骨折部位、Load-sharing评分、手术时机等方面比较差异无统计学意义。所有患者术前进行了常规的X线、CT及MRI检查,并对椎体、椎间盘及后方韧带复合体损伤情况进行了评估。
2手术方法
2.1微创经皮组 本组选用山东威高生产的UPASSⅡ脊柱微创内固定系统。患者采用全身麻醉,取俯卧位,胸部、骨盆垫软垫,使腹部悬空,对骨折椎体进行体位复位初步矫正后凸角。C型臂X线机透视下确认伤椎椎弓根位置,并在皮肤上进行划线标记。常规消毒、铺巾,在皮肤标记处取长1.0~1.5 cm纵向切口,切开皮肤至深筋膜。在正位X线透视引导下将穿刺针穿入至上关节突和横突的交点,在正位X线片透视下针尖位于椎弓根外上缘,将穿刺针沿终板平行方向置入至针尖到达椎弓根内缘,并在侧位X线透视下确认针尖已经超过椎体后缘。取出针内芯,置入导针并取出针管,沿导针置入丝攻并对椎弓根进行攻丝,攻丝完毕后将中空万向椎弓根钉通过导针和透视引导下置入椎弓根,取出导针。同法完成伤椎上下两个椎体的椎弓根钉的植入,共植入6枚螺钉。 C型臂X线机透视确认螺钉位置良好。装置持棒器,直视下将连接杆插入上、下位椎弓根钉尾槽中,C型臂X线机透视观察连接杆位置,先对伤椎上位椎椎弓根螺塞进行预紧,必要时根据椎体压缩情况适当撑开或压缩连接杆,然后锁紧下位椎椎弓根螺塞,最后经C型臂X线机透视确定椎体复位良好后,锁紧所有螺塞,逐层缝合腰背筋膜、皮下组织及皮肤。
2.2经肌间隙组 本组选用山东威高生产的UPASS脊柱内固定系统。患者麻醉以及体位准备与微创经皮组相同。C型臂X线机透视下确认伤椎位置,并在皮肤上以伤椎为中心进行划线标记。常规消毒、铺巾,在皮肤标记处取长8.0~10.0cm纵向切口,沿棘突两侧纵向切开腰背筋膜并适当潜行分离,用手指寻找最长肌与多裂肌之间的自然分界面并沿肌纤维方向钝性分开多裂肌和最长肌,向下触及椎体关节突关节及横突,显露伤椎上关节突和横突基底部。采用人字嵴定位法于伤椎植入椎弓根钉,C型臂X线机透视确认螺钉位置良好。同法完成伤椎上下两个椎体的椎弓根钉的植入,共植入6枚螺钉。C型臂X线机透视确认螺钉位置良好。连接杆约10°前凸预弯,先对伤椎上位椎椎弓根螺塞进行预紧,必要时根据椎体压缩情况适当撑开或压缩连接杆,然后锁紧下位椎椎弓根螺塞,最后经C型臂X线机透视确定椎体复位良好后,锁紧所有螺塞,缝合腰背筋膜、皮下组织及皮肤。
3术后处理
两组术后处理相同。手术切口均不放置引流管。术后常规静脉使用抗生素24h,活血消肿及定期换药。通过常规X线及CT检查评估骨折复位情况及螺钉位置。术后次日指导患者进行适当腰背肌锻炼,并在支具保护下下床活动。
4观察项目
记录两组手术切口长度、手术时间、术中出血量、术中透视时间;采用视觉模拟评分法(VAS)[8]评估术后第1天切口疼痛情况;术后3个月随访时采用腰痛失能问卷(ODI)[9]评估患者恢复情况。分别测量术前、术后即刻及末次随访时的伤椎椎体前缘高度、后凸Cobb角等。
5统计学分析
结 果
79例患者均手术顺利,未出现神经损伤、伤口感染、内固定失败等并发症。术后通过门诊随访,平均随访时间为18个月(12~30个月)。两组相比,微创经皮组手术切口长度较短,术后第1天切口疼痛较轻;经肌间隙组术中透视较少、时间稍短,差异均有统计学意义(P<0.05)。见表1。两组手术时间、出血量的比较差异无统计学意义(P>0.05);术前、术后即刻、末次随访的伤椎前缘高度比值及后凸Cobb角的比较以及术后ODI评分差异无统计学意义(P>0.05)。术后伤椎前缘高度及矢状面Cobb角与术前相比均得到明显矫正(P<0.05),而末次随访时的伤椎前缘高度及矢状面Cobb角均有所丢失,但差异无统计学意义(P>0.05)。见表2。典型病例见图1、2。

表1 胸腰椎骨折两组观察指标比较
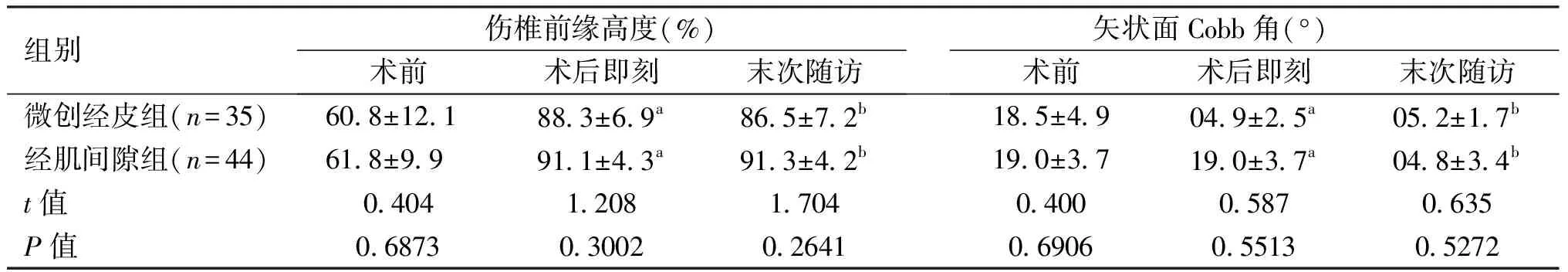
表2 胸腰椎骨折两组伤椎前缘高度和矢状面Cobb角比较
与术前比较:aP<0.05;与术后即刻比较:bP>0.05

a b
图1 患者女性,52岁。L1椎体骨折,AO分型为A3型,行后路经皮椎弓根螺钉复位固定手术。a、b.术前、术后侧位X线片

a b
图2 患者女性,52岁。L1椎体骨折,AO分型为A3型,行后路经肌间隙椎弓根螺钉复位固定手术。a、b.术前、术后侧位X线片
讨 论
1微创术式与传统术式的比较
胸腰段椎体骨折是一种常见的脊柱损伤,根据骨折的类型、稳定性、后方韧带复合体的完整性、椎管占位情况、有无神经损伤表现等的不同,有不同的手术方式可供脊柱外科医生选择。对于无神经损伤的AO分型A型骨折,经后路手术复位、椎弓根螺钉内固定术能达到复位骨折、稳定脊柱、纠正后凸畸形的良好效果[10]。相较于非手术治疗,手术治疗能显著减少长期卧床的并发症,降低压疮、深静脉血栓、坠积性肺炎等并发症的发生率。后正中入路手术作为一种经典的脊柱手术入路,被脊柱外科医生广泛接受,并经过了大量的验证,取得了较好的治疗效果[11-12]。但是,后正中入路手术存在其固有的缺陷。后正中入路手术需要经棘突两侧剥离、牵拉多裂肌,大范围地显露棘突、椎板、关节突关节以及横突,术中存在显露范围大、出血多、多裂肌损伤重、关节囊损伤可能等问题,术后存在伤口出血渗出较多、感染风险增加、多裂肌纤维化等问题。已有大量研究报道[13-14],后正中入路手术会出现肌肉组织出血、坏死、肌肉失神经损害、腰痛、脊柱后柱稳定系统的损害等。Stephen[15]研究表明,肌肉组织的失神经改变和功能丧失是术后腰痛发生的主要原因。
微创一直是外科手术发展的方向。鉴于后正中入路手术对于脊旁肌肉组织的损害,如何减少手术本身的损伤一直是研究的热点。对于没有神经损伤、不需要椎管减压的单节段胸腰段椎体骨折患者,多裂肌的剥离,棘突、椎板的暴露并不是必须的手术步骤。目前,脊柱后路手术主要有经肌间隙入路和经皮两种微创入路。这两种微创术式有效避免了对多裂肌的剥离、牵拉损伤,避免了对脊柱后方韧带复合体的损伤,避免了骨关节的损伤。Kim等[16]通过核磁共振检查,对比了微创手术和开放手术后多裂肌在核磁共振横截面上的面积,发现微创手术前后多裂肌面积无显著变化,而开放手术后多裂肌面积明显减少。张锦洪等[5]、Andrew等[17]分别比较了后路两种微创术式与开放术式在治疗胸腰椎骨折中的疗效,证实微创术式具有创伤小、出血少、恢复快、安全性高等优点。笔者通过研究发现,微创经皮组和经肌间隙组的术中出血量分别为(48.3±8.9)mL和(51.0±12.2)mL,出血量较文献报道的常规后正中入路明显减少。但对于存在神经损伤表现、需要椎管减压的患者,以上两种技术减压较困难,因此笔者选择没有神经损伤表现、不需要椎管内减压的单节段胸腰段椎体骨折患者作为研究对象。
2微创经皮入路和经肌间隙入路的比较
早在1968年,Wiltse等[18]便开始从棘突旁多裂肌与其外侧的最长肌之间的间隙进行腰椎内固定手术。随后,该入路逐渐被应用于胸腰椎骨折的手术中,即肌间隙入路。此入路有明确的解剖学依据,多裂肌紧贴棘突两侧,并向下逐渐变粗,在最长肌与多裂肌之间有明显的肌间隙形成,间隙内存在少量脂肪组织填充。与后正中入路相比,肌间隙入路是从椎体棘突旁自然肌肉间隙进入,快速准确到达置钉部位,不需要对多裂肌附着处进行剥离,不需要暴露棘突、椎板,不损伤后方韧带复合体和关节突关节。同时,肌间隙入路与椎弓根置钉轴线相一致,能够避免术中对多裂肌的过度牵拉损伤,置钉方便、容易。
后路经皮椎弓根螺钉内固定手术相对于肌间隙入路来说,发展相对较晚,是随着脊柱后路内固定系统的发展而出现。经皮入路主要通过借助微创器械及术中不断透视的方法实现微创治疗胸腰椎骨折的目的。经皮入路不通过确切的解剖间隙,通过透视直接穿刺进入椎体内,其理论依据主要是基于皮下肌肉隧道沿肌纤维钝性分开,肌肉组织穿透损伤的损伤程度低于传统剥离损伤,通过穿刺进入椎体和对多裂肌附着点的剥离、避免了对肌肉的牵拉损伤[19]。经皮入路通过器械的改进,达到微创治疗效果。
经皮入路与肌间隙入路两种微创术式均能够取得优于传统后正中入路的治疗效果,能达到微创治疗的目的。两者有创伤小、出血少、手术时间短、患者恢复快、痛苦小等相同点。两者的手术适应范围也相似,主要包括:(1)无神经损伤的胸腰椎压缩骨折,或不能忍受长期卧床、长期佩戴支具等非手术治疗的患者;(2)无神经损害的椎体爆裂骨折,椎弓根完整,椎管内无占位或占位<1/3的患者;(3)不需要进行截骨矫形重建的椎体骨折,并满足前两条适应证的患者[20-21]。两者从基础理论到具体操作均有不同。经皮入路术式基于器械的发展,依赖于术中的不断透视,对术者要求较高。肌间隙入路术式基于对脊旁肌肉解剖的精确认识,对最长肌、多裂肌间隙的运用。笔者比较了两组患者切口长度、手术时间、出血量、放射透视次数、骨折复位程度、患者疼痛评分等临床资料以及手术器械操作情况,发现经皮组切口长度较小、术后切口疼痛明显减轻;经肌间隙组术中透视次数较少,医生患者放射暴露少。在手术时间、术中出血量、骨折复位程度及后凸 Cobb 角方面,两组无明显差异。另外笔者认为,经皮入路需借助微创器械植入椎弓根钉棒装置,手术步骤与传统开放技术差异较大,术中需在C型臂透视定位下穿刺置钉,对解剖和影像学基础及临床技能要求较高,医生需要通过长时间的练习才能掌握相关技巧。而经肌间隙入路使用常规手术器械,直接暴露椎弓根进针点,可在直视下置入椎弓根钉,与传统开放型手术过程较为相似,医生容易学习掌握。
综上所述,对于无神经损伤的单节段胸腰段椎体骨折,微创经皮入路和小切口经肌间隙入路手术治疗均有良好的临床效果。从减少医生患者医源性放射暴露、降低患者治疗费用方面,经肌间隙入路具有更多优势。而且经肌间隙入路可以使用传统开放手术器械实现微创治疗胸腰椎骨折,医生学习掌握相关技术快,对在基层医疗单位的医疗工作者来讲,建议优先考虑使用。
参考文献:
[1] 程立明,曾志立.脊柱脊髓损伤流行病学特点分析和手术疗效探讨[J].中华创伤骨科杂志,2008,10(3):245-248.
[2] 方向前,胡志军,范顺武,等.胸腰段骨折经肌间隙入路与传统入路内固定的比较研究[J].中华骨科杂志,2009,29(4):315-319.
[3] 李方财,陈其昕,陈维善,等.经皮椎弓根螺钉内固定结合椎体内植骨治疗胸腰椎骨折[J].中华骨科杂志,2011,31(10):1066-1071.
[4] 薛文,管晓鹂,刘姝娆,等.微创经皮与传统开放椎弓根螺钉固定治疗胸腰椎骨折的Meta分析[J/CD].中华临床医师杂志:电子版,2015,9(23):4403-4412.
[5] 张锦洪,殷国勇,曹晓建,等.开放手术与微创手术治疗胸腰椎骨折的疗效对比[J].脊柱外科杂志,2015,13(6):364-368.
[6] Vaccaro AR,Oner C,Kepler CK,et al.AO spine thoracolumbar spine injury classification system: fracture description,neurological status,and key modifiers[J].Spine(Phila Pa 1976),2013,38(23):2028-2037.
[7] McCormack T,Karaikovic E,Gaines RW.The load sharing classification of spine fractures[J].Spine(Phila Pa 1976),1994,19(15):1741-1744.
[8] Huskisson EC,Jones J,Scott PJ.Application of visual analogue scales to the measurement of functional capacity[J].Rheumatol Rehabil,1976,15(3):185-187.
[9] Jeremy CT.The oswestry disability index[J].Spine,2000,25(22):2940-2953.
[10] Cahueque M,Cobar A,Caldera G.Management of burst fractures in the thoracolumbar spine[J].J Orthop,2016,13(4):278-281.
[11] Mohanty SP,Bhat SN,Ishwara-Keerthi C.The effect of posterior instrumentation of the spine on canal dimensions and neurological recovery in thoracolumbar and lumbar burst fractures[J].Musculoskelet Surg,2011,95(2):101-106.
[12] Oprel P,Tuinebreijer WE,Patka P,et al.Combined anterior-posterior surgery versus posterior surgery for thoracolumbar burst fractures: a systematic review of the literature[J].Open Orthop,2010,4:93-100.
[13] Inamasu J,Guiot BH,Nakatsukasa M.Posterior instrumentation surgery for thoracolumbar junction injury causing neurologic deficit[J].Neurol Med Chir,2008,48(1):15-21.
[14] Kallemeier PM,Beaubien BP,Buttermann GR,et al.In vitro analysis of anterior and posterior fixation in an experimental unstable burst fracture model[J].J Spinal Disord Tech,2008,21(3):216-224.
[15] Stephen T.Failed back syndrome[J].Neurologist,2004,10(5):259-264.
[16] Kim DY,Lee SH,Chung SK,et al.Comparison of multifidus muscle atrophy and trunk extension muscle strength: percutaneous versus open pedicle screw fixation[J].Spine(Phila Pa 1976),2005,30(1):123-129.
[17] Andrew J,Nader S,Taylor J,et al. Flexion-distraction injuries of the thoracolumbar spine: open fusion versus percutaneous pedicle screw fixation[J].Neurosurg Focus,2013,35(2):1-6.
[18] Wiltse LL,Bateman JG,Hutchinson RH,et al. The paraspinal sacrospinalis-splitting approach to the lumbar spine[J].J Bone Joint Surg(Am),1968,50(5):919-926.
[19] Lowery GL,Kulkarni SS.Posterior percutaneous spine instrumentation[J].Eur Spine J,2000,9(1): 126-130.
[20] Alpantaki K,Bano A,Pasku D,et al.Thoracolumbar burst fractures: a systematic review of management[J].Orthopedics,2010,33(6):422-429.
[21] Dai LY,Jiang SD,Wang XY,et al.A review of the management of thoracolumbar burst fractures[J].Surg Neurol,2007,67(3):221-231.
