盐酸利多卡因眼用凝胶中细菌内毒素检测方法学验证
2018-05-15周晓惠张军东
周晓惠 张军东

摘 要 目的:建立盐酸利多卡因眼用凝胶中细菌内毒素检查法。方法:按照中国药典2015版四部 1143 细菌内毒素检查法,确定盐酸利多卡因眼用凝胶的有效稀释浓度和细菌内毒素限值。结果:盐酸利多卡因眼用凝膠经稀释4倍后不干扰鲎试剂与细菌内毒素的凝集反应,其细菌内毒素均小于0.5 EU/ml。结论:本研究的方法简便、准确、可靠,可用于盐酸利多卡因眼用凝胶中细菌内毒素的检查。
关键词 利多卡因眼用凝胶 细菌内毒素 鲎试剂
中图分类号:R944.15; R927.11 文献标识码:A 文章编号:1006-1533(2018)05-0073-04
Validation of the methods for testing bacterial endotoxin in lidocaine hydrochloride ophthalmic gel
ZHOU Xiaohui*, ZHANG Jundong
(Shanghai Haohai Biological Technology Co., Ltd., Shanghai 201613, China)
ABSTRACT Objective: To establish a method for the detection of bacterial endotoxins in lidocaine hydrochloride ophthalmic gel. Methods: The valid dilution concentration and limit value of the gel for the detection of bacterial endotoxin were tested based on the Chinese pharmacopoeia 2015 edition (Volume 4). Results: The gel sample with 4-fold dilution would not interfere with the agglutination reaction between tachypleus amebocyte lysate and bacterial endotoxins and the values of bacterial endotoxin were all less than 0.5 EU/ml. Conclusion: The established method is simple, rapid, reliable and feasible for the detection of the bacterial endotoxins in lidocaine hydrochloride ophthalmic gel.
KEY WORDS lidocaine hydrochloride ophthalmic gel; bacterial endotoxins; tachypleus amebocyte lysate
盐酸利多卡因为酰胺类麻醉药,临床上已使用多年。将盐酸利多卡因制成眼用凝胶为新型眼表麻醉用药,起效快,眼部停留时间长,在眼科手术上有重要用途。为保证药品质量,降低使用风险,本研究参考中国药典2015年版四部1143细菌内毒素检查法[1]及文献[2-4]建立了鲎试剂检查眼用凝胶的方法,简便可行,结果满意。
1 实验材料与方法
1.1 仪器
Eppendorf微量取液器(50~1 000 ml);QL-901型漩涡混匀器(海门市其林贝尔仪器制造有限公司); LRH-70生化培养箱(上海一恒科学仪器有限公司);细菌内毒素检查用具(厦门鲎试剂实验厂)。
1.2 药品与试剂
细菌内毒素检查用水(厦门鲎试剂实验厂,批号160702,每支2 ml);细菌内毒素工作标准品(厦门鲎试剂实验厂,批号160301,每支15 EU);鲎试剂(厦门鲎试剂实验厂,批号160306,灵敏度0.125 EU/ml);鲎试剂(湛江安度斯生物有限公司,批号1511202,灵敏度0.125 EU/ml);眼用凝胶(上海昊海生科自制,批号160101、160102、160103,规格5 ml/支)。
1.3 方法
1.3.1 细菌内毒素限值(L)的确定
参照中华人民共和国医药行业标准YY0861-2011眼科光学眼用粘弹剂细菌内毒素检查限值为0.5 EU/ml[5]和《中国药典》2015年版(四部)附录0128冲洗剂细菌内毒素限制为0.5 EU/ml[1],确定本品细菌内毒素检查限值为0.5 EU/ml。
1.3.2 鲎试剂灵敏度复核
将细菌内毒素工作标准品用细菌内毒素检查用水溶解,在漩涡混合器上混匀15 min,然后稀释成2.0,1.0,0.5,0.25 λ(λ灵敏度标示值)4个浓度等级,按细菌内毒素检查法[1]进行灵敏度复核试验,灵敏度测定值λc均在0.5~2.0 λ之间,符合规定。
1.3.3 最大有效稀释倍数(MVD)的确定
根据公式MVD=cL/λ[5],式中L为供试品的细菌内毒素限值即0.5 EU/ml;c为供试品溶液的浓度,当L以EU/ml表示时,则c等于1.0 mg/ml;λ为主凝胶法中鲎试剂的标示灵敏度,目前市售鲎试剂的λ通常为0.5 EU/ml,0.25 EU/ml,0.125 EU/ml,0.06 EU/ml,0.03 EU/ml,故盐酸利多卡因眼凝胶的MVD分别为1、2、4、8和16倍。
1.3.4 干扰预实验
将眼用凝胶用细菌内毒素检查用水分别稀释成1、2、4、8和16倍的溶液,测定pH值在6.0~7.0范围内,符合细菌内毒素检查的pH值要求,作为供试品阴性对照(NPC)系列。另制备同样浓度的供试品系列溶液,使每一浓度的供试品溶液中都含有2 λ内毒素,作为供试品阳性对照(PPC)系列。用来自2个厂家灵敏度均为0.125 EU/ml的鲎试剂与上述NPC和PPC系列溶液进行反应,每一供试品浓度平行两管,按常规设立阳性对照(PC)管和阴性对照(NC)管,混匀后封口,置37℃恒温培养箱中反应60 min。
1.3.5 干扰试验
为了最终确认是否存在抑制因素的影响,进行正式干扰试验。取3批眼用凝胶用BET水分别稀释为若干倍稀释液,用該稀释液和细菌内毒素检查用水分别稀释细菌内毒素工作标准品,配成细菌内毒素最终浓度分别为0.25(2 λ)、0.125(λ)、0.062 5(0.5 λ)、0.031 25(0.25 λ)EU/ml的系列溶液,与2个厂家的灵敏度为0.125 EU/ml的鲎试剂反应,每个浓度平行做4管,另取供试品溶液平行2支,细菌内毒素检查用水作为阴性对照,依法进行干扰试验。
1.3.6 样品的细菌内毒素检查
取3批眼用凝胶按规定倍数稀释,使用2个厂家灵敏度λ为0.125 EU/ml的鲎试剂,按中国药典2015年版(四部)附录细菌内毒素检查法检查。
2 结果
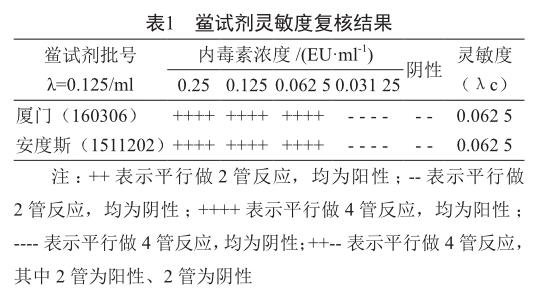
2.1 鲎试剂灵敏度复核
对2个厂家的鲎试剂进行灵敏度复核,经细菌内毒素工作标准品检测λc在0.5 ~2.0 λ之间,符合标准规定,可用于试验(表1)。
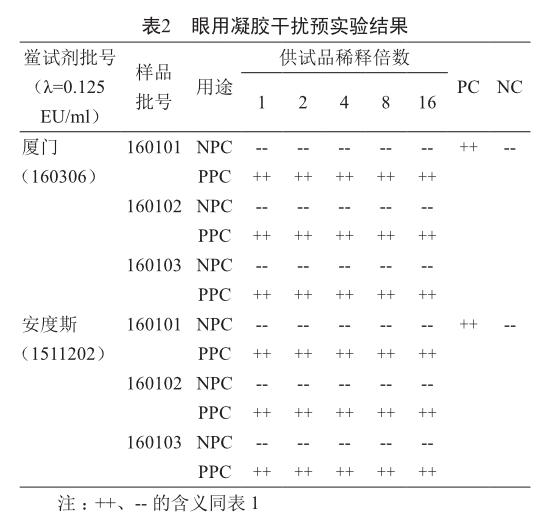
2.2 干扰预实验结果
眼用凝胶对鲎试剂与细菌内毒素之间的聚集反应无干扰,考虑到原液为凝胶状,用微量移液器无法准确吸取,稀释4倍后可准确吸取,因此选择稀释4倍为最终稀释倍数。结果见表2。
2.3 干扰试验
两个厂家鲎试剂的Es均在0.5~2.0 λ(包括0.5 λ和2.0 λ)之间,且Et在0.5~2.0 Es(包括0.5 Es和2.0 Es)的范围内(Es为用细菌内毒素检查用水制成的细菌内毒素标准溶液反应终点浓度的几何平均值,Et为用供试品溶液制成的内毒素标准溶液反应终点浓度的几何平均值),表明稀释4倍的供试品溶液对试验无干扰,可在低于或等于此浓度的情况下使用细菌内毒素检查法(表3)。
2.4 样品中细菌内毒素检测结果
3批眼用凝胶样品稀释4倍后进行细菌内毒素检测,结果表明,3批样品细菌内毒素检测均小于0.5 EU/ml,符合规定(表4)。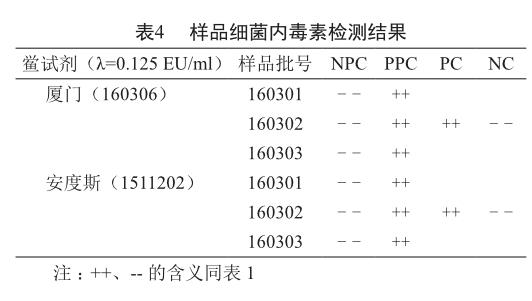
3 讨论
眼用凝胶稀释后pH为6.0~7.0,符合细菌内毒素检查供试液pH 要求标准,不干扰凝胶反应,无需调节可直接取供试品用BET 水稀释。
干扰初筛试验的目的是初步筛选出对检查无干扰的样品稀释倍数范围及相应的鲎试剂灵敏度,最终要经干扰试验验证,从表2结果初步判断样品2~16倍稀释液对细菌内毒素检查无干扰作用.理论上可选择样品2、4、8、16倍稀释液中的任一溶液,采用相应灵敏度的鲎试剂进行干扰试验,为了简化样品的稀释操作步骤并使稀释液能被准确量取,本试验选择稀释倍数为4,用灵敏度为0.125 EU/ml的鲎试剂进行干扰确证试验。
表3干扰试验结果显示,3批样品经稀释4倍后,分别使用两个不同厂家生产的鲎试剂(灵敏度均为0.125 EU/ml)进行试验,其Et/Es均在0.5~2.0之间,按照中国药典附录细菌内毒素检查干扰试验项下的判断标准,认为样品在该稀释倍数下不干扰细菌内毒素检查.
根据实验结果,确定眼用凝胶细菌内毒素检查方法如下:将本品用细菌内毒素检查用水稀释4倍,依据中国药典[1]附录细菌内毒素检查法进行检查,细菌内毒素限值定为0.5 EU/ml.
参考文献
[1] 国家药典委员会,中华人民共和国药典2015版(四部)[M]. 北京: 中国医药科技出版社,2015: 附录0128, 附录1143.
[2] 范志云, 国明.眼用平衡盐溶液细菌内毒素检查标准的制定[J].齐鲁药事, 2013, 31(8): 454-455.
[3] 陈丹丹, 付海洋, 付步芳. 纳米银妇女外用抗菌凝胶的细菌内毒素检测[J]. 生物医学工程与临床, 2010, 14(4): 282-284.
[4] 赵昕, 贺康洪, 赵文军, 等. 碘化钠注射液细菌内毒素检查方法的研究[J]. 实用药物与临床, 2014, 17(10): 1295-1297.
[5] 国家食品药品监督管理局. 眼科光学眼用粘弹剂[EB/OL]. (2011-12-31)[2017-09-17]. http://www.doc88.com/ p-9823778633625.html.
