“溶液中离子能否大量共存”的判定与应用
2018-05-09陆桂斌
陆桂斌
(江苏省泰州市智堡实验学校 225300)
多数可溶物质溶于水,会以离子的形式分散到水中,形成均匀、稳定的混合物——溶液.离子在溶液中能够大量“共存”,通俗地说是指不同离子在同一溶液中不发生化学反应;反之,不同离子相互接触后能生成气体、水或沉淀等,即发生化学反应,这类离子在同一溶液中则不能“共存”.
离子共存类试题在历年各地的中考试题中频繁出现,而因缺少系统的知识储备,多数学生对其都有一种天然的“恐惧”感,严重影响了学生对酸碱盐类化合物性质规律的学习.本文拟对其作系统梳理、归纳,以提高学生综合解题能力.
一、溶液中不能大量共存(即相互能发生化学反应)的离子组
参考《义务教育化学课程标准(2012修订稿)》,结合笔者多年教学实践,现归纳出九年级化学学科中以下十组不可共存离子最为典型:
1.反应时有气体生成(多数还有水)的离子组



2.反应时有水生成的离子组
(4)H++OH-→H2O
3.反应时有沉淀生成的离子组
(5)Ag++Cl-→AgCl↓






(10)Fe3++ OH-→Fe( OH)3↓

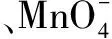
二、“离子共存”类中考试题分类评析
1.直接考查溶液中离子能否大量共存
例1(2016·江苏南京)下列各组离子在水中能大量共存的是( ).
B.H+、K+、Cl-、OH-
C.Cu2-、Ba2+、Cl-、SO42-
D.K+、NH+、Cl-、NO3-
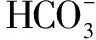
2.“隐身”关键离子,考查溶液中离子能否大量共存
例2 (2016·湖南湘潭)下列各组离子在pH=1的溶液中能大量共存,并形成无色透明溶液的是( ).

3.以宏观物质为载体,间接考查溶液中离子能否大量共存
例3 (2016·湖北襄阳)下列各组物质分别加入到足量水中,最终能得到无色、透明溶液的是( ).
A.NaOH、NaCl、KNO3、MgCl2
B.NaOH、Na2CO3、NaCl、H2SO4
C.NaCl、Na2SO4、AgNO3、HNO3
D.FeSO4、NaNO3、KCl、 HCl
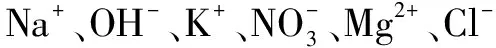
4.综合考查化学方程式与离子方程式关系,揭示复分解反应实质


(1)下列各组中的离子,在pH=3的水溶液中能大量共存的是____.
(2)写出稀盐酸滴在石灰石上所发生反应的离子方程式____;
(3)写出一个与离子方程式

相对应的化学方程式____;
(4)酸、碱、盐在水溶液中发生的复分解反应实质上就是两种化合物在溶液中相互交换离子的反应,只要具备生成物中有气体或沉淀或____生成,反应就能发生.


再删去方程两边不参加反应的Cl-.(3)与(2)的解题思路互逆,反向考虑即可.(4)依据前述分析可知:离子间反应可生成气体、沉淀或水,即复分解反应的实质和发生条件.

5.联系生活实际,变换考查溶液中离子能否大量共存
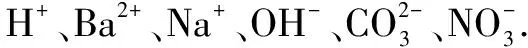
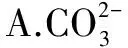

C.H+和Ba2+一定不在同一工厂

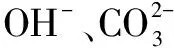
参考文献:
[1]郑永红.义务教育化学“科学探究”内容解析[J].新课程学习(中),2014(11).
