纳米Ag包覆Bi2O3颗粒的制备及其可见光催化性能评价
2018-05-08亚鲁
,,,,亚鲁
(1.天津大学理学院化学系,天津 300354; 2.天津大学化工学院,津南区海河教育园区,天津 300354)
1 前 言
Bi2O3是一种重要的P型半导体材料[1],具有较宽的带隙能范围2~3.96eV,对太阳光的响应明显好于TiO2[2-3]。Bi2O3主要有四种晶相,分别为单斜α-Bi2O3、四方β-Bi2O3、体心立方γ-Bi2O3、面心立方δ-Bi2O3[4-5],其中β-Bi2O3的光催化活性较显著。纯相Bi2O3表现出较差的光催化活性,这与其表面存在较少的有效陷阱,阻止光生电子-空穴复合能力相对有限有关。欲提高Bi2O3的光催化活性,其一是增强材料的可见光利用率,其二是有效抑制光生电子与光生空穴的复合[6]。
利用具有纳米结构的贵金属如Au、Ag、Pt等沉积或掺杂,可有效改善半导体材料TiO2的光催化活性[7-8]。适量的贵金属沉积在TiO2的表面,不仅能增加催化剂的比表面积,还可使电子从费米能级高的半导体流向费米能级低的贵金属,从而使载流子重新分布,形成肖特基势垒,抑制光生电子与空穴的复合。通过贵金属修饰也同样可改善Bi2O3的光催化性能,Pugazhenthiran等[9]通过水热法和超声合成法制备Au沉积的Bi2O3,Au/Bi2O3复合材料具有纳米棒和纳米颗粒混合形貌,相比纯相Bi2O3其光催化性能提升了3.5倍,对酸性橙10表现出了良好的矿化效果。Jiang等[10]通过化学沉淀法制备α-Bi2O3颗粒,进而在碱性条件下水解HAuCl4,使Au单质沉积于α-Bi2O3表面,在可见光下降解罗丹明B和2,4-二氯苯酚,Au/α-Bi2O3的降解效果明显好于纯相Bi2O3,其中1.0wt% 的Au/α-Bi2O3催化效果最佳。Li等[11]通过光还原法制备Pt/Bi2O3复合催化剂,该催化剂对甲醇、甲醛等有机组份均可进行光催化,且Pt的沉积量为3%(质量比)时其光催化效果最好,随着沉积量继续增大,其光催化效果则呈现降低趋势。考虑到Au、Pt等原料成本较高,故本研究选择较为廉价的Ag对Bi2O3进行表面修饰。
2 实验方法
2.1 实验试剂
实验原料为分析纯的硝酸铋、硝酸、硝酸银、硼氢化钠、甲基橙、无水乙醇等,实验用水为去离子水。
2.2 样品制备
化学共沉淀工艺制备Bi2O3光催化剂:分别配制0.2mol·L-1Bi(NO3)3溶液和1.2mol·L-1的氨水溶液(作沉淀剂),在强力机械搅拌作用下,逐滴加入pH值为9~10的基液中,控制滴加速率1d·s-1。待滴加完毕后继续搅拌30min,陈化1h,抽滤、水洗4~5遍、醇洗2遍后,80℃真空干燥,研磨过筛,按一定升温程序于450℃煅烧2h,制得Bi2O3纳米粉体。将纯相Bi2O3纳米粉体标记为A0。
室温原位还原法制备Ag/β-Bi2O3光催化剂:将上述方法制备的纯相Bi2O3为载体,按Ag/Bi2O3(质量比)为1.0%、2.0%、3.0%的比例加入AgNO3溶液,分别配制成一定体积的悬浮液,超声振荡30min,使β-Bi2O3充分分散,加入适量NaBH4将AgNO3还原成单质Ag颗粒沉积于Bi2O3纳米粉体上,静置30min后离心洗涤4~5遍,于80℃真空干燥后制得Ag/β-Bi2O3光催化剂,分别标记为A1、A2和 A3。
2.3 样品表征
采用RigakuD/max-2500型X射线衍射仪对样品的相组成进行分析,Cu Kα辐射,管电压为40kV,管电流为200mA,扫描范围为10~80°。采用JEM-2100F型场发射透射电镜观察样品形貌及元素分布。采用UV-3600型紫外-可见分光光度计测定固体样品的紫外-可见(UV-Vis)漫反射光谱(UV-Vis DRS),以光谱纯BaSO4做参照。采用F-380型荧光分光光度计测定固体样品的荧光强度,光源为氙灯。
2.4 样品的光催化性能评价
向50mL 浓度为20mg·L-1的甲基橙模拟有机染料废水溶液中,分别加入0.1g所制备的四种样品。将悬浊液转移到自制夹套式光催化反应器中进行可见光下降解MO的实验,光反应器的光源为用滤镜滤去紫外光的300W可见光光源(λ=400~780nm)。光源距离液面约为10cm。夹套中通循环水使反应体系温度维持室温。每隔一定时间取反应溶液,经针头过滤器得到光降解后的底物溶液。然后采用UV/V-1600紫外可见分光光度计测定其在464nm波长处的吸光度,以反应前后溶液吸光度的变化率表示MO的降解率。降解率的计算公式为:D=(c0-c)/c0×100%,式中:D为降解率,c0和c分别为MO的初始浓度和反应后浓度。
3 结果与讨论
3.1 X射线衍射(XRD)分析
图1列出未沉积Ag的样品A0和沉积Ag的样品A2的XRD图谱,其它Ag沉积样品A1和A3的相组成与A2相同,此处略。从图1看出,A0样品的三强衍射峰分别出现在2θ为 27.80°、32.71°、45.82°处,为β-Bi2O3(201)、(220)、(222)晶面衍射所致,与标准图谱(JCPDS No.76-0147)相吻合,证明A0样品为β-Bi2O3相,属四方晶型。结合Scherrer公式[12]D=Kλ/βcosθ, 式中:D为晶体尺寸(nm);K为Scherrer常数,其值为0.89;β为强衍射峰的积分半高宽度(rad);λ为X射线波长,为0.154nm;θ为衍射角(rad)。计算得出A0样品的平均晶粒尺寸为26.98nm,粒径较小,比表面积大,对光催化性能有利。样品A2的XRD图谱中除包含β-Bi2O3的特征衍射峰外,在2θ为38.12°、44.28°及77.47°处还出现单质Ag的特征峰,分别为Ag(111)、(220)、(311)晶面衍射所致,与JCPDS No.04-0783标准图谱[13]相吻合。单质Ag的特征峰相对较弱,表明晶体结晶度程度不高。
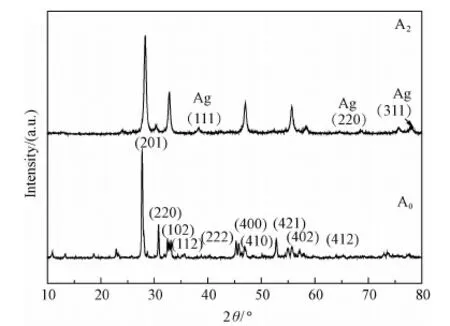
图1 样品A0和A2的XRD谱图Fig.1 XRD patterns of sample A0 and A2
3.2 TEM及HRTEM分析
以典型样品A2为例,由图2(a)可见,纳米Ag均匀包覆于β-Bi2O3颗粒表面。中间团聚程度较大的颗粒为β-Bi2O3,形貌不规则,粒径约30nm;表层包覆着分散较好的纳米Ag颗粒,粒径在20nm以内。图2(b)显示晶粒为典型的多晶结构。图中标出了β-Bi2O3的(201)衍射晶面,对应晶面间距 d=0.321nm,与文献[14]一致。外部标出了纳米Ag的晶面间距 d=0.231nm,对应单质Ag的(111)晶面衍射,与文献[15]相符。图2(c)示出样品中O、Bi、Ag的元素比例。图2(d)、(e)、(f)、(g)则示出样品A2中的O、Bi、Ag元素的mapping分布, Ag元素主要分布在β-Bi2O3颗粒表面。包覆于Bi2O3颗粒表面的纳米Ag会进一步增大原β-Bi2O3颗粒的比表面积,且结合紧密,不会脱落。
3.3 紫外-可见漫反射光谱分析

图2 (a)A2样品的低分辨TEM照片;(b)HRTEM照片及(c)EDS能谱;(d)A2样品中的颗粒照片;(e)、(f)、(g)分别表示A2样品中的O分布,Bi分布和Ag分布Fig.2 TEM image (a), HRTEM image (b) and EDS spectrum (c) of sample A2; A2 particles (d) and its element distribution of O (e), Bi (f) and Ag (g)
图3为纯相β-Bi2O3样品A0及Ag/β-Bi2O3样品A2的UV-Vis漫反射吸收光谱。所制备样品在400~800nm的可见光波段均显示出不同程度的吸收。利用经验公式Eg=1240/λg,式中Eg为能级带隙,λg为样品的光吸收阈值,通过对UV-Vis漫反射吸收曲线作切线,切线与x轴相交点即为样品的光吸收阈值λg[16],样品A0、A2的λg值分别为560nm和580nm,代入经验公式计算得到A0、A2样品的能级带隙分别为2.21eV和2.14eV。Ag沉积Bi2O3样品的带隙能有所减小。带隙能的大小决定了光催化剂对光的利用情况,随着带隙能减小,吸收波长红移,对可见光的利用率提高。对于Ag/β-Bi2O3复合颗粒,带隙能减小可能是由于Ag和Bi2O3有不同的费米能级,可以在接触面上形成肖特基势垒,这意味着在可见光照射下能产生更多的光生电子和空穴对,从而提高了催化剂的光催化反应效率。

图3 样品A0和A2的UV-Vis漫反射吸收光谱图Fig.3 UV-Vis diffuse reflectance spectra of sample A0 and A2
3.4 荧光光谱分析
图4 为A0、A2样品的光致发光光谱图。两个样品在350~600nm范围内的光致发光图谱基本一致。只是对荧光的响应强度不同,A2样品的荧光强度明显低于A0样品。研究表明半导体氧化物的荧光现象与荧光激发的光生电子和空穴的复合有关[17],光生电子与空穴的复合速率越快,荧光强度越大。结合PL谱图结果,不难发现A2中光生电子与空穴的复合速率要比A0样品中小。

图4 样品A0和A2的光致发光光谱图Fig.4 PL spectra of sample A0 and A2
3.5 样品的催化活性
图5(a)为A0及不同Ag沉积量的A1,A2和A3样品对甲基橙的光催化降解率图。由图可知,三种Ag沉积Bi2O3样品的光催化效果都明显优于纯相Bi2O3,且Ag沉积量为2.0%的A2样品的光催化降解的效果最佳。实验结果表明光催化剂投加量为2g·L-1时,A0、A1、A2和A3样品在可见光催化作用下,降解20mg·L-1甲基橙1h的降解率D分别为48.93、82.60、95.48和75.56%。Ag沉积量控制在2.0%时,A2样品的光催化降解率高达95%以上。当Ag沉积量超过2.0%,光催化活性反而降低。这可能是由于Bi2O3表面沉积的Ag量过多,阻碍了Bi2O3光催化剂对可见光的利用,影响其光催化效果。

图5 (a)实验所制备光催化剂样品对MO的降解率; (b)MO降解的准一级动力学曲线Fig.5 Photocatalytic degradation ratio of MO as a function of irradiation time (a) and Pseudo-first-order kinetics curves of MO degradation(b)
非均相光催化反应速率方程可用L-H方程描述[18],当溶液浓度较小时,该方程经转化后积分得到准一级动力学方程:-ln(c/c0)=kt[19],其中c0为MO的起始浓度,c为反应后浓度,k为表观速率常数。以ln(c/c0)对t作图即绘制出图5(b),为MO光催化降解的准一级反应动力学图,其相关系数R2均大于0.98。通过直线的斜率可求解降解反应速率常数k,光催化剂样品A0,A1,A2和A3在可见光下降解20mg·L-1MO的速率常数k分别为0.678、1.639、3.064、1.332 h-1。即1 h 内的平均降解速率分别为4.90、8.26、9.54和7.56mg·(h·g)-1,即随着Ag沉积量的增加,光催化降解甲基橙的速率呈现先增加后减小的趋势。与商业TiO2光催化剂P25比较,A0、A1、A2和A3样品在可见光下的催化活性显著提高[20]。

图6 Ag/Bi2O3光催化剂降解MO的氧化反应机理图Fig.6 MO degradation reaction mechanism by oxidation process of Ag/Bi2O3 photocatalysts

4 结 论
1.采用化学共沉淀法,以硝酸铋为原料,氨水为沉淀剂,成功制备了四方晶型β-Bi2O3纳米颗粒。采用室温原位还原法制备三种不同Ag沉积量的Ag/β-Bi2O3复合颗粒。纳米Ag包覆于β-Bi2O3的表面,粒径控制在20nm。Ag沉积后样品对可见光的吸收能力增加,带隙能降低。
2.当Ag沉积量为2.0%时,Ag/β-Bi2O3样品的光催化性能最好。即催化剂投加量为2g·L-1时,在可见光下光照 1h对20mg·L-1的甲基橙溶液降解率可达 95.48%。对甲基橙光催化降解过程符合准一级反应动力学特征。
3.Ag/β-Bi2O3样品相比纯相Bi2O3催化性能提高的主要原因是贵金属Ag作为电子陷阱,延长电子和空穴的复合路径,有效抑制了光生电子与空穴的复合,从而提高催化剂的光催化活性。
[1] Hsieh S H, Manivel A, Lee G J, et al. Synthesis of Mesoporous Bi2O3/CeO2Microsphere for Photocatalytic Degradation of Orange II Dye[J]. Materials Research Bulletin, 2013, 48(10): 4174~4180.
[2] Qin W, Qi J, Wu X H. Photocatalytic Property of Cu2+-doped Bi2O3Films under Visible Light Prepared by the Sol-gel Method[J]. Vacuum, 2014, 107(3):204~207.
[3] Dai H, Song Z. One-step Electrochemical Synthesis and Visible-light Photocatalytic Activities of Bismuth Titanate Coatings: Effect of Voltage[J]. Ceramics International, 2015, 41(1):853~857.
[4] Ai Z, Huang Y, Lee S, et al. Monoclinic α-Bi2O3Photocatalyst for Efficient Removal of Gaseous NO and HCHO under Visible Light Irradiation[J]. Journal of Alloys & Compounds, 2011, 192(509):2044~2049.
[5] Cabot A, Marsal A, Arbiol J, et al. Bi2O3as a Selective Sensing Material for NO Detection[J]. Sensors & Actuators B Chemical, 2004, 99(1):74~89.
[6] Raza W, Haque M M, Muneer M, et al. Synthesis, Characterization and Photocatalytic Performance of Visible Light induced Bismuth Oxide Nanoparticle[J]. Journal of Alloys & Compounds, 2015, 648:641~650.
[7] 李贵安, 焦飞, 邓仲勋,等. Ag掺杂APS改性的TiO2颗粒的制备及其光催化降解作用[J]. 材料科学与工程学报, 2011, 29(5): 702~706.
[8] 王佳, 胡荣, 王智宇. 紫外诱导水相条件下Ag修饰TiO2纳米棒的制备及光催化性能[J]. 材料科学与工程学报, 2013, 31(4): 521~524.
[9] Pugazhenthiran N,Sathishkumar P,Murugesan S, et al. Effective Degradation of Acid Orange 10 by Catalytic Ozonation in the Presence of Au-Bi2O3Nanoparticles[J]. Chemical Engineering Journal, 2011, 168(3):1227~1233.
[10] Jiang H Y, Cheng K, Lin J. Crystalline Metallic Au Nanoparticle-loaded α-Bi2O3Microrods for Improved Photocatalysis[J]. Physical Chemistry Chemical Physics, 2012, 14(35):12114~12121.
[11] Li R H, Chen W X, Kobayashi H, et al. Platinum- nanoparticle-loaded Bismuth Oxide: an Efficient Plasmonic Photocatalyst Active under Visible Light[J]. Green Chemistry, 2010, 12(2):212~215.
[12] Liu X, Deng H, Yao W, et al. Preparation and Photocatalytic Activity of Y-doped Bi2O3[J]. Journal of Alloys & Compounds, 2015, 651(4):738~742.
[13] 杨靖, 李悦, 李鹏程. Ag/SiO2抗菌材料的制备及抗菌性能研究[J]. 材料导报, 2014, 28(20):34~37.
[14] Hao Y J, Li F T, Wang S S, et al. One-step Combustion Synthesis of β-Bi2O3-NiO/Ni Composites and their Visible Light Photocatalytic Performance[J]. Materials Science & Engineering B, 2014, 186(1):41~47.
[15] Akaighe N, Depner S W, Banerjee S, et al. The Effects of Monovalent and Divalent Cations on the Stability of Silver Nanoparticles Formed from Direct Reduction of Silver Ions by Suwannee River Humic Acid/Natural Organic Matter[J]. Science of the Total Environment, 2012, 441C(20):277~289.
[16] Zhong J, Li J, Feng F, et al. Improved Photocatalytic Decolorization of Methyl Orange over Pd-doped Bi2O3[J]. Environmental Progress and Sustainable Energy, 2014, 33(4):1229~1234.
[17] 刘国聪,李海斌,董辉. La 掺杂 TiO2介孔微球的超声水热合成和光催化性能[J]. 无机材料学报, 2011, 26(7): 739~746.
[18] Xu J J,Chen M D,Fu D G. Preparation of Bismuth Oxide/Titania Composite Particles and their Photocatalytic Activity to Degradation of 4-chlorophenol[J].Transactions of Nonferrous Metals Society of China, 2011,21(2):340~345.
[19] Bessergenev V G, Mateus M C, Botelho do Rego A M, et al. An Improvement of Photocatalytic Activity of TiO2Degussa P25 powder[J].Applied Catalysis A General, 2015,500:40~50.
[20] Zou H, Song J X, Liu P, et al. Photocatalytic Research of Bi2O3/TiO2Composite Catalysts on Methyl Orange[J].Journal of Wuhan University of Technology,2014,36(9):12~16.
