UPLC-MS分析柴胡、白芍水煎液的化学成分及其对逍遥散的贡献
2018-05-08高晓霞田俊生秦雪梅杜冠华周玉枝
贺 晶,高晓霞,田俊生,秦雪梅,杜冠华,2,周玉枝*
(1山西大学中医药现代研究中心,太原 030006;2中国医学科学院药物研究所;*通讯作者,E-mail:zhouyuzhi@sxu.edu.cn)
逍遥散源于仲景四逆散与当归芍药散合方,其方名首见于宋代《太平惠民和剂局方》[1],其“消散其气郁,摇动其血郁,皆无伤乎正气也”,为疏肝解郁、养血健脾的代表方,亦为养血调肝的基础方,更是妇科调经的常用方,还能辅助治疗抑郁症,为临床常用药,疗效好[2],并衍化出了许多有效良方,代表性者如丹栀逍遥散,柴胡疏肝散等,形成了逍遥散类方[3]。柴胡、白芍作为逍遥散主要组成药味,为多个抗抑郁疗效确切的复方如《太平惠明和剂局方》逍遥散[4-6]、《景岳全书》柴胡舒肝散[7-9]、《伤寒论》四逆散[10]等的基础药物,在方中柴胡为君药,白芍为臣药。施学丽等[11]对128首治疗抑郁症的中药专利复方进行研究,结果发现配伍频数较高的中药中柴胡居首,白芍位列第三,常用的药对中柴胡-白芍居首。因此柴胡、白芍对抗抑郁发挥重要作用。本实验室对逍遥散的抗抑郁作用进行了大量研究,因此,采用超高效液相色谱质谱联用(UPLC-MS/MS)技术分析柴胡、白芍化学成分及对逍遥散的贡献十分必要。
超高效液相色谱质谱联用(UPLC-MS/MS)技术作为一种新型的分析技术可以提供良好的分离效果,具有高分辨、高灵敏的定性能力和强大的结构表征能力,已广泛运用到中药药效物质基础、中药化学成分分析、代谢组学等研究领域中。本文采用UPLC-ESI-Q/exactive-orbitrap技术对柴胡、白芍水煎剂中化学成分进行快速分析,最终确认其作为君臣药对逍遥散的贡献,为后期研究柴胡-白芍药对抗抑郁作用及其配伍前后化学成分的变化奠定基础。
1 材料
超高效液相色谱与质谱联用仪(Thermo Scientific Q Exactive LC-MS),美国Thermo公司;色谱柱:ACQUITY UPLC HSS T3(2.1 mm×100 mm,1.8 μm),十八烷基键合硅胶为填充剂,美国Waters公司;超声波清洗器(KQ5200E),昆山市超声仪器有限公司;分析天平(XPE205,梅特勒-托利多国际股份有限公司);色谱乙腈(Fisher scientific);纯净水(杭州娃哈哈集团有限公司);色谱甲酸(Fisher scientific);柴胡、白芍等饮片由安徽安国市祁澳中药饮片有限公司提供。
2 方法与结果
2.1 方法
2.1.1 样品制备 白芍供试液制备:准确称取白芍饮片5 g,置200 ml烧瓶中,加10倍量水煎煮,第1次煎煮2 h,第2次煎煮1.5 h。合并煎煮液,放冷、高速离心(15 000 r/min)、抽滤。取10 ml滤液,过0.22 μm微孔滤膜,得供试液。
柴胡供试液制备:准确称取柴胡饮片5 g,置200 ml烧瓶中,加10倍量水煎煮,第1次煎煮2 h,第2次煎煮1.5 h。合并煎煮液,放冷、高速离心(15 000 r/min)、抽滤。取10 ml滤液,过0.22 μm微孔滤膜,得供试液。
逍遥散供试液制备:柴胡、当归、白芍、白术、茯苓、炙甘草、薄荷、生姜按6 ∶6 ∶6 ∶6 ∶6 ∶3 ∶2 ∶2比例称取药材,第1次煎煮2 h,第2次煎煮1.5 h。合并煎煮液,放冷、高速离心(15 000 r/min)、抽滤。取10 ml滤液,过0.22μm微孔滤膜,得供试液。
2.1.2 色谱条件 ACQUITY UPLC HSS T3(2.1 mm×100 mm,1.8 μm)色谱柱;柱温20 ℃;流动相为含乙腈(A)-0.1%的甲酸水溶液(B);梯度洗脱程序:0-8 min,5%-10%A;8-18 min,10%-17%A;18-26 min,17%-20%A;26-31 min,20%-26%A;31-39 min,26%-31%A;39-44 min,31%-35%A;44-52 min,35%-40%A;52-62 min,40%-60%A;62-65 min,60%-100%A;65-66 min,100%-5%A;66-68 min,5%A。体积流量为0.3 ml/min;进样量为1 μl。
2.1.3 质谱条件 采用电喷雾离子源正负离子检测的电离模式,雾化气体为高纯度氮气(N2),碰撞气体为高纯度氦气(He)。采用全扫描和二级质谱扫描,质量扫描范围:100-1 500 Da,毛细管电压正负离子模式下分别为3.5 kV、2.5 kV,碰撞能量为50-80 V,脱溶剂气体温度正负离子模式下300 ℃。毛细管温度320 ℃,脱溶剂气体流速600 L/h,锥体气孔流量50 L/h。
2.2 结果
2.2.1 柴胡、白芍化学成分分析及其对逍遥散归属 按1.3下色谱条件以乙腈-0.l%甲酸水溶液为流动相进行梯度洗脱可得到较好的高效液相色谱分离效果,采用UPLC-MS对柴胡、白芍、逍遥散水提成分进行定性分析,负离子总离子流(TIC)图见图l。通过UPLC-MS检测得到柴胡、白芍、逍遥散中各化学成分的保留时间和质谱信息,结合提取离子流图及相关文献数据对比进行化学成分确认,结果见表1。
2.2.2 柴胡中皂苷类化合物结构解析及对逍遥散的归属
2.2.2.1 柴胡中皂苷类化合物结构解析 对于柴胡白芍来说,皂苷类化合物主要来源于柴胡。柴胡皂苷类成分均属于齐墩果烷型衍生物,并含有葡萄糖、呋糖、鼠李糖等糖链结构,呈现一定的质谱裂解规律,结合文献[14-21]共鉴定柴胡中皂苷类成分13个,分别为柴胡皂苷c、柴胡皂苷a、柴胡皂苷g、柴胡皂苷b2、2"-O-乙酰化柴胡皂苷a、3"-O-乙酰化柴胡皂苷a、4"-O-乙酰化柴胡皂苷a、6"-O-乙酰化柴胡皂苷a、2"-O-乙酰化柴胡皂苷d、3"-O-乙酰化柴胡皂苷d、4"-O-乙酰化柴胡皂苷d、柴胡皂苷d、6"-O-乙酰化柴胡皂苷d。现以柴胡皂苷b2为例,解析柴胡皂苷类成分的裂解规律(见图2)。
柴胡皂苷b2的二级质谱图有m/z779.458 9、m/z617.405 8、m/z439.321 6三个主要碎片离子,m/z617.405 8碎片是由m/z779.458 9丢失162 Da的中性碎片所致,而m/z617.405 8碎片丢失146 Da的碎片得m/z471.351 8碎片,m/z471.351 8碎片丢失32 Da的碎片得m/z439.321 6碎片。按照柴胡皂苷c的裂解规律及其参考文献指认其他柴胡皂苷类成分。

图1 逍遥散、柴胡、白芍负离子模式下TIC图Figure 1 TIC of Xiaoyao powder, Bupleurum, Radix Paeoniae Alba under the negative ion mode
2.2.2.2 柴胡中皂苷类化合物对逍遥散的归属 为了确定逍遥散中鉴定出的某一物质确实来源于柴胡,采用对比单味药柴胡及复方逍遥散的一级、二级质谱图,加以确认。具体以柴胡皂苷b2为例,柴胡皂苷b2的一级质谱图见图3,柴胡皂苷b2的二级质谱图见图4。
2.2.3 单萜苷类化合物结构解析及对逍遥散的归属
2.2.3.1 单萜苷类化合物结构解析 白芍中的单萜苷类化合物主要有白芍苷、芍药苷、氧化芍药苷、苯甲酰芍药苷、苯甲酰芍药苷亚硫酸酯等。结合文献[22-32]及其裂解规律,白芍中鉴定的31个化合物,其中单萜苷类有22个。现以芍药苷为例,解析白芍单萜苷类成分的裂解规律见图5。tR为14.23 min,负离子模式下准分子离子峰为479.155 8[M-H]-,脱去1分子HCHO后形成449.145 3[M-H-CH2O]-碎片离子,脱去1分子苯甲酸后形成357.119 2[M-H-benzoic acid]-碎片离子,再脱去1分子HCHO后形成327.108 6[M-H-benzoic acid-CH2O]-碎片离子,最后形成苯甲酸121.028 7[ben-zoic acid-H]-碎片离子。按照芍药苷的裂解规律[29]及参考文献指认其他单萜苷类成分。
表1柴胡、白芍水煎液化学成分分析及对逍遥散的归属
Table1ChemicalconstituentsofBupleuriRadixandPaeoniaeRadixAlbadecoctionandtheirascriptiontoXiaoyaopowder
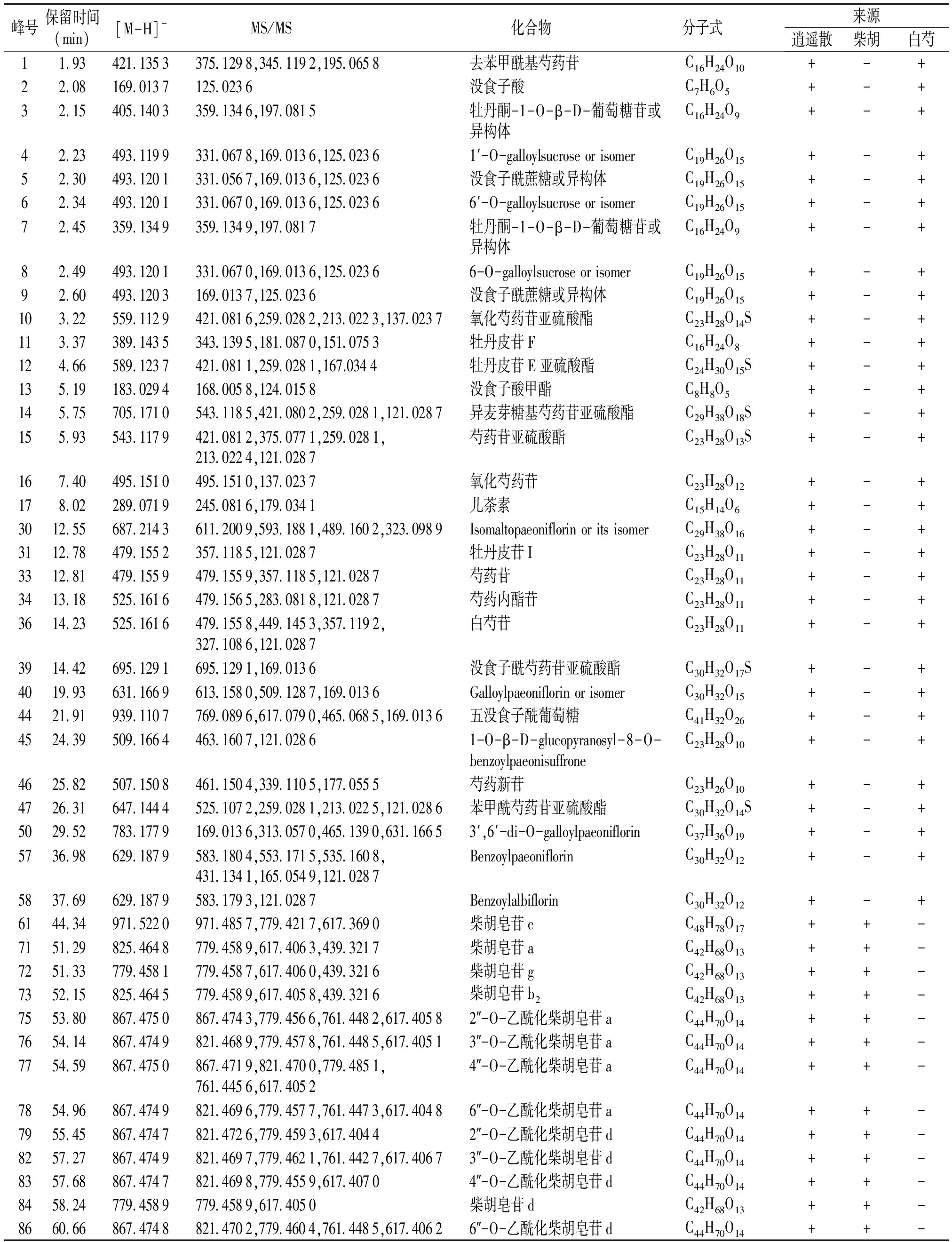
峰号保留时间(min)[M-H]-MS/MS 化合物 分子式 来源逍遥散柴胡白芍119342113533751298,3451192,1950658去苯甲酰基芍药苷C16H24O10+-+220816901371250236没食子酸C7H6O5+-+321540514033591346,1970815牡丹酮-1-O-β-D-葡萄糖苷或异构体C16H24O9+-+422349311993310678,1690136,12502361′-O-galloylsucroseorisomerC19H26O15+-+523049312013310567,1690136,1250236没食子酰蔗糖或异构体C19H26O15+-+623449312013310670,1690136,12502366′-O-galloylsucroseorisomerC19H26O15+-+724535913493591349,1970817牡丹酮-1-O-β-D-葡萄糖苷或异构体C16H24O9+-+824949312013310670,1690136,12502366-O-galloylsucroseorisomerC19H26O15+-+926049312031690137,1250236没食子酰蔗糖或异构体C19H26O15+-+1032255911294210816,2590282,2130223,1370237氧化芍药苷亚硫酸酯C23H28O14S+-+1133738914353431395,1810870,1510753牡丹皮苷FC16H24O8+-+1246658912374210811,2590281,167.0344牡丹皮苷E亚硫酸酯C24H30O15S+-+1351918302941680058,1240158没食子酸甲酯C8H8O5+-+1457570517105431185,4210802,2590281,1210287异麦芽糖基芍药苷亚硫酸酯C29H38O18S+-+1559354311794210812,3750771,2590281,2130224,1210287芍药苷亚硫酸酯C23H28O13S+-+1674049515104951510,1370237氧化芍药苷C23H28O12+-+1780228907192450816,1790341儿茶素C15H14O6+-+30125568721436112009,5931881,4891602,3230989IsomaltopaeoniflorinoritsisomerC29H38O16+-+31127847915523571185,1210287牡丹皮苷IC23H28O11+-+33128147915594791559,3571185,1210287芍药苷C23H28O11+-+34131852516164791565,2830818,1210287芍药内酯苷C23H28O11+-+36142352516164791558,4491453,3571192,3271086,1210287白芍苷C23H28O11+-+39144269512916951291,1690136没食子酰芍药苷亚硫酸酯C30H32O17S+-+40199363116696131580,5091287,1690136GalloylpaeoniflorinorisomerC30H32O15+-+44219193911077690896,6170790,4650685,1690136五没食子酰葡萄糖C41H32O26+-+45243950916644631607,12102861-O-β-D-glucopyranosyl-8-O-benzoylpaeonisuffroneC23H28O10+-+46258250715084611504,3391105,1770555芍药新苷C23H26O10+-+47263164714445251072,2590281,2130225,1210286苯甲酰芍药苷亚硫酸酯C30H32O14S+-+50295278317791690136,3130570,4651390,63116653′,6′-di-O-galloylpaeoniflorinC37H36O19+-+57369862918795831804,5531715,5351608,4311341,1650549,1210287BenzoylpaeoniflorinC30H32O12+-+58376962918795831793,1210287BenzoylalbiflorinC30H32O12+-+61443497152209714857,7794217,6173690柴胡皂苷cC48H78O17++-71512982546487794589,6174063,4393217柴胡皂苷aC42H68O13++-72513377945817794587,6174060,4393216柴胡皂苷gC42H68O13++-73521582546457794589,6174058,4393216柴胡皂苷b2C42H68O13++-75538086747508674743,7794566,7614482,61740582″-O-乙酰化柴胡皂苷aC44H70O14++-76541486747498214689,7794578,7614485,61740513″-O-乙酰化柴胡皂苷aC44H70O14++-77545986747508674719,8214700,7794851,7614456,61740524″-O-乙酰化柴胡皂苷aC44H70O14++-78549686747498214696,7794577,7614473,61740486″-O-乙酰化柴胡皂苷aC44H70O14++-79554586747478214726,7794593,61740442″-O-乙酰化柴胡皂苷dC44H70O14++-82572786747498214697,7794621,7614427,61740673″-O-乙酰化柴胡皂苷dC44H70O14++-83576886747478214698,7794559,61740704″-O-乙酰化柴胡皂苷dC44H70O14++-84582477945897794589,6174050柴胡皂苷dC42H68O13++-86606686747488214702,7794604,7614485,61740626″-O-乙酰化柴胡皂苷dC44H70O14++-
[M-H]-表示化合物在负离子模式下的一级碎片离子;MS/MS表示该化合物在负离子模式下的二级碎片离子

图2 柴胡皂苷b2的裂解规律Figure 2 Proposed fragmentation pathways of saponins b2

图3 柴胡皂苷b2的一级质谱图Figure 3 MS spectra of Bupleurum saponins b2

图4 柴胡皂苷b2的二级质谱图Figure 4 MS2 spectra of Bupleurum saponins b2
2.2.3.2 单萜苷类化合物对逍遥散的归属 为了确定逍遥散中鉴定出的某一物质确实来源于白芍,采用对比单味药白芍及复方逍遥散的一级、二级质谱图,加以确认。具体以芍药苷为例,芍药苷的一级质谱图见图6,芍药苷的二级质谱图见图7。
2.2.4 其他化合物结构解析及对逍遥散的归属
2.2.4.1 其他化合物结构解析 白芍的水提物中共分离提取出的酚类化合物和没食子酰基葡萄糖类化合物在逍遥散中分离提取出两个,分别为没食子酸和6-O-没食子酰蔗糖或异构体(6-O-gal-loylsucrose or isomer)。其裂解规律如下:没食子酸tR为2.08 min,负离子模式下准分子离子峰为m/z169.013 7 [M-H]-,脱去1分子CO2形成特征碎片m/z125.023 6[M-H-CO2]-。6-O-没食子酰蔗糖或异构体tR为2.49 min,负离子模式下准分子离子峰为m/z493.120 1[M-H]-,脱去1分子葡萄糖(Glc)形成特征碎片m/z331.067 0[M-H-C6H10O5]-,再脱去1分子Glc后形成169.013 6[M-H-2C6H10O5]-碎片离子、在此基础上再脱去1分子CO2后形成125.023 6[M-H-2C6H10O5-CO2]-碎片离子。没食子酸的裂解规律见图8。
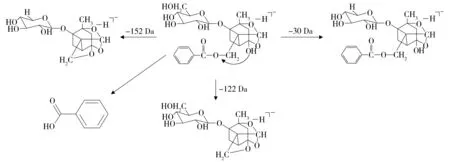
图5 芍药苷裂解规律Figure 5 Proposed fragmentation pathways of paeoniflorin
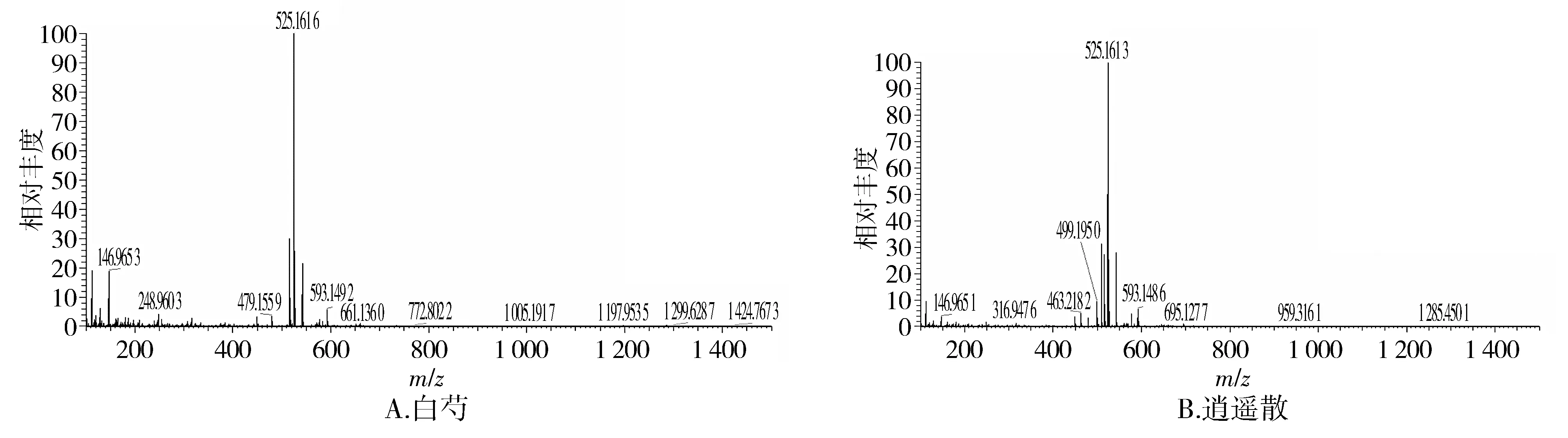
图6 芍药苷的一级质谱图Figure 6 MS spectra of paeoniflorin

图7 芍药苷的二级质谱图Figure 7 MS2 spectra of paeoniflorin
2.2.4.2 其他化合物对逍遥散的归属 为了确定逍遥散中鉴定出的某一物质确实来源于白芍,采用对比单味药白芍及复方逍遥散的一级、二级质谱图,加以确认。具体以没食子酸为例,没食子酸的一级质谱图见图9,没食子酸的二级质谱图见图10。
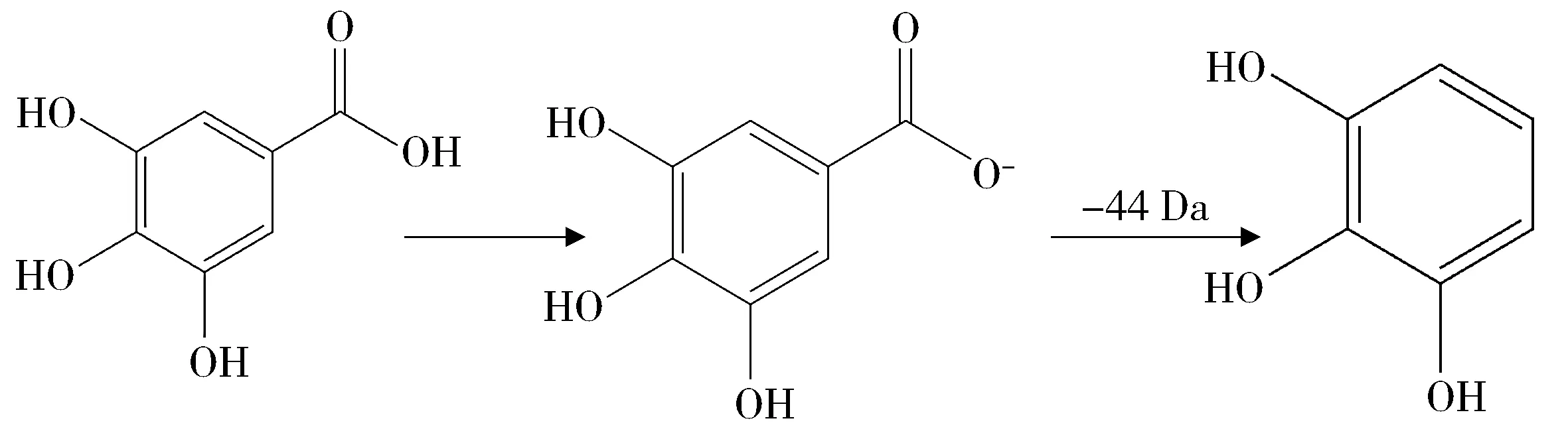
图8 没食子酸的裂解规律Figure 8 Proposed fragmentation pathways of gallic acid
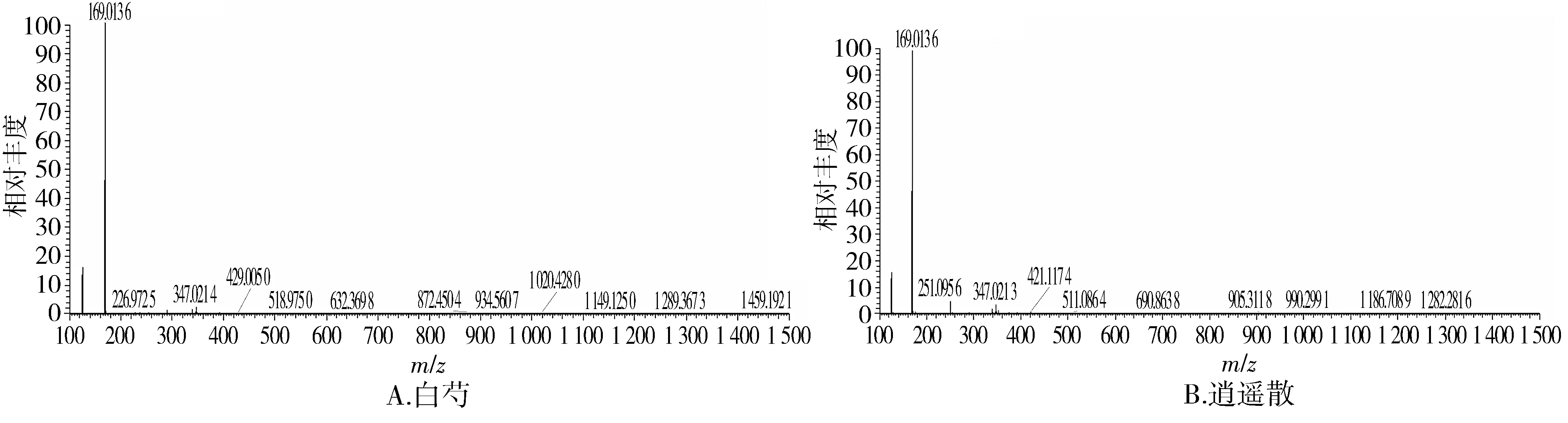
图9 没食子酸的一级质谱图Figure 9 MS spectra of gallic acid
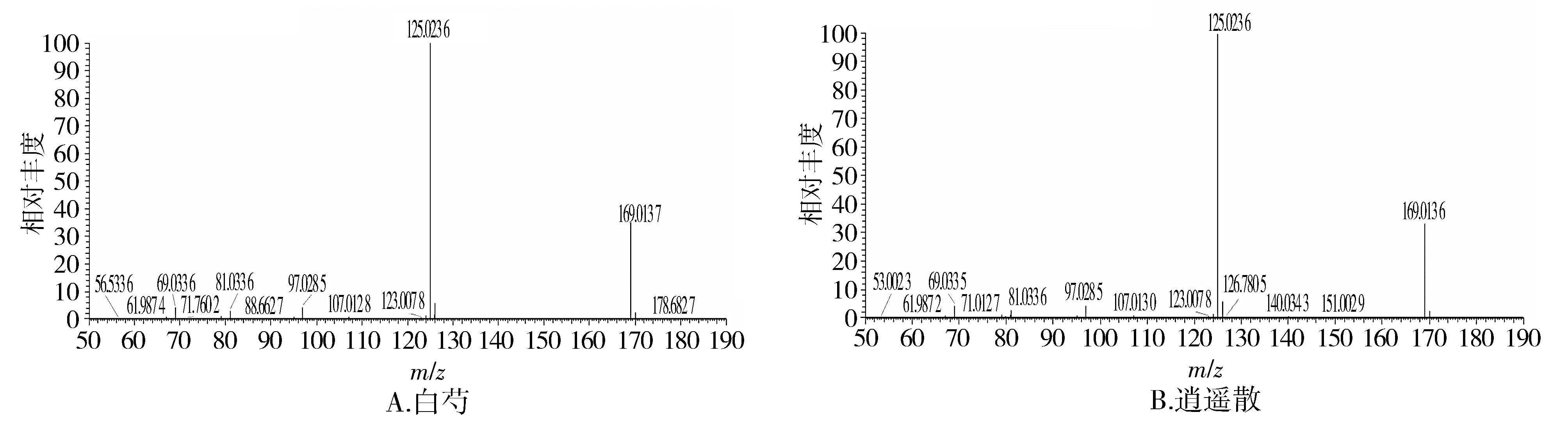
图10 没食子酸的二级质谱图Figure 10 MS2 spectra of gallic acid
3 讨论
对于逍遥散及其柴胡、白芍化学成分的研究,大多研究者采用NMR、HPLC等技术,且多数是对其醇提成分及药理活性成分进行定性定量分析,而本实验运用UPLC-ESI-Q/exactive orbitrap技术,利用质谱的高分辨率优势获得色谱的准分子离子峰,通过二级质谱扫描并根据碎片离子信息,结合文献全面分析其水煎液中的化学成分,并对这些成分进行定性分析,最终在逍遥散复方中表征出86个化合物,其中鉴定出44个,13个来源于柴胡,31个来源于白芍。从逍遥散及柴胡、白芍化学成分指认结果可以看出,柴胡、白芍作为逍遥散核心药对在化学成分定性方面对其有重要贡献,并且从逍遥散、柴胡、白芍的液质总离子流图也可以直观地看到柴胡、白芍主要化学成分含量对逍遥散的贡献,从定性及定量两方面都可以确认柴胡、白芍作为核心药对逍遥散的贡献。因此本课题组接下来对柴胡、白芍对逍遥散贡献成分的定量研究进行分析。
参考文献:
[1] 马克信,苏芮,范吉平,等.逍遥散处方来源探讨[J].山东中医药杂志,2014,33(2):88-90.
[2] 王虎平,吴红彦.逍遥散功用述评[J].中国中医药信息杂志,2014,21(1):126-128.
[3] 何伦,顿宝生.逍遥散类方鉴别运用[J].陕西中医,1985,6(2):80-81.
[4] Dai Y, Li Z, Xue L,etal. Metabolomics study on the anti-depression effect of xiaoyaosan on rat model of chronic unpredictable mild stress[J]. J Ethnopharmacol, 2010, 128(2): 482-489.
[5] Zhou Y, Lu L, Li Z,etal. Antidepressant-like effects of the fractions of Xiaoyaosan on rat model of chronic unpredictable mild stress[J]. J Ethnopharmacol, 2011, 137(1):236-244.
[6] Zhang Y, Mei H, Liu Z,etal. Chinese herbal formula Xiao Yao San for treatment of depression: a systematic review of randomized controlled trials[J]. Evid Based Complement Alternat Med, 2012, 2012:931636.
[7] Kim SH, Han J, Seog DH,etal. Antidepressant effect of Chaihu-Shugan-San extract and its constituents in rat models of depression[J]. Life Sci, 2005, 76(11): 1297-1306.
[8] Wang Y, Fan R, Huang X. Meta-analysis of the clinical effectiveness of traditional Chinese medicine formula Chaihu-Shugan-San in depression[J].J Ethnopharmacol, 2012,141(2): 571-577.
[9] Zhang Y, Huang X, Wang Y,etal. Ferulic acid-induced anti-depression and prokinetics similar to Chaihu-Shugan-San via polypharmacology[J]. Brain Res Bull, 2011, 86(3):222-228.
[10] Wang YT, Tan QR, Sun LL,etal. Possible therapeutic effect of a Traditional Chinese medicine, Sinisan, on chronic restraint stress related disorders[J]. Neurosci Lett, 2009,449(3):215-219
[11] 施学丽,邓家刚,蒋筱,等.195首治疗乳腺增生中药专利复方的用药规律分析[J].世界科学技术:中医药现代化,2013,15(7):1544-1551.
[12] 左亚妹.复方柴归方超临界CO2萃取组分的化学、质量及制剂研究[D].太原:山西大学,2014.
[13] 任艳玲,周玉枝,马致洁,等.逍遥散抗抑郁有效部位指纹图谱归属分析[J].山西医科大学学报,2011,42(8):636-640.
[14] 孙健,张立富,范斌,等.柴胡皂苷类化学成分的LC-MS分析[J].中国药物警戒,2012,9(12):725-727.
[15] 梁鸿,赵玉英,邱海蕴,等.北柴胡中新皂甙的结构鉴定[J].药学学报,1998,33(1):37-41.
[16] Ono M, Yoshida A, Ito Y,etal. Phenethyl alcohol glycosides and isopentenol glycoside from fruit of Bupleurum falcatum[J]. Phytochemistry, 1999, 51(6):819-23.
[17] 田振坤,张雅贤.长白柴胡皂甙成分研究[J].沈阳药科大学学报,1993,10(2):82-84.
[18] Ebata N, Nakajima K, Taguchi H,etal. Isolation of new saponins from the root of Bupleurum falcatum L.[J]. Chem Pharmaceutic Bull, 1990, 38(5):1432-1434.
[19] 张如意,陈喜奎,杨宪斌,等.柴胡皂甙m和柴胡皂甙n的结构鉴定[J].药学学报,1994,29(9):684-688.
[20] 郭敏娜,刘素香,赵艳敏,等.基于HPLC-Q-TOF-MS技术的柴胡化学成分分析[J].中草药,2016,47(12):2061-2068.
[21] 刘晓帆,娄子洋,朱臻宇,等.采用HPLC-TOF/MS对中药复方小柴胡汤中化学成分的快速分析鉴别[J].第二军医大学学报,2009,30(8):941-946.
[22] Wen X,Huang M,Huang L,etal.Chemical profiling and quantification of Gua-Lou-Gui-Zhi decoction by high performance liquid chromatography/quadrupole-time-of-flight mass spectrometry and ultra-performance liquid chromatography/triple quadrupole mass spectrometry[J]. J Chromatogr B, 2015, 986—987 C: 69-84.
[23] Wang S, Chen L, Jing L,etal. Fragment ion diagnostic strategies for the comprehensive identification of chemical profile of Gui-Zhi-Tang by integrating high-resolution MS, multiple-stage MS and UV information[J]. J Pharm Biomed Anal, 2014, 98(11):22-35.
[24] Li SL, Song JZ, Choi FFK,etal. Chemical profiling of Radix Paeoniae evaluated by ultra-performance liquid chromatography/photo-diode-array/quadrupole time-of-flight mass spectrometry[J]. J Pharm Biomed Anal,2009, 49(2):253-266.
[25] Yan Y, Chai CZ, Wang DW,etal. HPLC-DAD-Q-TOF-MS/MS analysis and HPLC quantitation of chemical constituents in traditional Chinese medicinal formula Ge-Gen Decoction[J]. J Pharm Biomed Anal, 2013, 80(3):192-202.
[26] Chen L, Qi J, Chang YX,etal. Identification and determination of the major constituents in Traditional Chinese Medicinal formula Danggui-Shaoyao-San by HPLC—DAD—ESI-MS/MS[J]. J Pharm Biomed Anal,2009, 50(2):127.
[27] 刘杰,陈琳,范彩荣,等.基于HPLC-DAD-Q-TOF-MS/MS的白芍和赤芍主要成分定性定量研究[J].中国中药杂志,2015,40(9):1762-1770.
[28] Yin Q, Wang P, Zhang A,etal. Ultra-performance LC-ESI/quadrupole-TOF MS for rapid analysis of chemical constituents of Shaoyao-Gancao decoction[J]. J Sep Sci, 2013, 36(7):1238-46.
[29] 母会丹,朱靖博,丁燕,等.白芍化学成分的UPLC/Q-TOF-MS分析[J].分析试验室,2013,32(7):113-117.
[30] Yao Q, Li S, Pi Z,etal. Chemical profiling of Wu-tou decoction by UPLC—Q-TOF-MS[J]. Talanta, 2014, 118:21-29.
[31] Yan Z, Chen C, Xie X,etal. Rapid screening and quantification of sulfonate derivatives in white peony root by UHPLC-MS-MS.[J]. Anal Bioanal Chem, 2012, 402(6):2173-2182.
[32] Ding HY, Wu YC, Lin HC,etal. Glycosides from Paeonia suffruticosa[J]. Chem Pharmaceut Bull, 1999, 47(5):652-655.
