呼吸功能锻炼联合营养护理对COPD稳定期患者生命质量的影响*
2018-05-03王锋刘璐饶志勇
王锋 刘璐 饶志勇
(四川大学华西医院 1. 呼吸内科 ; 2.临床营养科, 四川 成都 610041)
慢性阻塞性肺疾病( chronic obstructive pulmonary disease,COPD) 是一种常见的以持续性气流受限为特征的疾病。COPD具有发病率高、病死率高等特点[1-2]。研究表明,COPD患者多伴有营养不良,而长时间营养不良则会显著影响疾病的预后[3];国内外部分学者对COPD患者采用高蛋白质、低碳水化合物营养方案,取得了较好的结果[4-6]。因此,COPD患者的护理中提供合理的营养支持是非常有必要的[7]。本研究以四川大学华西医院呼吸与危重症医学科收治并坚持随访的COPD稳定期患者为研究对象,在呼吸功能锻炼的基础上联合高蛋白低碳水化合物营养护理,旨在探索联合护理干预方案对COPD稳定期患者肺功能及生命质量的影响。
1 资料与方法
1.1 一般资料 选取2015年1月~2017年1月四川大学华西医院呼吸与危重症医学科收治并坚持随访的92例COPD稳定期患者为研究对象,其中男性59人,女性33人,年龄41~77岁,平均年龄(65.54±11.16)岁,病程5~14年,平均(10.01±3.52)年。按随机数字表法将研究对象随机分为研究组和对照组,每组46例,研究组采用呼吸功能锻炼联合营养护理,对照组采用常规护理。两组患者在年龄、性别、体重指数等方面比较差异无统计学意义。所有患者均签署知情同意书,并报医院伦理委员批准,见表1。
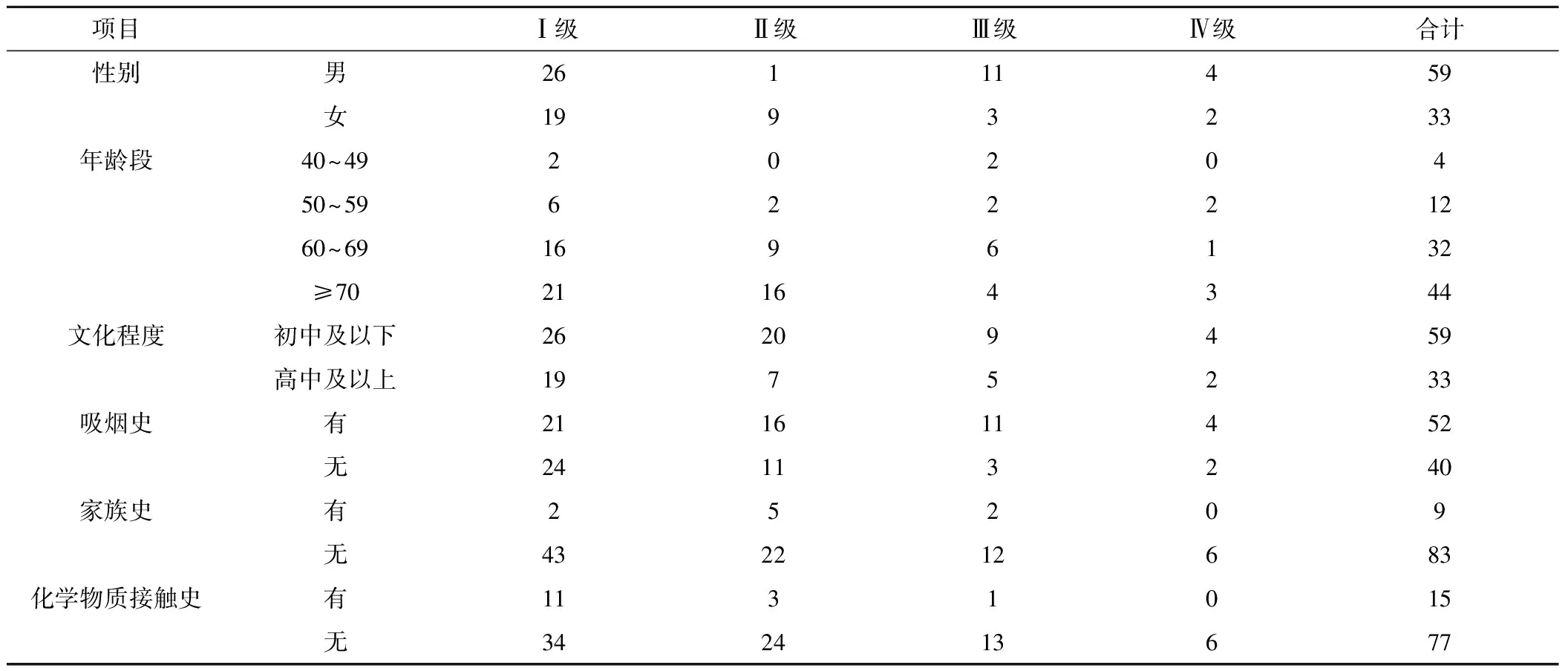
表1 COPD患者的一般资料Table 1 General information on COPD patients
1.2 纳入标准及排除标准 纳入标准:①诊断符合《慢性阻塞性肺疾病诊治指南》(2013年修订版)[8];②年龄≥40岁;③患者咳嗽、咳痰、气促等症状稳定或症状轻微;④经调查者讲解能够理解SGRQ并独立完成。排除标准:①有肢体活动障碍的COPD患者,如肌肉骨骼疾病,运动能力受限、老年痴呆、及神经病者;②充分休息心率大于120次/分,收缩压高于180mmHg,舒张压高于100mmHg;③急性发作期患者或入选后因急性加重需住院治疗者;④合并急性心梗、脑梗死等心脑血管病、严重肝肾慢性疾病或肿瘤者;⑤不愿意配合、填写问卷困难的患者。
1.3 研究方法 研究组患者除给予常规护理外,还进行呼吸功能锻炼及营养护理。对照组患者仅给予常规护理。常规护理:住院期间保持病房光线柔和、明亮、通风良好,保持室内空气新鲜,定期做好空气及物品的消毒工作,室温维持在18~20℃,湿度50%~60%,病房内不宜摆设花草,避免烟雾及灰尘刺激,注意保暖。出院后要求环境通风好、采光好,注意远离厨房,避免油烟等刺激气体,温湿度要求与病房一致,勤搞卫生,减少灰尘,减少进出患者卧室人员,避免感冒。发放COPD患者健康教育手册,呼吸功能锻炼:包括①呼吸训练器:吸气时依靠主动收缩使胸腔扩大,使肺内压力降低;当肺内压力低于大气压时,空气便会吸入肺中。呼气的机理与吸气一样,但呼气是因为肺内压力大过于大气压。②坐式八段锦:包括宁神静坐、手抱昆仑、指敲玉枕、微摆天柱、手摩精门、左右辘轳、托按攀足、任督运转等。③有效咳嗽练习:将上身向前倾的同时,慢慢吸气,在咳嗽时收紧腹肌,内缩腹壁,一次吸气,连咳3声,停止咳嗽后,将剩余气体缩唇呼出。④全身呼吸体操锻炼法:保持呼吸平静,前倾呼气,立体吸气;双手压腹呼气,单举上臂吸气;双臂下垂呼气,平举上肢吸气;转体呼气,抱头吸气;蹲位呼气,立体上肢上举吸气。营养护理:采用高蛋白低碳水化合物的营养配餐方案,营养配餐中碳水化合物占总能量的50%,脂肪占比20%,蛋白质占比30%,一日三餐,干预时间3个月。
1.4 评价指标 肺功能评价指标:用力肺活量(FVC)、第1秒用力呼气量(FEV1)、第 1 秒用力呼气容积占用力肺活量的百分比(FEV1/FVC)、第1秒用力呼气容积占预计值百分比(FEV1%pred)、呼气峰值流速(PEF)。生命质量评价指标:采用SGRQ问卷进行评价[9],包括症状部分、活动部分、日常生活影响部分,共76个条目。量表和各维度信度Cronbach’s α为0.696~0.874,分半信度为0.685~0.801,重测信度为0.675~0.880。
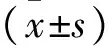
2 结果
2.1 联合护理干预对患者生命质量的影响 研究组患者在SGRQ症状部分、活动部分、影响部分得分及总分与对照组比较降低,差异均有统计学意义(P<0.05),见表2。
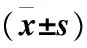
表2 两组患者SGRQ各能区分值比较Table 2 Comparison of the differences in SGRQ scores between the two groups
注:与对照组比较,①P<0.05
2.2 联合护理干预对患者肺功能的影响 与对照组比较,研究组患者FVC、FEV1、FEV1/FVC、PEF等指标升高,差异均有统计学意义(P<0.05);两组FEV1%pred比较无显著性差异(P>0.05),见表3。
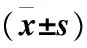
表3 两组患者各肺功能指标比较Table 3 Comparison of lung function in both groups
注:与对照组比较,①P<0.05
3 讨论
目前针对COPD开展肺功能检查是诊断COPD的金标准,但其仍不能全面反映疾病的临床特点以及风险评估,还需结合一些相关量表进行评估。SGRQ量表是目前国内外使用最广泛的用于评定呼吸系统疾病患者生命质量的特异性量表,具有良好的信效度[10-11],较非特异性量表更为可靠、有效、敏感[12-13]。本研究结果发现研究组患者在SGRQ症状部分、活动部分、影响部分得分及总分显著低于对照组,提示研究组患者生命质量显著得到改善。
FEV1是检测大、小气道气流受阻的肺功能指标,在COPD的诊断、分级、病程、气道阻塞可逆性以及预后等方面具有重要意义。与其他指标相比,FEV1能更加准确地反映COPD 患者的肺功能、气流受限严重程度。FEV1%pred是反映气流阻塞程度的指标,COPD患者的FEV1%pred下降表示疾病严重性的等级加重,但单纯的FEV1%pred指标不能全面反映COPD患者的整体健康状况程度。PEF是反映呼吸功能的一项重要指标。研究发现,PEF也可以较好地检测COPD患者的气流受限,其敏感性和特异性均高于单纯依靠临床症状判断[14]。本研究结果发现,研究组患者FVC、FEV1、FEV1/FVC、PEF等指标显著升高,提示研究组患者肺功能在一定程度上得到改善。
研究表明,有效的呼吸功能锻炼能同时锻炼患者的肩部、胸部、胸肌、背肌、肋间肌,从而提高呼吸肌的功能,使肺通气量增加,同时可促进全身血液循环,改善机体功能,改善患者的喘息、咳嗽、气短、腰膝酸软等症状[15]。营养不良是COPD患者常见且重要的并发症,其机制可能与以下因素等有关:①能量摄入不足。COPD患者由于心肺功能不全导致进食活动受限,此外长期缺氧、通气不足,易使胃肠淤血,造成消化功能减退[16];长期服用茶碱类药物刺激胃肠,引起菌群失调,从而影响了食物的消化、吸收,造成营养素缺乏[17]。②能量消耗增加。COPD患者长期呼吸道阻力增加、肺顺应性降低,因此呼吸做功增加,使其基础代谢高出正常人30%左右[18]。③其他因素。感染、缺氧、焦虑、排痰等均参与了营养不良的进展。研究发现,COPD患者发生的营养不良多属于蛋白质热量型营养不良,高蛋白低碳水化合物营养方案具有较好的效果。侯维维等[4]报道,高蛋白膳食组患者在干预8周后肺功能相关指标得到改善;Deutz等[5]报道在营养干预期间COPD患者体质量显著增加,表明高蛋白低碳水化合物饮食有助于改善患者的身体状况。本研究结果发现研究组患者在呼吸功能锻炼的同时联合高蛋白低碳水化合物营养护理后肺功能及生命质量显著高于对照组,与上述结论相似。这可能是因为给予营养护理干预后,有效提高了患者FEV1、FVC的水平,从而减轻了呼吸阻塞症状,提高了患者的耐受水平[19]。此外,营养护理干预可有效提高运动耐力[20],改善患者6min步行距离[21],减少再次入院次数,从而延缓患者的病情发展,提高生命质量。
4 结论
呼吸功能锻炼联合营养护理干预能有效改善COPD稳定期患者的肺功能及生命质量;本研究为COPD患者呼吸功能锻炼联合营养护理的干预措施提供了一定的循证医学证据,值得临床推广应用。
【参考文献】
[1]Wenzel SE, Jayawardena S, Graham NMH,etal. Severe asthma and asthma-chronic obstructive pulmonary disease syndrome-Authors' reply [J]. The Lancet, 2016, 388(10061): 2742-2746.
[2]Schroff P, Hitchcock J, Schumann C,etal. Pulmonary Rehabilitation Improves Outcomes in Chronic Obstructive Pulmonary Disease Independent of Disease Burden [J]. Annals of the American Thoracic Society, 2017, 14(1): 26-32.
[3]Schroff P, Hitchcock J, Schumann C,etal. Pulmonary Rehabilitation Improves Outcomes in Chronic Obstructive Pulmonary Disease Independent of Disease Burden [J]. Annals of the American Thoracic Society, 2017, 14(1): 26-32.
[4]侯维维, 徐玲芬, 陆永良. 蛋白质饮食支持治疗对稳定期 COPD患者营养及其康复的影响[J]. 湖州师范学院学报, 2013, 35(6): 66-68.
[5]Deutz NE, Matheson EM, Matarese LE,etal. Readmission and mortality in malnourished, older, hospitalized adults treated with a specialized oral nutritional supplement: A randomized clinical trial[J]. Clin Nutr, 2016, 35(1): 18-26.
[6]吕小英, 徐玲芬, 陈海燕. 不同营养比例的支持治疗对慢性阻塞性肺疾病患者营养状况的影响[J]. 解放军护理杂志, 2012, 29(2): 16-18.
[7]李晓萍. 慢性阻塞性肺疾病患者营养状况临床相关因素分析[D]. 银川: 宁夏医科大学, 2013.
[8]中华医学会呼吸病学分会慢性阻塞性肺疾病学组. 慢性阻塞性肺疾病诊治指南( 2013 年修订版)[J]. 中华结核和呼吸杂志, 2013, 36(4): 255-264.
[9]王莹. 健康信念模式在改善中重度COPD患者健康状况中的应用[D]. 天津:天津医科大学, 2011.
[10] Tashkin DP, Bateman ED, Jones P,etal. Consistent improvement in health-related quality of life with tiotropium in patients with chronic obstructive pulmonary disease: Novel and conventional responder analyses [J]. Respiratory medicine, 2016, 120(9): 91-100.
[11] Müllerova H, Gelhorn H, Wilson H,etal. St George’s Respiratory Questionnaire Score Predicts Outcomes in Patients with COPD: Analysis of Individual Patient Data in the COPD Biomarkers Qualification Consortium Database [J]. Chronic Obstructive Pulmonary Diseases, 2017, 4(2): 141-147.
[12] Hasanpour N, Moghadam B A, Sami R,etal. Cross-Cultural Adaptation, Reliability and Validity Study of the Persian Version of the Clinical COPD Questionnaire [J]. Acta Medica Iranica, 2016, 54(8): 518-524.
[13] Morishita-Katsu M, Nishimura K, Taniguchi H,etal. The COPD assessment test and st george’s respiratory Questionnaire: are they equivalent in subjects with COPD [J]. International journal of chronic obstructive pulmonary disease, 2016, 11(3): 1543-1549.
[14] 田佳. 成人PEF预计值公式建立及其在COPD患者气流受限初筛中作用研究[D]. 广州医学院, 2010.
[15] 张丹. 呼吸功能锻炼及饮食护理干预对慢性阻塞性肺疾病患者生活质量影响的研究[D]. 长春中医药大学, 2013.
[16] Raguso CA, Luthy C. Nutritional status in chronic obstructive pulmonary disease: Role of hypoxia [J]. Nutri, 2011, 27(2): 138-143.
[17] Wang Y, Shen Y, Zuo Q,etal. Evaluation of ghrelin level and appetite regulation in patients with acute exacerbations of chronic obstructive pulmonary disease [J]. Int J Chron Obstruct Pulmon Dis, 2014, 9(1): 863-870.
[18] Rabinovich RA, Vilaro J. Structural and functional changes of peripheral muscles in chronic obstructive pulmonary disease patients [J]. Curr Opin Pulm Med, 2010, 16(2): 123-133.
[19] Hanson C, Lyden E, Rennard S,etal. The relationship between dietary fiber intake and lung function in the national health and nutrition examination surveys [J]. Ann Am Thorac Soc, 2016, 13 (5) : 643-650.
[20] Almagro P, Castro A. Helping COPD patients change health behavior in order to improve their quality of life [J]. Int J Chron Obstruct Pulmon Dis, 2013,12(8): 335-345.
[21] 许亚丽, 潘磊, 钱进. 营养支持对稳定期慢性阻塞性肺疾病患者肺功能及6 min步行距离的影响[J]. 中国老年学杂志, 2013, 33(9): 2008-2010.
