血液透析滤过对维持性血液透析失眠患者睡眠及生活质量的影响
2018-04-27束长东
束长东,滕 玲
(宣城市人民医院 肾内科,安徽 宣城 242000)
随着慢性肾脏病发病率的不断增加,接受维持性血液透析(maintenance hemodialysis,MHD)治疗的患者数量也呈现逐年增长的趋势,目前我国MHD患者在22.8万人左右[1]。MHD患者中睡眠障碍发生率普遍较高,主要表现为入睡困难、夜间易醒、透析相关的骨病及皮肤瘙痒引起入睡障碍等[2];有研究表明其发生率为49%,且与MHD患者的病死率独立相关[3]。因此,探讨影响MHD患者失眠的危险因素、采取有效措施提高MHD患者睡眠质量具有重要的临床意义。我院对MHD失眠患者实施规律的血液透析滤过(hemodiafiltration,HDF)治疗,有效改善MHD患者的睡眠质量及生活质量,现报道如下。
1 资料与方法
1.1 研究对象 选取2016年1月~2017年4月我院MHD患者127例,已排除严重躯体疾病(如糖尿病足、骨折、外伤、头痛、骨痛等)、未控制的急性左心衰、急性感染、进入血液透析前已存在睡眠障碍、言语或智力障碍等。根据《中国成人失眠诊断与治疗指南》[4]中失眠的诊断标准分为失眠组68例与对照组59例。
1.2 治疗方式 两组患者均采用费森尤斯4008B透析机、一次性尼普洛中空纤维透析器150G行MHD治疗(每周2~3 次,每次4 h)。失眠组在此基础上加用HDF治疗3个月(费森尤斯4008S透析机、一次性费森尤斯中空纤维透析器FX80,每周1次,每次4 h)。
1.3 调查评分 采用匹兹堡睡眠质量指数(Pittsburgh sleep quality index,PSQI)量表、通过现场问卷调查形式对入组患者的睡眠质量进行评定;同时,采用SF-36量表评估上述患者的生活质量。
1.4 观察指标 对比两组患者的年龄、性别、肾功能不全病因、血液透析龄、血液透析频次等一般资料,以及血浆白蛋白(Alb)、血红蛋白(Hb)、铁蛋白(SF)、血钙(Ca2+)、血磷(P)、甲状旁腺激素(iPTH)、血肌酐(SCr)、血尿素氮(BUN)等生化指标,所有生化指标检测时间均为参与调查问卷时当次血液透析上机前。
1.5 研究方法 筛选出MHD患者失眠的危险因素;对比失眠组实施HDF治疗前后PSQI量表评分及SF-36量表评分的变化。

2 结果
2.1 两组患者一般资料比较 两组患者在性别、年龄、肾功能不全病因及血液透析频次上均无显著差异,组间血液透析龄差异具有统计学意义(P=0.001),见表1。
2.2 两组患者生化指标比较 两组生化指标中,血磷、甲状旁腺激素及血肌酐水平差异有统计学意义(P<0.05),血红蛋白、血尿素氮、总钙、白蛋白及血清铁蛋白水平差异均无统计学意义,见表2。
2.3 MHD患者失眠的危险因素分析 通过两组间一般资料及生化指标的对比,我们发现两组患者性别、年龄、肾功能不全病因、血液透析频率、Hb、BUN、Ca2+、Alb、SF差异无统计学意义,而血液透析龄、SCr、P及iPTH差异有统计学意义。以MHD患者入组组别为应变量(对照组赋值为0,失眠组赋值为1),以上述单因素分析有意义的各项影响因素为自变量(均为连续变量,以其原始数据赋值),进行非条件Logistic回归分析,结果显示血磷和甲状旁腺激素水平是MHD患者失眠的危险因素,见表3。
表1 失眠组与对照组一般资料比较
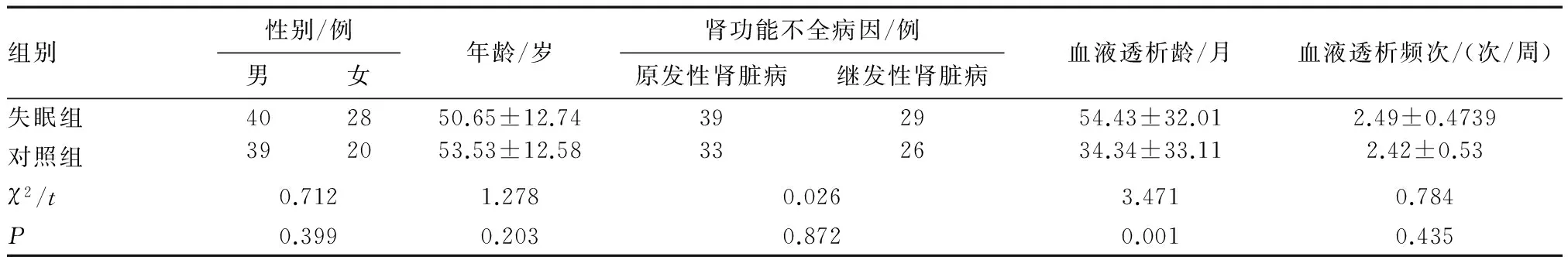
组别性别/例男女年龄/岁肾功能不全病因/例原发性肾脏病继发性肾脏病血液透析龄/月血液透析频次/(次/周)失眠组402850.65±12.74392954.43±32.012.49±0.4739对照组392053.53±12.58332634.34±33.112.42±0.53χ2/t0.7121.2780.0263.4710.784P0.3990.2030.8720.0010.435
表2 失眠组与对照组生化指标比较

组别Hb/(g/L)SCr/(μmol/L)BUN/(mmol/L)Ca2+/(mmol/L)P/(mmol/L)iPTH/(ng/L)Alb/(g/L)SF/(μg/L)失眠组105.07±17.55924.83±238.1023.28±8.372.36±0.252.61±0.68683.15±430.9837.30±4.31724.13±1175.47对照组101.93±19.56802.04±194.8020.88±7.712.29±.0271.78±0.42270.41±190.5438.01±5.78656.18±957.05t0.9513.1331.6571.4708.0847.1340.7600.332P0.3440.0020.1000.144<0.001<0.0010.4490.740
Hb:血红蛋白;SCr:血肌酐;BUN:尿素氮;Ca2+:血钙;P:血磷;iPTH:甲状旁腺激素;Alb:血白蛋白;SF:血清铁蛋白。
表3 MHD患者睡眠质量多因素分析结果
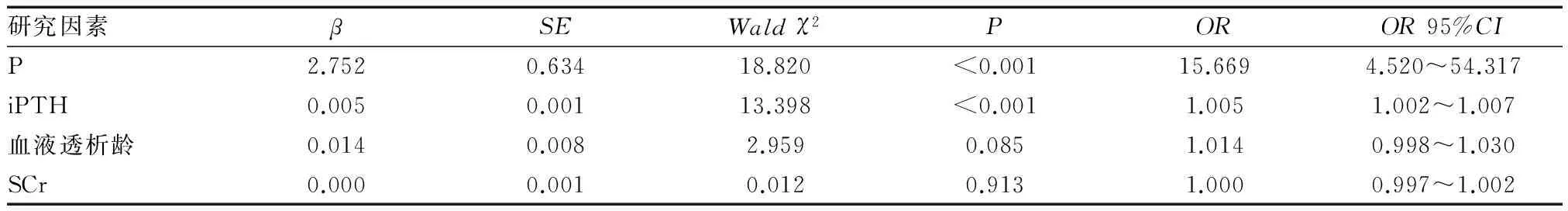
研究因素βSEWaldχ2POROR95%CIP2.7520.63418.820<0.00115.6694.520~54.317iPTH0.0050.00113.398<0.0011.0051.002~1.007血液透析龄0.0140.0082.9590.0851.0140.998~1.030SCr0.0000.0010.0120.9131.0000.997~1.002
2.4 MHD失眠患者接受HDF治疗前后PQSI评分及SF-36评分对比 失眠组患者接受3个月的规律MHD+HDF治疗,治疗前后PQSI评分及SF-36评分差异有统计学意义(P<0.05),见表4。
表4 失眠组HDF治疗前后PQSI评分及SF-36评分

PQSI评分SF-36评分HDF治疗前9.13±3.0851.03±6.04HDF治疗后5.50±1.4758.09±3.73t12.05312.699P<0.001<0.001
3 讨论
随着我国人口老龄化问题的日益突出,慢性肾脏病患者数量逐年增加,由此进展至终末期肾脏病者亦逐渐增多;同时医疗保险制度不断完善,终末期肾脏患者存活时间得以相应延长。MHD是目前应用最为广泛的肾脏替代治疗,MHD患者在社会中已然形成一个庞大的群体[1]。国内外研究发现MHD患者普遍存在失眠的问题,睡眠障碍的发病率49%~80%[2-3]。本研究显示MHD患者存在不同程度的睡眠问题,睡眠障碍的发生率为53.54%,与国内外报道基本一致。失眠与MHD患者生活质量显著相关[5],同时可增加MHD患者心血管事件的发生率及病死率[6],因此了解MHD患者失眠的影响因素意义重大,不仅利于提高MHD患者的睡眠质量、改善其生活质量,且有助于提高此类患者的长期生存率。
目前,随着透析龄增加,各种透析相关的并发症亦逐渐出现,如钙磷代谢异常致不安腿综合征、皮肤瘙痒、透析相关淀粉样变、异位钙化等并发症可严重影响患者的睡眠质量。Merlino等[7]报道,不同的透析模式、透析时间亦可影响患者的睡眠质量。本研究通过单因素分析发现,透析龄、血磷、血肌酐、iPTH能够影响MHD患者的睡眠质量,国内外研究也有报道透析龄及血肌酐水平均与睡眠障碍发生相关[8-9];进一步通过多因素分析发现血磷及iPTH水平是MHD患者失眠的危险因素。2012年的DOPSS研究[10]显示,我国MHD患者中高磷血症的发生率达57.4%,高血磷可以促进甲状旁腺的增生,还通过稳定甲状旁腺素mRNA促进其信号传导增加甲状旁腺素的合成,且持续的高磷血症还会抑制肾脏1α-羟化酶的活性,拮抗活性维生素D对iPTH的抑制作用,在尿毒症患者iPTH与血钙呈负相关、与血磷呈正相关,提示高血磷、低血钙是导致尿毒症患者iPTH升高的重要因素[11],而iPTH被公认为引起尿毒症症状最重要的物质[12]。国外有研究提示较高的iPTH水平可能导致MHD患者睡眠质量较差[13],国内亦有相关研究结果表明高iPTH水平的患者睡眠障碍发生率较高[14],其原因可能为高磷血症及高iPTH血症易导致皮肤瘙痒、不安腿综合征等各种并发症,进而严重影响此类患者的睡眠质量,导致其生活质量下降。
MHD是目前应用最多的一种透析方式,主要是通过弥散方式清除毒素,清除效果以小分子物质为佳,PTH等中、大分子物质的清除不够理想。磷属于小分子物质,但周围有水分子包绕,清除机制类似中分子物质[15]。而HDF则可通过弥散和对流两种方式进行毒素清除,对中、大分子物质清除较血液透析理想,且对血流动力学的影响亦较小。本研究发现,失眠组患者在MHD基础上每周增加1次HDF后,其PQSI评分及SF-36评分均可显著改善。HDF膜孔径大、超滤系数高,血磷及iPTH主要依靠对流方式得以清除,故HDF能够将患者体内各种代谢产物及有毒物质更加彻底地清除,同时减少皮肤瘙痒、不安腿综合征等血液透析相关并发症,进而较大程度地改善MHD患者的睡眠质量及生活质量。
综上所述,HDF可显著改善MHD患者的睡眠质量及生活质量,值得临床推广应用。鉴于本研究样本量较小,相关结论有待于大样本多中心随机对照研究加以证实。相信随着血液净化技术的不断更新以及转化医学成果的不断推广,MHD患者的睡眠问题能够得到更为圆满的改善。
【参考文献】
[1] 陈香美.中国肾脏病学进展[M].北京:人民军医出版社,2011:235-240.
[2] 王饶萍,唐春苑,陈小帆,等.维持性血液透析患者症状困扰与睡眠质量的相关性研究[J].中国中西医结合肾脏病杂志,2016,17(8):717-719.
[3] ELDER SJ,PISONI RL,AKIZAWA T,etal.Sleep quality predicts quality of life and mortality risk in haemodialysis patients:results from the Dialysis Outcomes and Practice Patterns Study (DOPPS)[J].Nephrology Dialysis Transplantation,2008,23(3):998-1004.
[4] 中华医学会神经病学分会睡眠障碍学组.中国成人失眠诊断与治疗指南[J].中华神经科杂志,2012,45(7):534-540.
[5] 张敬丽,李寒,张庆来,等.维持性血液透析患者抑郁与睡眠质量相关性研究[J].中国病案,2014,15(3):79-81.
[6] 李九红,任小红,赵静.维持性血液透析患者睡眠障碍的影响因素及干预疗法研究现状[J].中国血液净化,2013,12(12):690-691.
[7] MERLINO G,PIANI A,DOLSO P,etal.Sleep disorders in patients with end-stage renal disease undergoing dialysis therapy[J].Nephrology Dialysis Transplantation,2006,21(1):184-190.
[8] BURROWES JD,RUSSELL GB,UNRUH M,etal.Is nutritional status associated with self-reported sleep quality in the HEMO study cohort[J]?Journal of Renal Nutrition,2011,22(5):461-471.
[9] 刘国锋,吕春晓,闫红霞,等.漯河市维持性血液透析患者睡眠障碍的多中心研究[J].中国实用神经疾病杂志,2016,19(4):53-55.
[10] KONG X,ZHANG L,ZHANG L,etal.Mineral and bone disorder in Chinese dialysis patients:a multicenter study[J].BMC Nephrology,2012,13(1):116-122.
[11] 王超民,王赫男,薛增芬,等.量化管理对血液透析患者血钙、血磷、iPTH达标率的影响[J].中国医刊,2016,51(6):50-52.
[12] 柳咏梅.血液透析联合血液灌流治疗尿毒症患者皮肤瘙痒的疗效[J].国际移植与血液净化杂志,2017,15(3):43-44.
[13] GADE K,BLASCHKE S,RODENBECK A,etal.Uremic Restless Legs Syndrome (RLS) and sleep quality in patients with end-stage renal disease on hemodialysis:potential role of homocysteine and parathyroid hormone[J].Kidney & Blood Pressure Research,2013,37(4-5):458-463.
[14] 周刚,孔亚玲,牟洪宾,等.甲状旁腺激素水平对血液透析患者心理状态与生活质量的影响[J].内科,2016,11(5):677-680.
[15] 焦春红,高丽,周洁,等.高通量透析器对高磷血症的疗效观察[J].天津医药,2013,41(1):33-36.
