永久起搏器术后少见并发症4例分析
2018-04-20姚丙南仇萍
姚丙南 仇萍
心脏起搏器是目前治疗病态窦房结综合征(病窦综合征)以及高度或三度房室阻滞的有效手段,已广泛应用于临床。手术相关并发症的发生率约2%~10%[1]。如何减少起搏器并发症的发生、提高起搏器疗效,越来越受到临床医师的关注。起搏器并发症按出现时间可分为术中及术后相关并发症,其中常见的术后并发症包括导线移位、囊袋出血或感染、术后阈值增高、膈神经刺激或腹肌刺激性收缩、感染性心内膜炎、血栓形成等。术后出现感染性心内膜炎而自行拔出导线等少见并发症则多属个案。
对2006至2017年我院安装的共832例永久起搏器患者的相关并发症资料进行回顾性研究,其中,囊袋血肿约20例,未抽吸,均通过间断压迫后吸收;起搏器导线移位2例,术后重新手术重置导线位置,均得到解决;囊袋感染5例,其中2例通过起搏器移位辅以抗感染治疗均有效解决,2例经局部换药及抗感染治疗后症状好转,1例出现感染性心内膜炎;1例出现锁骨下动脉假性动脉瘤形成后两次大出血;三尖瓣导线相关巨大血栓1例,采用华法林抗凝治疗,半年后血栓消失;起搏器电池提前耗竭1例。本文从上述起搏器并发症中选取4例少见并发症,对其临床资料和诊疗情况进行总结,以期探讨并发症的防治措施,有效减少术后并发症的发生。
病例1:患者男,75岁,因“胸闷、气短一年,伴晕厥一次”于2008年5月入院。入院前20 d,患者查24 h动态心电图示病窦综合征,入院第3日行永久起搏器植入术。由于患者身体偏瘦,起搏器突出于皮肤表面,张力大。术后常规予以预防感染治疗,术后一周患者术口愈合,好转出院。术后次年,患者由于劳动时用力划船,皮肤表面出现红肿,未及时处理,最终起搏器表面突出的皮肤出现破口、感染,并出现间断高热,可见脓性分泌物。血培养:表皮葡萄球菌。临床处置:先局部手术清创,原导线包埋,对侧重新植入起搏系统,给予青霉素、头孢三代抗生素等治疗两个月。患者热退,但原切口仍有破溃处,并可见少量脓性分泌物,多次建议心胸外科手术治疗取出电极,患者拒绝。从患者清创重新于对侧埋入起搏器一年后,原切口处皮肤出现破口、感染,出现间断高热,可见脓性分泌物,每年反复住院3~4次,给予青霉素、头孢三代抗生素等治疗,给予局部换药等处理。行永久起搏器植入术后的第4年,即2012年9月,该患者切口处皮肤再次出现破口,伴以间断高热,且脓性分泌物增多,破口处露出起搏导线。一个月后患者再次来院就诊,破口处未见导线。该患者夜间自行轻松拔出完整导线。目前切口处皮肤已完全愈合,体温正常。
病例2:患者男,66岁,于2015年11月2日17:58因“突发晕厥伴小便失禁2 h”至我院急诊。既往在他院诊断为“三度房室阻滞”,于2010年6月23日行“单腔起搏器植入术”;曾于2010年6月及2014年11月行起搏器程控,示起搏器工作良好。患者否认糖尿病、高血压病等病史。当日急诊心电图提示三度房室阻滞,予以急诊行临时起搏器植入术。次日,起搏器程控提示:起搏器停止工作,不能进行起搏器程控,当天行双腔永久起搏器植入术。取出原起搏器送公司检测,增加心房电极;术中测试心室导线电极阈值、阻抗均正常。与患者家属沟通后重新植入心室电极,此后随访起搏器工作正常。
病例3:患者男,83岁,有高血压病史20余年,10年前因病窦综合征行起搏器植入术(VVI),行起搏器程控显示电池耗竭。术前完善胸部CT等检查。在起搏器更换过程中,出现单极起搏失夺获、双极起搏夺获现象(图1、图2),术中测试导线阈值、阻抗、感知均在正常范围内,未更换导线,术后随访至今起搏器工作良好。

图1 病例3术后双极起搏状态下心电图
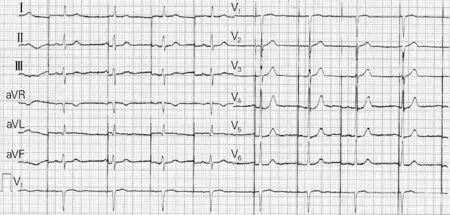
图2 病例3术后单极起搏状态下心电图
病例4:患者男,74岁,因“阵发性胸闷心悸不适晕厥半个月”于2017年5月10日入院。入院诊断:① 病窦综合征;② 冠心病,心功能Ⅱ级。次日下午行起搏器植入术。腋静脉穿刺,手术顺利,术后予以哌拉西林他唑巴坦预防感染治疗。
患者于术后第二天凌晨2时出现术口及左侧胸壁疼痛明显,行胸部CT检查示左胸壁软组织明显肿胀。对症予以升压、补液、输血等抢救,请胸外科会诊,考虑为胸壁血肿。当天上午在局麻下对患者行第二次手术,即左胸壁血肿切开清除引流术,探及胸大肌、胸小肌后方、前胸壁及多处存在少量血肿,胸壁组织水肿明显,未见明显活动性出血,予置胸壁引流管一根,接负压吸引。术后予以补液、输血、补充凝血因子等治疗,约10 d后患者症状好转。复查胸部CT示患者左侧胸壁下血肿较前明显缩小,左侧胸壁囊性包块。
起搏器植入术第23天,患者再次出现左侧胸壁肿胀疼痛,肩背部明显肿胀。再次行胸壁血肿清除及引流术。手术期间患者出现血压低、一过性抽搐两次,对症予以输血、升压等。全麻下胸壁探查见腋动脉假性动脉瘤形成,局部有活动性出血,立即予以纱布填塞加压包扎转移至导管介入室行左腋造影及支架植入术。术后对症采取预防感染、补充白蛋白、术口引流、换药等治疗措施。左侧上肢多普勒示:左侧上肢动静脉未见明显异常。起搏器术后54 d患者胸壁肿胀完全消退,好转出院。
讨论术后切口感染主要为继发感染及直接感染,其中直接感染主要在术后一个月内发生,多是由环境无菌条件差、切口暴露时间过长、起搏器灭菌不当等引起的。当起搏器囊袋受到累及时,导线同时受到累及,患者伴发败血症;继发感染主要在术后一个月后发生。目前,心律植入装置(cardiovascular implantable electronic device,CIED)感染的发生率呈上升趋势,以永久心脏起搏器的感染为主——除了永久心脏起搏器植入率升高,其原因可能还与高龄、合并多种疾病患者的比例增大有关。来自美国出院调查处(NHDS)的资料显示,2004年美国CIED年感染人数为8273人,2006年为12 979人,升高约57%[2]。国内开展人工心脏起搏技术已有40余年历史。据报道,1997至2005年,感染、电极移位、导线折断等起搏器并发症的发生率约1.4%~1.9%[3-4]。本研究中,病例1为术后一年囊袋继发性感染,未及时处理导致反复感染性心内膜炎。该导线为被动电极,在感染初期患者曾尝试拔出导线未成功,而在反复感染、发热4年后,导线能轻松拔出,考虑是当时拔除技术不佳或使用拔除方法不当所致。该患者随访至今未再出现发热等症状。患者反复感染性心内膜炎,重新埋于对侧的起搏导线及起搏器是否受累,是否安全?对此,国内目前尚无相关报道。起搏器电池提前耗竭的主要原因多为起搏阈值升高[5],病例2出现起搏器电池突然耗竭,而术中导线阻抗阈值等正常,行起搏器程控时无法打开程控界面,目前文献中未见类似的个案报道。在行起搏器更换术前与患者及家属沟通,患方表示要求重新植入起搏导线。病例3中,出现起搏器双极起搏而单极无法起搏,结合患者胸部CT,考虑电极头端部分穿透心肌的可能,但无法证实。术中与患者家属充分沟通,建议重新植入起搏导线,患者家属考虑到患者高龄,导线阻抗阈值正常,自起搏器植入后起搏功能良好,要求暂行观察。术后随访至今,起搏器工作良好。起搏器术中术后出血,以囊袋出血和血气胸为多见[6],病例4于术后形成锁骨下动脉假性动脉瘤,反复两次大出血,临床较少见,且假性动脉瘤与导线无关,考虑是由穿刺过程中误穿并损伤锁骨下动脉所致。该病例提示我们,术中如果穿刺到动脉,应予以充分压迫止血后再进行重新穿刺。因此,在预防起搏器术后出血相关并发症方面,应考虑术后锁骨下假性动脉瘤形成,尽可能做到早期发现、准确诊断和及时处理。
[1] 张竞涛, 陈柯萍, 华伟, 等. 1 023台永久起搏器脉冲发生器更换原因分析[J]. 中国循环杂志, 2009, 24(5):360-363.
[2] Voigt A, Shalaby A, Saba S. Continued rise in rates of cardiovascular implantable electronic device infections in the United States:temporaltrends and causative insights[J]. Pacing Clin Electrophysiol, 2010, 33(4):414-419.
[3] 中国生物医学工程学会心律分会. 心律植入装置感染与处理的中国专家共识2013[J]. 临床心电学杂志, 2013, 22(4):241-253.
[4] Saito Y,Nakamura K,Ito H. Cell-based biological pacemakers:progress and problems[J]. Acta Med Okayama, 2018, 72(1):1-7.
[5] 沈法荣, 张澍. 起搏器更换或升级:经验与指南[J]. 中华心律失常学杂志, 2012,16(3):166-167.
[6] Stewart MH,Morin DP. Management of perioperative anticoagulation for device implantation[J]. Card Electrophysiol Clin, 2018, 10(1):99-109.
