肝转移性胸腺瘤自发破裂1例
2018-04-11陈元蔡丽萍刘轩
陈元 蔡丽萍 刘轩
1 临床资料
患者,男,58岁,2011年5月在我院健康体检,X线胸片提示纵隔增宽,胸部CT检查发现前纵隔约4.5 cm肿块影(图1)。患者自诉既往无明显症状,入院血常规、肝肾功能、心电图、腹部超声检查均未见明显异常,无明显手术禁忌证,于2011年6月行纵隔肿块切除术,术后组织病理学检查提示为A型胸腺瘤(图2),根据Masaoka分期系统,肿瘤分期为2A期。患者术后接受放疗,照射野包括瘤床外2 cm;采用前正中野+两背部斜野,剂量分配为4∶1∶1;采用10 MV X线直线加速器分次治疗,50Gy/6周,2 Gy/次。放疗后患者出现食欲不振、疲乏、轻度恶心呕吐等不良反应,未出现骨髓抑制现象。2012年1月患者返院复查,X线胸片及胸部CT检查均未见明显异常,此后患者自觉身体状况良好。2016年11月因突发右上腹疼痛入院。查体:面容痛苦,口唇苍白,腹部无外伤,无发热,无呕吐、腹泻等,体温:36.8℃,血压:10.11/6.78 kpa,心率:89次/min,白细胞:12.2×109/L,红细胞:4.3×1012/L,血红蛋白:105 g/L,血小板:162×109/L。腹部彩超示:肝右前叶见一108 mm×97 mm×91 mm不均质低回声区,局部肝包膜中断,腹腔大量积液。腹部增强CT示:肝脏S5段、S8段直径约10 cm的低密度肿块影,脾周见液性密度影环绕(图3)。初步诊断为肝肿瘤破裂伴腹腔大出血,急诊实施血管造影及肝动脉栓塞术。术后第6天,患者病情体征稳定时行全麻下肿块组织活检,组织病理学分析符合A型转移性胸腺瘤(图4)。患者转入肿瘤科接受化疗;环磷酰胺500mg/m2,静脉滴注,d1;顺铂50 mg/m2,静脉滴注,d1;14 d为一个周期。化疗4个周期后行肝转移瘤灶切除术,手术顺利。患者术后一般情况良好,随访至2017年9月CT检查未发现明显纵隔及肝脏复发灶。
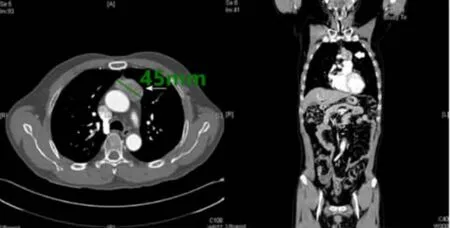
图1 纵隔胸腺瘤患者胸部CT图片

图2 纵隔胸腺瘤的组织病理学检查图片
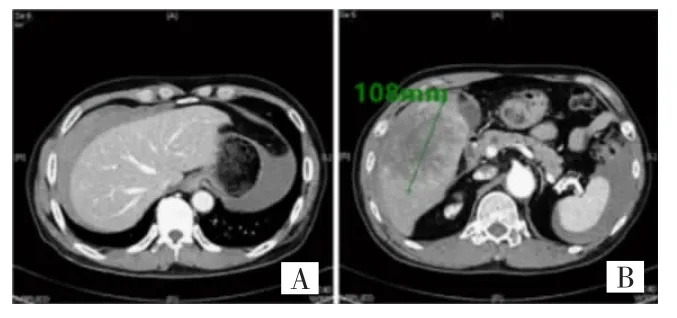
图3 肝转移性胸腺瘤患者腹部CT增强图片
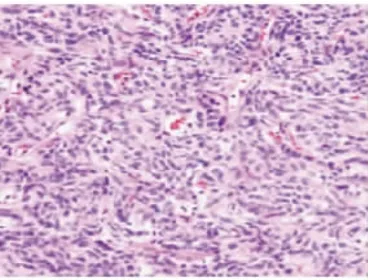
图4 肝转移性胸腺瘤组织病理学检查图片(HE染色,×100)
2 讨论
肝转移性肿瘤自发破裂既往已有报道,原发灶多为肺癌、胃癌、乳腺癌等[1]。源于胸腺上皮细胞的胸腺瘤约90%位于前纵隔,其余可转移至其他脏器,其中肺转移最多见,占所有转移病例的23.5%~43.7%,而肝转移只占11.6%~32.1%,故肝转移性胸腺瘤合并自发破裂在临床极为罕见。胸腺瘤病程进展缓慢,肿瘤生长可长期处于静止期,通常在偶然检查中发现[2]。迄今为止,手术联合放化疗是胸腺瘤主要的治疗方法[3],具体方案取决于肿瘤的位置、大小和出血严重程度。肝肿瘤自发破裂的治疗方式可分为保守型和侵入型,后者包括肝切除术和经导管动脉栓塞术(transcatheter arterial embolization,TAE)。Zhong等[4]回顾性研究162例自发性肝细胞癌破裂继发失血性休克的患者,治疗方法包括保守治疗、TAE和肝切除术,并分析患者30 d和1年生存率。结果接受肝切除术的患者30 d和1年生存率分别为92.5%和59.4%,明显高于单纯接受TAE的患者(30 d和1年生存率分别为66.7%和28.6%)。对于肝功能受损严重或者血流动力学不稳定的患者,TAE是首选[5]。需要指出的是TAE须谨慎施行,因其可导致再出血和肿瘤腹膜种植等并发症[5-6]。Rijckborst等[7]回顾性研究11例欧洲三级医疗中心肝癌破裂患者的临床资料,接受TAE治疗7例(其中2例接受延期肝切除术)、紧急切除术1例、保守治疗3例。经随访,3例患者仍存活(接受TAE治疗+延期肝切除术2例、接受单纯TAE治疗1例),余8例死亡,生存期为7~417 d(中位数为88 d),接受保守治疗的3例患者生存期均未超过1年。故延期肝切除术可显著提高患者远期存活率。本例患者由于低血容量性休克,经紧急施行肝动脉栓塞,完成止血,并对肝转移瘤灶行限期切除。目前,患者状况尚可,未发现明显纵隔及肝脏复发。
[1] Duan YF,Tan Y,Yuan B,et al.Spontaneous rupture of hepatic metastasis from small cell neuroendocrine carcinoma of maxillary sinus[J].World JSurg Oncol,2014,12:126.
[2] Scorsetti M,Leo F,Trama A,et al.Thymoma and thymic carcinomas[J].Crit Rev Oncol Hematol,2016,99:332-350.
[3] Gubens MA.Treatment updates in advanced thymoma and thymic carcinoma[J].Curr Treat Options Oncol,2012,13(4):527-534.
[4] Zhong F,Cheng XS,He K,et al.Treatment outcomes of spontaneous rupture of hepatocellular carcinoma with hemorrhagic shock:a multicenter study[J].Springerplus,2016,5(1):1101.
[5] 张华,罗诗樵,吴忠均.肝癌破裂出血的诊断和治疗[J].中国普外基础与临床杂志,2011,18(12):1338-1343.
[6] Tu J,Jia Z,Ying X,et al.The incidence and outcome ofmajor complication following conventional TAE/TACE for hepatocellular carcinoma[J].Medicine(Baltimore),2016,95(49):e5606.
[7] Rijckborst V,Ter Borg MJ,Tjwa ET,et al.Short article:Management of ruptured hepatocellular carcinoma in a European tertiary care center[J].Eur JGastroenterol Hepatol,2016,28(8):963-966.
