HPLC法测定红羚清散中西红花苷I和西红花苷II的含量
2018-04-04袁娟丽刘明智张钰祺萍乡市食品药品检验所江西萍乡337000
★袁娟丽 刘明智 张钰祺(萍乡市食品药品检验所 江西 萍乡 337000)
红羚清散是萍乡市中医院应用多年的纯中药制剂,是依据仲景《伤寒论》六经辨证理论衍化而来,具有平肝祛风,清热镇惊,解毒的作用。主要用于热盛、神昏,谵语发狂,惊痫抽搐,目赤头痛等症。红羚清散主要由羚羊角、西红花2味中药组成。目前,红羚清散的现行质量标准为《江西省食品药品监督管理局医疗机构制剂》GZJ-0289-(1)-2006,检验项目包括“性状”“鉴别”“检查”等,暂无含量测定项。为进一步保证该制剂的临床疗效,有效控制其质量,提高其质量标准,本实验选取红羚清散中西红花的主成分西红花苷I和西红花苷II为定量指标,采用高效液相色谱法,对其进行含量测定方法的研究。
1 仪器与试药
高效液相色谱仪(Agilent 1200四元低压梯度泵系列,Agilent1200化学工作站,DAD检测器);西红花苷I对照品(Stanford Chemicals,批号:PR151116-08,含量以98.52%计),西红花苷II对照品(Stanford Chemicals,批号:PR160225-17,含量以98.61%计)。水为超纯水,甲醇为色谱纯,其它试剂均为分析纯。实验用样品由萍乡市中医院提供。
2 方法与结果
2.1色谱条件 Agilent 5 TC-C18色谱柱(250mm×4.6mm,5μm),流动相:甲醇-水(49∶51),检测波长为440nm;流速:1.0mL/min;柱温为35℃;进样量为10μL。理论板数按西红花苷I峰计算均应不低于3500。
2.2溶液制备
2.2.1对照品溶液的制备 取西红花苷I对照品、西红花苷II对照品适量,精密称定,分别加稀乙醇制成每1mL含20µg和5µg的溶液,即得。
2.2.2供试品溶液的制备 取本品约0.5g,精密称定,置具塞锥形瓶中,精密加入稀乙醇10mL,称定重量,冰浴超声处理(功率500W,频率40KHz)20min,放冷,称定重量,用稀乙醇补足减失的重量,摇匀,滤过,取续滤液,即得。
2.3方法学考察
2.3.1系统适用性实验 取对照品溶液、供试品溶液及空白溶剂,按2.1项下色谱条件测定,比较供试品溶液色谱、混合对照品色谱及空白溶剂色谱,结果供试品中西红花苷I和西红花苷II色谱峰有较好的色谱分离,见图1。
2.3.2线性关系考察 精密称取西红花苷I对照品9.93mg,置50mL量瓶中,加稀乙醇使溶解并稀释至刻度,摇匀,作为西红花苷I对照品母液;取母液逐级稀释成4.8915,9.7830,19.5661,23.4793,39.1321µg/mL的溶液,精密吸取上述对照品溶液及西红花苷I对照品母液10μL注入液相色谱仪,以峰面积积分值为纵坐标,对照品浓度为横坐标,绘制标准曲线,求得回归方程为Y=58.91X-4.1531,r=0.9999,结果西红花苷I在4.8915~195.6607µg/mL之间呈良好线性关系。
另精密称取西红花苷II对照品9.82mg,置50mL量瓶中,加稀乙醇使溶解并稀释至刻度,摇匀,作为西红花苷II对照品母液。取母液逐级稀释成0.9684,1.9367,3.8734,7.7468,19.3670µg/mL的溶液,精密吸取上述对照品溶液及西红花苷II对照品母液10μL注入液相色谱仪,以峰面积积分值为纵坐标,对照品浓度为横坐标,绘制标准曲线,求得回归方程为Y=73.687X-3.0682,r=0.99981,结果西红花苷II在0.9684~193.6700µg/mL之间呈良好线性关系。

图1 高效液相色谱图
2.3.3精密度试验 精密吸取混合对照品(西红花苷I对照品溶液19.5661µg/mL、西红花苷II对照品溶液3.8734µg/mL),按2.1项下色谱条件,重复进样6次,结果西红花苷I峰面积RSD为1.70%;西红花苷II峰面积RSD为2.89%。表明精密度良好。
2.3.4重复性试验 取同批样品(批号20151106),照2.3项下平行制备供试品溶液6份,照2.1项下色谱条件测定。结果西红花苷IRSD为2.34%;西红花苷IIRSD为1.80%,表明此方法的重复性良好。
2.3.5加样回收试验 精密称取已知含量的本品(批号20151106)约0.25g,置具塞锥形瓶中,精密添加混合对照品溶液(西红花苷I对照品:19.6449µg/mL,西红花苷II对照品:4.4769µg/mL)10mL,按2.1项下方法试验,计算回收率,结果见表1-2。

表1 西红花苷I回收率试验结果(n=6)
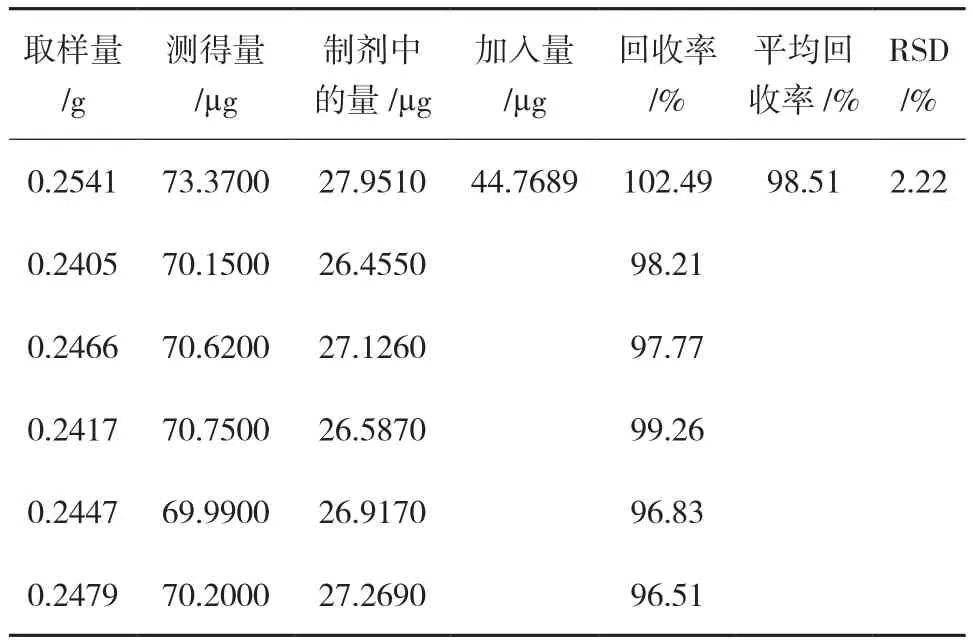
表2 西红花苷II回收率试验结果(n=6)
2.3.6稳定性 精密吸取供试品溶液(批号20151106),分别在0、2、4、6、8、12h进样,按2.1项下色谱条件记录西红花苷I和西红花苷II的峰面积,结果供试品溶液中西红花苷I和西红花苷II在12h内峰面积无明显变化,西红花苷I RSD为0.79%(n=6),西红花苷II RSD为0.1.34%(n=6),表明样品溶液在12h内稳定。
2.3.7样品测定 取本品5批,照2.1项下方法试验,测定结果见表3。

表3 样品测定结果(n=5) mg/g
3 讨论
3.1色谱条件的选择 参考中国药典[1]及有关文献[3],选择440nm作为检测波长,甲醇-水(49∶51)为流动相,在此条件下,各组分的峰型及分离效果良好,同时未见其他成分干扰。
3.2供试品溶液的制备 参考中国药典[1],采用超声提取法,以稀乙醇为提取溶剂。分别对10min、20min、30min提取时间进行比较,结果表明20min已提取完全。同时,因西红花苷稳定性差,且对温度非常敏感[10],分别对供试品在冰浴中和常温下超声处理方法进行了对比研究。结果表明,冰浴比常温提取所测得的西红花苷Ⅰ和西红花苷Ⅱ含量略高,故采用冰浴超声提取作为红羚清散中西红花苷Ⅰ和西红花苷Ⅱ的提取方法。此外,考察了避光条件下与未避光条件下操作,最后确定供试品溶液制备应避光操作,并置于棕色瓶中避光保存。
根据实验结果可知,不同批次样品中西红花苷I与西红花苷II含量差异显著,提示西红花原药材的质量存在差别,为避免由原药材引起中成药的疗效差异,有必要对西红花进行质量控制。本研究建立了同时测定红羚清散中西红花苷I与西红花苷II含量的HPLC方法,经方法学验证,该方法准确、快速,操作简便,专属性强,重现性好,可用于红羚清散的质量控制。
[1]国家药典委员会.中华人民共和国药典·一部[S].北京:中国医药科技出版社, 2015:129-130.
[2]周素娣,仲惠娟. HPLC测定西红花提取物及其片剂中各西红花苷含量[J]. 药物分析杂志, 1998, 18(3):159-162.
[3]杨博涵,朱旭江. HPLC法测定藏药仁青芒觉胶囊中西红花苷-I和西红花苷-II的含量[J]. 中国民族民间医药, 2015, 24(20):159-162.
[4]马慧萍,李兰茹,董志臣,等. HPLC法测定红花益气养血胶囊中西红花苷-I和西红花苷-II的含量[J]. 解放军医学学报, 2013,29(6):512-514.
[5]戴智慧, 黄士文,倪穗, 等. HPLC法测定浙江慈溪水稻田栽培的西红花中西红花苷I、II含量的研究[J]. 中国野生植物资源, 2016,35(2):14-18.
[6]刘瑛,张浩. RP-HPLC法测定栀子中西红花苷-1和西红花总苷含量[J]. 中国民族民间医药, 2007, 89(6):337-339.
[7]张蕾,周帼维,周素娣.不同引种产地西红花的含量测定[J]. 中国中药杂质, 1997, 22(11):657-659.
[8]何常明,谢晓梅,何美莲,等. 西红花中西红花苷-1和西红花苷-2含量测定方法的建立[J]. 药物分析杂志, 2006, 26(9):1 270-1 273.
[9]金春女,李云峰. 西红花的真伪鉴别及主要成分西红花苷I、II的含量测定[J]. 中医中药, 2014, 28(15):188-189.
[10]付小梅,王峥涛.西红花苷-Ⅰ的稳定性研究[J].食品科学,2012, 33(5):71-73.
