胃食管吻合术联合Nissen胃底折叠术对食管中段癌患者术后胃食管反流的影响
2018-04-02隋丰光金澄宇
隋丰光 金澄宇
食管癌是我国常见的消化道肿瘤之一,食管癌切除术仍是治疗食管肿瘤的有效手段,术后生存率为20%~36%[1]。食管胃吻合术是食管癌与贲门癌切除术后主要的重建方式,胃食管吻合术中由于切除了食管下括约肌和食管膈裂孔结构遭到破坏,术后常出现胃食管反流(gastroesophageal reflux,GER)[2]。胃食管吻合术后胃食管返流物长期刺激食管可引起器质性损失或食管溃疡,影响患者终身,严重可引起吸入性肺部感染甚至窒息死亡[3]。胃底折叠术是治疗胃食管反流病(gastroesophageal reflux disease,GERD)标准术式,其效果确切,手术通过增强食管下括约肌功能,发挥抗反流功能,从而使大部分患者摆脱药物治疗,生命质量明显提高[4]。
资料与方法
一、对象
选取2015年9月至2017年3月,新疆维吾尔自治区人民医院住院并行食管癌切除术31例食管中段癌患者临床资料,根据其手术方式不同,将其分为胃食管吻合术联合Nissen胃底折叠术组(观察组)和非胃底折叠全胃代食管吻合术组(对照组)。其中观察组15例,对照组16例,男性19例,女性12例,平均年龄(68.2±8.11)岁,身高(167.6±7.3)cm,体重(67.6±8.9)kg,BMI(23.8±4.7)kg/m2,2组患者性别、年龄、体重、BMI、肿瘤大小、肿瘤分期及术前胃食管反流发生情况等一般临床资料比较,差异无统计学意义(P>0.05),组间具有可比性(表1)。纳入标准:(1)食管中段,并病理学检查确诊为食管癌;(2)无明显手术禁忌证,可耐受食管癌切除治疗。排除标准:(1)非食管中段癌(上端、下段);(2)合并严重呼吸、循环系统疾病,不能耐受手术者;(3)中度以上营养不良者。
二、方法
1.手术方法:所有患者均接受食管癌切除术,采取右胸腹联合切口,常规游离食管,切除肿瘤,胃食管吻合术,清扫淋巴结。观察组胃食管吻合基础上采取胃底折叠术:充分游离胃底后,用无损伤抓钳抓持胃底大弯边缘处胃壁组织,经食管后方将胃底大弯侧部分胃壁拉至食管右侧,自口腔插入食管扩张器至胃内,于食管下端用0号不吸收线间断缝合2~3针,完成宽约2 cm的Nissen胃底折叠,缝线可穿透胃壁全层或胃壁浆肌层并固定于食管下段前壁。
2.食管酸度测定方法:术后2周后对所有患者进行24 h pH监测,检查前3 d停止使用胃肠动力及抑制胃酸分泌类药物,禁食6 h;使用DigitrapperMKHI型便携式pH值监测仪(CTDSYNECTICS公司生产)胃肠功能动态pH值监测仪动态监测食管24 h pH值,pH锑电极经鼻孔插入胃内,注意插入力度,固定电极和记录仪,常规24 h连续记录,记录24 h酸反流次数、最长酸反流时间和pH值<4的总时间等。
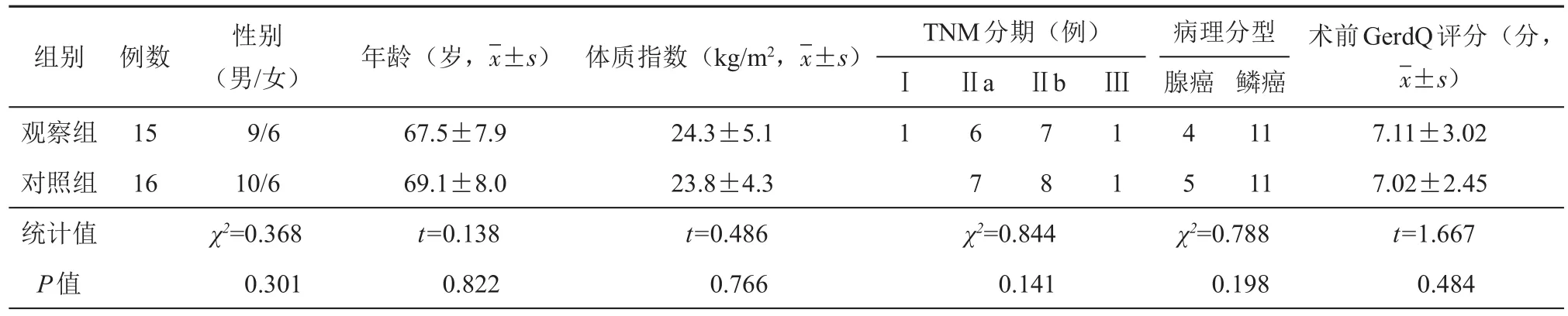
表1 胃食管吻合术联合Nissen胃底折叠术组与非胃底折叠全胃代食管吻合术组组患者一般临床资料比较
3.胃食管反流病调查问卷(gastroesophageal reflux disease questionnaire, GerdQ) 评 分 表[5]:所有患者术后1、3、6、12个月均在培训医师指导下认真填写GerdQ调查表,根据患者回忆过去1周内烧心、反流、上腹痛、恶心、有无反流相关睡眠障碍、是否需要服用非处方药物等6项症状情况,根据1周内症状发作频率进行评分,将烧心、反流、有无睡眠障碍、非处方药物服用情况,按0、1、2~3、4~7 d分别评为0、1、2、3分,将上腹痛、恶心的发作频率,按0、1、2~3、4~7 d分别评为3、2、1、0分,总积分0~18分。
三、统计学处理
采用SPSS 23.0统计软件进行数据分析,计量资料以-x±s表示,组间比较采用t检验;计数资料以率表示,组间比较采用χ2检验,以P<0.05为差异有统计学意义。
结 果
2组患者均未出现死亡病例,均获随访,且术后均未发生有吻合口瘘及胸胃排空障碍等并发症。观察组患者术后2周24 h酸反流次数显著少于对照组,最长酸反流时间和pH值<4的总时间短于对照组,DeMeester评分显著低于对照组,组间比较均有统计学意义(P均<0.05,表2)。观察组术后3、6、12个月GerdQ评分显著低于对照组,组间比较差异均有统计学意义(P均<0.05,表3)。
表2 2组患者术后2周24 h食管内pH监测指标(±s)
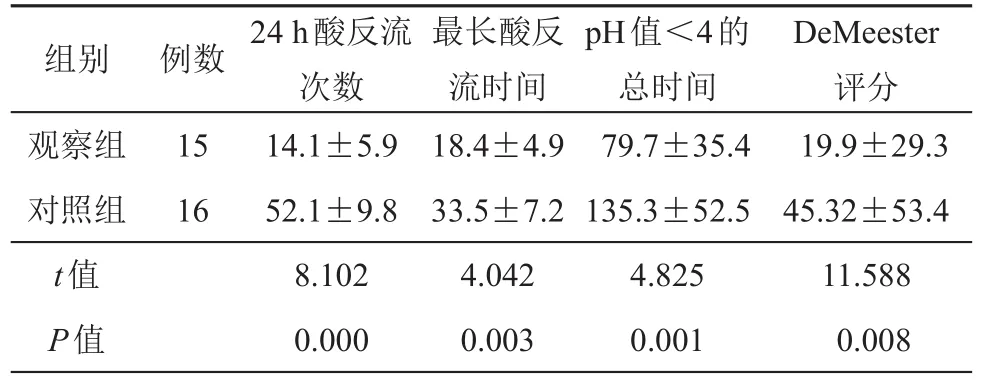
表2 2组患者术后2周24 h食管内pH监测指标(±s)
例数15 16组别观察组对照组t值P值24 h酸反流次数14.1±5.9 52.1±9.8 8.102 0.000最长酸反流时间18.4±4.9 33.5±7.2 4.042 0.003 pH值<4的总时间79.7±35.4 135.3±52.5 4.825 0.001 DeMeester评分19.9±29.3 45.32±53.4 11.588 0.008
表3 2组患者术后GerdQ评分量表积分(分,±s)
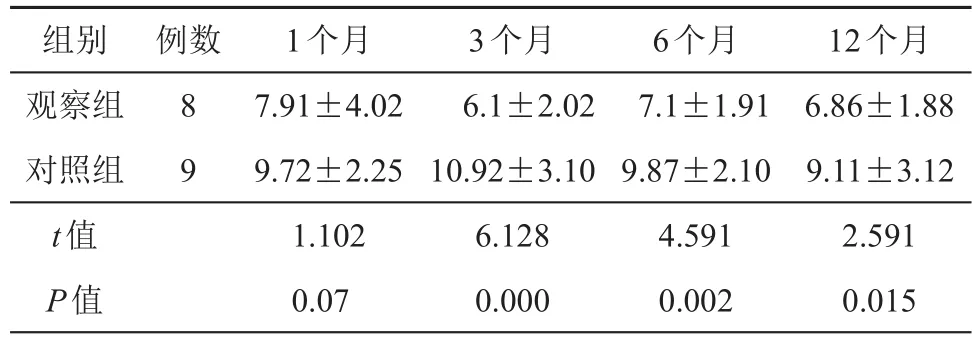
表3 2组患者术后GerdQ评分量表积分(分,±s)
例数8 9组别观察组对照组t值P值1个月7.91±4.02 9.72±2.25 1.102 0.07 3个月6.1±2.02 10.92±3.10 6.128 0.000 6个月7.1±1.91 9.87±2.10 4.591 0.002 12个月6.86±1.88 9.11±3.12 2.591 0.015
讨 论
手术是治疗食管癌的首选方法,消化道的重建是食管手术的关键所在。GER是食管癌切除术后常见并发症之一,其长期甚至终身影响患者术后生活质量。本研究中,以GerdQ≥8为诊断GERD标准[5],术后非折叠组3、6、12个月均发生GERD,由于食管癌切除术食管上括约肌、膈食管韧带、膈肌脚均遭到严重破坏,导致患者食管下括约肌功能障碍及食管体部运动异常而术后反流发生,同时术中胃迷走神经干被切断及术后胸胃生理解剖改变导致术后胸胃排空延迟,进一步导致或加重GERD[6]。以往研究中有多种外科策略被用来预防食管、贲门切除术后的GER的发生,尽管有些方法可以成功控制术后反流的发生,但因为操作起来比较复杂,限制条件多,而难以得到广泛应用[7]。因此,如何减少食管癌术后GER发生,提高患者生命质量成为研究的重点,胃底折叠术是治疗胃食管反流的一项标准术式,在减少食管癌术后GER方面具有一定的作用[8]。
本研究中,胃食管吻合术联合胃底折叠术后术后3、6、12个月GerdQ评分积分显著低于对照组(P<0.05),提示该术长期疗效可,王中秋等[7]报道,在食管癌切除术中附加“残胃闭合角”折叠术起到明显的术后抗反流效果,与本研究结果相似。胃底折叠术通过简单的操作可以实现类似生理结构的食管前壁嵌插和吻合口上方环形高压,术后结构和位置接近消化道正常生理结构,是防止GER基础[9]。然而,食管癌外科治疗规范标准对食管切除范围是有严格要求的,这使得下段食管癌及贲门癌患者很难有足够长的残余食管或残余胃来进行胃底折叠术。本研究中,为了研究结果的可靠性、准确性,研究对象均选取食管中段癌患者,对手术患者均采用相同手术径路、吻合方法,所有手术患者残留食管的长度均>5 cm,保证了测量的准确性,排除了吻合口部位及吻合方法对术后GER产生的影响。正常食管腔内pH值为5~7,当pH值<4时提示存在GER,根据24 h食管内pH监测,胃-食管吻合联合胃底折叠组和单纯胃-食管吻合术后均存在不同程度的病理性胃食管反流,而胃-食管吻合联合胃底折叠组的反流程度明显减轻,24 h酸反流次数、最长酸反流时间和pH值<4的总时间均明显降低(P<0.05)。提示与胃食管吻合术比较,接受胃食管吻合术联合Nissen胃底折叠术组的GER病情获得了更好的控制效果,其原因可能是:(1)胃底折叠后,减少了分泌胃酸的壁细胞有效面积,而最大限度减少了胃酸的分泌;(2)胃底折叠后,其有效直径与食管相近,更接近消化道重建后生理解剖要求,胃容积缩小,主要起食物通道的作用,食物进入残胃后可快速通过,避免了食物的潴留;另一方面,该术式人工重建反流屏障,防止胃内容物反流;(3)由于胸胃体积减小,使得肺扩张时对胸胃的挤压减轻,有效减少了每次反流的持续时间和反流量。
综上,胃-食管吻合联合胃底折叠术对外科技术不需改变太多,即使在根治性切除后,行改良的胃底折叠术仍然可行,并未增加手术风险[10],也可明显减轻胃食管反流症状,改善了患者的术后生活质量。本研究为食管癌患者手术方式的选择提供一定的临床理论依据,但本研究样本量少,尚不足于证实胃-食管吻合联合Nissen胃底折叠术安全性、实用性,笔者拟在后续的工作中扩大样本进一步确定胃-食管吻合联合Nissen胃底折叠术对食管癌切术后GER病情的控制效果。
