超声检测肺动脉参数及肺动脉瓣环Z值在小儿法乐四联症根治术式选择中的临床价值
2018-03-28李静雅李嵘娟金兰中王芳韵孙妍杨娇杨娅马宁
李静雅,李嵘娟,金兰中,王芳韵,孙妍,杨娇,杨娅,马宁
法乐四联症(TOF)在我国是紫绀型先天性心脏病中最常见的一种,占12%~14%,其自然预后不佳,需要手术矫治[1]。TOF 患儿病情程度差异很大,手术方式因人而异,截止目前根治手术对右心室流出道的处理有两种主流方式,一是切开肺动脉瓣环扩大流出道(简称“跨环”),二是保留肺动脉瓣环(简称“留瓣”)。经胸超声心动图(TTE)作为术前诊断TOF的重要检查手段,可以测量和评价心内结构的发育情况,但是在不同的根治术选择中,哪些TTE参数具有重要指导意义尚不明确。本研究探讨TTE检测肺动脉参数及肺动脉瓣环Z值在小儿TOF根治术式选择中的临床价值。
1 资料与方法
研究对象:回顾性分析2012-01至2016-06在我院确诊并实施TOF根治手术治疗的患儿143例,中位数年龄为8(1~171)个月,男性91例(63.6%);合并的心脏畸形有:卵圆孔未闭(79例,55.2%)、侧枝血管(43例,30.1%)、右位主动脉弓(35例,24.5%)、动脉导管未闭(18例,2.6%)、左上腔静脉残存(14例,1.0%)、房间隔缺损和肌部室间隔缺损(各12例)、主动脉瓣右冠瓣脱垂(10例)、迷走左锁骨下动脉和双主动脉弓、主动脉瓣上隔膜(各1例)。本研究排除TOF合并肺动脉瓣闭锁或缺如的患者。143例患儿根据TOF根治术式分组,行跨环补片扩大修补右心室流出道者为跨环组(n=100),行保留肺动脉瓣环者为留瓣组(n=43)。
仪器与方法:(1)TTE常规测量:使用Philips iE33彩色多普勒超声诊断仪(Philips,荷兰),选用探头为S8-3/S5-1(频率3-8MHz/1-5MHz)。常规参数测量包括左心室舒张末期前后径(LVDd),右心室舒张末期前后径(RVDd),左心室射血分数(LVEF),均由M型获得,取样线置于二尖瓣瓣尖至乳头肌水平。(2)右心室流出道相关参数测量:依据2010年美国超声心动图协会成人右心超声心动图指南[2],测量:右心室流出道远心端内径(RVOT)、肺动脉瓣环内径(PVD)、主肺动脉内径(MPAD)、左肺动脉内径(LPAD)和右肺动脉内径(RPAD)。(3)计算Nakata指数:Nakata指数又称肺动脉指数,本研究采用TTE测量得到的左、右肺动脉内径估测Nakata指数的方法,计算公式如下:Nakata指数=π×(LPAD2+RPAD2)/4×BSA。BSA为体表面积,计算公式BSA=体重×0.035+0.1。(4)转换肺动脉瓣环Z值:依据参考文献[3]绘制的肺动脉瓣环Z值表,根据本研究患者体表面积与PVD查表,明确对应肺动脉瓣环Z值,以肺动脉瓣环Z值≥0,-1≤肺动脉瓣环Z值<0,-2≤肺动脉瓣环Z值<-1,肺动脉瓣环Z值<-2进行分层,对不同肺动脉瓣环Z值的患儿进行比较。 (5)术中测量PVD及术式选择依据:术中所测量PVD是术者在建立体外循环并切开右心室流出道显示肺动脉瓣后,此时以血管探子对瓣环及主肺动脉进行探查,通过探子的直径即记录为PVD。术中测得PVD与正常儿童的PVD相比较[4],小于正常值者考虑应用跨环术式,大于等于正常值者考虑应用留瓣术式。
统计学分析:本研究采用 SPSS 21.0 软件进行统计学分析。计量资料的比较采用两组独立样本 t 检验,以均值±标准差表示,对不服从正态分布或方差不齐的两组资料采用秩和检验,以中位数(四分位数)表示。计数资料为二分类变量时采用卡方检验,为有序多分类变量时采用两独立样本秩和检验。相关性分析采用Spearman秩相关。P<0.05为差异有统计学意义。
2 结果
两组患儿性别及一般资料比较:两组患儿术前月龄(69.79月 vs 77.15月)和体表面积(69.01 mm2vs 68.98 mm2)比较差异均无统计学意义(P>0.05)。两组患者均实行TOF一期根治手术,心内畸形矫正均较满意,室间隔补片修补良好, 无残余漏,右心室流出道及肺动脉疏通满意。术后两组患者病情稳定,无因发生严重低心排血量综合征而死亡的病例。
两组患者 TTE测量值比较(表1):跨环组与留瓣组相比,LVDd、PVD和MPAD均较低,差异均有统计学意义(P均<0.05)。其余测值差异无统计学意义(P>0.05)。Nakata指数以150 mm2/m2为界值调整为二分类变量,Pearson卡方检验提示P=0.390,提示不同术式患者间Nakata指数差异无统计学意义(P>0.05)。

表1 两组患者经胸超声心动图参数比较
两组不同肺动脉瓣环Z值患儿构成比的比较:依据肺动脉瓣环Z值划分四个分层。两组不同肺动脉瓣环Z值患者的构成比呈有序分布,随着肺动脉瓣环Z值减小,留瓣组比例逐渐降低,跨环组比例逐渐增加(图1)。肺动脉瓣环Z值≥0时,留瓣组与跨环组的构成比分别为52%(17例)和48%(16例);-1≤肺动脉瓣环Z值<0时,留瓣组与跨环组的构成比分别为26%(9例)和74%(25例);-2≤肺动脉瓣环Z值<-1时,留瓣组与跨环组的构成比分别为27%(9例)和73%(24例);肺动脉瓣环Z值<-2时,留瓣组与跨环组的构成比分别为22%(8例)和78%(29例)。不同肺动脉瓣环Z值患儿间构成比差异均有统计学意义(P均<0.05)。

图1 两组不同肺动脉瓣环Z值患儿构成比
TTE与术中测量肺动脉瓣环径的相关分析(图2):两者的相关系数为r=0.581,双侧Spearman检验P=0.000,提示两者有相关性,直线相关性中等。
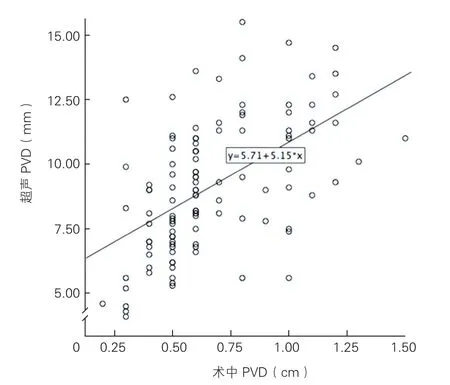
图2 经胸超声心动图与术中测量肺动脉瓣环内径的散点图
3 讨论
1955年,Lillehei等[5]报道了第一例TOF手术。1976年,室间隔缺损修补的手术入路转换至心房,术者需经心房入路进行室间隔修补并行跨瓣环补片扩大右心室流出道。目前,术者对“跨环”和 “留瓣”两种术式的选择主要依据术中测量所得PVD及其肺动脉瓣环Z值。该方法存在几点不足:(1)该数据为单一参数,仅反应了右心室流出道瓣环水平的发育情况;(2)该参数为术中体外循环建立后获得,不能反应患者生理状态;(3)目前国内外临床医师通过PVD及肺动脉瓣环Z值决定术式选择上尚未形成明确共识[6-8]。虽然该方法在术中应用简便,但由于存在以上不足,仍应进一步探索其它客观参数的应用价值。
TTE在TOF诊疗中具有明确的临床价值,二维TTE结合多普勒技术于患者术前常规应用于疾病诊断和合并心内畸形的判断,术后可评价手术矫治效果。了解TOF患者左心室及肺动脉发育情况是实施一期手术的必要条件,通过TTE可获得左心室舒张末期容量指数、McGoon比值、Nakata指数,以选择实施姑息术式还是根治术式[9]。应用TTE也可获得肺动脉瓣环Z值为评价不同根治术提供依据。
本研究回顾分析跨环组和留瓣组不同术式患者的TTE资料,跨环组和留瓣组比较, LVDd、PVD和MPAD均较低(P<0.05)。提示留瓣组左心室与肺动脉均较跨环组发育好。说明较好的左心室与肺动脉发育是行留瓣术式的基本条件,且二者的关系密切。因为严重的肺动脉发育不良可造成肺部和心房血流少,影响左心室发育,加之右心压力高,经室水平大量右向左分流,体循环的血流一部分来源于右心室,右心室参与对抗循环阻力,则进一步造成左心室废用性缩小[10]。
在右心室流出系统相关的TTE参数中,本研究采用了RVOT、PVD、MPAD及Nakata指数进行两组比较,其中PVD与MPAD存在差异,RVOT与Nakata指数无差异。TTE获取的PVD和MPAD在术式选择中有较为明确的临床意义。当肺动脉瓣及主肺动脉发育较差时,扩大补片修补需延续到肺动脉主干甚至分支方可解除流出道梗阻,故跨环术式则势在必行。而这两者均发育较好时,则可考虑保留,因Rao等[11]发现应用保留肺动脉瓣术式的28例患者术后虽残留了右心室流出道狭窄,但在患者生长过程中狭窄逐渐减轻。 而RVOT与Nakata指数无差异与术中解除右心流出系统梗阻的方式有关,TOF患者右心室流出道的处理在两种术式中较为一致,均为清除隔束、壁束肥厚肌束后扩大补片修补,故右心室流出道的狭窄程度与术式选择的关系不大,而Nakata指数主要应用于姑息和根治术式的选择,所以在两组患者中无明显差别。
通过对PVD进行肺动脉瓣环Z值转换,我们也发现随着肺动脉瓣环Z值减小,即PVD的减小,选择跨瓣术式的比例增加,两种术式的构成比在不同肺动脉瓣环Z值的患儿间存在统计学差异,这说明TTE测量获得的肺动脉瓣环Z值与术中获得的一样,同样作用于术者对术式的选择。而且经由TTE测量的肺动脉瓣环Z值在术前即可获得,为术前做出预判提供了客观依据。在TTE与术中测量的PVD相关性分析中,二者的相关性为中等,主要原因在于术中获取的PVD测量较粗糙,与人为操作有关,且非生理状态下测量,故导致目前较为一般的直线相关结果。因此,若从更符合生理状态条件的评估来说,TTE在术前测得的肺动脉瓣环Z值更具有客观性。
众所周知,不同根治手术方式针对不同病情的TOF患儿,具有各自的优点和局限性[12-14]。通过谨慎的术前评估和术式选择,患者也可获得较好的远期生存,本研究针对不同术式分组研究术前哪些TTE参数更具有临床价值,并没有对不同术式患儿随访结果进行分析讨论,这将是作者下一步拟进行的研究。TTE在TOF术式选择中具有重要的临床价值,TTE测量的PVD、MPAD及肺动脉瓣环Z值均在术前即可作为选择术式的客观参数。在根治术不同术式选择中术者可依据以上参数做出术式的预判,并结合术中测量的肺动脉瓣环Z值给予患儿最优化的临床解决方案。
[1]汪增炜. 心脏血管外科学[M]. 第2版. 北京: 人民卫生出版社,2002: 658.
[2]Rudski LG, Lai WW, Afilalo J, et al. Guidelines for the echocardiographic assessment of the right heart in adults: a report from the American Society of Echocardiography endorsed by the European Association of Echocardiography, a registered branch of the European Society of Cardiology, and the Canadian Society of Echocardiography[J]. J Am Soc Echocardiogr, 2010, 23 (7): 685-713.DOI: 10. 1016/j. echo. 2010. 05. 010.
[3]Pettersen MD, Du W, Skeens ME, et al. Regression equations for calculation of z scores of cardiac structures in a large cohort of healthy infants, children, and adolescents: an echocardiographic study[J]. J Am Soc Echocardiogr, 2008, 21(8): 922-934. DOI: 10. 1016/j. echo. 2008.02. 006.
[4]Rowlatt UF, Rimoldi HJA, Lev M. The quantitative anatomy of the normal child. Pediatr Clin North Am, 1963, 10: 499.
[5]Lillehei C, Walton CM, Warden Herbert E, et al. Direct vision intracardiac surgical correction of the tetralogy of Fallot, pentalogy of Fallot and pulmonary atresia defects[J]. Ann Surg, 1955, 142(3): 418-445.
[6]Awori MN, Leong W, Artrip JH, et al. Tetralogy of Fallot repair:optimal z-score use for transannular patch insertion[J]. Eur J Cardiothorac Surg, 2013, 43 (3): 483-486. DOI: 10. 1093/ejcts/ezs372.
[7]Ito H, Ota N, Murata M, et al. Technical modification enabling pulmonary valve-sparing repair of a severely hypoplastic pulmonary annulus in patients with tetralogy of Fallot[J]. Interact Cardiovasc Thorac Surg, 2013, 16(6): 802-807. DOI: 1093/icvts/ivt 095.
[8]白凯, 苏肇伉, 张儒舫, 等. 婴儿早期法洛四联症的外科治疗. 中国胸心血管外科临床杂志[J], 2011, 18: 313-316. DOI: 1093/icvts/ivt095.
[9]贺新建, 董凤群, 魏九茹, 等. 超声估算左心室舒张末容积指数、McGoon比值和Nakata指数对法洛四联症术前评估的对比研究[J].中国超声医学杂志, 2010, 26(08): 716-719. DOI: 10. 3969/j. issn.1002-0101. 2010. 08. 015.
[10]朱晓东, 张宝仁. 心脏外科学[M]. 北京: 人民卫生出版社, 2007:570-572.
[11]Rao V, Kadletz M, Hornberger LK, et al. Preservation of the pulmonary valve complex in tetralogy of Fallot: how small is too small? [J]. Ann Thorac Surg, 2000, 69(01): 176-179.
[12]Gatzoulis MA, Balaji S, Webber SA, et al. Risk factors for arrhythmia and sudden cardiac death late after repair of tetralogy of Fallot: a multicentre study[J]. Lancet, 2000, 356(9234): 975-981.
[13]万俊义, 陆敏杰, 张戈军, 等. 经皮肺动脉瓣植入术后患者心功能的变化8例分析[J]. 中国循环杂志, 2016, 31(07): 683-686. DOI:10. 3969/j. issn. 1000-3614. 2016. 07. 015
[14]Bacha E. Valve-sparing options in tetralogy of Fallot surgery[J]. Semin Thorac Cardiovasc Surg Pediatr Card Surg Annu, 2012, 15 (1): 24-26.DOI: 10. 1053/j. pcsu. 2012. 01. 006.
